改性角蛋白基吸水性保水剂的制备及其性能
2022-10-13李闻欣陈玉柔岳明明张素风
李闻欣, 陈玉柔, 岳明明, 张素风
(1.陕西科技大学 轻工科学与工程学院, 陕西 西安 710021; 2.山东德信皮业有限公司, 山东 淄博 256410)
0 引言
土壤高吸水性保水剂又称为吸水树脂(Absorbent Polymer),是一种人工合成的具有强吸水、保水性能的材料,其优异的吸水能力和良好的保水性可缓解水土流失、农林受旱和土地荒漠化等问题[1-3].农用保水剂主要用于作物的抗旱节水,能稳定土壤结构,降低土壤容重,提高土壤毛管持水量、增加水分入渗,控制土壤水分的蒸发,缓慢释出水分供植物吸收利用[4-5].目前,聚丙烯酸、聚乙烯酸、乙烯酸、异丁烯无水顺式丁烯二酸、淀粉聚丙烯酸、聚乙烯、纤维素等高分子材料均可作为其合成材料[6].合成树脂类保水剂吸水、保水能力强,但可降解性差;淀粉类保水剂吸水后凝胶强度低,耐霉性差;纤维素类保水剂吸水率略低,但是其吸盐性能好,且pH值易调节,可生物降解[7].随着人们绿色环保意识、资源意识的不断增强,研究开发绿色可降解的保水剂成为一个新的研究课题.
制革废弃牛毛是牛皮制革过程中产生的一种可再生角蛋白资源,主要富含C、O、N、H、S五种元素,其中硫元素和氮元素,可作为硫肥和氮肥补充农作物的营养.保毛脱毛回收牛毛由于在脱毛过程中经氢氧化钙作用,其分子内部形成了特殊的-S-O-Ca-S-交联键,故其除了富含五种常见元素外,Ca2+含量也很高[8].目前大量的废弃牛毛堆置或焚烧处理,浪费了蛋白质资源,因此,研究和开发利用废弃牛毛,既可实现制革废弃物高附加值转化,还可节约资源,降低对环境的污染[9].
利用制革废弃牛毛提取角蛋白进行接枝改性制备土壤保水剂,不仅是实现制革废弃物资源化高效利用的一种新方法,同时也有利于农业经济的绿色可持续发展[10].本文以制革废弃牛毛提取的角蛋白为主要原料、AA为接枝单体、加入MBA使角蛋白主链与AA支链之间相互交联,形成复杂的三维网状结构,有利于提高其吸水率.通过接枝聚合反应,制备具有较高吸水率的新型角蛋白基保水剂.以单因素法优化了制备工艺,并对吸水特性和结构形态进行表征.
1 实验部分
1.1 实验材料与仪器
1.1.1 主要材料
水解角蛋白粉,自制.
氢氧化钾(KOH)、丙烯酸(AA)、过硫酸钾(KPS),天津市大茂化学试剂厂;N,N-亚甲基双丙烯酰胺(MBA),天津市福晨化学试剂厂;上述试剂均为分析纯;凹凸棒土(ATP,200目),常州鼎邦矿产品科技有限公司.
1.1.2 主要仪器
Cary-5000紫外可见光分光光度计,Agilent Technologies有限公司;STA449F3-1053-M同步TG-DSC热分析仪,德国Netzsch公司;Vertex70傅里叶红外光谱仪、D8 Advance X-射线衍射仪、JSM-6460扫描电子显微镜,均为德国Bruker公司.
1.2 角蛋白基保水剂(KAP)的制备
将适量的角蛋白水解产物和凹凸棒石(ATP)添加到烧瓶中,连续搅拌并加热至65 ℃.同时,引入氮气30 min.随后,将AA(质量分数为70%的AA用质量分数为20%的KOH溶液中和)、MBA和KPS溶液相继加入.1 h后,将产物完全浸入蒸馏水中以除去未反应的单体,并在50 ℃下干燥.
1.3 KAP结构形态表征与吸水特性
1.3.1 KAP相关表征
(1)红外光谱(FT-IR)表征分析:将相关样品经烘干,研磨,得固体粉末,采用溴化钾压片法测定样品在400~4 000 cm-1的吸收.
(2)X-射线衍射(XRD)表征分析:采用X射线衍射仪对相关样品进行分析,扫描速率6°/min,扫描电压40 kV,以Cu-Kα作为射线源,角度范围5°~70°.
(3)热重(TG-DTG)表征分析:采用热重分析仪检测角蛋白和KAP样品的热性能,温度范围是30 ℃到500 ℃,升温速率10 ℃/min.
(4)扫描电镜(SEM)表征分析:将所制备的KAP样品经吸水溶胀,冷冻干燥,表面喷金处理后采用场发射扫描电镜观测其形貌结构.
1.3.2 KAP的性能检测
(1)KAP在去离子水中的吸水率测定
称取干燥的KAP(0.1 g,小于30目),在室温下完全浸入250 mL蒸馏水中,直到达到溶胀平衡(约90 min).然后,将溶胀的样品通过尼龙网(100目)过滤以除去游离水.溶胀平衡吸水率(Qeq,g/g)按式(1)计算.
Qeq=(m1-m)/m
(1)
式(1)中:m为干燥后试样的质量(g);m1为达到膨胀平衡后试样的质量(g).
(2)KAP在不同温度下的吸水率测定
将称取的KAP(m)浸入各种温度(5 ℃、15 ℃、25 ℃、35 ℃和45 ℃)的蒸馏水中.然后,将溶胀的KAP通过100目尼龙网过滤并称重(m1).由公式(1)计算出Qeq,g/g.
(3)对不同pH值土壤溶液的吸水率测定
用0.1 mol/L HCl或NaOH水溶液调节模拟的土壤溶液[7].在室温下,将称取的KAP(m)浸入50 mL pH分别为2至11的土壤溶液中.接下来,将溶胀的样品用尼龙网过滤并称重(m1),由公式(1)计算出Qeq,g/g.
(4)对不同pH土壤溶液的影响
在室温下,将称重的KAP浸入50 mL具有不同pH值的模拟土壤溶液中.用尼龙网过滤后,用pH计测定滤液的pH.
(5)土壤中KAP的降解实验
将干燥过的KAP放在一个尼龙袋中称重(标记为Q0),将其埋在土壤下10 cm的塑料杯中.土壤湿度保持在30%.间隔一定时间取出样品,用蒸馏水洗涤,并在65 ℃下干燥至恒重(标记为Qi).测试不同降解时间失重率的变化.降解率(De%)通过公式(2)计算.
De(%)=[(Q0-Qi)/Q0]×100
(2)
式(2)中:Q0为装有样品和尼龙袋的质量(g);Qi为用蒸馏水洗涤并干燥恒重的样品和尼龙袋质量(g).
(6)保水性能检测
保水性能是指吸水剂在充分吸水饱和后,当所处环境变化(如温度)时,仍可以保持一定的水分[11].以一定时间保水率的变化情况来表示保水剂的保水性能.称取50 g吸水饱和后的保水剂置于培养皿中,放入55 ℃的恒温箱中,每隔20 min取出称量其质量至质量稳定为止,每组试验重复8次.保水率计算式为:
R=(M1-M0)/(M2-M0)
(3)
式(3)中:R为保水率(%);M0为培养皿的质量(g);M1为某一时段保水剂和培养皿的质量和(g);M2为吸水饱和的保水剂和培养皿的质量和(g).
2 结果与讨论
2.1 单因素优化KAP的合成条件对吸水率的影响
角蛋白是由氨基酸组成的一种天然高分子材料,可以增加微生物的活性,改善土壤环境.图1(a)表明,当角蛋白与AA的质量比为2.5∶1时,KAP的最大吸水率达到587.9 g/g.当角蛋白与AA的质量比小于2.5∶1时,单体AA将更多地接枝到角蛋白的骨架上,导致吸水率增加.当角蛋白与AA的质量比大于2.5∶1时,吸水率降低.主要原因是体系中交联点增加,导致单体和角蛋白的接枝率降低,从而降低了KAP的吸水率.
众所周知,交联密度对于吸水剂的吸水率至关重要.图1(b)表明,当交联剂MBA用量为0.1%时,KAP的吸水率最大.当MBA用量小于0.1%时,可溶性共聚物增加,导致吸水率降低.当MBA用量大于0.1%时,由于较高的MBA含量和更多的交联点将形成额外的网络,减少亲水基团,从而导致吸水率下降.该结论与Flory的网络理论是一致的[12].
图1(c)表明,当KPS用量为1.5%时,KAP的最大吸水率可达到593.0 g/g.当KPS用量小于1.5%时,这导致反应缓慢并且形成无效的交联网络,使吸水性变差.此外,较高的KPS含量将导致反应速率更快,这意味着增加交联密度,使KAP的吸水率降低.
ATP作为一种填料,可作为土壤改良剂,并含有矿物质元素,可以改善土壤的理化性质.图1(d)表明,当ATP含量低时,会降低聚合反应中的接枝率,吸水率降低.但是,较高的ATP含量会导致更多的交联点,这也导致交联密度增加,吸水率降低[13].


图1 不同因素对吸水率的影响
2.2 KAP表征结果分析
2.2.1 FT-IR结果分析
图2表明,对于ATP,在3 580 cm-1、3 287 cm-1(-OH拉伸振动)处出现特征峰.在1 034 cm-1(Si-O-Si的拉伸振动),591 cm-1(硅-氧弯曲振动)处观察到特征峰.对于角蛋白,在3 632 cm-1、1 662 cm-1和1 456 cm-1的谱带分别属于酰胺基(N-H)拉伸振动,酰胺I和酰胺II带.对于AA,特征峰在1 718 cm-1处归属于C=O拉伸振动.比较KAP和ATP,KAP在3 287 cm-1和1 034 cm-1处的峰减弱,在591 cm-1处的峰消失,这表明,与角蛋白相比,酰胺I和酰胺II带的特征峰从1 662 cm-1和1 456 cm-1蓝移到1 672 cm-1和1 538 cm-1.这可能是由于角蛋白和AA之间的羰基峰重叠所致,这表明AA已接枝到角蛋白上[14].此外,在1 451 cm-1处的谱带(C-N的吸收峰)表明成功制备了KAP.
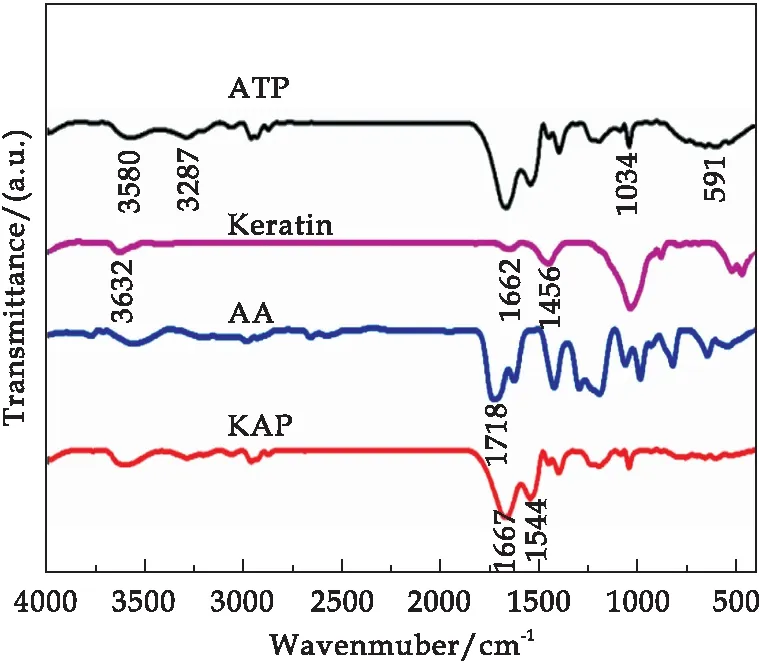
图2 不同样品的FT-IR红外光谱图
2.2.2 XRD结果分析
图3表明,在ATP的图谱中观察到20.4°,26.1°,30.3°和34.0°处的特征峰.角蛋白的谱图在20.3°处出现一个弱而宽的峰,表明其为无定形性质.反应后ATP的特征峰消失,说明ATP的有序结构在与单体反应中被破坏,ATP在KAP的三维网络中均匀分散和剥落[15].
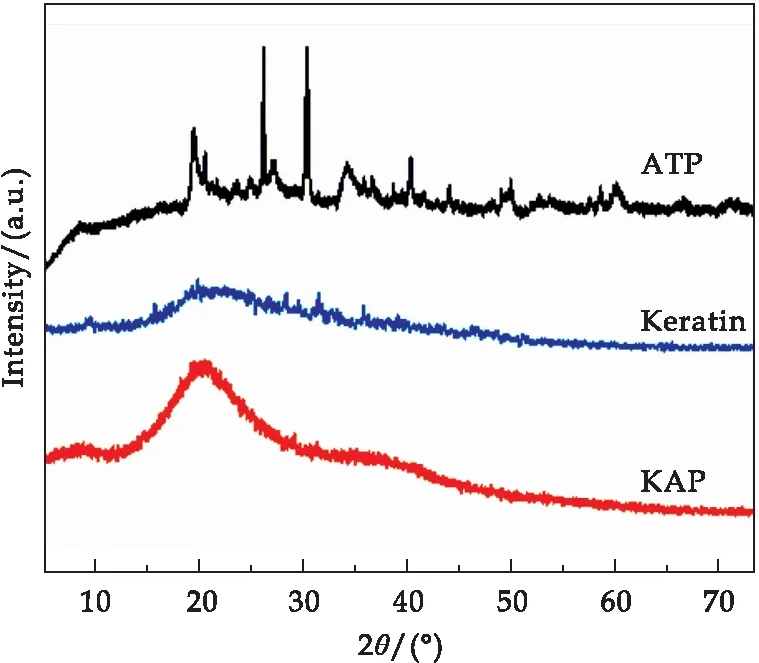
图3 不同样品的XRD图
2.2.3 TG-DTG结果分析
图4表明角蛋白发生了两个降解阶段(图4(a)),第一阶段是从30 ℃到193 ℃,由于水的气化作用,第二阶段是从193 ℃到600 ℃角蛋白骨架分解.KAP分解过程分为以下三个阶段:水分流失,角蛋白和聚合物网络结构的分解以及残留主链聚合物的进一步分解.从角蛋白和KAP的DTG曲线(图4(b))看出,KAP的最高分解温度为379 ℃,超过了角蛋白298 ℃.这种差异可归因于AA与角蛋白发生了接枝反应,分子链之间结合力增强,形成了高密度网络结构,从而提高了KAP的热稳定性[16].
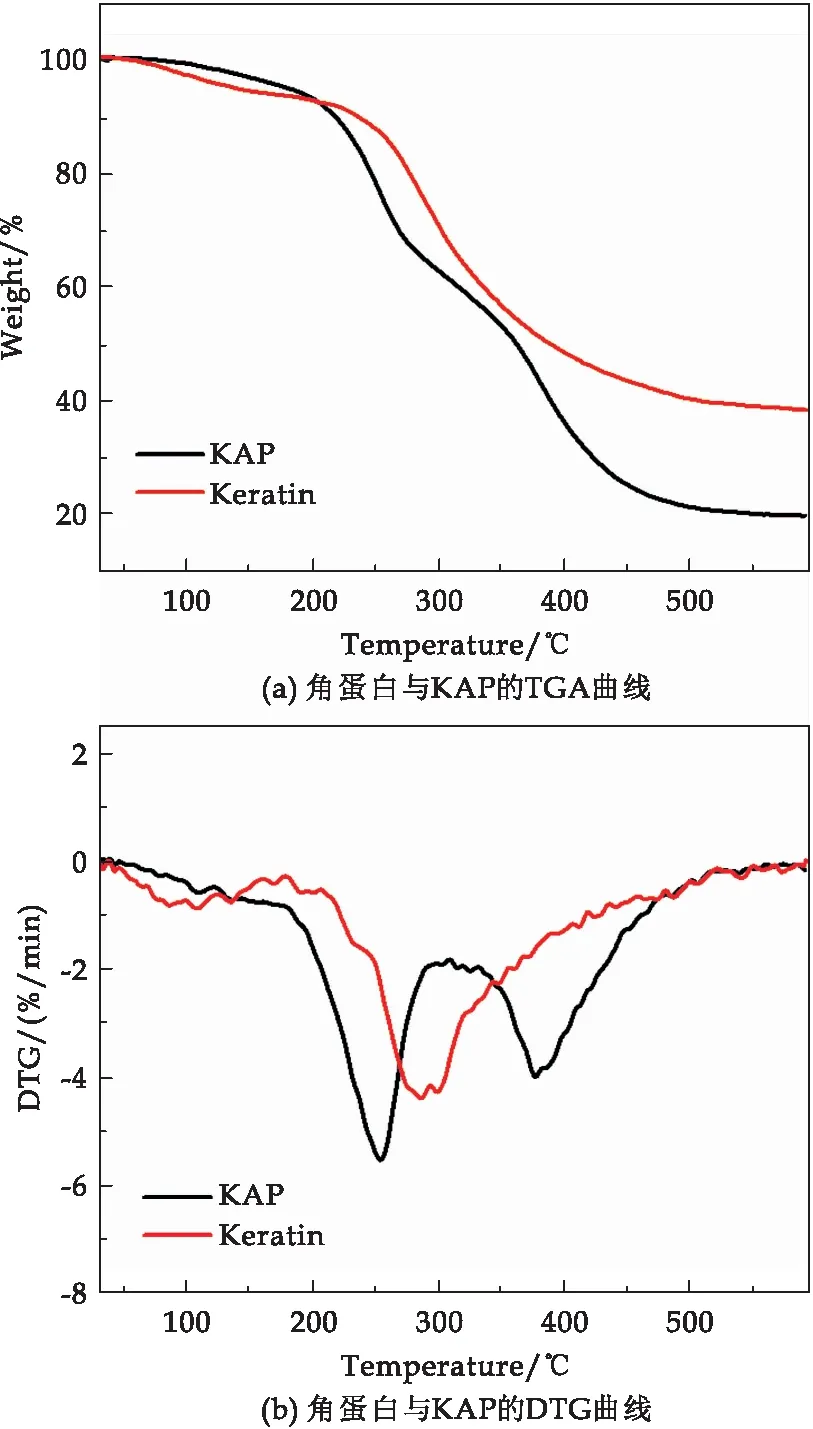
图4 角蛋白和KAP的TG-DTG曲线
2.2.4 吸水冷冻干燥后的KAP形貌
由图5看出,KAP吸水膨胀后再冷冻干燥,其表面呈现多孔状结构,这种结构特性使其具有较高的比表面积.这种高比表面积可以提高吸水性和保水性能.

图5 KAP吸水冷冻干燥后的SEM形貌图
2.3 KAP在不同温度下的吸水率
在5 ℃、15 ℃、25 ℃、35 ℃和45 ℃下测试了KAP的吸水率(图6),分别代表了不同季节的土壤温度.KAP的吸水率随温度升高而增加.因为随着温度的升高,聚合物链的热运动加快,KAP内部的三维网络结构被充分扩展,然后分子扩散被加速,导致吸水率增加[16].当温度为5 ℃时,KAP的吸水率达到218.8 g/g.当温度以每10 ℃升高时,在15 ℃、25 ℃和35 ℃的温度下,KAP的吸水率分别为352.9 g/g,609.3 g/g和712.2 g/g.当温度达到45 ℃时,KAP的吸水率上升到1 201.5 g/g.这些结果表明,KAP在寒冷和炎热季节均具有良好的吸水性能.
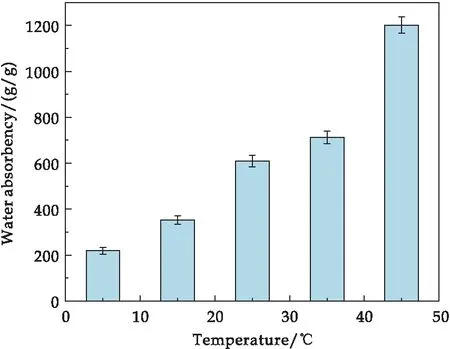
图6 不同温度对KAP吸水率的影响
2.4 土壤溶液pH值对KAP吸水率的影响
由于不合理使用肥料,大面积土地被污染,土壤在一定程度上呈酸性或碱性.在pH为2到11的土壤模拟溶液中检测KAP的吸水率,如图7所示.pH值从2增加到8时,KAP吸水率增加,在pH为8时达到最大吸水率.这可能归因于在低pH下,—COO-质子化和—COOH基团之间的氢键结合,从而使吸水率降低.随着pH增加,—COOH离子化形成—COO-,—COOH基团之间的氢键断裂,吸水率增加.然而,值得注意的是,当pH>8时,KAP的吸水率下降,这可能归因于KAP与土壤溶液中的离子在高pH值下发生中和作用,从而导致分子间的静电排斥力降低,吸水率降低[17].
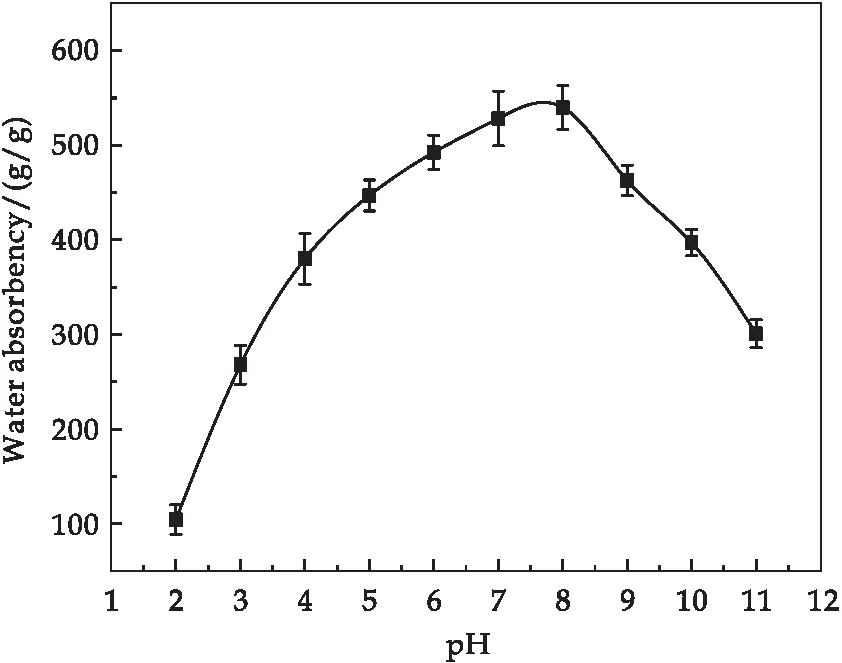
图7 土壤溶液pH值对KAP吸水率的影响
2.5 KAP对土壤pH值的影响
土壤pH值不仅影响土壤的理化性质,而且在植物生长中起关键作用.据报道,当pH值在5.5至7.0之间时,土壤微生物量和微生物活性趋于稳定.此外,当土壤的pH值从5.5升高至7.0时,土壤中的养分最容易被植物根吸收和利用[18].
从图8可以看出,用KAP处理后,不同pH值的土壤模拟溶液被调节为弱酸性或接近中性.这是因为KAP的主要成分是角蛋白,其中包含许多—COO-和—COOH基团.—COOH基团可以在碱性条件下与土壤溶液中的OH-反应,而—COO-基团可以在酸性条件下与H+反应.这些结果表明,KAP可以作为土壤酸碱调节剂,调节土壤的pH值,修复土壤的酸碱度,从而改善土壤环境.

图8 KAP对土壤pH值的影响
2.6 KAP的降解性能
通过土埋实验,以样品的重量损失来评估样品的降解性.从KAP的降解曲线(图9)看出,40天后,KAP的降解率为23.54%,这主要是由于角蛋白分子骨架被土壤中的微生物和酶分解引起的,说明KAP具有可降解性.
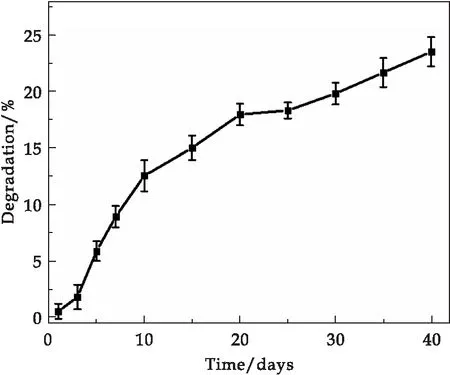
图9 KAP的降解曲线
2.7 KAP的保水性能
图10为KAP在55 ℃恒温箱中的保水率变化特性曲线.可以看出,前350 min内保水剂保水率的下降较快,保水率降到接近30%;350~500 min 保水剂保水率从30%~20%下降变缓,500 min后保水率下降很慢20%~18%,之后基本不变.综合来看,KAP保水剂在55 ℃温度下持续保水时间超过12 h.
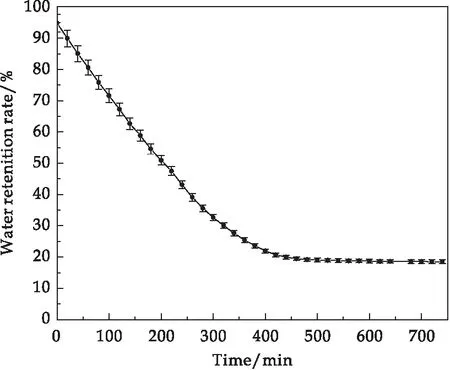
图10 KAP的保水特性曲线
3 结论
利用制革废弃牛毛提取角蛋白采用溶液聚合法进行接枝改性,制备出微粒表面多孔结构的角蛋白基吸水性保水剂(KAP),当温度从5 ℃~45 ℃变化时,KAP的吸水率从218.8 g/g,达到1 201.5 g/g.并且在55 ℃温度下可以持续保水超过12 h,具有较好的吸水保水性;KAP可调节土壤溶液的pH为弱酸性或接近中性;可以作为土壤pH调节剂,修复土壤的酸碱度,从而改善土壤环境.土埋40天后KAP的降解率为23.54%.具有可降解性.
以废弃牛毛为原料制备的土壤保水剂,不但缓解制革废弃物对环境的生态压力,也是实现废弃物资源化高效利用的一种新方法.
