超声引导下真空辅助切除手术对乳腺导管内乳头状瘤的诊断和治疗价值
2022-09-22周婕左艳玲王倩姜明吴丹丹李洪胜
周婕,左艳玲,王倩,姜明,吴丹丹,李洪胜
随着筛查技术和影像学诊断技术的发展,越来越多的乳腺乳头状瘤在体检中被发现。乳头状瘤在乳腺活检中很常见,在过去的十年中发病率稳步上升。乳头状病变包括良性乳头状瘤、不典型增生和乳头状癌。因此,判断病变的良恶性是很重要的。空芯针活检(core needle biopsy,CNB)已广泛应用于乳腺疾病的诊断。一些研究表明,空芯针活检诊断的无不典型增生的导管内乳头状瘤(intraductal papilloma,IDP)癌变率低,而存在不典型增生的乳头状瘤发展为恶性的风险增加[1]。与开放手术活检相比,CNB 检查更容易被患者接受。然而,由于CNB 取材的病变部分很小,有时病理医生很难区分良恶性[2]。此外,良性增生和不典型增生(atypical hyperplasia,AHP)在组织学上的区别可能是微妙的,而CNB 取材的乳头状病变的诊断通常对病理医生来说具有挑战性。因此,足够数量的标本是正确诊断的必要条件。
真空辅助针芯活检(vacuum-assisted core needle biopsy,VACB)作为一种微创诊断方法,与传统的空芯针活检相比,可以从一次穿刺中提供足够的样本[3]。VACB 在很大程度上消除了CNB 的缺陷,用于诊断乳腺局灶性病变,对乳腺肿块的诊断准确率为98%~100%[3]。VACB 不仅是一种临床诊断方法,在某些情况下,特别是对较小的病变,也是一种治疗方法,被称为真空辅助切除法(vacuumassisted excision,VAE)。据报道,92%直径小于15 mm 的乳腺良性病变可以用VAE 完全切除[4]。此外,VAE 可用于空芯针穿刺活检无异型性的良性导管内乳头状瘤的进一步诊断[5]。鉴于VAE的这些优势以及在处理乳腺乳头状病变时的困境,本研究评估了超声引导下的VAE 在未进行空芯针穿刺活检的乳腺乳头状病变诊断和治疗中的价值。
1 资料和方法
1.1 研究对象
回顾性分析2018年2月至2021年2月期间,在广州医科大学附属肿瘤医院乳腺外科应用VAE诊断的89 例乳头状病变患者的资料。所有乳腺病变在超声图像或乳房X 线图像上归类为BIRADS 2~4a,均使用VAE 完全切除。所有参与研究的女性都接受了超声检查,40 岁以上的女性还接受了乳房钼靶检查。排除了5 例在VAE 上诊断为恶性乳头状病变的患者,并排除了随访中未做术后乳房影像的患者。最后,33 例完成VAE 手术、且定期返院进行彩超影像学检查导管内乳头状瘤患者被纳入本研究。33 例患者中,8 例有双侧病变。所有的VAE 手术均使用了8G 真空辅助活检针(麦默通微创旋切系统SCM23 型,美国强生公司),超声引导使用GE 公司的LOGIQ P9 型号彩超检查仪器12 mHz 高频线性探头(图1)。
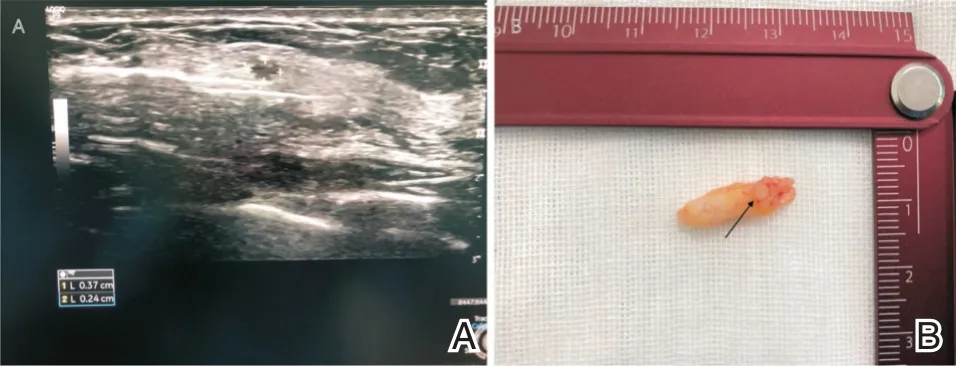
图1 乳腺导管内乳头状瘤的VAE 操作过程
1.2 主要临床表现
患者平均年龄47.9 岁(25~69 岁)。33 例患者中,19 例无症状(19/33,57.6%),仅影像学检查异常,另外10 例表现为乳头溢液,3 例可触及肿块,仅有1 例患者就诊主诉为乳房疼痛。所有患者超声均表现为结节,活检病灶大小为2.4~20 mm(平均9 mm)。双侧乳腺导管内乳头状瘤和单侧乳腺多局灶性乳头状瘤不常见。BI-RADS 4a 是活检前图像中最常见的类别(20/33,60.6%),入组病人的临床及病理特征详见表1。

表1 33 例乳头状瘤病人的临床及病理特征(病灶数量n=41)
1.3 病理诊断及随访
由两位在乳腺病变方面具有广泛专业知识的病理学家回顾了所有病例。良性导管内乳头状瘤包括良性增生性病变,如常见的导管增生或腺病、纤维囊性变和柱状细胞的变化。导管内乳头状瘤伴不典型增生包括小叶上皮内瘤变和导管不典型增生。术后3月、6月临床随访及超声检查,每年进行一次超声及钼靶(40 岁以上患者)检查。随访时间14~50 个月,平均25.7 个月。
1.4 统计分析
使用SPSS 21.0 软件(IBM 公司,阿蒙克,美国)进行统计分析。用t检验比较导管内乳头状瘤病变与导管内乳头状瘤伴不典型增生病变的平均直径。采用卡方检验比较有乳头溢液与无乳头溢液的乳腺导管内瘤患者,其超声识别效果。P值<0.05 为差异具有统计学意义。
2 结 果
33 例完成随访入组研究的患者中,有8 例患者被诊断为双侧乳腺导管内乳头状瘤,共计41 个导管内乳头状瘤病灶,其中病理诊断35 例为导管内乳头状瘤,6 例为导管内乳头状瘤伴不典型增生。导管内乳头状瘤伴不典型增生病灶的平均直径明显大于导管内乳头状瘤(导管内乳头状瘤伴不典型增生组患者平均病变直径11.3 mm,导管内乳头状瘤组患者平均病变直径8.6 mm,表2)。

表2 导管内乳头状瘤与导管内乳头状瘤伴不典型增生病变直径比较
除了病灶直径外,导管内乳头状瘤伴不典型增生组与导管内乳头状瘤组相比无特殊特征。对于导管内乳头瘤的超声识别率,乳头溢液患者高于无乳头溢液患者(表3)。

表3 41 例VAE 中的导管内乳头状瘤超声识别与乳头是否溢液
定期随访的33 名VAE 术后乳腺导管内乳头状瘤患者中,有2 名(2/33,6.06%)在随访期间出现原发部位(4~10 mm)低回声病变,2 名患者再次接受VAE。组织病理学诊断分别为导管内乳头状瘤和腺病,2 例患者(2/33,6.06%)有直径小于5 mm的新结节,但并非在原发部位,超声分类为BIRADS 2 级和BIRADS 3 级。这2 名患者未再接受VAE,随访中未发现病变未发生变化。在3 例多病灶患者中,直径小于5 mm 的结节在初次VAE 手术中未予切除。其中2 例患者随访期复查彩超,提示结节消失,另1 例患者随访期复查彩超,提示结节未发生变化(表4)。

表4 33 例乳头状瘤病人的随访结果[n(%)]
3 讨 论
乳头状病变包括良性乳头状瘤、不典型乳头状瘤和乳头状癌。导管内乳头状瘤通常表现为乳头溢液或可触及肿块,手术是常见的处理方法。然而,越来越多的乳头状瘤偶尔在临床前阶段通过影像筛查发现,通常无临床症状。在本研究中,我们发现57.6%的乳头状瘤患者就诊时无症状,60.6%的患者在超声图像上被归类为BI-RADS 4a。仅有26.8%的导管内病变在超声检查中被发现。然而,乳头溢液的患者在超声检查中更容易被发现(7/10,70%),这可能是因为乳头状瘤位于充满液体的扩张导管中更加易于分辨。在我们的研究中,乳头状瘤的平均大小为9 mm(2.4~20 mm),因此很难区分小的、不可触及的乳头状病变。对如此小的病灶进行诊断有一定困难,超声引导下的CNB 收集的组织标本量不足,所以,CNB 很难区分良恶性乳头状病变[6]。有研究建议,CNB 诊断的乳头状病变,尤其是不典型性病变,应该进一步接受开放性手术以获得准确的诊断,排除恶性的可能[7,8]。因为没有伴随不典型病变的导管内乳头状瘤的恶化率较低[9,10],所以,通过CNB 诊断的良性导管内乳头状瘤是否需要扩大切除仍然存在争议。有研究表明,开放性切除术后的病理结果恶性诊断率与CNB 活检行病变取样的典型性及充分性相关[11]。在我们的研究中,一例经VAE初步诊断为导管内乳头状瘤伴硬化性腺病后,术后免疫组化检测后,病理诊断为导管内乳头状癌。这例患者,同时患有对侧浸润性导管癌,因此,应用VAE 治疗时应特别注意乳腺癌高危患者。2016年,Tatarian 教授的研究结果显示,经CNB 最初诊断为良性乳头状瘤的患者中,21.3%的患者在手术切除后出现了异型性导管内乳头状瘤,大多数不典型病变来自乳头状瘤周围的组织[12]。我们患者低估率低的原因可能是使用VAE(8G 活检针)可以获得足够的样本(每条标本量长度2 cm,宽度3 mm)。Cassano 教授的研究结果也认为,对于经VAE 诊断为良性病变的患者,无需进一步开放切除验证。他们发现,经VAE 诊断为导管内乳头状瘤的患者,经过6~12 个月的影像学随访,没有复发或进展。我们的研究对行VAE 的患者平均随访了25.7 个月,在影像检查随访过程中,未发现异常,这意味着VAE 是诊断和治疗乳腺乳头状病变的一种适用方法。然而,在本研究中,我们发现导管内乳头状瘤伴不典型增生患者的平均病变直径(11.3 mm)大于导管内乳头状瘤患者(8.6 mm),但是,不典型增生与病变大小并没有明确的相关性。60.6%的乳头状病变在图像上可被分类为BI-RADS-4a,而C2、C3 类仅占全部患者的39.4%(13 例)。因此,当超声图像将乳腺病变归类为4a时,必须注意乳头状病变的可能。
Kibil 教授的研究认为,在95%以上的患者中,超声引导的VAE 可以完全切除小于15 mm 的乳头状瘤,因此具有治疗价值,避免了开放手术[5]。在本研究的病例中,病变的最大直径为20 mm,我们在超声引导下通过VAE 将病灶完全切除。在随访期间,12.1%(4/33)的患者在超声发现低回声病变,其中,2 名患者再次接受VAE 组织病理诊断为导管内乳头状瘤和腺病。另外2 例未行治疗,定期随访,影像未见新的可疑病变。由于只有2 例患者再次进行了VAE 手术,所以无法确定复发率。在这些患者中,因为病灶的大小大于针槽,并且超声无法检测到微小的残留病灶,我们可能无法完全切除所有的病灶,在本研究中,3 例病例首次超声检查发现多灶性病灶,直径小于5 mm 的病灶均未切除,平均随访31 个月后,这3 例患者中2 例未再发现新的病灶,1例患者病灶未见增大。
2018年,Donaldson 等[13]发现经CNB 活检诊断为乳腺不典型增生的患者中,7年累计乳腺癌发病率仅为10%,因此他们认为密切的影像学随访更适用于这些患者。并且,乳腺乳头状癌仅占所有乳腺恶性肿瘤的1%~2%[14],发病率低。因此,我们认为对于直径小于5 mm 的病灶,特别是对于多局灶性乳头状瘤,不一定需要再次手术扩大切除。由于本组研究的随访时间平均仅25.7 个月,所以,真空辅助切除手术后乳头状瘤复发率值得进一步研究。
由于真空辅助切除手术能够获取足够的组织样本进行病理检查,经VAE 诊断的导管内乳头状瘤不仅假阴性率低,而且复发率也低。因此,我们的研究认为,对于直径小于20 mm 的乳腺导管内乳头状瘤,包括存在不典型增生的乳头状瘤,经真空辅助切除手术后,不需要进行扩大切除,影像学随访即可。
