香兰素热稳定性及热分解过程机理研究
2022-09-19靳苗苗滕富全刘吉波章平毅毛海舫
靳苗苗,滕富全,刘吉波,章平毅,毛海舫
(上海应用技术大学 化学与环境工程学院, 上海 201418)
香兰素(vanillin),即3-甲氧基-4-羟基苯甲醛,又名香草醛,外观为白色至微黄色针状或粉末状结晶,其结构如图1所示。香兰素具有浓郁的奶香味,起增香和定香作用,广泛应用于食品、化妆品及烟草等行业,在抗氧化、抗微生物、抗癌、抗诱变、降血脂及抗血清活性等方面也具有潜在的应用前景[1-3]。
图1 香兰素分子结构Fig. 1 Molecular structure of vanillin
香兰素是目前全球产量最大的合成香料之一,生产方法主要包括天然提取、化学合成和生物制备等。受原材料的产量和价格限制,天然提取法难以满足不断增加的生产需求。通过生物转化法和化学合成法(包括光/电催化方法等)将丁香酚、阿魏酸、愈创木酚、木质素、对羟基苯甲醛、香兰醇以及对甲酚等转化为香兰素,是香兰素的主要来源[4-5]。目前国内外大多数企业主要采用的是愈创木酚-乙醛酸法合成香兰素[6-7],工艺路线为愈创木酚和乙醛酸在碱性条件下缩合生成3-甲氧基-4-羟基苯乙醇酸,其在碱性条件下被铜离子氧化成3-甲氧基-4羟基苯乙醛酸,然后在酸性条件下脱羧得到粗品,再通过精制提纯工艺得到精制香兰素。反应过程如图2所示。此法生产香兰素工艺简单,收率高,三废少,易治理。
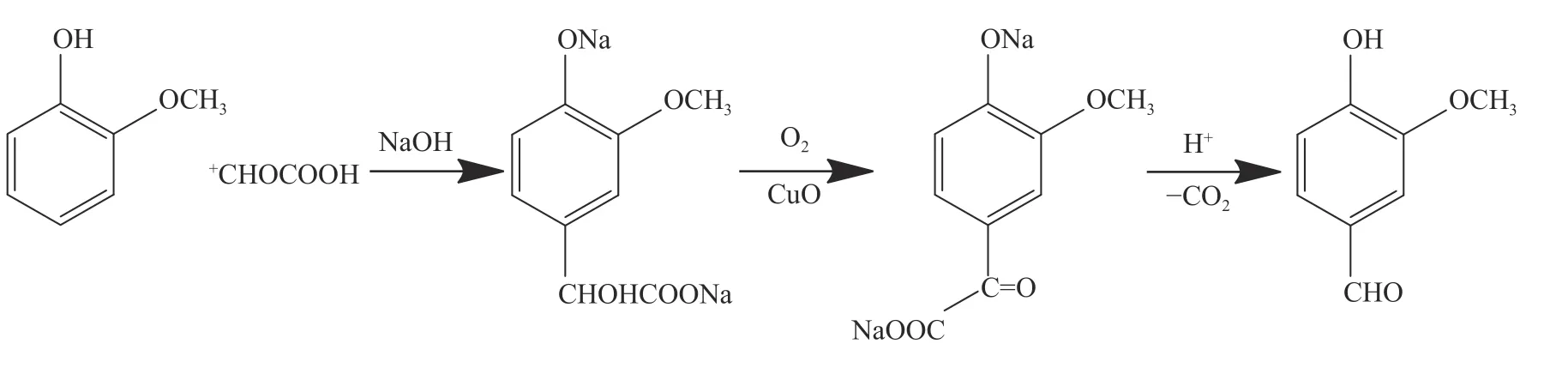
图2 愈创木酚-乙醛酸法合成香兰素Fig. 2 Synthetic route of vanillin by guaiacol - glyoxylic acid method
在香兰素的生产过程中,精制提纯工艺一般相当复杂。工业上常用的方法是对反应液进行萃取,然后蒸发萃取物脱去溶剂后得到粗品。香兰素粗品通过减压精馏,脱去轻、重杂质,再进行溶剂重结晶,可得到纯度大于99%的产品。但精馏过程的操作温度高达130~150 ℃。香兰素属热敏性物质,因其分子中包含活性官能团(如甲氧基、羟基和甲酰基),其长时间受热易导致聚合焦化等副反应的发生。此类副反应影响产品质量及收率,导致香兰素的精馏收率一般不超过90%。目前关于香兰素的热分解研究集中在高温下的热解及裂解机理研究[8-11],但是关于香兰素在较低温度下长时间加热后的热分解过程还未见报道。本文重点研究香兰素在130~150 ℃长时间加热后的热分解产物、热分解机理及动力学。
1 实验部分
1.1 仪器与试剂
1.1.1 试剂
香兰素(3-甲氧基-4-羟基苯甲醛,RG 99.9%,上海泰坦科技股份有限公司);香兰酸(3-甲氧基-4-羟基苯甲酸,HPLC≥98%,上海泰坦科技股份有限公司);乙腈(99.9%,色谱纯,FisherScientific),磷酸(85%水溶液,超纯,上海泰坦科技股份有限公司);实验室用水均为去离子水。
1.1.2 仪器
集热式恒温加热磁力搅拌器(DF-101S,上海豫康科教仪器有限公司);电子天平(AUY 220,精度为0.000 1 g,岛津公司);有机相过滤膜(0.22 μm,上海泰坦科技股份有限公司);高效液相色谱仪(high performance liquid chromatography,UltiMate 3000,赛默飞世尔科技(中国)有限公司);X-射线粉末衍射仪(X-ray Powder diffractometer,D/max 2200PC,日本理学电机株式会社);综合热分析仪(thermogravimeter-differential scanning calorimeter,梅特勒25-800/耐驰25-1300);气相色谱-质谱联用仪(gas chromatography-mass spectrometer,GC7890-5975MS,美国安捷伦科技公司)。
1.2 热稳定性实验
香兰素的热稳定性实验在250 mL三口圆底烧瓶中进行。在三口烧瓶中加入100 g香兰素,将烧瓶放入恒温加热磁力搅拌器中,采用磁力搅拌混合。安装回流装置及温度计(控温精度0.1 ℃)。采用油浴加热,待温度计达到实验预设温度(考察温度为130、140或150 ℃)后开始计时,每1 h取样1次。取样后的样品迅速放入真空干燥器内,待冷却至室温后用研钵充分研磨,留样待测试。单次实验总时长为24 h。
1.3 高效液相色谱实验
高效液相色谱(high performance liquid chromatography,HPLC)测试条件:色谱柱为Diamonsil C18反相色谱柱(250 mm×4.6 mm,5 μm);柱温为25 ℃;进样量为10 μL;流速为1.0 mL/min;紫外检测波长为280 nm;流动相A为乙腈;流动相B为0.1%磷酸水溶液;流动相梯度为配置的混合溶液(30%乙腈+70%水)。
标准溶液的配置:通过前期预实验已知香兰素在130~150 ℃加热24 h后主要物质仍为香兰素,且含量在90%以上,因此香兰素标曲区间设置较窄。称取一定量香兰素标准物质,使用上述配置的混合溶液定容,分别配置0.13、0.14、0.15、0.16、0.17 mg/mL浓度的香兰素标准溶液。
样品前处理:称取充分研磨后的香兰素热解样品0.20 g(精确至0.1 mg),转移至100 mL容量瓶中,用混合溶液定容至刻度,再用移液管移取2 mL溶液至25 mL容量瓶中,用混合溶液定容至刻度。取10 μL进样,进行液相色谱分析。
1.4 X-射线粉末衍射实验
对香兰素热分解24 h后样品的晶型进行X-射线粉末衍射 (X-ray powder diffraction,XRD)表征。测试管电压40 kV,管电流30 mA,Cu靶靶源,λ=0.154 06 nm,扫描范围5°~50°,扫描速度2°/min。
1.5 综合热分析实验
对香兰素加热24 h后产品进行综合热分析(thermogravimetery and differential scanning calorimetery,TG-DSC)检测,设置程序控温30~300 ℃,升温速率5 ℃/min,N2吹扫。
1.6 气相色谱-质谱联用实验
气相色谱-质谱联用(gas chromatographymass spectrometer,GC-MS)的气相色谱条件:色谱柱型号为INNOWAX(60 m×0.25 mm×0.25 μm);升温程序为柱初始温度60 ℃,以4 ℃/min的速率升至300 ℃,保持10 min;载气流速为2 mL/min;进样量为1 μL,分流进样,分流比100∶1;流量为1 mL/min;载气为高纯氦气(纯度为 99.999%)。
质谱条件:使用电子轰击离子源(electron impact ion source,EI);离子源温度230 ℃;质谱接口温度为250 ℃;电子能量为70 eV;溶剂延迟时间为4 min;质谱扫描模式为全扫描(SCAN);全扫描范围(m/z)为 30~300。
2 结果与讨论
2.1 香兰素热分解过程
香兰素含量随加热温度和加热时间的变化如图3所示。从图中可以看出,随着加热时间的延长,香兰素热分解比例增加,香兰素热分解比例随时间的变化大致呈线性关系。且随着加热温度的升高,香兰素热分解比例也相应增加,温度升高会加速香兰素的热分解。在150 ℃加热24 h后,香兰素热分解比例达到4.96%。
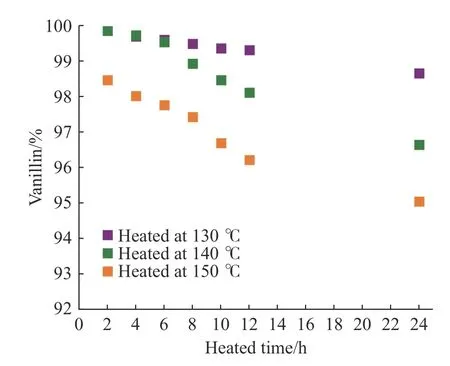
图3 香兰素在不同温度下热分解情况Fig. 3 Thermal decomposition data of vanillin heated at different temperatures
为了分析香兰素热分解主要产物,以香兰素、香兰酸和香兰醇标准品在150 ℃加热24 h后的样品作为试样,在相同测试条件下进行HPLC测试(见图4)。如图4(a)所示,标准品出峰顺序和时间依次为香兰醇(3.737 min)、香兰酸(4.593 min)、香兰素(6.607 min)。上述色谱分析条件对香兰素和香兰酸分离效果较好。如图4(b)所示,香兰素在150 ℃下加热24 h后,在香兰酸响应位置(4.593 min)有明显出峰,说明香兰素在150 ℃下加热24 h后可能有少量被氧化成香兰酸,但是HPLC出峰面积比例很小,4.593 min位置的峰面积只占总峰面积的4%左右,说明该温度下长时间加热的香兰素热分解程度并不高。图4(b)中,香兰素在150 ℃加热24 h后样品中未检测到香兰醇(或低于检出限)。
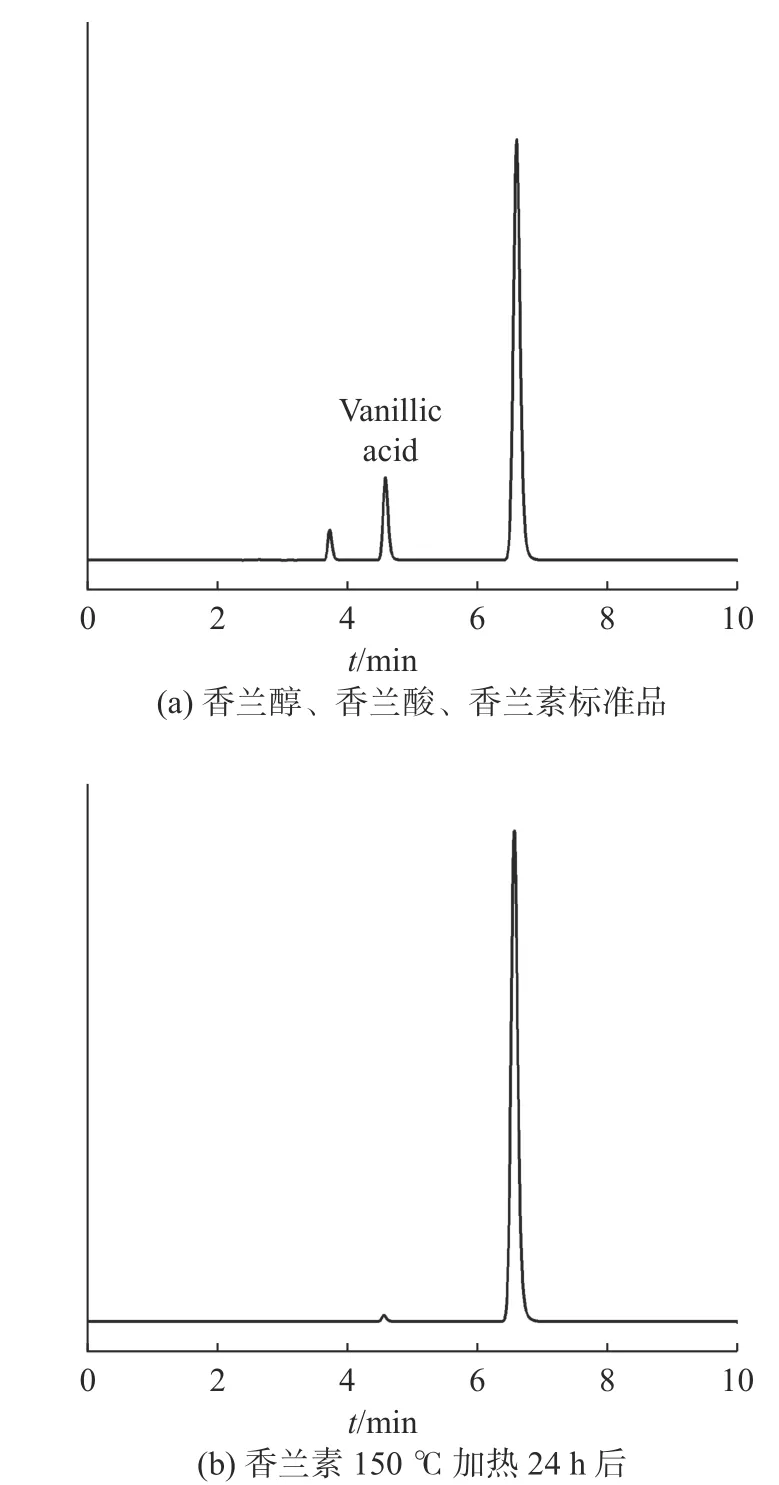
图4 香兰素高效液相色谱结果分析Fig. 4 HPLC analysis of vanillin
2.2 XRD结果分析
对香兰素产品及纯品进行XRD测试。测试结果如图5所示,谱线自上至下依次为130 ℃、140 ℃和150 ℃加热24 h后的香兰素产品、香兰素纯品以及香兰酸纯品。由图可见,130 ℃、140 ℃和150 ℃加热24 h后的香兰素产品与香兰素纯品特征峰基本一致,在2θ为13.0°、17.1°、25.8°、26.8°处均有明显特征峰。XRD数据证实香兰素原料与不同温度下加热后的样品均为同一种晶型。香兰素纯品在36.7°和39.8°位置有较明显的特征峰,而这2处在加热后的产品中则无明显的特征峰。分析原因,可能是由于热解过程存在加热→融化→重结晶→研磨等过程,导致香兰素结晶度变差,部分特征峰变得不明显。通过液相色谱分析,我们认为香兰素热解产品中应有少量香兰酸生成。但对比不同温度下香兰素热解产品与香兰酸纯品XRD谱图可以发现,热分解产品在香兰酸特征峰位置如9.2°、10.1°和16.4°等位置无明显的出峰。因此,不能通过XRD验证香兰素热分解产物中是否含有香兰酸。
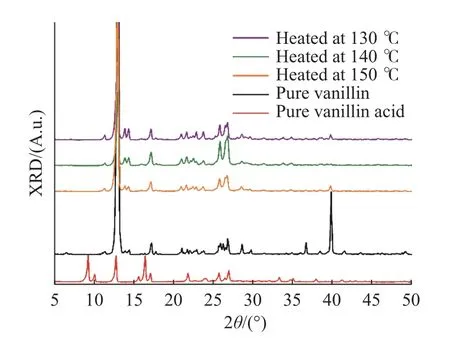
图5 不同温度下香兰素热解产物及纯品XRD图谱Fig. 5 XRD patterns of vanillin products heated at differenttemperatures
2.3 TG-DSC结果分析
香兰素在不同温度下加热24 h以及香兰素纯品的TG-DSC谱图见图6。纯品香兰素在T=88.6 ℃处存在一个吸热峰。随着香兰素样品加热温度的升高,其吸热峰峰值位置相对于纯品逐渐向低温方向移动,峰值位置分别为T=85.6 ℃(加热温度为130 ℃)、T=85.0 ℃(加热温度为140 ℃)和T=84.3 ℃(加热温度为150 ℃)。香兰素样品的吸热峰出峰温度降低,也证明了了香兰素在低温下长时间加热后出现了其他的杂质,使得熔点发生了变化。而且随着香兰素加热温度升高,其热解产物熔点依次降低,也可从侧面说明随着加热温度的升高,热解产物中杂质含量逐渐增加。
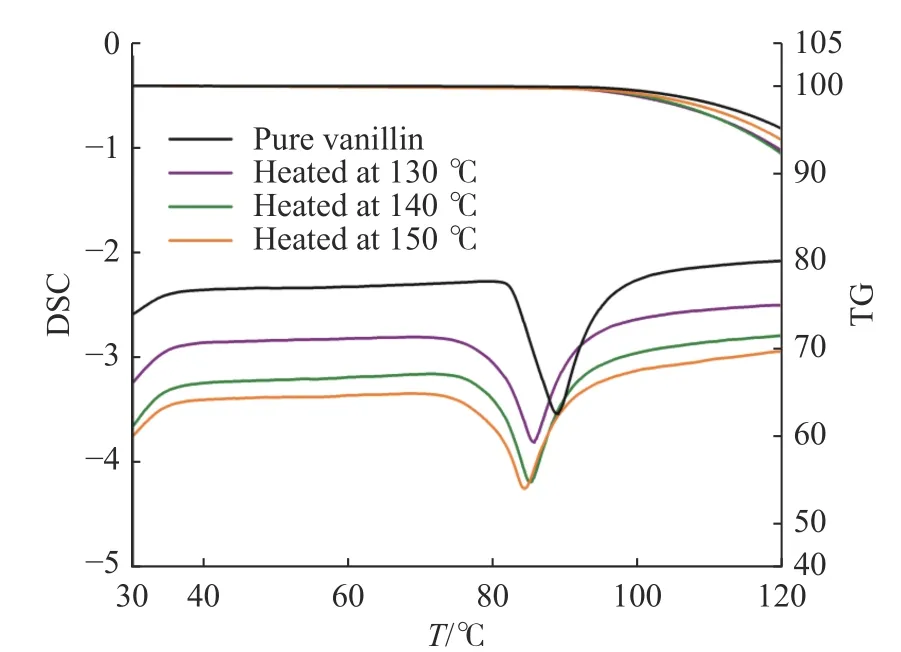
图6 在不同温度下加热24 h后的香兰素以及纯品香兰素的TG-DSC谱图Fig. 6 TG-DSC spectra of vanillin heated at different temperatures for 24 h and pure vanillin
2.4 GC-MS对分解产物的分析
对香兰素在150 ℃加热24 h的样品进行GCMS分析,探究其产物分布。如表1所示,香兰素样品在150 ℃下加热24 h后的主要氧化产物为香兰酸,占总峰面积的0.94%。在加热后的样品中,仍有峰面积比为98.90%的香兰素。样品中还有2-甲氧基对苯二酚和异香兰素等杂质。部分未知杂质尚需进一步进行定性表征。
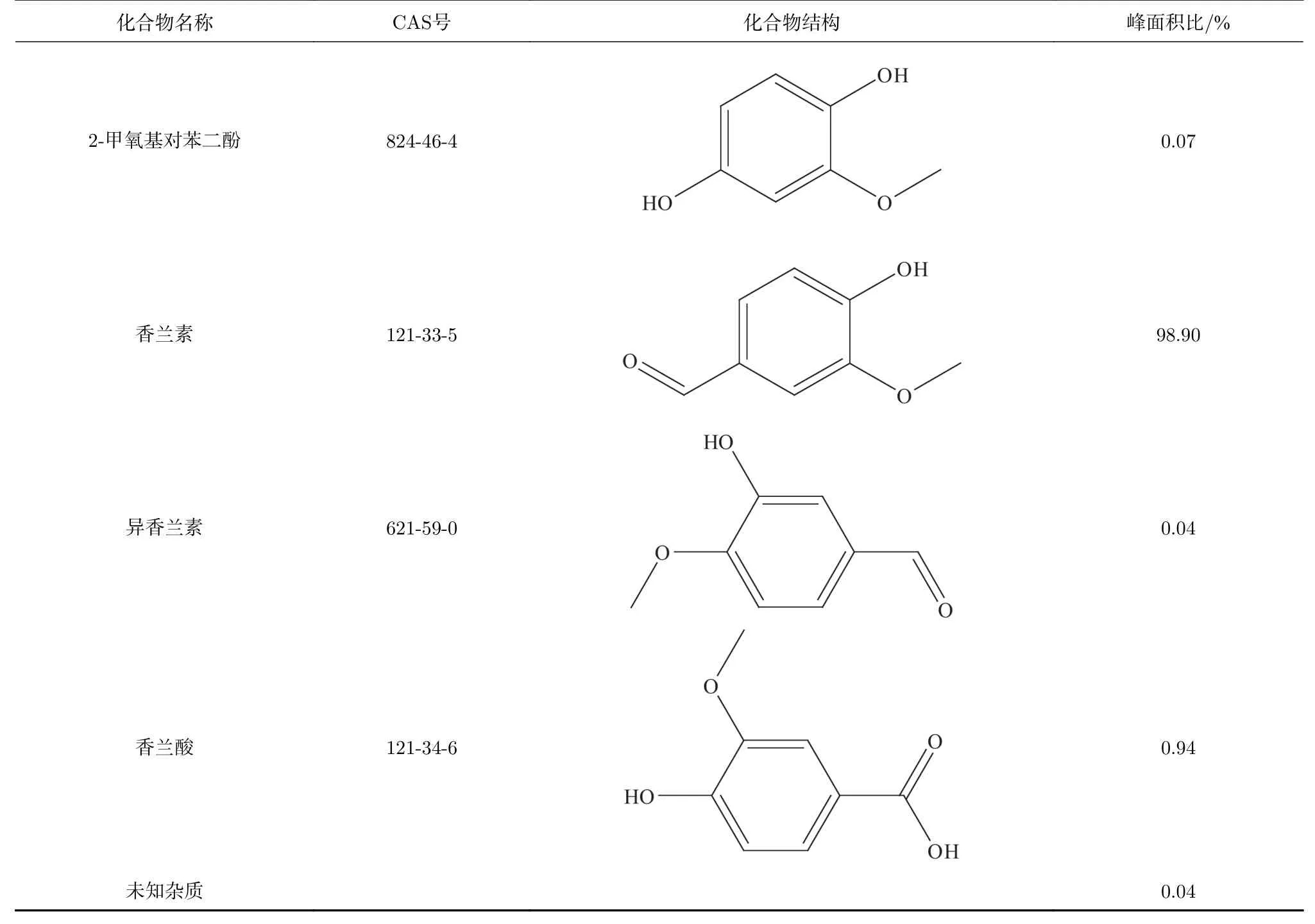
表1 香兰素150 ℃加热24 h后产物分析Tab. 1 Products analysis of vanillin heated at 150 ℃ for 24 h
2.5 香兰素热分解动力学
在加热条件下,空气中的氧气的氧化活性增强,产生活性氧。香兰素分子中含有酚羟基、醛基等活性官能团,在加热条件下可与体系中的活性氧发生反应,被氧化成醌、羟基等,从而裂解得到2-甲氧基苯酚、2-羟基苯甲醛和4-羟基苯甲醛等物质。2-甲氧基苯酚、2-羟基苯甲醛和4-羟基苯甲醛进一步裂解,可生成苯酚和苯二酚[8-11]。
最后,对不同温度下香兰素样品的热分解过程采用一级动力学方程分析,并对热分解数据进行拟合。如图7所示,随着加热时间的延长,香兰素热分解程度也随之增加,变化趋势呈现一定的线性关系。加热温度为130 ℃条件下香兰素的热解程度和趋势最低(一级动力学方程斜率为-5.585×10-4)。140 ℃条件下的曲线斜率与150 ℃的曲线斜率差别不大,但150 ℃的热分解趋势(一级动力学方程斜率为-0.001 64)仍高于140℃的热分解趋势(一级动力学方程斜率为-0.001 57)。随着加热温度的升高,香兰素热分解比例增加,温度升高会加速香兰素的热分解。
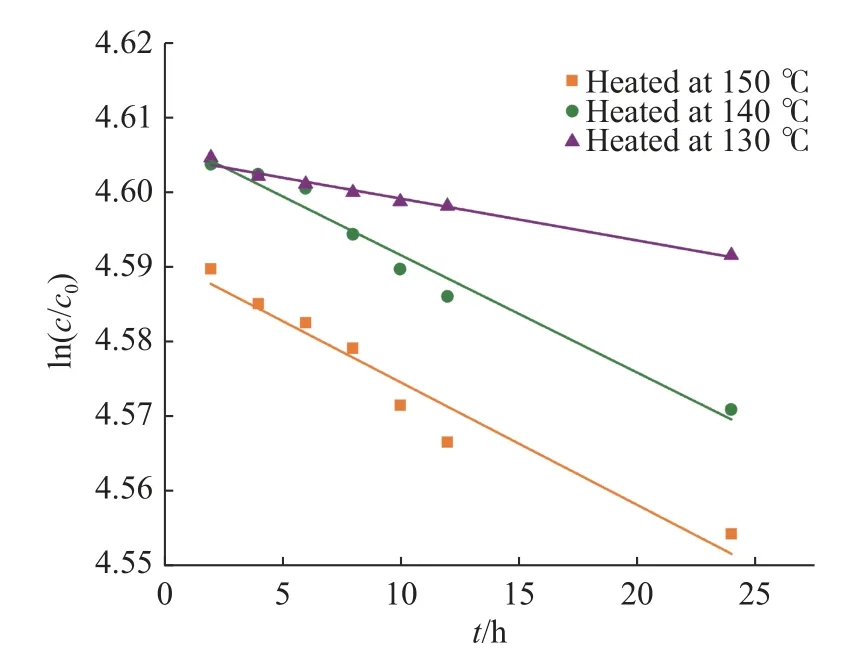
图7 香兰素在不同温度下的热解趋势Fig. 7 Pyrolysis trend of vanillin at different temperatures
3 结 语
本文研究了香兰素在较低温度下长时间加热后的热分解过程,采用HPLC、XRD、TG-DSC和GC-MS等方法,对加热温度为130~150 ℃,加热1~24 h条件下的香兰素热分解过程及产品进行表
征分析。结果表明,香兰素在不同温度下的产物与香兰素纯品晶型一致,在热分解过程中没有发生晶型的转变。随着热分解温度增加和热分解时间的延长,香兰素热分解比例增加。香兰素产品在150 ℃加热24 h后,质量降低至95.04%,在液相色谱中有明显的杂质峰,出峰位置与香兰酸纯品出峰位置一致,但是在XRD结果中并未检测到香兰酸的特征峰。通过TG-DSC发现,随着加热温度升高,香兰素产物中杂质含量增加。GC-MS结果分析表明,热分解后的产品其杂质主要是香兰酸、以及浓度相对较低的2-甲氧基对苯二酚和异香兰素等。由一级动力学函数曲线可知,130 ℃下的热分解程度最低,随着加热温度的升高,香兰素的热解趋势增大。
