妇科调经片成型工艺的优化及其稳定性研究
2022-09-19郭田甜关永霞刘震远毕艳艳陈意菲房兆营崔海霞
郭田甜,关永霞,张 微,刘震远,张 兰,韩 培,毕艳艳,陈意菲,房兆营,崔海霞
(1.鲁南厚普制药有限公司,山东 临沂 276000;2.中药制药共性技术国家重点实验室,山东 临沂 276000;3.鲁南贝特制药有限公司,山东 临沂 276000;4.临沂市兰山区市场监督管理局,山东 临沂 276000)
妇科调经片收载于中华人民共和国卫生部药品标准《中药成方制剂》[1],由当归、川芎、白芍等十味药材组成,具有养血、止痛、调经之功效,常用于月经不调、经期腹痛等临床症状,适用人群数量多且治疗效果显著,市场需求量较高[2-3]。
妇科调经片成型工艺过程是由多味药材提取浓缩的浸膏中加入当归、川芎、醋香附、麸炒白术等4味药材的生药粉,混匀后添加适量润湿剂制粒,最后加入适量辅料后压片即得[4-5]。但因妇科调经片为半浸膏片剂,制剂成型过程复杂,影响片剂制备工艺的因素较多,所以对其成型工艺的优化有利于提高药物生产产业化效率,改进产品质量[6]。近年来国内外对妇科调经片的研究报道主要集中在质量标准提升和方法改进方面,而对其成型工艺优化相关内容报道较少,市场对优质药品的需求迫在眉睫,因此优化妇科调经片的成型工艺显得尤为重要[7-9]。
本研究采用响应面分析法对妇科调经片制剂成型工艺优化,试验以素片的重量差异、脆碎度和崩解时限三项指标综合评分作为考察目标,探究了浸膏相对密度、润湿剂浓度、物料液固比以及助流剂用量4 个重要参数对妇科调经片品质的影响,并且对优选出的工艺条件下生产的成品进行了加速与长期稳定性对比研究,明确了妇科调经片最佳成型工艺生产条件,为妇科调经片的批量上市生产提供了一定科学理论依据。
1 材料与方法
1.1 仪器
BT-1001 型智能粉体特性测定仪(丹东百特仪器有限公司);CJY-300C 型片剂脆碎度测定仪LB-2D型崩解时限测定仪(上海黄海药检仪器有限公司);CH-20 型卧式混合机、YK-140 型摇摆式颗粒机(丹东市五龙背制药设备厂);ZPT-20 型旋转式压片机(辽宁天用于亿机械有限公司);HE83 型快速水分测定仪[梅特勒-托利多科技(中国)有限公司];ZSH-100B 型恒温恒湿箱(上海侦翔机电科技有限公司)。
1.2 试药
当归(批号:190311)、川芎(批号:190313)、醋香附(批号:190425)、麸炒白术(批号:190427)、白芍(批号:190410)、赤芍(批号:190405)、醋延胡索(批号:190402)、熟地黄(批号:190520)、大枣(批号:190518)、甘草(批号:190305)均来源于鲁南厚普制药有限公司,经鲁南厚普制药有限公司质检中心高级工程师范建伟鉴定为正品。药用辅料:羧甲基淀粉钠(批号:20181202)、硬脂酸镁(批号:20190122)均购于曲阜市天利药用辅料有限公司,淀粉(批号:20181109)购于山东聊城阿华制药股份有限公司,绿色胃溶型薄膜包衣预混剂(批号:190627)购于上海新菲尔生物制药工程技术有限公司;阿魏酸对照品(批号:190315-1,纯度:99.0%),芍药苷对照品(批号:190124-4,纯度:99.0%)均购于中国食品药品检定研究院;甲醇(色谱纯)购于安徽天地高纯溶剂有限公司;水为超纯水。
1.3 妇科调经片成型工艺
1.3.1 浸膏的制备 取“1.2”项下十味药材,其中麸炒白术、醋延胡索、当归、川芎粉碎成细粉过筛;其余醋香附等六味加水煎煮二次,第一次3 h,第二次2 h,滤过,合并滤液,浓缩至浸膏,备用[10]。
1.3.2 颗粒的制备 加入麸炒白术等细粉,将浸膏与填充剂淀粉混匀,以适量乙醇做润湿剂制软材,混匀,用14 目筛制湿颗粒,60℃以下干燥,16 目筛整粒,计算颗粒的合格率[10]。
1.3.3 片剂的制备 整粒后的颗粒加入崩解剂羧甲基淀粉钠、助流剂硬脂酸镁,压片,片重0.31 g,包薄膜衣[10]。
1.4 单因素试验设计
经预实验明确妇科调经片成型主要影响因素分别为浸膏相对密度、润湿剂浓度、物料液固比、助流剂用量4 项,试验结果初步给出了各指标参数范围,其中浸膏相对密度为1.10 ~ 1.30 g/mL,润湿剂浓度为70% ~ 90%,物料液固比20% ~ 40%,助流剂用量0.2% ~ 1.0%,由此设计单因素试验,见表1。单因素试验时固定其余参数恒定均取范围中值,依次将浸膏相对密度(A)、润湿剂浓度(B)、物料液固比(C)、助流剂用量(D)作为考察因素,分别选取5 个响应面水平来研究对压片成型综合评分的影响。

表1 单因素试验因素水平与编码Tab. 1 Level of test factors and codes
1.5 响应面试验设计
本试验以妇科调经片的重量差异、脆碎度、崩解时限三项指标综合评分作为片剂成型工艺评价标准,明确重量差异、脆碎度、崩解时限的权重分别为0.4、0.3、0.3。经预实验与《中国药典》要求给出评分梯度范围,具体见表2。

表2 片剂成型品质评价标准Tab. 2 Evaluation standard of tablet forming quality
根据响应面试验设计原理和单因素试验结果,筛选浸膏相对密度(A)、润湿剂浓度(B)、物料液固比(C)、助流剂用量(D)4 个影响因素,以综合评分作为响应值,各取三个水平进行响应面优化试验,试验因素与水平见表3。

表3 响应面试验因素水平与编码Tab. 3 Level of test factors and codes
1.6 稳定性考察
1.6.1 加 速 试 验 取 样 品( 批 号:190912、191017、191103)在加速条件下[温度:(40 ± 2)℃,湿度:(75 ± 5)%]放置6 个月,分别于0、1、2、3、4、5、6 个月取样检测,考察吸湿率、崩解时限、阿魏酸含量、芍药苷含量和微生物限度指标变化情况。
1.6.2 长 期 试 验 取 样 品( 批 号:190912、191017、191103)在常规条件下[温度:(25 ± 2)℃,湿度:(60 ±10)%]放置24 个月,分别于0、3、6、9、12、18、24 个月取样检测,考察吸湿率、崩解时限、阿魏酸含量、芍药苷含量和微生物限度指标变化情况。
1.7 指标测定
1.7.1 重量差异的测定 取20 片妇科调经片,精密称定后求平均片重,经精密称定得到每片的片重后,平均片重与每片的片重相比,超出重量差异限度±5%的不多于2 片,超出限度1 倍的不能出现[11]。
1.7.2 脆碎度的测定 取总重量小于等于6.5 g 的妇科调经片若干片,使用吹风机将片剂表面的粉末吹去,精密称重后置于脆碎度测定仪的圆筒中,转动100 次。取出后再吹去片剂表面的粉末,精密称重后,减失重量不大于1%,且不得检出龟裂、断裂及粉碎[12]。
1.7.3 崩解时限的测定 随机取样品12 片,均匀放置于吊篮玻璃孔内,加水适量,淹没过药片上部0.5 cm,盖上内盖,防止样品溢出,开启崩解仪测定崩解时限[13]。
1.7.4 吸湿率的测定 将适量氯化钠饱和溶液放于玻璃干燥器底部,将干燥器于25 ℃、相对湿度75%的环境中放置1 d,取样品12 片平铺于质量恒定的称量瓶内,开盖放在玻璃干燥器中定时称质量,按以下公式计算吸湿率[14]。
1.7.5 阿魏酸含量测定 (1) 色谱条件 Agilent ZORBAX Extend-C18柱(4.6 mm×250 mm,5 μm);流动相:乙腈-0.3%磷酸溶液(18.5 ∶81.5);柱温:50 ℃;流速:0.8 mL/min;检测波长:320 nm;进样量:20 μL。
(2) 对照品溶液的制备 取阿魏酸对照品适量,精密称定,置棕色容量瓶中,加50%乙醇制成每1 mL 含5 μg 的溶液,即得。
(3) 供试品溶液的制备 分别取本品20 片(批号:190912、191017、191103),除去包衣,精密称定,研细,取约0.5 g,精密称定,置具塞锥形瓶中,精密加入50%乙醇25 mL,超声处理(功率:320 W,频率:40 kHz)30 min,放冷,再称定重量,用50%乙醇补足减失的重量,摇匀,滤过,取续滤液,即得。
(4) 供试品含量的测定 分别精密吸取对照品溶液与供试品溶液各10 μL,注入液相色谱仪,测定,即得[15],见图1。
1.7.6 芍药苷含量测定 (1) 色谱条件Agilent ZORBAX Extend-C18柱 (4.6 mm×250 mm,5 μm);流动相:乙腈-0.1%磷酸溶液(14 ∶86);柱温:50 ℃;流速:0.8 mL/min;检测波长:230 nm;进样量:20 μL。
(2) 对照品溶液的制备 取芍药苷对照品适量,精密称定,加甲醇制成每1 mL 含45 μg 的溶液,即得。
(3) 供试品溶液的制备 分别取本品20 片(批号:190912、191017、191103),除去包衣,精密称定,研细,取约2 g,精密称定,置具塞锥形瓶,精密加入水50 mL,密塞,称定重量,超声处理(功率:320 W,频率:40 kHz)15 min,放冷,再称定重量,用水补足减失的重量,摇匀,离心,精密量取上清液25 mL,置分液漏斗中,用水饱和正丁醇振摇提取4次,每次15 mL,合并正丁醇,蒸干,残渣加稀乙醇适量使溶解,转移至10 mL 容量瓶,加稀乙醇至刻度,摇匀,即得。
(4) 供试品含量的测定 分别精密吸取对照品溶液与供试品溶液各10 μL,注入液相色谱仪,测定,即得[16],见图2。
1.7.7 微生物限度的测定 固体制剂微生物限度测定参考2020 年版《中国药典》(四部)中的方法,细菌总数检出量≤103cfu/g,霉菌与酵母菌总数检出量≤102cfu/g,致病菌不得检出,即判定为合格[17]。
1.8 数据分析
利用Design-Expert 10.0 以及Excel 软件对试验数据进行分析处理,每个样品3 次重复,取平均值。
2 结果
2.1 单因素试验
经单因素试验可知,浸膏相对密度、物料液固比与润湿剂浓度直接影响物料的粘性大小,颗粒粒径受物料粘性制约,从而影响片剂的成型[18]。浸膏相对密度较大,物料液固比较小,润湿剂浓度偏低时,软材较为松散,颗粒粒径偏小、细粉多,粉体之间分子引力作用增大,导致粉体颗粒流动性变差,从而对片剂装量差异和片剂崩解时限产生影响;浸膏相对密度较小,物料固液比较大或润湿剂浓度偏高时,软材粘性大,颗粒粒径偏大,也会对片剂装量差异和崩解时限产生影响。助流剂用量过少时,颗粒流动性差,对装量差异产生影响,反之,则会由于硬脂酸镁的疏水性导致崩解变迟缓,从而综合评分降低。由图3 可知,浸膏相对密度为1.20 g/mL、润湿剂浓度为80%、物料液固比为30%、助流剂用量为0.6%时各组综合评分最高,各在此基础上取上下浮动两个水平进行后续响应面分析试验。
2.2 响应面试验设计
采用Design Expert 10.0 软件对试验数据进行二次响应面回归分析,得到的综合评分(Y)与各因变量的模拟方程为:Y= 91.46 + 1.97A- 2.67B+ 2.32C+1.83D+ 0.33AB+ 0.65AC+ 1.65AD+ 1.22BC- 0.65BD-2.52CD- 8.03A2- 3.52B2- 11.39C2- 7.26D2。见表4。

表4 响应面试验方案及结果Tab. 4 Response surface test scheme and results
2.3 回归模型显著性检验及方差分析
由表5 可知,回归模型处在极显著水平,P<0.001,表明该模型显著回归,方程可以正确表明综合评分与各因素关系[19]。多元相关系数R2为0.897 8,表明实测值和预测值间拟合度很高。表中失拟项P值(0.213 6)>0.05,表示极不显著,证明了该回归模型与试验拟合度极高。根据F值可以看出影响综合评分因素的主次顺序为:润湿剂浓度>物料液固比>浸膏相对密度>助流剂用量。
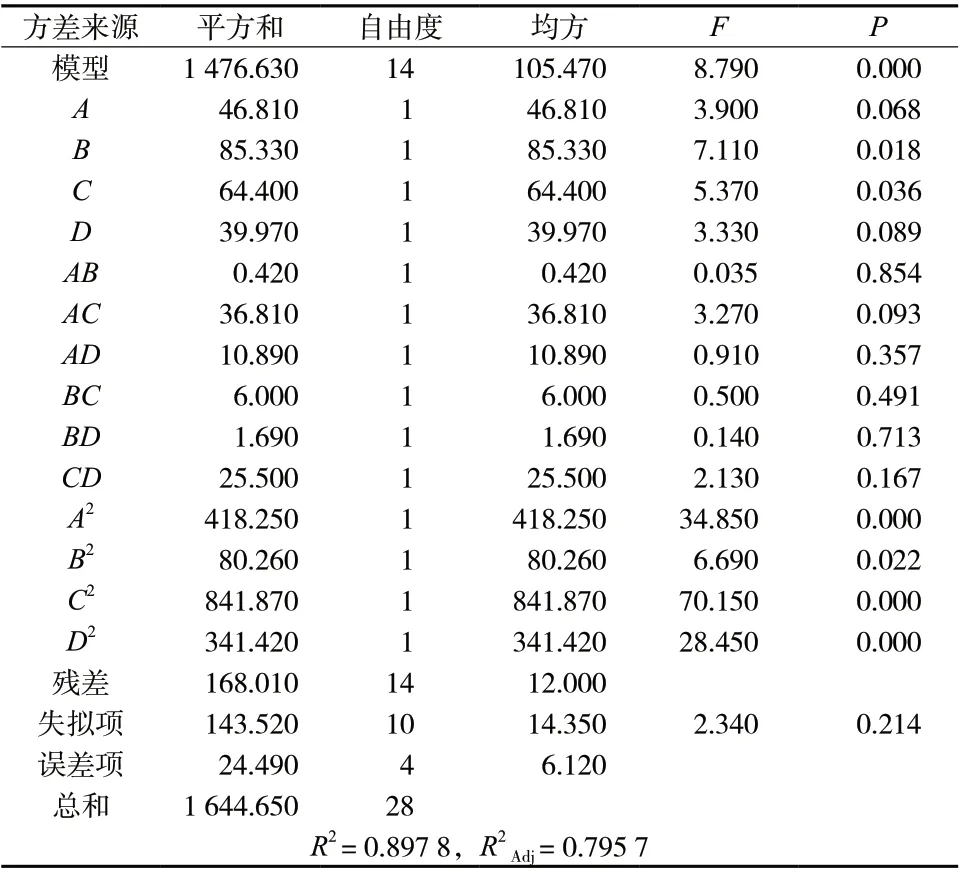
表5 响应面二次回归模型方差分析Tab. 5 Response surface quadratic regression model analysis of variance
2.4 响应曲面及等高线分析
等高线图和响应面图可以直观的反应出各因素交互作用对妇科调经片制剂综合评分的影响[20]。由图4a 可知,浸膏相对密度与物料液固比的交互作用对综合评分的影响与4b、4c 组比较相对较为显著,这与二次回归模型方差分析结果一致。各组中两因素的交互作用均在水平0 左右时取得峰值,这可能是因为当浸膏相对密度过高,物料液固比小及助流剂用量较少时会导致物料坚硬紧实、粘性差,压片后易皲裂,反之这些因素取值过高则会导致物料松散,成粒性差,挤压难以成片。
2.5 工艺验证
根据Design Expert 10.0 软件优化出响应面最优解为浸膏相对密度1.192 5 g/mL、润湿剂浓度78.28%、物料液固比30.415%、助流剂用量0.644 6%。根据实际生产条件将工艺参数优化为浸膏相对密度1.20 g/mL、润湿剂浓度80%、物料液固比30%、助流剂用量0.6%。此条件下制备3 批妇科调经片素片,试验数据见表6。试验结果与理论预测值相比相对误差小于0.05%,表明妇科调经片成型工艺条件参数准确可靠,具有实际生产价值。
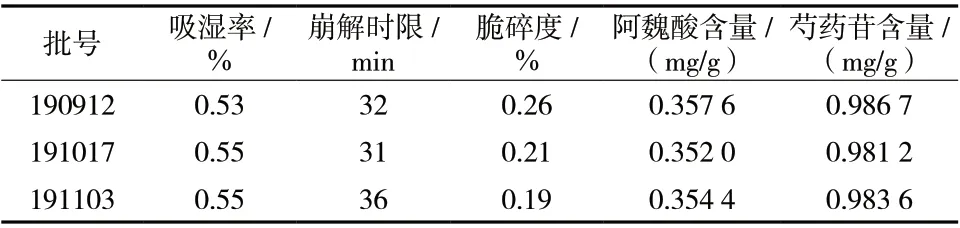
表6 妇科调经片成型工艺结果验证Tab. 6 Validation of molding process results of gynecological menstruation tablets
2.6 稳定性试验
取妇科调经片素片(批号:190912、191017、191103)进行薄膜包衣后开展加速与长期稳定性试验,结果见表7、8。数据表明试验期结束时片剂外观性状表现为平整、光滑,未出现裂纹、碎片等现象,检测药片的吸湿率、崩解时限、阿魏酸苷含量、芍药苷含量以及微生物限度也均在2020 年版《中国药典》要求范围内,药品符合规定。

表7 稳定性加速试验结果Tab. 7 Stability accelerated test results

表8 稳定性长期试验结果Tab. 8 Long-term stability test results
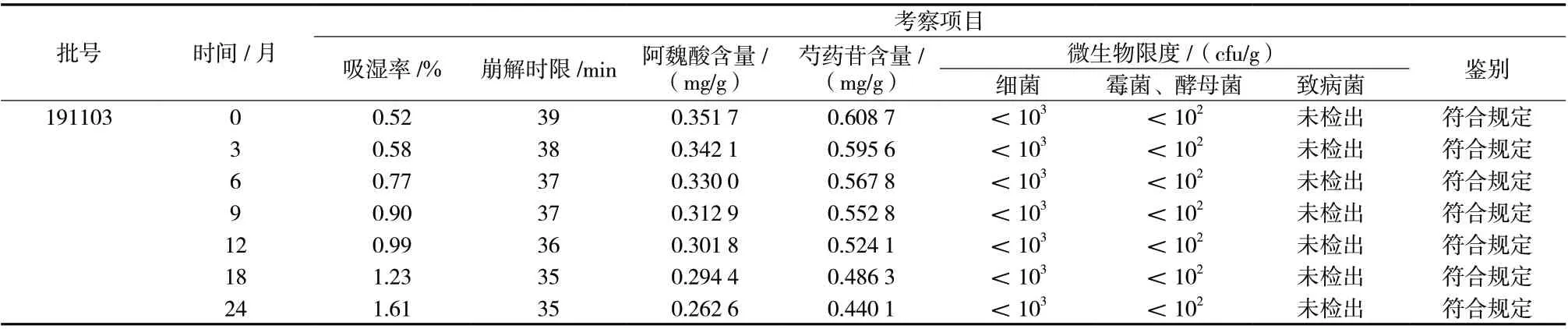
续表8
3 讨论
为了有效提高妇科调经片药品质量及发挥其最佳药用价值,同时提升车间产能以满足广泛的市场需求。本试验利用响应面法对妇科调经片成型工艺进行了优化,该方法能够有效解决多因素的试验设计问题,优选出最佳生产条件参数,此条件下生产的药物与优化前的工艺相比,可操作性、重复性强,药物有效成分检出量高,有效延长了药物保质期。经优化后验证的三批药品检测结果与理论预测值相似,药品在后期加速及长期稳定性试验中外观性状、吸湿率、崩解时限、阿魏酸、芍药苷含量及微生物限度等指标均符合2020 年版《中国药典》要求。
4 结论
本试验利用响应面法优化出的妇科调经片成型工艺条件参数准确、可靠,与前人进行的研究相比,此工艺条件的应用显著提高了车间生产效率,扩大了车间生产批次量,为妇科调经片的生产上市提供了理论依据的支持与实际生产的保障。另外,本研究主要考察的内容为妇科调经片素片成型工艺,而对后期包衣条件的筛选未进行深入研究,为了进一步优化生产工艺,提高车间生产效率,后续可以继续开展妇科调经片包衣工艺条件优化的相关试验研究。
