柴苓舒肝丸药物代谢动力学及毒理学的研究
2022-09-15张培会朱玉苹杜希扬
张培会,汤 晓,朱玉苹,杜希扬
(临沂市中医医院,山东 临沂 276002)
柴苓舒肝丸(备案号:鲁药制备字Z20210069000)为我院名老中医经验方,其由茯苓、柴胡、党参、黄芪、薏苡仁、郁金、赤芍等19味中药材制备而成的水丸,用于治疗肝郁脾虚、湿毒内蕴之证。药物代谢动力学是贯穿药物发现、研究、开发和临床应用全过程的重要学科[1],研究药物在体内吸收、分布、代谢和排泄的过程及其动态变化,并用动力学原理阐明动态变化规律[2]。毒理学是一门研究外源因素(化学、物理、生物因素)对生物系统的有害作用的应用学科,其中肝、脾、心、脑等脏器的绝对重量及脏器系数作为了解脏器生长发育以及病理损伤情况的指标被列为安全性毒理学评价的观察指标[3]。本研究在对柴苓舒肝丸严格质控的基础上[4],充分借助于CUMS大鼠模型,对其药动学特征和脏器毒性进行探讨。
1 材料与方法
1.1 实验动物
健康SPF级Wistar大鼠60只,6~8周龄,体质量(200±20)g。
1.2 仪器
Acquity UPLC( 美 国Waters公 司);TSQ Endura MS(美国Thermo Fisher公司);XS205电子天平(METTLER TOLEDO公司);3K15型高速冷冻离心机(Sigma 公司);Z326K型高速冷冻离心机(Hermle 公司);KQ-500E超声波清洗器(昆山市超声仪器有限公司);DW-86W100医用低温保存箱(青岛海尔特种电器有限公司)。
1.3 动物分组和干预方法
所有动物适应性饲养1周,随机分为对照组、模型组、阳性药组及中药组,各组15只。对照组正常饲养,其余各组采用慢性温和应激(CUMS)法制备大鼠抑郁模型,在此基础上,阳性药组及中药组分别采用氟西汀和柴苓舒肝丸悬浊液(无菌蒸馏水配置)灌胃,给药量为人体8倍量,持续灌胃6个月。
CUMS方法:使用7种不可预知的温和性刺激(包括夹尾3 min、震荡30 min、束缚2 h、夜间光照12 h、断食24 h、断水24 h 和潮湿垫料24 h)持续刺激21 d,平均每种刺激使用3次,每日的刺激不应在同一时间段进行,避免大鼠产生耐受性,影响实验结果。实验过程中注意保持室内整洁、安静,温度、湿度适宜,尽量减少空气流动,实验人员操作力度适当,避免影响实验结果。
给药方法:灌胃,氟西汀和柴苓舒肝丸均以无菌蒸馏水溶解,制备混悬液,给药剂量为人体8倍量。每天早上8:00灌胃,每日1次,连续6个月。
1.4 药物代谢动力学
1.4.1 试验过程 给各组健康SPF级Wistar大鼠每天早上8:00灌胃,每日1次,连续6个月。第1天给药前和给药后 0.083 h、0.25 h、0.5 h、1 h、2 h、4 h、8 h、24 h锁骨下颈静脉采集血液,获得单次给药的血药浓度数据;第4、5、6天给药前和给药后0.5 h采集血液,观察稳态谷、峰浓度;第7天给药前和给药后 0.083 h、0.25 h、0.5 h、1 h、2 h、4 h、8 h、24 h采集血液,获得多次给药的血药浓度数据。采集的血液4 000 rpm离心10 min,分离血浆后,用UPLC-MS/MS法测定血浆中柴胡皂苷D和黄芪甲苷的含量。
1.4.2 血浆样品检测前的预处理方法 50 μL含药血浆样品,加入5 μL内标工作液,100 μL甲醇沉淀液,涡旋,9 100 g离心10 min,取上清液100 μL,加入100 μL 80%甲醇水混匀,涡旋,9 100 g离心10 min后,取 120 μL 上清液进样 5 μL。
1.5 毒理检测
灌胃时间6个月,灌胃结束时处死剩余大鼠,解剖主要组织器官(心、肝、脾、肺、肾),精密称量、计算脏器指数,同时HE 染色观察各组织器官病理改变情况。
2 结果
2.1 药物代谢动力学结果分析
2.1.1 个体动物的平均血药浓度—时间数据 大鼠单次给药前的血药浓度均低于定量下限。灌胃给药后,柴胡皂苷D和黄芪甲苷的血药浓度在0.5 h最高。随着时间增加,血药浓度逐渐降低,24 h时均低于定量下限(见表1)。

表1 大鼠单次灌胃柴苓舒肝丸后的平均血药浓度—时间数据 ng·mL-1
多次给药期间的谷浓度和第7天给药前的血药浓度均低于定量下限,多次给药期间的峰浓度与单次给药一致;多次给药后,血药浓度趋势没有明显的变化(见表2)。

表2 大鼠多次灌胃柴苓舒肝丸水溶后的平均血药浓度—时间数据 ng·mL-1
2.1.2 平均血药浓度—时间曲线 大鼠单次灌胃给药后,柴胡皂苷D和黄芪甲苷的血药浓度均在0.5 h达峰,说明吸收快,随后逐渐下降(见图1);由半对数曲线图可见,柴胡皂苷D的消除速率比黄芪甲苷快(见图2)。

图1 大鼠单次灌胃柴芩舒肝丸后柴胡皂苷D和黄芪甲苷的平均血药浓度—时间曲线

图2 大鼠单次灌胃柴芩舒肝丸后柴胡皂苷D和黄芪甲苷的半对数平均血药浓度—时间曲线
大鼠多次灌胃给药后,柴胡皂苷D和黄芪甲苷在第4、5、6天的峰浓度与第1天和第7天接近,无明显变化。柴胡皂苷D和黄芪甲苷在第1天和第7天给药后的消除过程是一致的,柴胡皂苷D的消除速率比黄芪甲苷快(见图3、图4)。
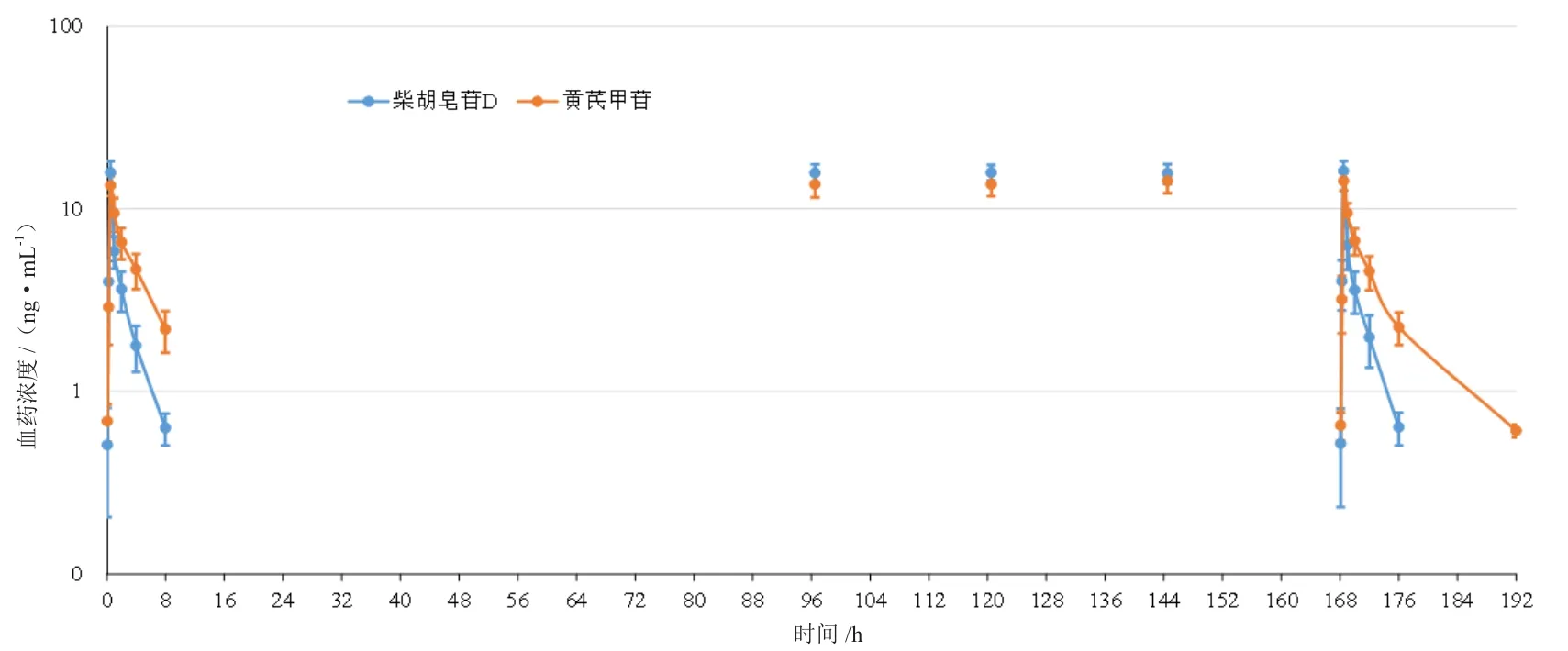
图3 大鼠多次灌胃柴芩舒肝丸后柴胡皂苷D和黄芪甲苷的平均血药浓度-时间曲

图4 大鼠多次灌胃柴芩舒肝丸后柴胡皂苷D和黄芪甲苷的半对数平均血药浓度-时间曲线
2.1.3 药代参数计算
2.1.3.1 个体动物的平均药代参数 大鼠单次和多次灌胃柴芩舒肝丸后,血浆中柴胡皂苷D的平均AUC(0-t)分别为 22.0 μg·L-1·h-1、22.9 μg·L-1·h-1,平均 Cmax分别为 15.9 μg·L-1、16.1 μg·L-1,t1/2分别为2.07 h、2.27 h,表观分布容积Vd分别为124 L·kg-1、130 L·kg-1;血浆中黄芪甲苷的平均AUC(0-t)分别为49.3 μg·L-1·h-1、48.3 μg·L-1·h-1,平均 Cmax分别为13.5 μg·L-1、14.2 μg·L-1,t1/2分别为 4.04 h、3.61 h,表观分布容积 Vd分别为 103 μg·L-1、94 L·kg-1(见表3、表4)。这些数据表明大鼠单次和多次灌胃柴芩舒肝丸后,柴胡皂苷D具有消除快、分布广的特点,黄芪甲苷消除较慢、分布广。

表3 大鼠单次灌胃柴苓舒肝丸后柴胡皂苷D和黄芪甲苷的药代动力学参数

表4 大鼠多次灌胃柴苓舒肝丸后柴胡皂苷D和黄芪甲苷的药代动力学参数
2.1.3.2 多次给药后的药代动力学参数变化 大鼠多次灌胃柴苓舒肝丸后,柴胡皂苷D的AUC(0-t)和Cmax分别为单次注射的1.04、1.07倍,无明显变化,说明连续给药7 d大鼠血液中没有柴胡皂苷D蓄积。除此之外,t1/2、CL、Vd和MRT(0-t)分别为单次给药的1.10、0.95、1.05和1.51倍,差异均在2倍以内。这些数据表明,多次灌胃柴苓舒肝丸,大鼠体内没有柴胡皂苷D蓄积,与单次给药相比,主要药代动力学参数没有发生显著改变(见表5)。

表5 大鼠单次和多次灌胃柴苓舒肝丸后柴胡皂苷D的药代动力学参数比较
大鼠多次灌胃柴苓舒肝丸后,黄芪甲苷的AUC(0-t)和Cmax分别为单次注射的0.98、1.05倍,无明显变化,说明连续给药7 d大鼠血液中没有黄芪甲苷蓄积。除此之外,t1/2、CL、Vd和 MRT(0-t)分别为单次给药的0.89、1.04、0.91和0.95倍,差异均在2倍以内。这些数据表明,多次灌胃柴苓舒肝丸,大鼠体内没有黄芪甲苷蓄积,与单次给药相比,主要药代动力学参数没有发生显著改变(见表6)。

表6 大鼠单次和多次灌胃柴苓舒肝丸后黄芪甲苷的药代动力学参数比较
2.2 毒理检测结果分析
2.2.1 脏器湿重结果 灌胃6个月后各组大鼠解剖取脏器称重。与对照组相比,模型组平均脏器湿重无显著改变(P>0.05);同时各给药组脏器湿重与模型组相比也无显著性差异(P>0.05)(见表7)。

表7 柴苓舒肝丸灌胃给药对大鼠脏器湿重的影响
2.2.2 脏体系数结果 灌胃6个月后各组大鼠解剖取脏器称重,并计算脏体系数。与对照组相比,模型组平均脏体系数无显著改变(P>0.05);各给药组脏体系数与模型组相比也无显著性差异(P>0.05)(见表8)。

表8 柴苓舒肝丸灌胃给药对大鼠脏体系数的影响
2.2.3 HE染色结果 灌胃6个月后各组大鼠解剖取脏器进行HE染色观察脏器病理改变。与对照组相比,模型组脏器形态无显著改变(P>0.05);各给药组脏器形态与模型组相比也无显著性差异(P>0.05)(见图5)。综上所述,可知柴苓舒肝丸具有低的脏器毒性。
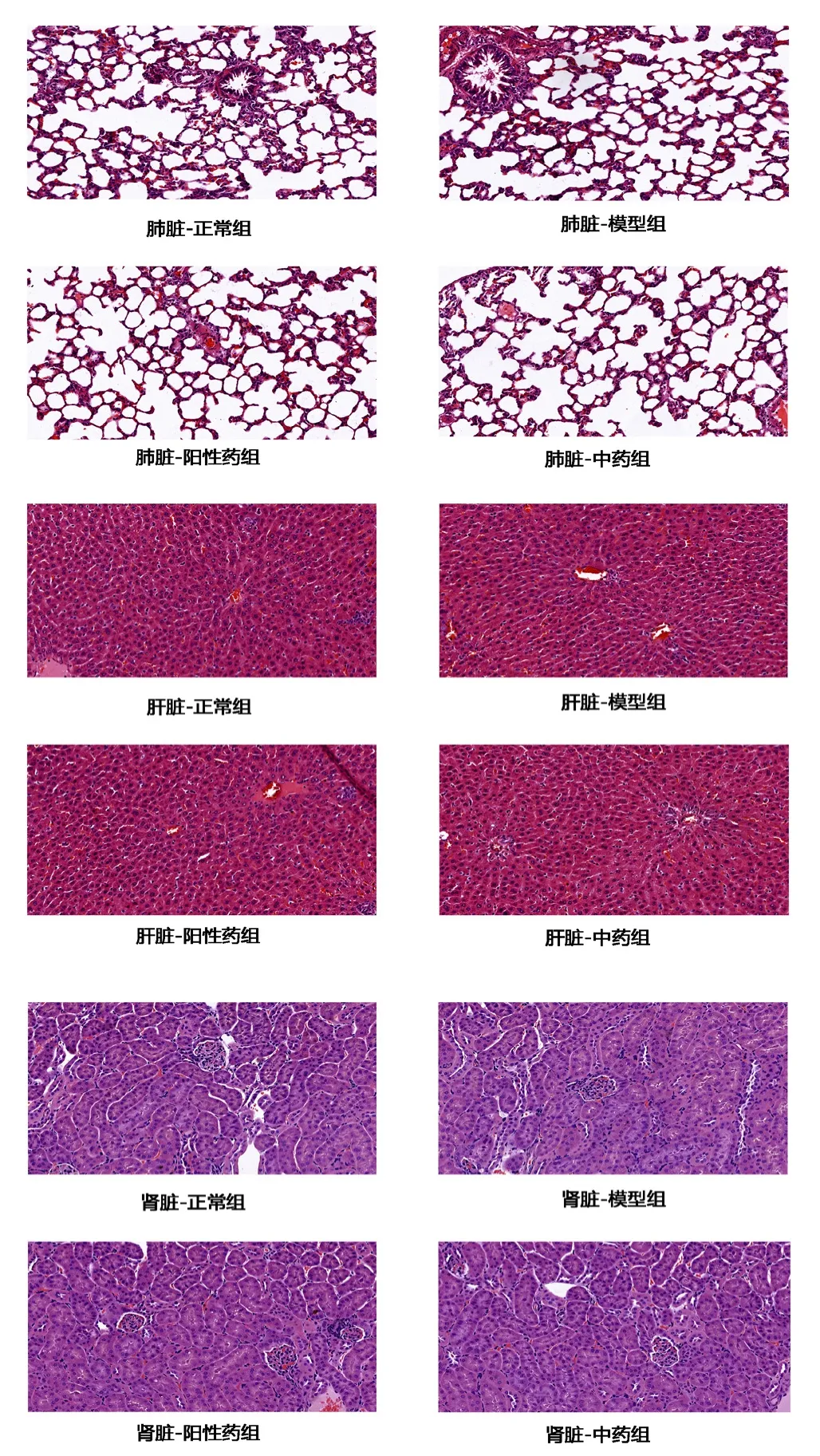

图5 各组大鼠脏器病理图
3 讨论
中药药物代谢动力学是一门新兴学科,开展中药药物代谢动力学研究对阐明和揭示中药药效物质基础和作用机制,设计及优选中药给药方案,促进中药新药研发、剂型改进及质量控制,均具有重要意义。柴苓舒肝丸属于水丸,克服了煎煮汤剂流程不可控、携带与服用不方便、口感差等缺点,但目前多数中药制剂的质量控制研究止步于成品本身的性状、特征及微生物检测等,而在体内药动学及毒理学分析方面相对薄弱。因此,本研究在此基础上,考察了其药动学特征和脏器毒性,结果发现,以其主要成分柴胡皂苷D和黄芪甲苷为代表,柴苓舒肝丸具有吸收快、分布广的优点,且在体内没有蓄积;通过脏器湿重、脏体系数和病理图结果可知,柴苓舒肝丸具有低脏器毒性的优点。通过探讨柴苓舒肝丸的药物代谢动力学及毒理学,为柴苓舒肝丸进一步的临床应用奠定基础。
