F-及对α型半水硫酸钙结晶成核及形貌的影响
2022-09-14张远永曹建新
张远永,杨 林,2,曹建新,2,刘 荣,张 煜
(1.贵州大学化学与化工学院,贵阳 550025;2.贵州省工业废弃物高效利用工程研究中心,贵阳 550025)
0 引 言
磷酸在农业、食品、制药等领域都有着广泛的应用,是一种重要的工业原料。湿法磷酸工艺是磷酸生产的重要工艺手段,根据所得水合物的不同可分为二水法、半水法和无水法工艺[1]。其中半水法湿法磷酸工艺不仅可以直接得到高浓度磷酸产品,而且还能获得具有胶凝强度的半水磷石膏,具有高效节能的优点[2-3]。可见,发展半水法湿法磷酸工艺具有重要的现实意义[4-7]。半水法湿法磷酸生产的主要原料是磷矿石,其主要成分为氟磷灰石Ca5F(PO4)3,这种矿石常伴生有大量镁、铁、铝、钠、氟、硅等杂质元素[8-10]。当磷矿被酸解后,磷矿中的氟、铝、铁、硅等杂质也会一同进入酸解液中。这些杂质的存在会影响α型半水硫酸钙(α-HH)晶体的结晶过程及晶体形貌。α-HH晶体的形貌会影响磷酸与磷石膏的分离效果以及洗涤效率,最终对磷酸的品质及生产效率造成影响[11]。

1 实 验
1.1 原 料
磷酸(85%P2O5,AR,成都金山化学试剂有限公司)、硫酸(98%H2SO4,AR,重庆川东化工有限公司)、氟硅酸(40%H2SiF6,AR,上海阿拉丁生化科技股份有限公司)、碳酸钙(99.5%CaCO3,GR,上海展云化工有限公司)、氢氟酸(40%HF,AR,重庆茂业化工试剂有限公司)、无水乙醇(99.7%CH3CH2OH,AR,成都金山化学试剂有限公司)、实验用水均为二次蒸馏水。
1.2 过饱和度的计算
溶液中过饱和度S的定义式为[17]:
(1)
式中:C表示溶液中总的Ca2+浓度;C*表示晶体生长达到平衡时溶液中总的Ca2+浓度。式中Ca2+平衡浓度由以下方法测得。
将一定质量的碳酸钙加入到200 mL 30%(质量分数,下同)P2O5溶液中配制成Ca(H2PO4)2溶液,并移至聚四氟乙烯三口烧瓶中,加热至95 ℃,以150 r/min恒速搅拌。按溶液中Ca2+浓度等量加入98%H2SO4,以一定时间间隔移取浊液过滤,使用火焰原子吸收分光光度计测定滤液中的Ca2+浓度,得到Ca2+浓度随时间变化曲线如图1所示。硫酸加入以后溶液中Ca2+浓度不断降低,最终趋于平稳。得到95 ℃,30% P2O5条件下Ca2+的平衡浓度C*=0.136 0 mol·L-1。
1.3 结晶诱导时间的测定

1.4 表面能、临界晶核半径和成核速率的计算
根据经典成核理论,初级成核可分为均匀成核和非均匀成核[18]。高过饱和环境下的成核方式通常为均匀成核。在一定高的初始过饱和度范围,结晶诱导时间的对数lgtind与过饱和度对数平方的倒数(lg2S)-1呈线性关系,见式(2)[19]:
(2)
式中:tind表示诱导时间(s);const表示无量纲经验常数;kf表示形状因子,对于球形晶核数值为16π/3;NA表示Avogadro常数为6.02×1023;σ表示表面能或界面张力(J·m-2);Vm表示摩尔体积,对于α-HH其值为5.317 6×10-5m3·mol-1;R表示气体常数为8.314 J·mol-1·K-1;T表示绝对温度(K);S表示α-HH的过饱和度。
以lgtind-(lg2S)-1作图得到一条直线,求得直线的斜率并通过式(2)得到表面能σ数据。再根据式(3)和式(4)计算得到临界晶核半径和成核速率[20]。
(3)
(4)
式中:rcrit表示临界核半径(nm);N表示成核速率(晶核数·cm3·s-1);kn表示成核过程速率常数1030。
1.5 样品表征
采用喷金处理样品,并通过扫描电子显微镜(SEM,S-3400 N,日本)研究其微观形貌。
得到的晶体产物采用光学显微镜(Industrial Digital Camera,E3ISPM20000KPA,Nikon)配合Nano measurer软件计算样品长度与直径数据(样品颗粒数≥100个),样品长度(L)、直径(D)和长径比(L/D)统计公式如下[21]。
(5)
(6)
(7)
式中:L为整体平均长度;li为单个颗粒的长度;D为整体平均直径;di为单个颗粒的直径;L/D为整体长径比;ni为相应颗粒长度为li、直径为di时的颗粒数。
使用X射线衍射仪(XRD,Bruker D8 Advance,德国)分析物相组成,条件为:铜靶,电压40 kV,电流40 mA,连续扫描,扫描速度10 (°)/min,扫描范围2θ=5°~90°。
使用X射线光电子能谱仪(XPS,K-Al pha Plus,美国赛默飞世尔)对α-HH晶体样品表面元素组成及结合能进行分析,射线源为Al Kα激发源,能量分辨率≤0.5 eV,最小能量步长3 meV。
2 结果与讨论
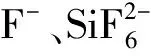
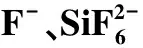
表1 不同过饱和度及浓度下α-HH结晶诱导时间Table 1 Induction time of α-HH crystallization at different supersaturation, F- and concentration
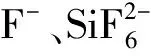
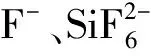
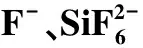
表2 不同浓度下α-HH的表面能Table 2 Surface energy of α-HH with different F- and concentration
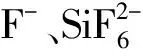
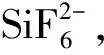
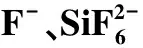
表3 不同过饱和度下,加入对α-HH成核速率与临界晶核半径的影响Table 3 Effect of F- and addition on the nucleation rate and critical nucleation radius of α-HH at different supersaturation
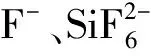
过饱和度S=1.64时,不同F-掺量下α-HH晶体长度、粒径、长径比数据图如图5所示。
当未加入F-时,α-HH晶体的平均长度为436.80 μm,平均直径为18.48 μm。由图5(a)可知,随着F-浓度增加,α-HH晶体的平均长度由436.80 μm减小至340.57 μm,平均直径由18.48 μm增大至19.68 μm。由图5(b)可知,平均长径比由24.21减小至19.59,F-的加入使得α-HH晶体的平均长径比减小,这是因为F-的加入抑制了α-HH晶体在C轴方向的的成核,在较低的成核速率下,更容易得到粗大的晶体。

2.4 α-HH晶体XRD分析
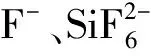

2.5 α-HH晶体的XPS分析
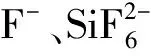

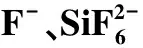
表4 不同掺量下α-HH晶体表面Ca的结合能化学位移Table 4 Chemical shifts of binding energy of Ca on the surface of α-HH crystals with different F- and
