SiO2@BiOCl-Bi24O31Cl10核壳微球的合成及光催化
2022-09-13张鑫许蕊路馨语牛永安
张鑫,许蕊,路馨语,牛永安
(1 沈阳化工大学化学工程学院,辽宁 沈阳 110142; 2 沈阳化工大学材料科学与工程学院,辽宁 沈阳 110142)
引 言
水污染及其防治问题的解决依赖于绿色低碳的光催化技术的广泛应用,半导体光催化作为一种环保、可循环使用的新技术在处理污水中有机染料方面具有重要应用前景。其中,Bi2O3的杂化轨道分布特性和Bi(Ⅲ)的6s2孤对电子的存在,使Bi—O 键具备较好的可变形性和极化能力,有利于光电荷的生成与转移,是一种十分具有应用前景的可见光催化剂[1-2]。
但是,Bi2O3的禁带宽度(Eg)相对大小限制了其光响应范围,导致光催化反应中可见光利用率较低,且光生电子-空穴对在迁移中易产生复合,影响Bi2O3的实际光催化效果[3]。为提升光催化效率,研究人员提出纳米化[4-6]、元素掺杂[7-9]、多相复合[10-12]等多种方法增强Bi2O3的光催化活性。目前,多相复合形成的新型半导体光催化剂备受关注[13-14]。Chen等[15]采用溶剂热法合成了尺寸可控的Bi@Bi2O3核壳纳米微球,通过对连续流反应器中NO 气体浓度的检测,发现其对NO 有明显的降解效果;Hu等[16]运用浸渍法将Cu(Ⅱ)簇附着到Bi2O3表面,清除激发电子进而增强光催化活性,可将气态2-丙醇分解为CO2;Lim 等[17]通过静电纺丝和精确控温热处理前体,在300~375℃的温度范围内制备了α-β 相异质结Bi2O3纳米纤维,具有较为突出的光催化性能。上述方法在Bi2O3光催化领域有一定的创新,但是预期性能和实际应用还存在一定距离。BiOCl 具有特殊的层状结构,其层内为共价键而层间为较弱的范德华力,这种差异有助于载流子分离,提高光催化性能[18]。纳米BiOCl 的合成主要采用溶剂热法,高温高压环境有利于相复合。例如,Chen 等[19]改变反应系统中的乙醇/水体积比来调整BiOCl/(BiO)2CO3复合光催化剂的化学成分和形态;He 等[20]合成了不规则h-BN/OV-BiOCl 复合材料。但是,溶剂热法合成BiOCl 反应耗时长、产量低,产物形貌不够规整且结构较为松散。
考虑到复合光催化剂的优势,本文设计一种步骤简洁、易于操作的单分散性SiO2@BiOCl-Bi24O31C10核壳微球的合成方法。首先,选择分散性良好且化学结构稳定的SiO2纳米微球为核,利于恒温溶液反应高效制备SiO2@Bi2O3核壳微球。然后,通过掺杂Cl 改变Bi2O3壳层的形貌和组分,研究单分散性SiO2@BiOCl-Bi24O31C10核壳微球的最佳合成工艺条件。最后,研究合成的核壳微球对RhB 可见光降解活性,分析SiO2@BiOCl-Bi24O31C10核壳微球可能遵循的光催化机理。
1 实验材料和方法
1.1 材料
五 水 硝 酸 铋[Bi(NO3)3·5H2O]、二 甘 醇(DEG,99.0%)和氯化钠(NaCl)购自国药集团化学试剂有限公司,氨水和乙醇购自天津市富宇精细化工有限公司,罗丹明B(RhB)购自天津市试剂研究所,SiO2微球根据文献[21]方法自制。以上所有化学品均为分析纯,使用前未经进一步纯化。
1.2 核壳微球的制备
1.2.1 SiO2@Bi2O3微球的制备 称取0.0500 g 的自制SiO2微球超声分散于100.0 ml 乙醇,待分散均匀后转移至250 ml三口烧瓶中,再加入0.5 ml氨水,搅拌均匀得到反应体系A。称取0.4043 g 的Bi(NO3)3·5H2O 溶于5.0 ml 二甘醇,搅拌溶解并缓慢将其滴入反应体系A 中。在25℃恒温水浴条件下反应12 h,得到的固体产物经离心收集,无水乙醇清洗3 次,60℃烘干12 h 后,得到SiO2微球与含Bi3+的复合前体,记为SB-1。参照上述步骤,改变Bi(NO3)3·5H2O与SiO2的投料摩尔比x(x=0.8,1.0,1.5,2.0),所得复合前体标记为SB-x,具体投料参数见表1。在400、450 和500℃的空气气氛中将SB-x煅烧4 h,得到SiO2@Bi2O3微 球,分 别 标 记 为SiO2@Bi2O3(400)-x、SiO2@Bi2O3(450)-x和SiO2@Bi2O3(500)-x。

表1 SiO2@Bi2O3样品前体的反应参数Table 1 Reaction parameters of some SiO2@Bi2O3 sample precursors
1.2.2 SiO2@BiOCl-Bi24O31Cl10的制备 称取0.0500 g 的SiO2微球超声分散于100.0 ml乙醇,待分散均匀后转移至三口烧瓶中,并加入0.5 ml氨水,搅拌均匀得到反应体系B。称取摩尔比为y(y=1,2,3,4)的Bi(NO3)3·5H2O 和NaCl 溶于5.0 ml 二甘醇,搅拌溶解后缓慢滴入剧烈搅拌的反应体系B 中,在25℃恒温水浴条件下反应12 h,离心收集固体产物,并用无水乙醇清洗3 次,60℃烘干12 h 后得到SiO2微球与含Bi3+/Cl-的复合前体,产物标记为SBC-y。
选定摩尔比为1,改变氨水加入量z(z=0.5,1.0,2.0,3.0 ml),按照上述步骤制备复合前体,所得产物标记为SBC-1-z,具体投料参数见表2。将SBC-y和SBC-1-z在450℃煅烧4 h 后,获得的产物分别标记为SiO2@BiOCl - Bi24O31Cl10(450) -y、SiO2@BiOCl-Bi24O31Cl10(450)-1-z。

表2 SiO2@BiOCl-Bi24O31Cl10样品前体的具体投料参数Table 2 Specific feeding parameters of SiO2@BiOCl-Bi24O31Cl10 sample precursors
1.3 分析测试方法
采用粉末X 射线衍射仪(XRD,D8,德国Bruker公司)在3 kW 功率下利用Cu 辐射对合成样品的晶体结构和相进行鉴定,扫描范围为10°~70°,扫描步长为0.02°;通过高低真空扫描电镜(SEM,JSM-6360LV,日本电子公司)、高分辨场发射扫描电子显微镜(SU8010,日本日立公司)和冷场发射扫描电镜(Regulus 8100,日本日立公司)对反应产物的形貌、结构进行测定,所有SEM 测试样品都通过溅射镀金;通过场发射透射电子显微镜(TEM,Tecnai G2F20,美国FEI 公司)对产物的结构进行进一步研究;运用综合热分析仪(STA-449C,德国Netzsch 公司)测量样品的热重(TG)与差示扫描量热(DSC)曲线,研究样品的热稳定性和组分变化,升温速率为10℃/min;运用紫外分光光度计(UV-vis,UV-1601,北京瑞利公司)测定样品的紫外吸收光谱,波长测试范围为200~1100 nm。
1.4 光催化性能测试
首先将20 mg合成的光催化剂分散于50.0 ml浓度为10 mg/L 的RhB 溶液中形成悬浮液,采用载有420 nm 截止滤光片的350 W 氙灯作为可见光源,测试离心分离所得上清液的紫外可见光谱。在可见光照射前,悬浮液在黑暗环境搅拌240 min 达到吸附-解吸平衡。照射过程中,每隔5 min 取出1.0 ml悬浮液经离心分离(8500 r/min,10 min)出上清液。整个光催化实验过程在25℃条件下进行,RhB 水溶液保持磁力搅拌,确保颗粒持续处于悬浮状态。RhB的降解效率用C/C0表示,其中C0是达到吸附-解吸平衡时的初始浓度,C是每个时间间隔内剩余污染物溶液的浓度。
2 实验结果与讨论
2.1 热分析
图1 为空气氛围下复合前体SB-1 的TG-DSC曲线。前体SB-1 在100℃左右出现吸热峰,并伴有明显的热失重,是由于SB-1 中的结合水蒸发导致的。在100~380℃温区出现急剧热失重,可能是SB-1 热分解形成SiO2@Bi2O3的结构变化导致的。在526℃左右出现明显的吸热峰,推测是在高温下部分Bi2O3与SiO2反应转变为由[SiO3]2-层和[Bi2O2]2+层构成的Bi2SiO5导致的[22]。高于600℃之后SB-1 的热失重过程趋于稳定,考虑到Bi2O3-SiO2二元系统能以不同化学计量比形成不同结构的硅铋酸盐复合物,在800℃左右的放热峰和1019℃左右的吸热峰可能是亚稳态的硅铋酸盐Bi2SiO5相发生结构变化造成的[23]。

图1 SB-1样品在空气条件的TG-DSC曲线Fig.1 TG-DSC curves of sample SB-1 under air condition
2.2 结构分析
为了深入分析受热过程中的结构变化,图2 所示为前体SB-x经不同煅烧温度热处理后所得样品的XRD 谱图。所有样品均为清晰且较为尖锐的衍射峰,表明它们的结晶程度较高。图2(a)中,经过400℃热处理后得到的SiO2@Bi2O3(400)-x样品均出现了符合β-Bi2O3(JCPDS No.78-1793)相衍射峰[24]。随着热处理温度升至450℃和500℃,图2(b)、(c)中主要结构仍符合β-Bi2O3相衍射峰。除铋源加入量较多的SiO2@Bi2O3(450)-2,其余450℃热处理后所得样品均出现了Bi2SiO5相(JCPDS No.36-0287)。在500℃热处理后所得样品的衍射峰变得更尖锐,此外还出现了微量Bi12SiO20相(JCPDS No.37-0485)。因此,相同摩尔比的SB-x随着热处理温度的逐渐升高,所得样品中都伴随β-Bi2O3的逐渐减少,硅铋酸盐复合物的逐步增加。
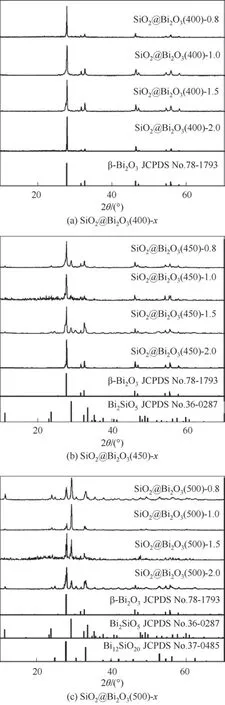
图2 经过不同温度热处理后所得样品的XRD谱图Fig.2 XRD patterns of as-obtained smaples after heat treatment at different temperatures
2.3 形貌分析
图3 所示为SB-x经过不同温度热处理后所得样品的SEM 图。图3(a)~(d)中,经400℃热处理,随着投料摩尔比x(x=0.8,1.0,1.5,2.0)的升高,SiO2微球表面包覆的Bi2O3颗粒也随之增多,并在x=1.0 时Bi2O3颗粒达到最多。当摩尔比x为2.0 时,SiO2微球表面甚至出现了六边形Bi2O3纳米板,可能是Bi(NO3)3·5H2O 浓度过高,导致初期快速成核,后生长为Bi2O3纳米板。图3(i)~(l)为SiO2@Bi2O3(500)-x样品的SEM图,所有样品在SiO2微球表面包覆形成的壳层结构十分明显。其中,SiO2@Bi2O3(500)-1.0 样品的壳层表面较为光滑,SiO2@Bi2O3(500)-2.0 样品中出现了较大的不规则块状结构,可能是Bi(NO3)3·5H2O 用量过多导致前体在煅烧过程中发生熔融产生了多个微球联结。因此,Bi2O3颗粒在SiO2微球表面的分布越均匀细小,越容易高温下发生界面反应而形成较为光滑的壳层。
图3(e)~(h)为经450℃热处理后的SiO2@Bi2O3(450)-x样品的SEM 图,所有样品较400℃和500℃热处理所得样品呈现出不同的形貌。其中,SiO2@Bi2O3(450)-0.8样品表面仍然生长着Bi2O3颗粒,有形成壳层的趋势;而SiO2@Bi2O3(450)-1.0 和SiO2@Bi2O3(450)-1.5 样品表面明显变得粗糙;摩尔比到达2.0时,SiO2@Bi2O3(450)-2.0 出现了结块使得不同微球联结在一起。为了使后续的反应更为稳定,分散性良好且形貌较为规整的SiO2@Bi2O3(450)-1.0 及其制备工艺成为了最优选择。

图3 SB-x经过400,450和500℃热处理后所得样品的SEM图Fig.3 SEM images of as-obtained samples after the heat treatment of SB-x at 400,450 and 500℃
2.4 SiO2@Bi2O3微球的形成机理
图4 提出了SiO2@Bi2O3微球可能的形成机理。溶液A 为SiO2乙醇分散液,其中单分散的SiO2微球表面分布着大量—OH,在与氨水充分作用后,将分布在纳米SiO2微球表面。溶液B 中Bi(NO3)3·5H2O 溶于二甘醇后,通过静电相互作用Bi3+和二甘醇的含氧官能团快速连接,滴入反应体系A后,由于存在适量的铵,Bi3+将从弱键合中解离出来[25-26],与氨水的OH-反应形成Bi(OH)3[27],溶液逐渐变成白色浑浊状。该反应使得溶液保持相对较低水平的Bi3+浓度,从而减缓均相成核。具体反应如式(1)~式(3)。



图4 SiO2@Bi2O3核壳微球可能的形成机理Fig.4 Possible formation mechanism of SiO2@Bi2O3 core-shell mircospheres
经过热处理后发生氧化得到SiO2@Bi2O3微球,由于不同热处理温度使其在氧化反应基础上与SiO2发生化学反应呈现出不同的形貌,随着热处理温度提升,SiO2表面形成光滑壳层且周围分布的微粒逐渐减少。
2.5 Cl掺杂
为提高光催化性能,通过Cl 掺杂改变SiO2@Bi2O3微球的壳层组成,形成BiOCl 壳层。为探究其物质组成与结构,对SBC-y经450℃处理后的产物进行XRD分析,结果如图5所示。SBC-y经过450℃热处理后的产物中显现出BiOCl和Bi24O31Cl10的衍射峰,说明所得产物应为多相复合物SiO2@BiOCl-Bi24O31Cl10。随着投料摩尔比y的提高,属于BiOCl的不同衍射峰逐渐变缓,同时Bi24O31Cl10的特征衍射峰逐渐变得清晰,说明Cl的增加有利于Bi24O31Cl10的生成,并且产物衍射峰位置出现一定偏移,预示着多相物质间的结合开始变得松散。

图5 SBC-y经450℃处理后所得产物的XRD谱图Fig.5 XRD patterns of SBC-y after heat treatment at 450℃
图6 为SBC-1、SBC-2 及分别热处理所得样品的SEM 图。图6(a)、(c)中,未经热处理的样品中SiO2微球表面形成了珊瑚状结构,且周围分散较多纳米颗粒。图6(b)、(d)中,热处理后的样品SiO2@BiOCl-Bi24O31Cl10(450)-1和SiO2@BiOCl-Bi24O31Cl10(450)-2的形貌发生了较大变化,其SiO2微球表面的壳层结构逐渐变得致密,随着摩尔比增加其周围分布的纳米颗粒有向纳米棒转变的趋势。

图6 SBC-1、SBC-2样品及其450℃处理后所得产物的SEM图Fig.6 SEM images of SBC-1 and SBC-2 samples and their products after 450℃treatment
为了更好地确定核壳微球的结构,图7(a)、(b)分别为掺Cl 前后的样品SiO2@Bi2O3(450) -1.0 和SiO2@BiOCl-Bi24O31Cl10(450)-1的TEM 图。可以明显看出SiO2@Bi2O3(450)-1 样品中SiO2核表面覆盖有一层较薄的Bi2O3壳层;而SiO2@BiOCl-Bi24O31Cl10(450)-1 样品中SiO2核表面仅有部分棒状结构包覆。对比可以得出,未掺Cl之前的SiO2@Bi2O3包覆非常均匀,而经过掺Cl 工艺使得壳层结构与形貌发生变化,增加了壳层结构的表面粗糙性。

图7 SiO2@Bi2O3(450)-1.0和SiO2@BiOCl-Bi24O31Cl10(450)-1的TEM图Fig.7 TEM images of SiO2@Bi2O3(450)-1.0 and SiO2@BiOCl-Bi24O31Cl10(450)-1 samples
图8 为SiO2@Bi2O3(450) -1.0 和SiO2@BiOCl-Bi24O31Cl10(450)-y产物以及SiO2@BiOCl-Bi24O31Cl10(450)-1-z产物的紫外可见吸收光谱。随着反应参数不同,所有样品都显示SiO2的吸收峰波长出现了变化。图8(a)中,与SiO2@Bi2O3(450)-1.0 相比,随着氨水加入量的增加,样品SiO2@BiOCl-Bi24O31Cl10(450)-1-z中的SiO2的吸收峰先向右后向左偏移且先变宽后变窄,还出现了少部分其他吸收峰,说明产物中含有微量的杂质相。SiO2@BiOCl-Bi24O31Cl10(450)-1-0.5 产物在200~400 nm 的紫外吸收峰明显比其余产物宽,说明该产物在该波长范围内有更好的吸收性。图8(b)中,提高Cl的加入量,样品对应的鼓包峰也呈现出先变窄后变宽的趋势。利用Tauc plot 法计算了掺杂Cl 前后的光学带隙变化,如图9所示。SiO2@Bi2O3(450)-1.0 的禁带宽度明显小于纯的Bi2O3,而 掺 杂Cl 后 的SiO2@BiOCl-Bi24O31Cl10(450)-1的禁带宽度进一步大幅下降,这为光催化性能的提升提供了理论基础。

图8 改变氨水添加量(z=0.5,1.0,2.0,3.0)和摩尔比(y=1,2,3,4)得到的SiO2@BiOCl-Bi24O31Cl10(450)的紫外可见吸收光谱图Fig.8 UV absorption spectra of as-obtained SiO2@BiOCl-Bi24O31Cl10(450)with altered ammonia content(z=0.5,1.0,2.0,3.0)and mole ratio(y=1,2,3,4)
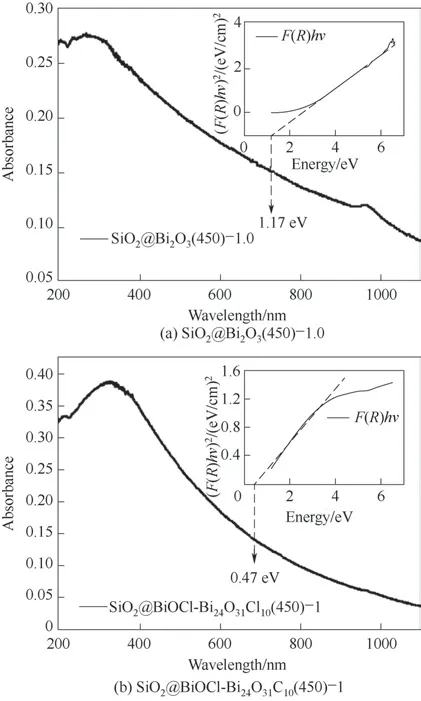
图9 Cl掺杂前后的SiO2@Bi2O3(450)-1.0产物的带隙图Fig.9 Band gap diagram of the SiO2@Bi2O3(450)-1.0 sample before and after Cl incorporation
2.6 光催化性能
为比较在可见光照射下上述样品对RhB 的降解活性和光催化性能,图10(a)、(c)、(e)以及图10(b)、(d)、(f)分别为光催化分解曲线以及表观速率常数图。如图10(a)所示,虽然SiO2@Bi2O3(450)-1.0 表现出了较好的光催化性能,但是对RhB 降解轻微,降解效率约10%,其光催化性能未达到预期。进一步选择掺入Cl 提高光催化性能,后续产物SBC-y选择450℃作为最佳热处理温度。图10(c)、(d)显示了SiO2@BiOCl-Bi24O31Cl10(450)-y随NaCl 用量不同对RhB 的降解曲线及其表观速率常数的变化。随着NaCl 用量的增加,摩尔比从1∶1∶1 到1∶1∶4 的光催化剂产物对RhB 的降解率呈逐渐下降趋势,其表观速率常数k也逐渐减小,其中摩尔比为1∶1∶1的产物SiO2@BiOCl-Bi24O31Cl10(450)-1,降解效率最快且45 min 降解量达到98.9% 左右,表观速率常数为0.08964;在此基础上,考察氨水用量对RhB 降解的影响,如图10(e)、(f)。发现随着氨水用量从0.5 ml逐步增加到3.0 ml,反应溶液的碱性不断提升,所合成出的光催化剂对RhB 降解率呈先下降后上升趋势,常数k的变化规律也如此。综合分析可以看出,本文掺入Cl 的合成反应体系中,在一定碱性的条件下,少量NaCl的加入便能大幅度提高其产物的光催化性能。

图10 不同热处理温度的SiO2@Bi2O3,不同投料摩尔比的SiO2@BiOCl-Bi24O31Cl10(450)-y和不同氨水添加量的SiO2@BiOCl-Bi24O31Cl10(450)-1-z对RhB的光催化降解曲线和表观速率常数Fig.10 The photocatalytic degradation curves and apparent rate constants of RhB obtained by SiO2@Bi2O3 with different heat treatment temperatures,SiO2@BiOCl-Bi24O31Cl10(450)-y with different feed mole ratios and SiO2@BiOCl-Bi24O31Cl10(450)-1-z with different ammonia additions
2.7 光催化机理
RhB 染料分子含有羧基(—COOH)和羟基(—OH)基团,能与SiO2@Bi2O3核壳微球表面的Bi2O3表面位点相连(通过表面—OH)。当它们强烈吸附在Bi2O3表面,导致染料在光照下产生光敏作用,然后光激发的e-和h+分别与染料溶液中的O2和H2O 分子反应生成活性氧自由基·O-2和羟基自由基·OH。光照过程中生成的·和·OH 等自由基有极强的氧化活性,能将有机污染物逐步降解生成CO2和H2O[28]。在合成过程中掺入Cl 后,后续产物的壳层为BiOCl和Bi24O31Cl10的复合物,Bi24O31Cl10和BiOCl 分别作为n 型和p 型光催化剂[29-30],当彼此接触时会在复合半导体界面附近产生空间电荷区,形成一个方向从n到p 的自建电场,该电场能使扩散到场区的光生载流子定向分离,电子逆着电场方向运动,向n型半导体一端集聚,而空穴顺着电场方向运动,在p型半导体一端集聚[31-32]。形成的p-n 异质结可以减少光生e--h+对的复合[33],从而提高所制备的复合光催化剂的光催化性能,其可能的光催化机理如图11 所示,在通过可见光照射激活后,光生e-从BiOCl 的价带(VB)迁移到其导带(CB),而h+保留在原VB 中,随后激发态e-注入Bi24O31Cl10的导带。在催化过程中,e--h+对会移动到光催化剂表面,通过氧化和分解发生光催化降解。其中,e-与O2反应生成·,·的产生可以消耗大量的光生e-,从而显著抑制光生载流子的复合,有利于光生h+引起的RhB氧化,通过中间反应不断与水反应生成·OH 自由基。另外,h+还与水反应形成·OH,这些自由基(·OH)会积极分解染料等有机化合物,因此更增强了对RhB的降解[34]。

图11 SiO2@BiOCl-Bi24O31Cl10核壳微球可能的光催化降解RhB机理Fig.11 Possible photocatalytic degradation of RhB by SiO2@BiOCl-Bi24O31Cl10 core-shell microspheres
3 结 论
本文设计了一种结构稳定且适应性广的SiO2@BiOCl-Bi24O31Cl10核壳结构的溶液合成方法。选取二甘醇作为稳定剂防止了Bi3+聚集并减缓了均相成核,通过改变热处理温度和投料比x来分别精准控制SiO2@Bi2O3复合材料的物质组成和形貌,其中热处理温度为450℃和投料比为1.0 时,形成的SiO2@Bi2O3核壳微球分散更均匀。为进一步提升光催化性能,选择Cl 掺杂改变SiO2@Bi2O3核壳微球的形貌和物质组成,通过微量调节氨水和NaCl用量探求最佳光催化性能下的配比,结果显示氨水用量为0.5 ml,SiO2、Bi(NO3)3·5H2O 和NaCl 的摩尔比为1∶1∶1 时达到了最佳参数配比,产物SiO2@BiOCl-Bi24O31Cl10微球对RhB 降解的光催化活性显著提高,对RhB 的45 min 降解率约98.9%。该研究为去除污水中有机染料提供了新的途径,在解决水污染问题方面具有一定的意义。
