TAVR术后患者发生明显急性肾损伤危险因素评估
2022-09-09周锦玲丘汉彬张萍珍
周锦玲 丘汉彬 张萍珍
主动脉瓣狭窄(aortic stenosis,AS)是一种涉及主动脉瓣的瓣膜性心脏病,主动脉瓣调节从左心室到主动脉及随后到身体其他部位的血流。主动脉狭窄导致主动脉瓣开口狭窄。典型症状是呼吸短促、疲劳、头晕或晕厥及胸痛[1-2]。这是老年人最常见的瓣膜病,如果不治疗,症状严重的主动脉瓣狭窄会导致高死亡率[3]。估计有12%的75岁以上的老年人患有主动脉瓣狭窄,这是目前美国老年人瓣膜置换最常见的原因[4-5]。几十年来,外科主动脉瓣置换术(surgical aortic valve replacement,SAVR)是治疗主动脉瓣狭窄的主要方法[6]。SAVR需要开胸手术、主动脉交叉夹闭和体外循环。SAVR的高手术死亡率使一些患者无法接受治疗。对于1/3不符合SAVR条件的主动脉瓣狭窄患者,医疗管理可以改善症状,但不能延长生命或减缓疾病进展。经导管主动脉瓣置换术(transcatheter aortic valve replacement,TAVR)是一种微创手术,可替代SAVR治疗无法手术或手术风险高的严重主动脉狭窄患者。研究表明,对于患有严重主动脉瓣狭窄的肾移植受者,与外科瓣膜置换术相比,TAVR具有较低的死亡率,第一次TAVR于2002年实施[6]。目前这种治疗已成为高风险严重AS患者的标准选择[7]。接受TAVR治疗的患者通常是老年人,这些患者进行SAVR的风险太高,而且考虑到与该人群相关的严重共病负担,确定TAVR术后不良结局的风险因素非常有意义,其中一个已经反复确定的预测因素是术后急性肾损伤(AKI)的发生[8]。TAVR后的AKI是一种已知的并发症,它与TAVR术后预后不佳相关[9]。因此,本研究主要通过探究影响TAVR术后患者发生明显AKI的危险因素,以期为该并发症的发生做出合理的预防和及时的处理,现报告如下。
1 资料与方法
1.1 一般资料
以北京大学深圳医院2020年1月-2021年5月接受TAVR的80例患者为研究对象,纳入标准:患有严重的主动脉瓣狭窄,并接受TAVR治疗;≥60岁,患有严重的钙化性主动脉瓣狭窄(主动脉瓣面积 <0.8 cm2,平均梯度 >40 mmHg 或喷射速度>4.0 m/s);有晚期主动脉瓣疾病的心脏症状。排除标准:二尖瓣或非钙化瓣;冠状动脉疾病需要血运重建;左室射血分数小于20%;主动脉环直径小于18 mm或大于25 mm;严重二尖瓣或主动脉瓣反流;有神经功能障碍;严重肾功能不全。通过患者接受TAVR术后是否发生明显AKI分为AKI组和非AKI组,AKI定义如下,1期:血肌酐(Scr)增加 1.5~2 倍,或增加 0.3 mg/dl(26.4 mmol/L),或尿量 <0.5 ml/(kg·h),持续时间 6~12 h;2 期:Scr增加 2~3 倍,或尿量 <0.5 ml/(kg·h),持续 12~24 h;3 期:Scr增加 3 倍或 Scr为 4 mg/dl(354 mmol/L),或持续 24 h 以上尿液输出 <0.3 ml/(kg·h),或无尿12 h。明显AKI被定义为2期或3期,无明显AKI被定义为1期。所有患者均签署知情同意书,且经北京大学深圳医院医学伦理委员会批准。
1.2 方法
所有患者根据外周动脉大小分别接受经股动脉或经升主动脉放置,使用专用输送导管和相同的人工瓣膜,将瓣膜通过左心室心尖上的肋间小切口放入心包。患者在手术期间接受肝素治疗,并在术后6个月接受双重抗血小板治疗(阿司匹林和氯吡格雷)。患者术前和术后接受静脉补水,预防性治疗如N-乙酰半胱氨酸,静脉碳酸氢盐的使用由执行该手术的医生决定。收集所有患者基线特征,主要包括年龄、性别、体重指数、体表面积、术前血清肌酐、肾小球滤过率(eGFR)、纽约心脏学会等级分级、共病(高血压、糖尿病、充血性心力衰竭、冠心病、脑血管病、外周血管疾病、慢性阻塞性肺疾病)、超声心电图数据(左室射血分数、主动脉瓣面积、收缩肺动脉压、主动脉环部内径、跨瓣压)、入路、麻醉状态、手术时间、对比剂用量、并发症(危及生命的心律失常、维持性低血压、主要及次要血管并发症)发生情况、最低血红蛋白和红细胞输注,估算eGFR用于评估肾功能。比较两组之间各因素的差异,并以差异有统计学意义的指标作为自变量,是否发生明显AKI作为因变量进行回归分析。
1.3 统计学处理
本研究均使用SPSS 22.0软件进行比较判断,计数资料如合并症人数等以率(%)表示,采用χ2/Fisher确切概率检验,计量资料如年龄等以(±s)表示,比较使用t检验。手术时间以中位数四分位数M(P25,P75)表示,进行Mann-WhitneyU检验,危险因素分析采用二元Logistic回归,若P<0.05则表示差异有统计学意义。
2 结果
2.1 TAVR术后急性肾损伤的发生率
TAVR术后7 d内,80例患者中有18例出现明显急性肾损伤,发生率为22.5%。平均发病时间为(2.00±1.46) d,发病时间分布在术后第 1、2、3、5、6天,发病例数分别为9、5、2、1、1例。
2.2 TAVR术后急性肾损伤的危险因素单因素分析
单因素分析显示,非AKI组出现慢性阻塞性肺疾病、主要及次要血管并发症发生率较AKI组明显更低,且手术时间更短,红细胞输注率更低,而跨瓣压较AKI组更高(P<0.05),见表1。
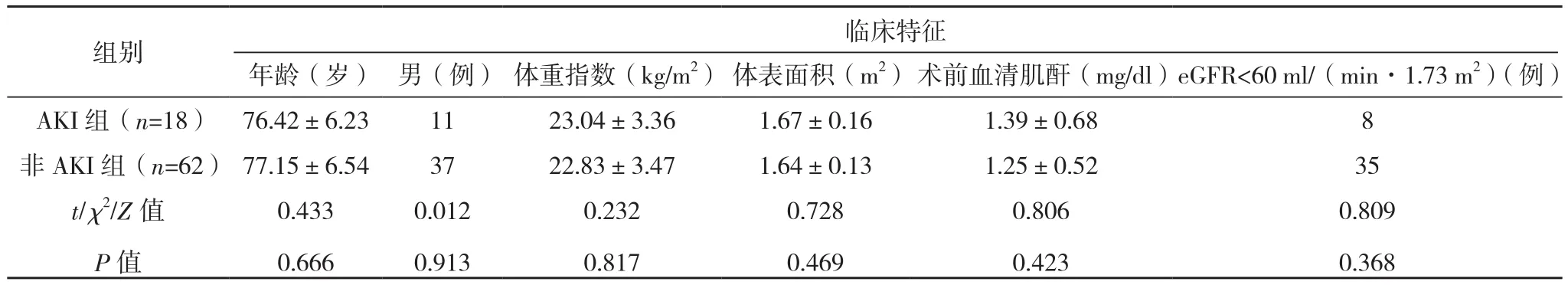
表1 TAVR术后患者急性肾损伤的危险因素单因素分析
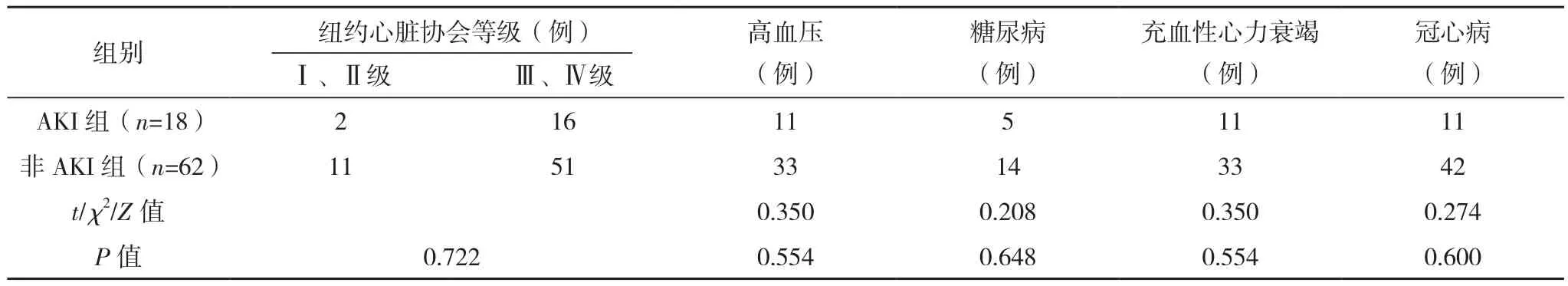
表1(续)

表1(续)
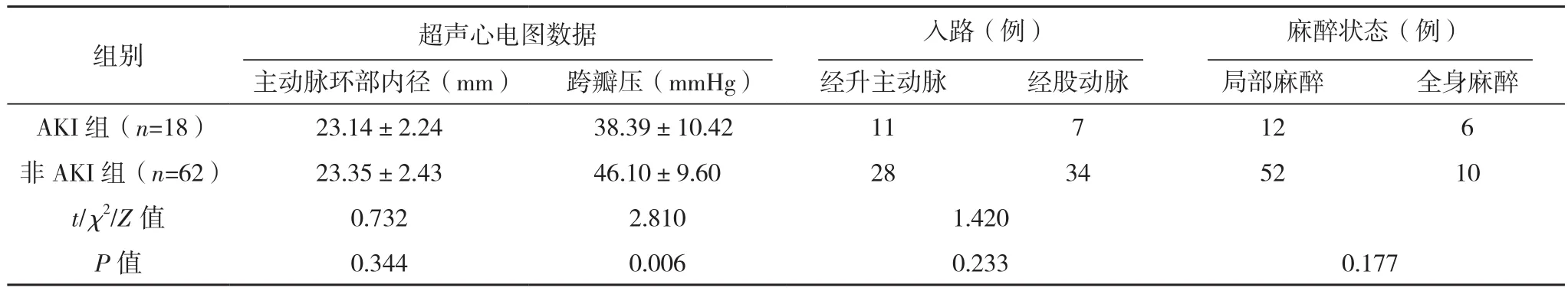
表1(续)
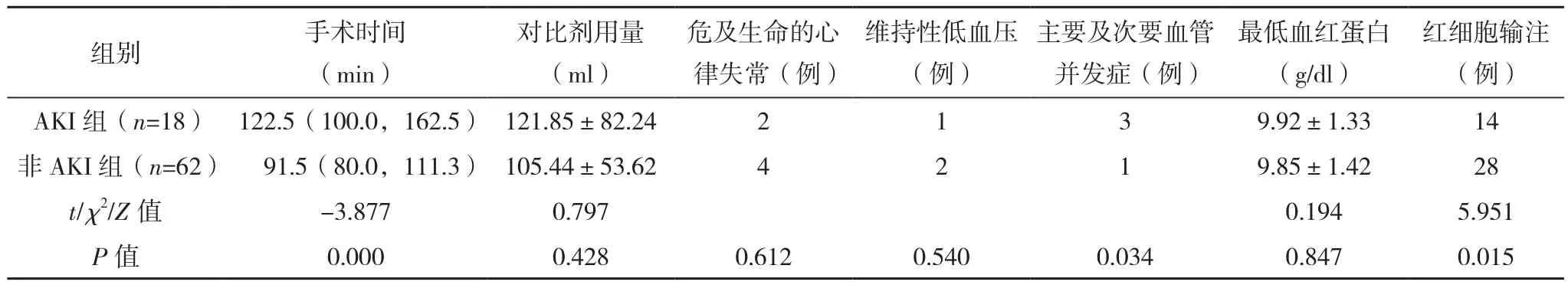
表1(续)
2.3 TAVR术后患者发生明显AKI的危险因素回归分析
将基本资料中的各项因素作为自变量,TAVR术后患者发生明显AKI作为因变量进行回归分析,主要及次要血管并发症、手术时间、慢性阻塞性肺疾病及红细胞输注是AS患者接受TAVR后出现明显AKI事件的独立危险因素(P<0.05),见表2。
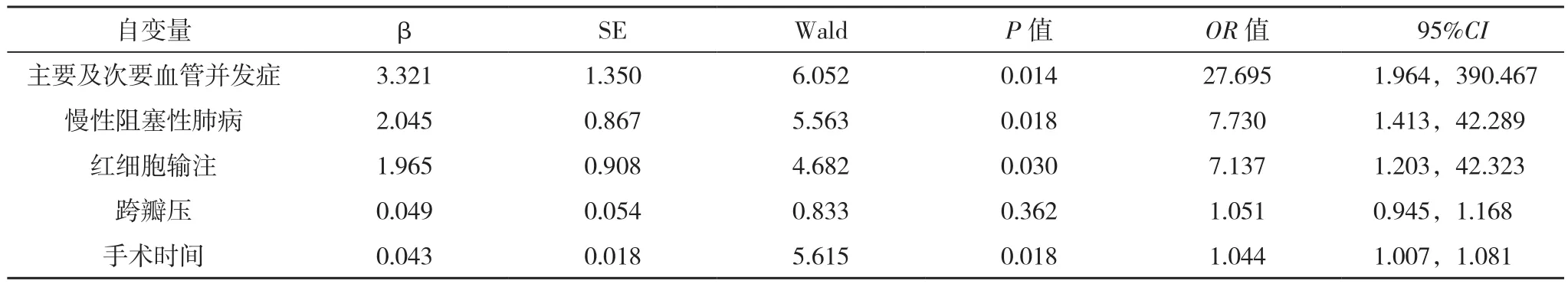
表2 TAVR术后患者发生明显AKI的危险因素Logistic回归分析
3 讨论
TAVI是一种新的治疗方法,适用于外科高危重症患者主动脉瓣狭窄,并且被广泛认为比外科瓣膜置换术具有更低的围手术期危险。它已成为严重主动脉瓣狭窄患者的一种安全有效的治疗选择。有Meta分析指出,TAVR和SAVR 2种手术方式对中低危患者短期和中期的死亡率无显著差异,但TAVR的并发症如卒中等的发生情况明显少于SAVR[10-11]。研究表明,TAVR后的AKI及其严重程度与不良预后相关。AKI持续时间(短暂或持续)及AKI严重程度是影响预后的独立因素[12]。AS主要以老年人为主体,他们经常有先前存在的肾功能损害和其他共同疾病,这会加重AKI的风险,但目前预测和预防这种并发症仍然具有挑战性。AKI的发生主要与早期死亡率增加有关,在手术过程中关注导致AKI的主要预测因素是预防患者发生急性围手术期危及生命的并发症的重要手段。本报告来自80例接受TAVR治疗的有严重主动脉狭窄的不能手术或高危患者队列,评估了TAVR术后AKI的发生率、预测因素和影响。TAVR后明显的AKI(2~3期)并不少见,据统计,TAVR术后AKI的发生率为5%~57%[13-14]。本研究明显AKI的发生率为22.5%。有报告称高血压增加接受体外循环心脏术患者发生院内AKI的风险,患者长时间血压过高会增大肾小球囊膜压力,引起肾小球发生纤维化,肾动脉血管逐渐硬化[15]。但本研究未发现高血压与TAVI后发生明显AKI的相关性,可能由于本研究样本量较少的缘故,需要进行更大样本量的进一步分析。从本研究可以看到,患者有慢性阻塞性肺疾病共病更易在术后发生明显AKI,慢性阻塞性肺疾病已被证明是接受心脏手术患者发生明显AKI的独立预测因子。有研究指出,慢性阻塞性肺疾病患者的肾血流量和肾小球滤过功能可能显著降低[16]。此外,慢性阻塞性肺疾病患者在围手术期更容易发生严重低氧血症和高碳酸血症,这可能导致肾功能进一步恶化。输注红细胞是公认的心脏手术后AKI的预测因子。通过本次试验观察到明显AKI患者对输血需求增加的趋势,与Babur等[16]结果一致。Aregger等[17]最近表明,输血次数也与TAVI后AKI风险增加相关。保存的红细胞经历渐进性的功能和结构变化,导致红细胞功能和活性降低,并积累炎症分子、游离铁和血红蛋白,所有这些变化可能导致肾功能不全,尤其是在肾自动调节受损的老年患者中。本研究表明,患者在TAVI过程中接受了红细胞输注,发生明显AKI风险大大增加。这一结果表明,在接受TAVI治疗时,应努力避免不必要的输血。此外,本研究意外发现,两组对比剂的用量比较,差异无统计学意义(P>0.05),明显AKI的发生与对比剂的用量无关,尽管如此,仍需尽量减少造影剂的用量,这对进一步降低TAVI后明显AKI的风险非常重要。
本研究中,AKI组在基线时的跨瓣压比非AKI组低10 mmHg左右。这一发现可能具有病理生理作用,较低的跨瓣压意味着更严重的疾病(低流量,低梯度),使患者在TAVR后更容易发生明显的AKI。然而,鉴于两组患者在基线时的射血分数相似,且本研究中患者例数较少,因此很难确定这一发现的确切性质(偶然性、关联性或因果关系),在多因素分析中也未见明显关联。此外,从本研究还可以看出,TAVI时间过长或手术过程中出现主要及次要血管并发症也会导致明显AKI发生率增加(P<0.05)。而这些因素的出现说明TAVI过程并不太顺利,这一发现表明,优化患者选择,改进植入和辅助技术,结合新兴的设备技术,可以显著减少出血并发症、血管并发症,最终减少明显AKI的发生。目前的分析有局限性,本研究患者人数少,限制了有意义和广泛的多变量分析的可能性回归分析。然而,在目前的模型中,围手术期出血和血管并发症与明显AKI之间的相关性仍然很强。此外,意外的混杂因素可能会影响试验的结果。因此,该研究结论还需要进一步研究进行验证。
综上所述,主要及次要血管并发症、手术时间、慢性阻塞性肺疾病及红细胞输注是严重主动脉瓣狭窄患者接受TAVR后出现明显AKI事件的独立危险因素。因此临床上应重点关注,尽量减少这些因素带来的风险,减少明显AKI事件的发生
