18岁以下患者使用头孢他啶阿维巴坦的安全性文献分析
2022-09-09贾号褚娜英韩洁陈慧慧刘源
贾号,褚娜英,韩洁,陈慧慧,刘源
商丘市第一人民医院,商丘 476100
多重耐药菌(multi~drug resistant organism,MDRO)是指对抗菌谱范围内三类或三类以上的抗菌药物不敏感的细菌。MDRO 极大地增加了医院抗感染的治疗难度 ,严重影响了患者的临床治疗效果和预后[1~2]。近年来,儿童患者中耐碳青霉烯类肠杆菌科(carbapenem~resistantEnterobacteriaceae,CRE)细菌感染越来越受到人们的关注。据《中国儿童细菌耐药监测组2019年儿童细菌耐药监测》[3]数据显示,儿童中非新生儿CRE检出率为7.6%,稍低于同期成人患者;新生儿CRE检出率为7.0%,接近同期成人患者检出率。目前,针对儿童抗CRE感染治疗可选用的药物有限,多是在成人研究的基础上超说明书用药[4],提示儿童抗MDRO感染仍面临极大挑战。新型抗菌药物头孢他啶阿维巴坦(ceftazidime avibactam,CAZ/AVI)于2019年9月在我国获批用于治疗CRE感染、革兰阴性菌感染尤其是耐药菌引起的严重感染。CAZ/AVI适应症主要为18岁及以上患者由敏感革兰阴性菌引起的复杂性腹腔内感染、复杂性尿路感染、医院获得性肺炎和呼吸机相关细菌性肺炎。目前,CAZ/AVI用于儿童MDRO感染的临床经验较少。基于此,本研究收集了国内外报道的使用CAZ/AVI的18岁以下病例,对其使用CAZ/AVI的安全性予以归纳分析,以期为临床合理用药提供参考。
1 资料与方法
1.1 资料来源
文献研究:中文以药品名“头孢他啶阿维巴坦”,再以“儿童”“婴幼儿”“早产儿”“新生儿”为范围,检索中国知网(CNKI)、万方数据库和维普数据库(VIP);英文以药品名“ceftazidime avibactam”,再以“children” “newborn”“premature infant”为范围,检 索 PubMed、ScienceDirect、Embase、Wiley Online Library数据库,均从建库检索至2022年3月。纳入标准:①18岁以下患者。②采用CAZ/AVI治疗,并且治疗后有安全性相关描述者。排除标准:重复的文献、综述。
1.2 研究方法
本研究对患者的性别、年龄、诊断、病原菌类型、用药方法、合并用药、药品不良反应(adverse drug reaction,ADR)/不良事件(adverse event,AE)发生情况等进行描述性汇总分析;根据2011年发布的《药品不良反应报告和监测管理办法》[5]、2020年发布的《药物临床试验质量管理规范》[6]的标准,对疑似CAZ/AVI引起的ADR/AE进行关联性评价,分析ADR/AE的严重程度和特点,并利用帕累托图法对其累及系统器官进行分析。ADR类型分为一般的、严重的、新的;AE分为一般的AE、严重不良事件(serious adverse event,SAE)、可疑非预期严重不良事件(suspected unexpected serious adverse events,SUSAE)。帕累托原理亦称“二八原理”,指80%的价值来自20%的因子。根据帕累托原理将相关影响因素分为A、B、C三类,A类为主要因素,影响程度累及构成比为0%~80%;B类为次要因素,影响程度累及构成比为80%~90% ;C类为一般因素,影响程度累及构成比为90%~100%。
2 结果
2.1 文献收集和患者临床资料
本研究共检索到有关文献16篇,排除重复的文献、综述7篇,共纳入文献9篇[7~15],收集病例176例(见图1和表1)。其中,检索到1项多中心、开放性、单剂量研究的I期临床试验[15],患者32例;检索到2项随机对照试验的Ⅱ期临床试验[13~14],患者 128例;检索到 1篇回顾性分析文献[11],患者8例;检索到5篇个例文献报道[7~10,12],患者 8 例。在明确统计性别的病例中,男性和女性分别占45.83%(77/168)和54.17%(91/168);统计病例涉及人群均为18岁以下患者,包括儿童、婴幼儿、新生儿、早产儿。176例诊断均为MDRO的重症感染,以肺部感染、血流感染为主,其次是中枢感染、骨髓炎、化脓性关节炎、腹腔感染、复杂性尿路感染等。此类感染病原菌不唯一,多以CRE为主,还包括多重耐药鲍曼不动杆菌(multi~resistantAcinetobacter baumannii,MDR~AB)、多重耐药的铜绿假单胞菌(multi~resistantPseudomonas aeruginosa,CRPA)。CAZ/AVI给药途径主要为静脉滴注,合并用药种类较多,如替加环素、美罗培南、磷霉素、阿米卡星、多黏菌素等。

图1 文献检索流程图
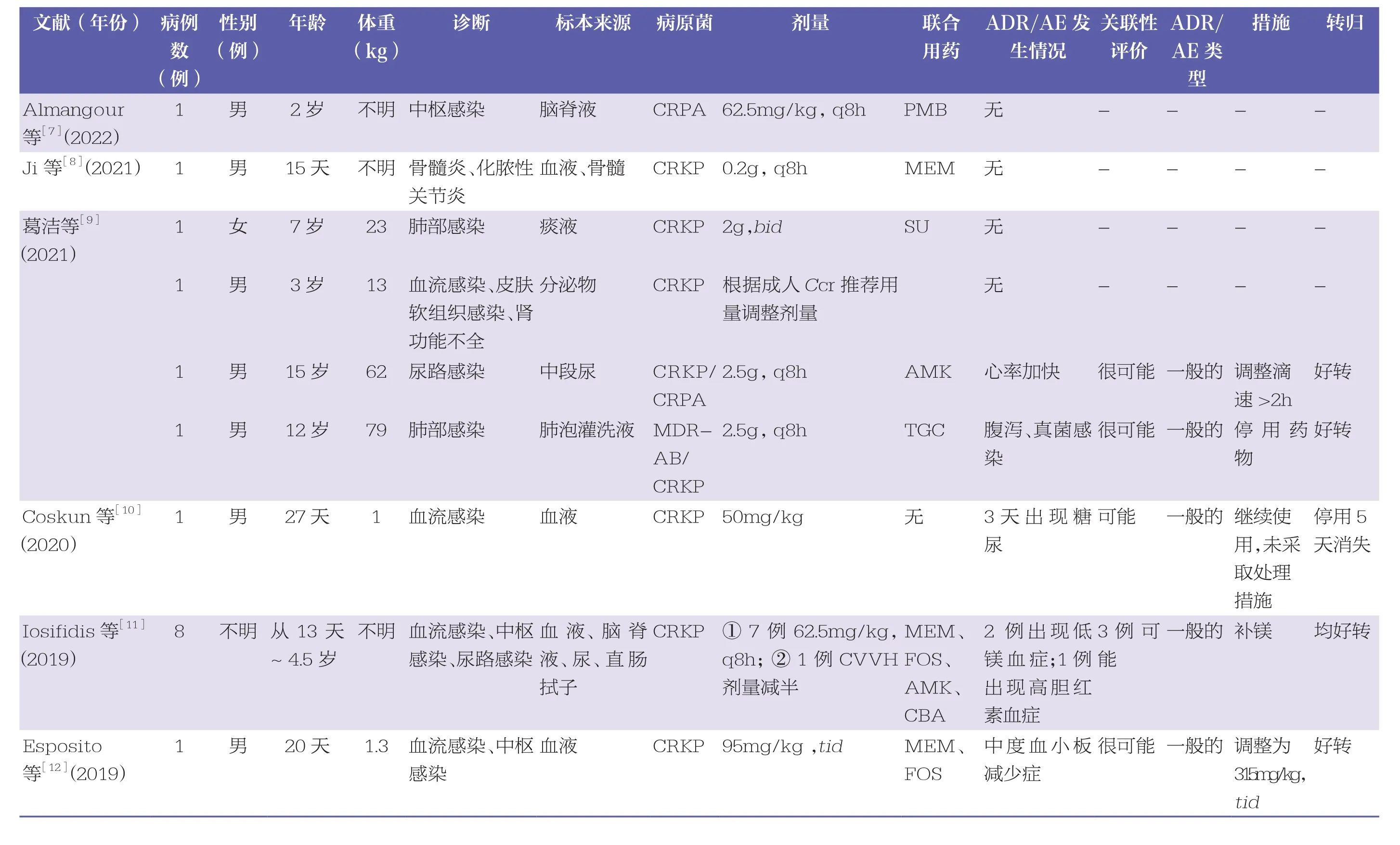
表1 18岁以下患者使用CAZ/AVI的病例资料

续表
2.2 18岁以下患者使用CAZ/AVI的安全性分析
2.2.1 ADR/AE关联性评价及发生情况
收集的176例病例中,共有21例发生ADR/AE,均发生在使用CAZ/AVI后,符合CAZ/AVI已有ADR的报道[16];5例停用或减量后症状表现逐渐减轻或消失;16例未停药,给予对症处理后症状表现逐渐消失。症状表现不可用患者病情的进展来解释。因此,判定21例ADR/AE是由CAZ/AVI引起,总发生率为11.93%(21/176),其中5例为很可能相关,16例为可能相关。类型以一般的ADR/AE为主[11.36%(20/176)],发生1例由CAZ/AVI引起的SAE,发生率为0.57%(1/176)。Ⅰ~Ⅱ期临床试验共涉及160例患者,其中AE 74例,14例考虑与使用CAZ/AVI有关;用于临床治疗的病例共16例(个例报道8例,回顾性研究8例),7例发生了一般的ADR。ADR/AE多发生在用药后数天,最早于用药后3天出现。均为已知的ADR,未发生新的ADR/AE,无导致死亡的病例。
2.2.2 ADR/AE累及系统器官情况
参照 ADR/AE 累及系统器官命名规则[5~6,17],ADR/AE累及系统器官主要有胃肠疾病(5例);肝胆疾病(3例);皮肤及皮肤附件疾病(3例);血液系统疾病(3例);神经系统疾病(2例);心血管疾病(2例);代谢及营养疾病(2例);免疫疾病及感染(1例);尿路疾病(1例),见表2。18岁以下患者使用CAZ/AVI的ADR/AE表现与成人使用CAZ/AVI发生的ADR类似,未发现新的、致死的ADR/AE。ADR/AE临床表现构成比帕累托图分析见图2。

表2 ADR/AE累及系统器官构成比 n=22
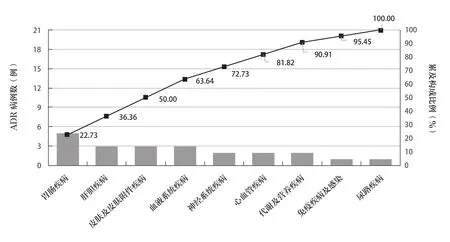
图2 ADR/AE累及系统器官构成比帕累托图分析
2.2.3 ADR/AE的治疗与转归情况
本研究收集文献中发生的一般的ADR/AE多数未经特殊处理,在治疗结束后可自行好转。其中,2例中止药物治疗:1例在使用CAZ/AVI第 2 天出现中度头晕、恶心和呕吐,遂停用CAZ/AVI,患者症状逐渐好转[14];1例使用CAZ/AVI 11天后出现肠道真菌感染、腹泻,停用后逐渐好转[9]。4例给予对症处理后好转:2例患者出现低镁血症,给予补镁对症治疗后血镁恢复正常[11];1例患者在输注CAZ/AVI过程中出现心率过快,给予减慢滴速(滴注时间>2h)后心率逐渐恢复正常[9];1例患者在使用8天后出现中度血小板减少,减少给药剂量(由95mg/kg,tid减为31.5mg/kg,tid)后血小板计数逐渐恢复[12]。其余一般的ADR/AE均未采取特殊处理措施,继续采用CAZ/AVI治疗,ADR/AE在几天后或治疗结束后逐渐好转[10,13~15]。CAZ/AVI引起1例SAE,表现为严重的神经系统症状,文献未描述具体表现,发生在输注CAZ/AVI开始后的几天,出现后立即停药,3天后患者恢复正常[14]。该患者有继发多囊肾病的焦虑、抑郁和高血压病史,且参加研究前出现过类似神经系统疾病。
3 讨论
3.1 CAZ/AVI在治疗儿童MDRO感染中的地位
儿童MDRO感染是临床治疗上的难题,目前尚无统一的抗菌药物推荐。CAZ/AVI作为第三代头孢菌素和新型β~内酰胺酶的复合制剂,能够治疗由大肠埃希菌、肺炎克雷伯菌、阴沟肠杆菌、弗氏柠檬酸杆菌复合体、奇异变形杆菌和铜绿假单胞菌等细菌引起的感染[16]。阿维巴坦是一种非β~内酰胺酶抑制剂,能够抑制Ambler A类[如超广谱β~内酰胺酶(extended~spectru beta~lactamases,ESBLs)]以及一些C和D类丝氨酸水解酶[如苯唑西林酶~48型,oxacillinase~48(OXA~48 )],大幅降低了头孢他啶对CRE的最低抑菌浓度(minimun inhibitory concentration, MIC),并能减弱由头孢菌素(AmpC)酶或ESBLs引发的头孢他啶耐药[18],但对产金属酶的 CRE 无效[19]。CAZ/AVI在儿童CRE感染的治疗中具有重要的临床价值,CAZ/AVI不仅对非金属酶的CRE临床治疗效果较好,在产金属酶的CRE中也发挥重要作用。大多数产金属酶的CRE菌株同时产生A类酶和D类酶,阿维巴坦可有效抑制丝氨酸碳青霉烯酶,目前已有CAZ/AVI和氨曲南联合使用治疗产生NDM、 CRE的成功案例报道[20]。自2019年9月起,美国食品药品监督管理局(FDA)批准了CAZ/AVI用于儿童 CRE感染[21],对于肾功能正常的3~6个月龄患儿,每次治疗剂量为50mg/kg;对于肾功能正常的6个月~18岁的患者,每次治疗剂量为62.5mg/kg,均为q8h。Iosifidis等[11]的回顾性临床研究,报道了使用CAZ/AVI成功治疗8例CRE感染的13天~4.5岁患儿。本研究还收集到2项随机对照研究,1项针对97例3个月~18岁并被确诊为严重泌尿道感染的患者进行的II期临床研究,其中67例单独使用CAZ/AVI进行治疗[14];另1项为针对83例3个月~18岁的复杂腹腔感染的患者进行的II期临床研究,其中61例使用CAZ/AVI联合甲硝唑进行治疗[13]。研究结果提示两组使用CAZ/AVI治疗的病例均取得了较好的临床治疗效果,且患者对CAZ/AVI的耐受性良好,与单独使用头孢他啶的安全性一致。
3.2 ADR/AE发生情况及应对措施分析
根据CAZ/AVI说明书,CAZ/AVI最常见的ADR是恶心、呕吐、腹泻、发热、腹痛、消化不良等胃肠道症状,并有阴道念珠菌感染、氨基转移酶升高、皮疹、失眠等神经系统症状和静脉炎等。本研究所收集病例的ADR/AE与CAZ/AVI说明书中成人的临床表现相似[16]。患者病例包括新生儿到18岁的患者,累及系统器官的主要因素为胃肠疾病、肝胆疾病、皮肤及皮肤附件疾病、血液系统疾病,提示对于伴有胃肠疾病或肝功能异常等基础病的患者使用该药时应加强监护及防治。CAZ/AVI引起的ADR/AE类型以一般的为主,多数未采取特殊措施,仅有3例因ADR/AE的发生而导致治疗中断:1例为使用CAZ/AVI 11天后出现继发的肠道真菌感染,表现为腹泻,停药后逐渐好转[9];1例为使用第 2 天出现中度头晕、恶心和呕吐,遂停药,患者症状逐渐好转[14];1例为使用CAZ/AVI数天后出现严重的中枢神经系统症状,出现后立即停药,3天后患者恢复正常,该患者有焦虑、抑郁病史,并于参加研究前出现过类似神经系统疾病[14],提示既往有神经系统疾病的患者使用CAZ/AVI更易发生神经系统症状,应密切监测。
FDA仅推荐CAZ/AVI用于3个月以上的儿童,本研究共收集到11例新生儿~4.5岁的儿童使用CAZ/AVI的资料,其中个案报道3例,均为新生儿;回顾性病例分析8例[11],年龄从13天~4.5岁,平均年龄为53天。其中,1例新生儿治疗3天出现糖尿,未采取特殊处理措施,治疗结束停用药物5天后糖尿逐渐消失[10],提示可能是由于在使用CAZ/AVI中出现肾小管功能的可逆性损害。11例病例中,共有5例新生儿发生ADR,均为一般的ADR,但发生率较高[45.45%(5/11)]。使用剂量超过FDA 批准的3~6个月患儿按体重给药的推荐剂量,因此,新生儿ADR发生率高不排除与使用剂量过高有关。从目前数据来看,新生儿使用CAZ/AVI的推荐剂量有待更多的临床研究证实。
通过文献检索发现,CAZ/AVI在18岁以下患者中临床治疗效果较好,且有良好的安全性;ADR的发生情况与成人使用CAZ/AVI情况相似,以一般的为主,多数可自行恢复;未发现潜在的严重ADR,但新生儿中ADR发生率较高。目前,由于临床资料有限,在我国CAZ/AVI用于儿童CRE感染的治疗方案,特别是在新生儿中的使用剂量仍需进一步探索,以期为18岁以下患者MDRO感染的治疗提供更佳选择。
