双黄连注射剂中异绿原酸C致敏兔抗体效价测定
2022-09-09邓颖颖徐丽婷赵晓佳张恩户陈世忠
邓颖颖,徐丽婷,赵晓佳,张恩户,陈世忠
(1.陕西省西安国际医学中心医院药学部,西安 710100;2.陕西中医药大学药理教研室,咸阳 712046;3.北京大学药学院天然药物学系,北京 100083)
双黄连注射剂的主要组成成分为金银花、黄芩、连翘,具有抑菌、抗炎等药理作用,临床用于外感风热所致发热、咳嗽等疾病的治疗[1-5]。然而,随着临床的广泛应用,有关其不良反应的报道也随之增多。崔盈盈等[6]应用关联规则Apriori算法发现,患者在使用双黄连注射剂后不良反应发生率占比约为5.62%。马婷[7]对辽宁某医院254例中药不良反应病例做了调查报道,发现病例所累及的器官、系统中以皮肤损害最为常见,占比高达53.87%,共计146例,临床表现多为皮疹、瘙痒等。双黄连注射剂组成成分复杂,导致过敏反应的具体成分至今尚不明确,有研究[8]指出,致敏成分的存在,是引起过敏反应的主要原因之一。北京大学陈世忠教授团队采用“在线化合物-牛血清白蛋白(BSA)荧光检测活性筛选”系统对双黄连注射剂中的化合物进行在线BSA结合活性筛选,通过对结合常数、结合位点、化合物与BSA结合强度等的测定和计算,分析出异绿原酸C具有疑似半抗原活性。本实验是在体外制得异绿原酸C抗血清,模拟双黄连注射剂进入家兔体内的致敏过程。运用ELISA法检测原理考证双黄连注射剂中疑似半抗原物质异绿原酸C是否具有致敏性。
1 资料与方法
1.1 材料
1.1.1 仪器与试剂 酶标仪(美国BioTek公司,型号Synergy LX);异绿原酸C(中国科学院成都生物研究所,生产批号:MUST-14111414);金黄色葡萄球菌细胞壁蛋白A交联的辣根过氧化物酶(HRP-SPA,北京博尔西科技有限公司,GP:2020.11.02);弗氏佐剂(美国SIGMA公司,10 mL,SLBD0736);兔免疫球蛋白E(IgE)ELISA试剂盒(上海酶联生物科技有限公司,GP:2020.12.30);牛血清白蛋白(BSA,上海顺勃生物工程技术有限公司,GP:2020.11.28)等。
1.1.2 实验动物 第四军医大学实验动物中心提供的体质量在2.5~3.5 kg的普通级雄性新西兰白兔,实验动物质量合格证号:No.61000400000021,生产许可证号:SCXK(军)20120007。动物分笼饲养,保持12 h昼夜节律,自由饮水摄食。
1.2 实验方法
1.2.1 异绿原酸C-血浆蛋白全抗原的制备 制备致敏前血清,先将家兔置于兔固定桶内固定,用乙醇擦拭耳朵,使其上的动脉扩张、清晰,采血10 mL。精密称取2 mg的异绿原酸C,用0.6 mL生理盐水将其溶解,制成每毫升生理盐水含有3.3 mg异绿原酸C的溶液,将0.4 mL的致敏前血清与配制好的异绿原酸C溶液混合,37℃温育2 h,然后将温育后的溶液与1 mL弗氏佐剂用漩涡混合器震荡,使其充分乳化混合。
1.2.2 异绿原酸C特异性抗体的测定 对家兔首次免疫使用的是现制备好的抗原液,用剃毛机将距离兔子背部脊柱线3 cm处的毛发处理干净,露出粉色皮肤,事先在脊柱两侧用标记笔每隔2 cm均匀地标记10个点,然后用注射器在标记处每点注射0.2 mL抗原液,注射完成后皮肤处有皮丘出现则代表免疫成功,第2天发现,家兔皮肤表面皮丘转变为结痂,随着时间的更迭,家兔皮肤逐渐恢复。10 d以后,对家兔进行加强免疫,使用与首次免疫剂量相同的弗氏不完全佐剂乳化的抗原液,之后每间隔1周对家兔进行1次加强免疫,加强免疫进行5次后,间隔7 d时间,麻醉家兔进行手术,用注射器自其腹主动脉采血,高速离心机分离全血,取上清液即制得异绿原酸C-血浆蛋白全抗原的抗血清。
1.2.3 试剂的配制1)制备Na2CO3缓冲溶液:取1.465 g Na2CO3和0.795 g NaHCO3置于50 mL量瓶中,用双蒸水将其完全溶解并定容至刻度处;2)制备2%BSA液:取一个50 mL量瓶,称取1 g BSA置于其中,用浓度为0.15 mol·L-1pH 7.4的磷酸盐缓冲液(PBS)将其溶解并定容至刻度处;3)制备磷酸盐吐温缓冲液(PBST):取一个100 mL量瓶,量取0.05 mL Tween20置于其中,用浓度为0.15 mol·L-1pH 7.4的PBS将其溶解并定容至刻度处;4)制备HRP-SPA、底物液、终止液。
1.2.4 抗体效价的检测方法[9]1)包被:将异绿原酸C-血浆蛋白全抗原用Na2CO3缓冲液稀释4倍作为包被原,取一块96孔板,将制备好的包被原用移液枪每孔滴加110 μL,置于冰箱4℃温度中包被过夜,取出96孔板,甩尽孔内的液体,然后用PBST洗涤,3次/4 min,每孔滴加2%BSA 130 μL,置于4℃冰箱中封闭过夜;2)加抗血清:洗涤结束后,每孔加入抗血清100 μL(用0.15 mol·L-1pH 7.4的PBS按1∶1~1∶128的比例逐倍稀释),37℃温育2 h;3)加酶标二抗:洗涤结束后,每孔加入100 μL HRP-SPA,37℃水预锅内孵育1 h;4)显色、终止、测定;5)判定:加致敏前血清的孔设置为阴性对照孔,不加血清的孔设置为空白对照孔,每个样品设置5个平行对照孔,阳性的评判准则为:相对于阴性对照孔OD≥2倍。
1.2.5 间接竞争ELISA测定抗体特异性 每孔滴加1 mg·mL-1的异绿原酸C-血浆蛋白110 μL作为包被原,封闭洗涤,用0.9%的NaCl2溶液将配制好的4 mg·mL-1的异绿原酸C溶液逐倍稀释至0.25 mg·mL-1,然后将稀释后的不同浓度溶液每孔加入50 μL,每孔再加入按1∶1稀释的抗血清100 μL,37℃孵育2 h;洗涤3次结束后,每孔加入100 μL按1∶200稀释的酶标抗体HRPSPA,37℃孵育1 h;洗涤、显色、终止、测定。加稀释液的孔设置为阳性对照孔,不加异绿原酸C的孔设置为阴性对照孔,并设置5个平行对照孔。应用公式I=(阴性对照孔OD-样品OD)/(阴性对照孔OD-阳性对照孔OD)×100%[10]计算异绿原酸C的抑制率I(%)。绘制抑制曲线的依据是,取异绿原酸C浓度的对数值作为横坐标,抑制率作为纵坐标。通过回归分析,建立回归方程并计算相关系数R2、IC5(0即指抑制率为50%时所对应的异绿原酸C浓度)、检测限(IC10)。
1.2.6 测定IgE型抗体浓度 本实验中,家兔IgE的水平由IgE ELISA试剂盒测定所得,详细操作依据说明书步骤进行。
1.3 统计学方法
采用SPSS 17.0统计学软件进行数据分析,计量资料以均数±标准差(±s)表示,组间比较采用t检验。P≤0.01为差异有统计学意义。
2 结果
2.1 兔抗异绿原酸C抗血清的效价测定
将兔抗异绿原酸C抗血清按1∶1逐倍稀释至1∶128,结果仍显示为阳性,说明外源性的抗体在家兔血清中已经产生。将稀释后的各组兔抗异绿原酸C血清抗体效价值与致敏前血清效价(OD值)进行比较,差异均有统计学意义(P均<0.01),从结果分析中得出,异绿原酸C具有致敏性,见表1。
2.2 间接竞争ELISA结果
2.2.1 建立回归方程I=0.430 lgC+0.319,R2=0.997,半数抑制浓度IC50=2.628 mg·mL-1,IC10=0.309 mg·mL-1,见图1。异绿原酸C随着浓度的增大对抗血清的抑制率逐渐升高,提示抗血清中的抗体是针对该药物产生的,具有特异性,见表2、图1。
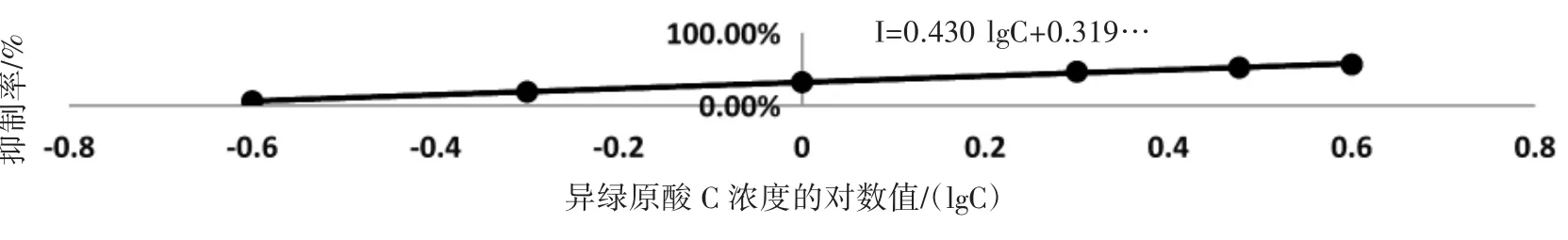
图1 异绿原酸C抑制率曲线
表1兔抗异绿原酸C血清效价测定(±s)
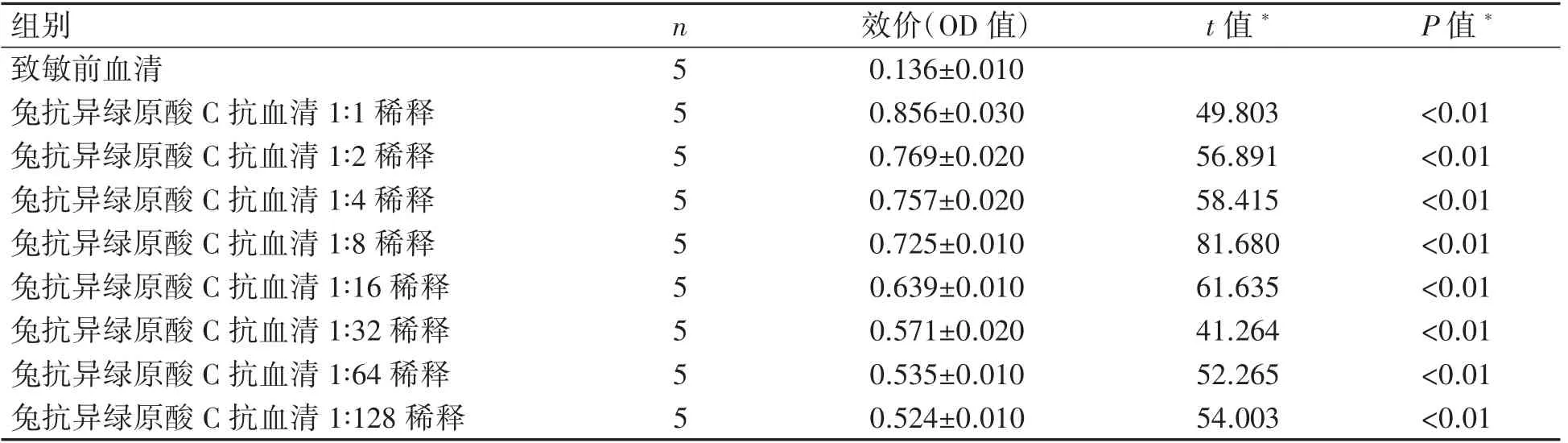
表1兔抗异绿原酸C血清效价测定(±s)
*为与致敏前血清效价(OD值)比较。
组别 n 效价(OD值) t值* P值*致敏前血清 异绿原酸C抗血清1∶1稀释 异绿原酸C抗血清1∶2稀释 异绿原酸C抗血清1∶4稀释 5 0.136±0.010兔抗5 0.856±0.030 49.803 <0.01兔抗5 0.769±0.020 56.891 <0.01兔抗5 0.757±0.020 58.415 <0.01兔抗异绿原酸C抗血清1∶8稀释 5 0.725±0.010 81.680 <0.01兔抗异绿原酸C抗血清1∶16稀释 5 0.639±0.010 61.635 <0.01兔抗异绿原酸C抗血清1∶32稀释 5 0.571±0.020 41.264 <0.01兔抗异绿原酸C抗血清1∶64稀释 5 0.535±0.010 52.265 <0.01兔抗异绿原酸C抗血清1∶128稀释 5 0.524±0.010 54.003 <0.01
表2异绿原酸C对抗血清的特异性研究(±s)
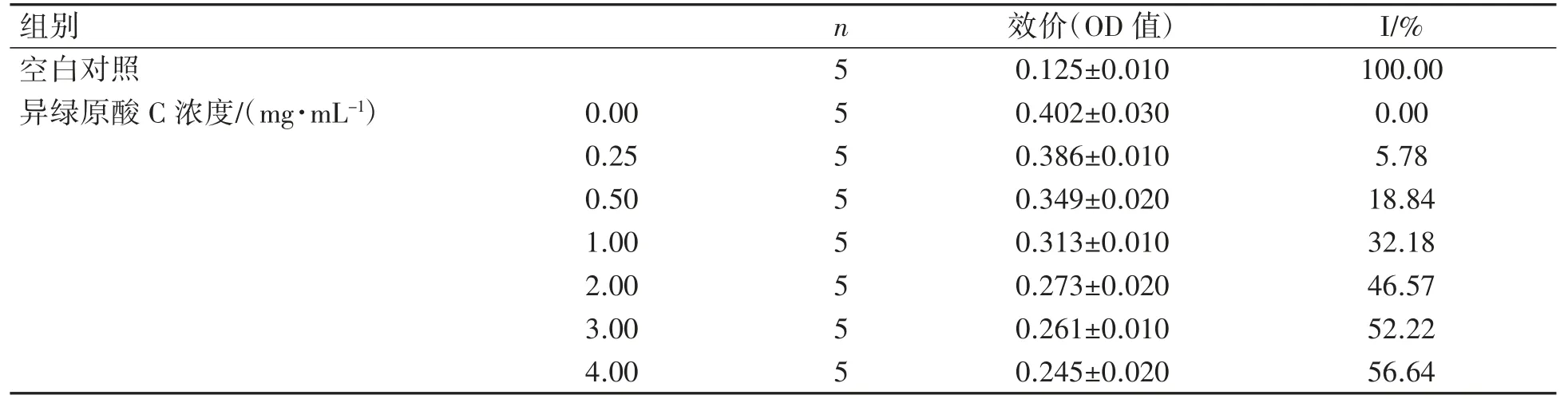
表2异绿原酸C对抗血清的特异性研究(±s)
组别 n 效价(OD值) I/%空白对照 5 0.125±0.010 100.00异绿原酸C浓度/(mg·mL-1) 0.00 5 0.402±0.030 0.00 0.25 5 0.386±0.010 5.78 0.50 5 0.349±0.020 18.84 1.00 5 0.313±0.010 32.18 2.00 5 0.273±0.020 46.57 3.00 5 0.261±0.010 52.22 4.00 5 0.245±0.020 56.64?
2.2.2 依据回归方程计算样本对应的IgE型抗体浓度 通过回归分析,建立曲线方程:Y=1.849X2+13.344X-0.308,R2=0.999,其中X代表效价(OD值),Y代表对应IgE型抗体浓度。空白组效价(OD值)为0.172,IgE型抗体浓度为2.038 μg·mL-1,异绿原酸C组效价(OD值)为0.398,IgE型抗体浓度为5.295 μg·mL-1,依据IgE型抗体浓度提高率=(C-C空白)/C空白,C空白代表未经过免疫的正常家兔血清检测出的浓度值,C代表异绿原酸C抗血清中IgE型抗体的浓度,计算得出,提高率达159.81%。
3 讨论
中药有组成成分复杂,致敏成分不确切,致敏机制不同的特性[11-12]。中药注射剂的有效成分通常为小分子物质而不具有免疫原性,但可能与体内的活性代谢产物蛋白质结合而形成超分子化合物,直接或通过药物代谢酶分解后与蛋白类载体连接形成载体复合物-超分子半抗原,进而通过抗原处理、提呈及免疫细胞的识别、增殖和反应等一系列机制诱发免疫应答发生[13],本实验应用该原理在体外制得异绿原酸C抗血清,模拟双黄连注射剂进入家兔体内所发生的一系列致敏过程,结果表明,异绿原酸C的抗体效价高于致敏前血清OD值的2倍,说明异绿原酸C有潜在的致敏性。间接竞争ELISA法测定抗体特异性结果表明,异绿原酸C免疫后的家兔抗血清中的抗体具有一定的特异性。IgE型抗体浓度的测定结果表明,经过多次免疫后的家兔体内产生了外源性IgE型抗体。综上所述,在本实验条件下双黄连注射剂中疑似半抗原物质异绿原酸C具有致敏性。运用ELISA法具有一定的通用性和可操作性,为日后研究双黄连注射剂中的致敏成分提供了借鉴方法。
