厚朴酚糖苷化衍生物的合成及生物信息学分析*
2022-09-05罗浩成杨诗雯张勇民董登祥
罗浩成,杨诗雯,李 军,张勇民,董登祥
(1贵州中医药大学药学院,贵州 贵阳 550001;2巴黎第六大学法国国家科研中心,巴黎 75005)
厚朴酚(magnolol)为烯丙基连苯二酚类物质,作为传统中药材中主要的有效活性成分,其具有多种药理作用,如抗炎[1]、抗肿瘤[2-3]、促进胃动力[4]、抗菌[5-6]、抗氧化[7]、降血糖[8]、降脂[9]、抗抑郁[10]、抗银屑病[11]、抗龋齿[12]等,拥有良好的开发前途和广阔应用前景。然而受限于厚朴酚水溶解性不好,故难以形成合适的给药剂型,生物利用度不高,生物活性并未得到充分的开发和利用,影响厚朴酚在临床上的应用,造成当前厚朴酚并无成熟可靠的临床应用剂型。因此,制备其衍生物以期提高水溶性,提高药理活性,为后续厚朴酚临床运用提供重要的基础支撑。
此前已有许多学者对厚朴酚进行了结构修饰与改造,如郭明鑫[13]等人通过对厚朴酚与和厚朴酚的酚羟基进行修饰,引入酯基、酰肼、1,3,4-噁二唑等结构,为天然产物的减毒增效衍生化设计提供了新的思路。庄文豪[14]在厚朴酚中酚羟基、苯基的基础上,合成一系列烯丙基被氧化的厚朴酚衍生物,结果表明厚朴酚衍生物抑菌活性均有所增加。但目前对于厚朴酚糖基化改造及修饰的研究较少。糖类化合物作为维持生命进程的重要物质之一,不仅仅是能量供给的来源,也同样参与许多生物识别过程,例如蛋白质折叠、细胞间通讯、细菌粘附等。此外其还参与形成具有生物学意义的生物分子,如糖蛋白、肽聚糖[15]。由于天然糖类化合物异头位置构型有α、β的区别,往往混杂在一起难以分离,所以纯天然糖类化合物的实用性仍然不足以应对日益增长的治疗需求。通过合成的方式,可获得大量结构明确及纯度高的糖化合物。且通过合成糖片段再与天然药物连接的手段,可为药物研究者提供一种改善天然化合物的水溶性、药物活性及药代动力学的新思路[16-17]。因此,化学合成是获取复杂的寡糖和糖类衍生物的重要来源。近年来,许多学者通过利用网络药理学将小分子化合物与系统生物学、计算机科学结合起来,采用生物信息学方法“药物-靶点-疾病”的靶标预测模型,能够系统地阐述药物与疾病的作用机制与作用靶点,为接下来的实验提供数据支持与道路指引[18-19]。
因此,本课题通过对mag结构进行糖基化修饰,引入多羟基水溶性基团(如葡萄糖、半乳糖、麦芽糖等)及用糖化学保护基团取代保护mag双羟基,以期改善厚朴酚难溶于水以及易氧化的特性;提高生物利用度、水溶性和稳定性;同时对3个糖苷衍生物进行生物信息学分析,为接下来的药理学实验提供道路指引。
1 实验部分
1.1 仪器与试剂
BSM220.4电子天平(上海卓精电子科技有限公司)、INOVA-500MHz超导核磁共振波谱仪(安捷伦科技有限公司)、OBS-2200旋转蒸发仪(倍捷科技(上海)有限公司)、FINNIGANLACQ-DECA质谱仪(美国菲尼根质谱公司)、721G-100紫外分光光度计(上海仪电分析仪器有限公司)、TL-200B电阻超纯水机(深圳亿利有限公司)、WTF-203B三用紫外分析仪(上海精科实业有限公司)。
D-(+)-半乳糖(AR批号20160712国药集团化学试剂有限公司)、D-(+)-麦芽糖(BR批号20170410天津大茂化学试剂厂)、D-(+)葡萄糖(AR批号20161219国药集团化学试剂有限公司)、吡啶(AR批号20140511国药集团化学试剂有限公司)、醋酸酐(AR批号20140923国药集团化学试剂有限公司)、三氯乙腈(AR批号20160402国药集团化学试剂有限公司)、三氟化硼乙醚(AR批号20171113国药集团化学试剂有限公司)、乙硫醇(AR批号20160814国药集团化学试剂有限公司),2,3,4,6-四-O-乙酰基-1-O-D-吡喃葡萄糖三氯乙酰亚胺酸酯(α),2,3,4,6-四-O-乙酰基-1-O-D-吡喃半乳糖三氯乙酰亚胺酸酯(β),2,3,4,6-四-O-乙酰基-β-D-吡喃葡萄糖-(1→4)-1,2,3,6-四-O-乙酰基-D-吡喃葡萄糖三氯乙酰亚胺酸酯(γ),实验室自制。
1.2 目标化合物合成(图1)
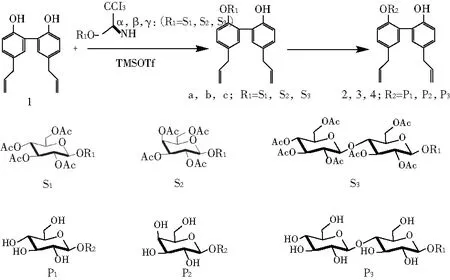
图1 目标化合物的合成路线Fig.1 Synthetic routes of the target compounds
(1)化合物2的合成
称量100 mg(0.38 mmol)mag和280 mg(0.57 mmol)化合物α,加入50 mL反应瓶内,加入100 mg活化过的4ÅMS和一个搅拌子,真空泵抽真空干燥0.5 h,通入惰性气体N2保护反应体系。加入约15 mLDCM作为溶剂溶解底物,在0 ℃的冰水混合浴中平衡反应10 min,然后加入5 μL(0.026 mmol)催化剂TMSOTf。反应用TLC跟踪点板,展开剂Cy∶EtOAc=3∶2。约1 h后,监测到反应完成,Rf值为0.53。加入饱和碳酸氢钠溶液中和体系中的三氟甲磺酸至pH中性,萃取过滤浓缩得粗产物,过硅胶柱纯化粗产物,过柱用洗脱剂为Cy和EtOAc混合配置(体积比3∶1)。得到白色粉末状固体物质89 mg,即化合物a,产率为39.28%。
称量500 mg金属Na,用Cy洗去表面煤油,快速加入装有50 mLMeOH的烧杯中,制得MeONa溶液。称量60 mg(0.10 mmol)化合物a,加入25 mL反应瓶内,放入搅拌子,加5 mL甲醇作溶剂溶解底物,然后缓慢倒入刚刚制备的MeONa溶液,直至反应体系pH值到达11~13之间。在r.t.条件下搅拌进行反应,TLC监测跟踪反应进程,展开剂Cy∶EtOAc=2∶3。约1 h后,监测到反应物消耗完毕,反应完成,Rf值为0。反应体系中加入强酸型阳离子交换树脂中和MeONa,使得体系pH中性,用MeOH作为溶剂,过滤除去树脂,减压旋蒸浓缩溶剂,粗产物用交联右旋葡聚糖HL-20凝胶柱纯化,得到淡黄色固体物质38.05 mg,即化合物2,产率88.86%,m.p.131~134 ℃。
波谱解析:ESI-MSm/z:451.2{[M+Na]+};
1H NMR(600 MHz,DMSO)δ:7.35 - 7.39(d,J =8.2Hz,3H,6-H,12-H,4- H),7.29(s,1H,10-H),7.20(s,1H,3-H),7.12(s,1H,9-H),7.06- 7.08(d,J =8.0Hz,2H,14-H,17-H),5.41(s,1H,1′-H),4.91(s,1H,OH),4.25 - 4.27(d,J =13.9Hz,4H,15-H,18-H),3.81(s,1H,2′-H),3.67(s,1H,5′-H),3.59(s,2H,6′-H),3.46(s,1H,3′-H),3.42(s,1H,4′-H),3.04(s,4H,13-H,16-H),2.51(s,1H,4H,OHGlu-H)
13C NMR(151 MHz,DMSO)δ:174.38(C2),173.69(C8),132.96(2C,C14,C17),130.52(C11),129.32(C12),128.40(C7),98.24(2C,C15,C18),97.26(C9),96.80(C3),92.46(C1′),75.56(C5′),72.42(C2′),71.23(C3′),70.53(C4′),61.58(C6′),39.81(2C,C13,C16)
(2)化合物3的合成
称量100 mg(0.38 mmol)mag和280 mg(0.57 mmol)化合物β,加入50 mL反应瓶内,加入100 mg活化过的4ÅMS和一个搅拌子,真空泵抽真空干燥0.5 h,通入惰性气体N2保护反应体系。加入约15 mLDCM作为溶剂溶解底物,在0 ℃的冰水混合浴中平衡反应10 min,然后加入5 μL(0.026 mmol)催化剂TMSOTf。反应TLC跟踪点板,展开剂Cy∶EtOAc=3∶2。约1 h后,监测到反应完成,Rf值为0.53。加入饱和碳酸氢钠溶液中和体系中的三氟甲磺酸至pH中性,萃取过滤.浓缩得粗产物,过硅胶柱纯化粗产物,过柱用洗脱剂为Cy和EtOAc混合配置(体积比3∶1)。得到白色粉末状固体物质96 mg,即化合物b,产率为42.37%。
称量500 mg金属Na,用Cy洗去表面煤油,快速加入装有50 mL甲醇的烧杯中,制得NaOMe溶液。称量60 mg(0.10 mmol)化合物b,加入25 mL反应瓶内,放入搅拌子,加5 mL甲醇作溶剂溶解底物,然后缓慢倒入刚刚制备的NaOMe溶液,直至反应体系pH值到达11~13之间。在r.t.条件下搅拌进行反应,TLC监测跟踪反应进程,展开剂Cy∶EtOAc=2∶3。约1 h后,监测到反应物消耗完毕,反应完成,Rf值为0。反应体系中加入强酸型阳离子交换树脂中和甲醇钠,使得体系pH中性,用MeOH作为溶剂,过滤除去树脂,减压旋蒸浓缩溶剂,粗产物用交联右旋葡聚糖HL-20凝胶柱纯化,得到淡黄色固体物质36.69 mg,即化合物3,产率85.69%,m.p.133~139 ℃。
波谱解析:ESI-MSm/z:451.2{[M+Na]+};
1H NMR(600 MHz,DMSO)δ:7.39(s,2H,6-H,12-H),7.38(s,1H,10-H),7.35(s,1H,4-H),7.34(s,1H,9-H),7.21(s,1H,3-H),7.08-7.11(d,J=29.2Hz,2H,14-H,17-H),5.43(s,1H,1′-H),4.79(s,1H,OH),4.53(s,4H,15-H,18-H),3.82(s,1H,5′-H),3.73(s,1H,2′-H),3.23(s,2H,CH2Gal-H),2.97(s,1H,3′-H),2.73(s,1H,4′-H),2.57(s,2H,13-H),2.50(s,2H,16-H),2.10-2.15(m,4H,OHGal-H)
13C NMR(151 MHz,DMSO)δ:174.24(C2),173.49(C8),138.17(2C,C14,C17),134.26(C11),129.68(C12),129.35(C10),127.91(2C,C4,C6),126.80(C7),123.32(C1),102.44(2C,C15,C18),98.89(C9),97.85(C3),92.84(C1′),75.18(C2′),70.28(C3′),69.90(C5′),68.49(C4′),61.03(C6′),39.80(2C,C13,C16)
(3)化合物4的合成
称量100 mg(0.38 mmol)mag和462 mg(0.57 mmol)化合物γ,加入50 mL反应瓶内,加入100 mg活化过的4ÅMS和一个搅拌子,真空泵抽真空干燥0.5 h,通入惰性气体N2保护反应体系。加入约15 mLDCM作为溶剂溶解底物,在0 ℃的冰水混合浴中平衡反应10 min,然后加入5 μL(0.026 mmol)催化剂TMSOTf。反应TLC跟踪点板,展开剂Cy∶EtOAc=3∶2。约1 h后,监测到反应完成,Rf值为0.57。加入饱和碳酸氢钠溶液中和反应体系中的三氟甲磺酸至pH中性,萃取过滤浓缩得粗产物,过硅胶柱纯化粗产物,过柱用洗脱剂为Cy和EtOAc混合配置(体积比3∶1)。得到白色粉末状固体物质127 mg,即化合物c,产率为37.79%。
称量500 mg金属Na,用Cy洗去表面煤油,快速加入装有50 mL甲醇的烧杯中,制得NaOMe溶液。称量120 mg(0.14 mmol)化合物c,加入50 mL反应瓶内,放入搅拌子,加10 mL甲醇作溶剂溶解底物,然后缓慢倒入刚刚制备的NaOMe溶液,直至反应体系pH值到达11~13之间。在r.t.条件下搅拌进行反应,TLC监测跟踪反应进程,展开剂Cy∶EtOAc=2∶3。约0.5 h后,监测到反应物消耗完毕,反应完成,Rf值为0。反应体系中加入强酸型阳离子交换树脂中和甲醇钠,使得体系pH中性,用MeOH作为溶剂,过滤除去树脂,减压旋蒸浓缩溶剂,粗产物用交联右旋葡聚糖HL-20凝胶柱纯化,得到淡黄色固体物质73.38 mg,即化合物4,产率91.62%,m.p.103~107 ℃。
波谱解析:ESI-MSm/z:613.2 {[M+Na]+};
1H NMR(600 MHz,DMSO)δ:7.40(s,2H,6-H,12-H),7.20(s,1H,4-H),7.07(s,1H,10-H),6.68-6.70(d,J18.1Hz,2H,3-H,9-H),6.35(s,2H,14-H,17-H),5.46(s,1H,1′-H),5.31(s,1H,1″-H),5.01(s,1H,OH),4.92-4.95(dd,J=35.4,6.9Hz,4H,15-H,18-H),4.53(s,1H,5′-H),4.39(s,1H,2′-H),3.68(s,1H,5″-H),3.61(s,1H,2″-H),3.48(s,1H,3′-H),3.37(s,4H,6″-H,6′-H),3.35(s,1H,3″-H),3.32(s,1H,4″-H),3.29(s,2H,13-H),3.21-3.25(dd,J=17.7,10.6Hz,2H,16-H),3.07(s,1H,4′-H),2.51-2.58(d,J=1.7Hz,7H,7OHMal-H)
13C NMR(151 MHz,DMSO)δ:150.57(C2),150.14(C8),135.84(2C,C14,C17),133.74(C11),132.89(C5),131.59(C12),131.06(C10),130.06(2C,C4,C6),129.49(C7),129.37(C1),128.64(2C,C15,C18),127.32(C9),127.16(C3),102.03(C1′),101.60(C1″),97.48(C2″),92.70(C5′),75.41(C2′),74.69(C5″),73.87(C3′),73.31(C3″),72.86(C4″),72.00(C4′),61.68(C6′),60.68(C6″),40.53(2C,C13,C16)
2 网络药理学预测厚朴酚衍生物抗中枢神经损伤的作用机制
2.1 厚朴酚衍生物作用靶点的预测
使用TargetNet平台,通过导入化合物的结构,对厚朴酚糖苷化衍生物(化合物2,3,4)进行靶点预测,取prob>0.5,得到潜在靶点。
2.2 中枢神经损伤靶点的建立
通过Genecardds在线数据库和OMIM数据库,搜索关键词“中枢神经损伤”,得到人类中枢神经损伤相关靶点基因,取Relevance>1,两者结果合并并删除重复数据。
2.3 疾病-药物网络构建
使用R软件进行“疾病-药物”靶点分析,进行交集操作,得到相同靶点,做出韦恩图,将靶点输入Uniprot数据库,得到交集靶标的gene symbol,以用于后续分析。
2.4 核心靶基因的筛选与PPI网络的构建
用String平台处理交集靶点,选择物种为“智人”,设置最小阙值为0.7,得到蛋白交叉作用,并构建靶标的PPI网络。接着用R软件筛选节点数最大(即交互关系最多)的几种靶标,并构建柱形图。
2.5 GO富集分析与KEGG信号通路富集分析
利用R软件将交集gene symbol转换为entrezID。使用DAVID数据库对得到的entrezID进行GO富集分析和KEGG信号通路富集分析,用R软件对其可视化处理。
3 结果与讨论
3.1 化学合成
本实验共合成厚朴酚糖苷衍生物3种,均未有文献记载,均通过1H-NMR、13C-NMR和MS确定结构,在酚类的糖基化反应中,与其他糖基供体相比,三氯乙酰基亚胺酸盐供体的合成更困难,但通常收率更高,尤其是使用更复杂的酚进行糖基化反应时,三氯乙酰基亚胺酸盐供体明显优于其他供体。因此酚类糖基化反应优先三氯乙酰亚胺酸盐方法进行糖苷化反应。
使用三氯乙酰亚氨基进行的糖基化反应,可能发生亚氨酸酯的酸催化重排,如葡萄糖与mag反应时可能出现N-三氯乙酰基吡喃葡萄糖胺副产物。在实验过程中,我们尝试了改变溶剂,反应温度或促进剂等手段来避免这种副产物。最后发现,在使用三氯乙酰胺基吡喃葡萄糖供体的情况下,仅使用β-糖苷,不使用α-糖苷,可以明显减少副产物的量,TLC检识表明几乎无副产物产生。
3.2 厚朴酚衍生物抗中枢神经损伤的作用机制
3.2.1 化合物2,3,4的结果
预测得到化合物2靶标74个,化合物3靶标21个,化合物4靶标25个,和“中枢神经损伤”靶点7137个,结果用R软件交集,化合物2得到62个交叉靶点,化合物3得到13个交叉靶点,化合物4得到17个交叉靶点,用生物信息学方法进行交集,线条表示之间存在关系,白色圆形框表示药物,黑色圆形框表示疾病,绘制韦恩图如图2。

图2 化合物与中枢神经损伤作用的靶点韦恩图Fig.2 Venn diagram of the targets of the compounds and CNS injury
3.2.2 PPI的构建
为了研究靶点之间在人体内的相互作用关系,将药物(化合物2,3,4)和疾病的交集靶点输入STRING平台中,设置阙值大于0.7,然后对潜在靶点进行PPI网络分析。化合物2共得到60个靶点之间存在相互关系,化合物3共得到12个靶点之间存在相互关系,化合物4共得到15个靶点之间存在相互关系。图3清晰表明了基因靶点之间的相互关系。

图3 化合物的PPI网络图Fig.3 PPI network diagrams of the compounds
用R软件处理得到PPI网络的核心基因,如图4。

图4 化合物的PPI网络核心基因图Fig.4 PPI network core gene map of the compounds
3.2.3 药物-疾病靶点的GO富集分析
将交互靶点映射入DAVID数据库中,进行GO生物过程富集分析,如图5(以各通路p.adjust大小排序)。

图5 化合物治疗中枢神经损伤作用的主要GO富集分析网络图Fig.5 Major GO enrichment analysis network of the treatment of CNS injury by the compounds
结果表现出,化合物2的交互靶点主要生物学功能有:蛋白质丝氨酸/苏氨酸激酶活性、蛋白质丝氨酸/苏氨酸/酪氨酸激酶活性、葡萄糖跨膜转运蛋白活性等。化合物3的交互靶点主要生物学功能有:碳酸盐脱水酶活性、葡萄糖跨膜转运蛋白活性、己糖跨膜转运蛋白活性等。化合物4的交互靶点主要生物学功能有:嘌呤能受体活性、葡萄糖跨膜转运蛋白质活性等。
3.2.4 药物-疾病靶点的KEGG分析
将交互靶点映射入DAVID数据库中,进行KEGG信号通路富集分析,如图6(以各通路0p.adjust大小排序)。
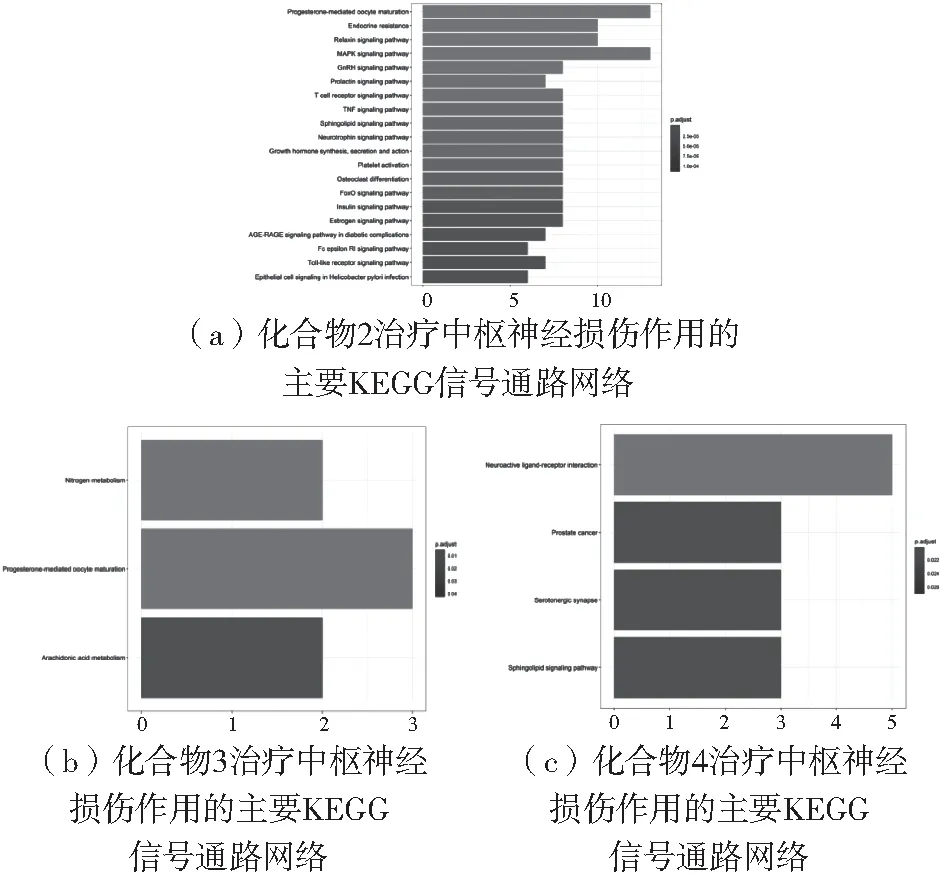
图6 化合物治疗中枢神经损伤作用的主要 KEGG信号通路网络Fig.6 Major KEGG signaling pathway network of the treatment of CNS injury by the compounds
结果表现出,化合物2的交互靶点主要信号通路有:孕激素介导的卵母细胞成熟通路、内分泌抵抗通路、松弛素信号通路等。化合物3的交叉靶点信号通路有:孕激素介导的卵母细胞成熟通路、氮代谢通路、四烯酸代谢通路。化合物4的交互靶点信号通路有:5-羟色胺能突触通路、神经活性配体-受体相互作用通路等。
以化合物4中p.adjust值最小的KEGG信号通路Neuroactive ligand-receptor interaction为例,作化合物4对中枢神经损伤作用的通路图,如图7。
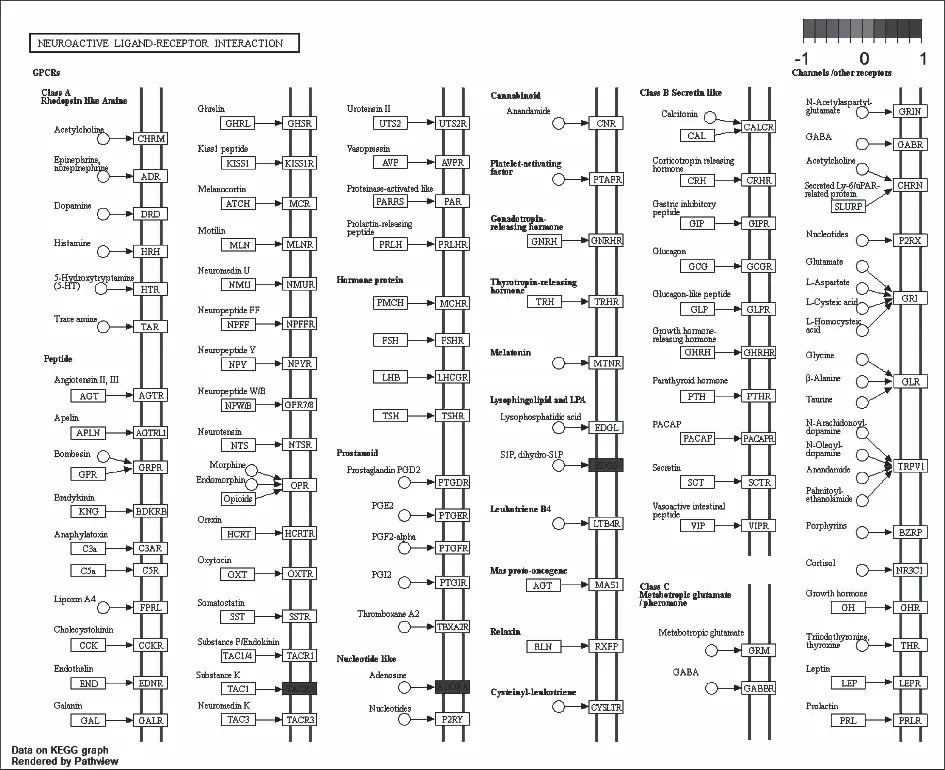
图7 化合物4对中枢神经损伤作用的通路图Fig.7 Pathway diagram of the effect of compound 4 on CNS injury
3.3 评价分析
3种化合物治疗中枢神经损伤疾病的共同潜在靶点有6个,为花生四烯酸-15-脂加氧酶(ALOX15)、碳酸酐酶9(CA9)、热休克蛋白90α(HSP90AA1)、前列腺素G/H合酶1(PTGS1/COX-1)、钠葡萄糖共转运载体1(SLC2A1)和钠葡萄糖共转运载体2(SLC5A2)。
综合上述的生物信息学GO生物过程分析数据,可以得到治疗作用的主要生物过程4条,即肾上腺素能受体活性、碳酸盐脱水酶活性、钠转运体活性和氧化还原酶活性。
根据之前3种糖苷化衍生物模拟出的KEGGPATHWAY数据,可以得出4条主要的信号通路,即氮素代谢、孕酮介导的卵母细胞形成代谢路径、5-羟色胺能突触和鞘脂信号通路。
4 结论
本研究合成了3种化合物,均为文献未报道的糖苷衍生物,已通过1H-NMR、13C-NMR及MS确认结构,通过本方法改善了水溶性差等问题,丰富了厚朴酚衍生物的种类,继而通过借助生物信息学的大数据方式,确定了mag糖苷化衍生物治疗中枢神经损伤的主要潜在靶点6个,主要潜在生物过程4条,主要潜在信号通路4条。为下一步WB和ELISA等药理学手段验证提供了依据,进而验证本研究所预测筛选出来的结果。以期对厚朴酚衍生物进一步进行药效学研究利用。
