克唑替尼治疗c-MET扩增合并ALK融合肺黏液腺癌1例
2022-09-05桂再欢冷哲枫戴元荣
桂再欢,冷哲枫,戴元荣
温州医科大学附属第二医院育英儿童医院 呼吸与危重症医学科,浙江 温州 325027
肺癌是世界上发病率和病死率最高的肿瘤之一,肺癌中有80%~90%为非小细胞肺癌(non-small cell lung cancer, NSCLC)[1],而肺黏液腺癌则是一种少见的特殊类型的肺腺癌,其年轻患者更为罕见。由于肺腺癌对化疗敏感性较差以及化疗所带来的不良反应众多,使得人们不断探索更多肺癌治疗的可能方法。自2004 年以来,研究者发现分子靶向治疗作为驱动基因指导下的治疗,具有“个体化”和“精准化”的优点,相比于传统化疗药物有较好的疗效。细胞间质上皮转化因子(cellarmesenchymal epithelial transition factor, c-MET)是肝细胞生长因子的酪氨酸激酶受体,位于人染色体7q21-q31,由α亚基和β亚基以二硫键形式连接[2]。c-MET通路异常激活主要包括MET14 外显子跳跃突变、MET扩增和MET蛋白过表达3 种类型,此三种突变均可导致肿瘤的发生。研究发现存在c-MET扩增的NSCLC可能对以间变性淋巴瘤激酶(anaplastic lymphoma kinase, ALK)、ROS1为主要靶点的酪氨酸激酶抑制剂克唑替尼敏感[3-5]。查阅PubMed、Web of Science、中国知网等文献数据库后,我们发现国内关于克唑替尼治疗c-MET扩增和ALK融合的黏液腺癌患者的报道很少。现笔者报告l例c-MET基因扩增阳性合并ALK融合阳性的局部晚期肺黏液腺癌患者,经克唑替尼治疗1个月后,肺部病灶完全缓解。
1 病例资料
患者,女,26岁,因“体检发现左肺部占位1 d”于2019年9月18日入院。胸部CT提示:左肺上叶占位性病变,大小为4.7 cm×3.5 cm,无咳嗽咳痰、胸痛咯血等不适。入院后于左肺下舌段行经支气管镜肺活检术,病理见少许游离黏膜上皮及纤维结缔组织伴炎细胞散在,未见恶性肿瘤细胞;同日行肺穿刺活检,病理报告:黏液腺癌。2019年9月25日PET/CT示左肺上叶后段不规则软组织肿块影,氟代脱氧葡萄糖(fludeoxyglucose, FDG)代谢增高。余器官FDG代谢未见异常。诊断为“左肺黏液腺癌”,术前分期T2bN0M0,IIA期。2019年10月8日于我院胸外科行“胸腔镜下左肺上叶切除+淋巴结清扫术”(见图1)。术中见肿瘤大小为5.2 cm×3.8 cm×4.0 cm,术后病理报告:左肺上叶周围型低分化黏液腺癌,癌组织侵及胸膜。支气管淋巴结(0/4),左第5组淋巴结(0/2),左第6组淋巴结(0/2),左第7组淋巴结(2/7)癌转移,左第10组淋巴结(0/1),左第11组淋巴结(0/1)。免疫组化结果显示:CD31(-)、CD56(-)、CDX-2(-)、CK20(-)、CK7(+)、D2-40(-)、Ki-67(5%~10%+)、Musin-2(-)、NapsinA(+)、p40(-)、p63(-)、S-100(-)、TTF-1(+)、Villin(-)。术后分期为sT3N2M0,IIIB期。肿瘤组织基因检测结果显示:ALK(Exon19)-EML4(Exon21),突变丰度9.98%。

图1 患者术前和术后胸部CT图像
患者为局部晚期肺癌,因经济问题,拒绝靶向治疗,2019年10月23日开始予含铂双药术后辅助化疗,化疗期间消化道反应明显,辅助化疗4周期完成后继续随访3个月,2020年5月于当地医院复查胸部CT提示纵隔淋巴结肿大,为求进一步评估,2020年5月28日再次行PET/CT提示纵隔双侧多发淋巴结转移,纵隔淋巴结较前增大,提示疾病进展。由于消化道反应明显,患者拒绝继续化疗,考虑基因检测为ALK融合突变,予阿来替尼600 mg 2次/d。2021年8月复查CT示:右肺散在慢性感染及多发结节,纵隔淋巴结肿大,于我科住院抗感染治疗5 d,并行超声内镜引导下的经支气管针吸活检(endobronchial ultrasound-guided transbronchial needle aspiration, EBUS-TBNA),7组及4R组淋巴结细胞蜡块见NSCLC细胞,2021年9月8日复查胸部CT提示两肺感染,多发结节,较2021年8月有所进展,转移可能,纵隔淋巴结肿大、融合。2021年9月15再次行CT引导下肺穿刺活检,病理报告为中-低分化肺腺癌;免疫组化:CK7(+)、TTF-1(+)、NapsinA(弱+)、CK5/6(-)、p40(-)、Ki-67(约80%+)。肿瘤组织基因检测提示MET扩增,拷贝数3.09,ALK(Exon20)-EML4(Exon20),突变频率2.97%,ALK(Exon19)-EML4(Exon21),突变频率9.95%,靶向治疗疗效评价为疾病进展。患者ALK融合突变及c-MET基因扩增,根据美国国家综合癌症网络(National Comprehensive Cancer Network, NCCN)指南,予克唑替尼250 mg,每天2次,口服,用药1个月后于2021年11月23日行胸部CT提示较2021 年9 月8 日两肺结节及纵隔、肺门淋巴结肿大基本吸收(见图2)。随访至2022年2月19日,未复发及转移。
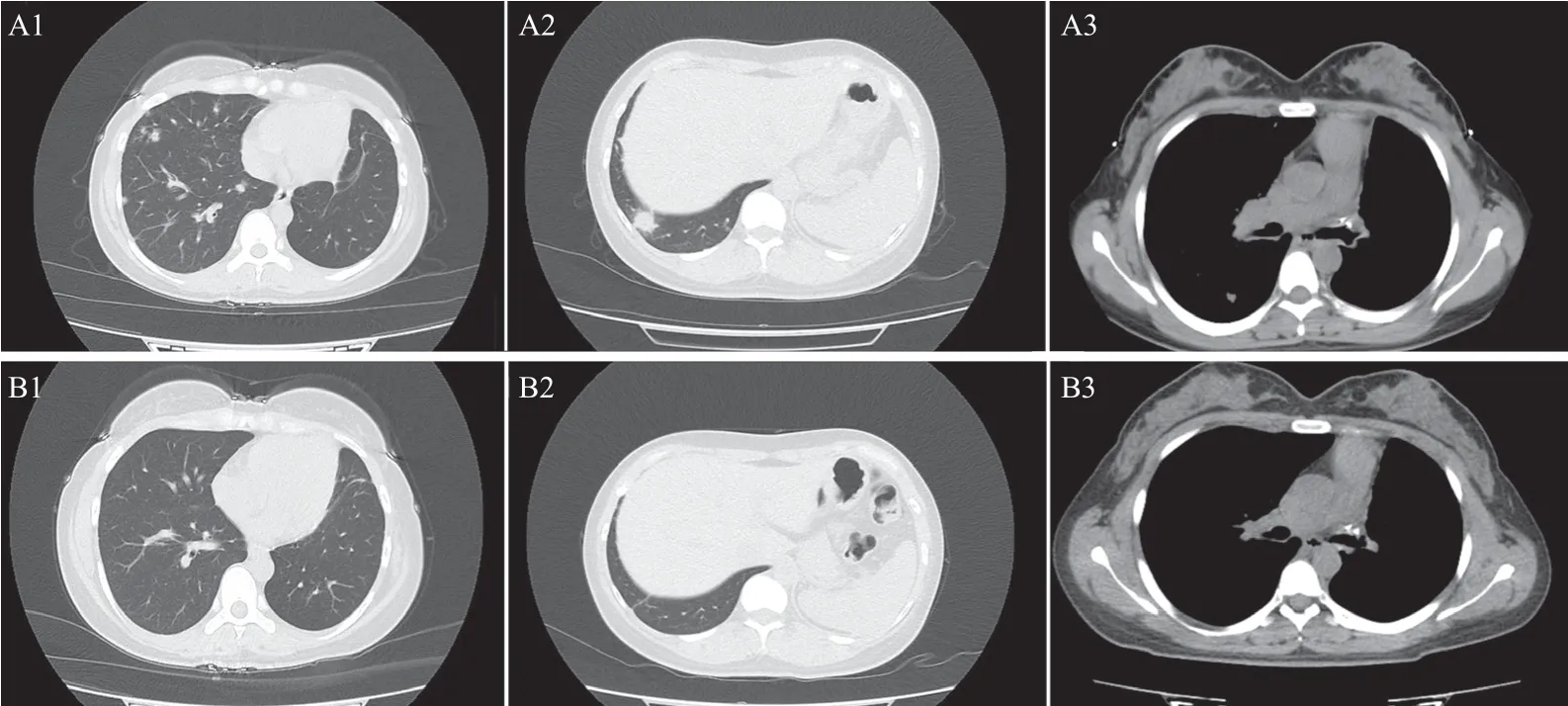
图2 克唑替尼治疗前后两肺及纵隔转移灶CT图像比较
2 讨论
近年来肺癌的靶向治疗领域取得重大突破,靶向治疗使得有相应基因突变的肺癌患者生存期显著延长,大大提高患者的生存质量。克唑替尼是一种小分子酪氨酸激酶抑制剂,于2011 年8 月26日获得美国食品药品监督管理局(Food and Drug Administration, FDA)批准使用[3-5]。目前已有研究证实对于ALK融合及ROS1 阳性的晚期NSCLC患者而言,克唑替尼有良好的有效性及安全性。
针对MET14外显子跳跃突变晚期NSCLC,有相关研究表明卡马替尼和特泊替尼有一定的有效性及安全性[6-7],FDA批准其用于局部晚期或转移性MET14跳跃突变的NSCLC患者。但对于c-MET扩增,各国指南尚无统一推荐药物。有研究显示克唑替尼治疗c-MET原发扩增和继发扩增的客观缓解率分别为75.0%和50%,并且发现c-MET基因拷贝数≥9.0的肺癌患者经克唑替尼治疗后无进展生存期更长[8]。相似地,蒋涛等[9]发现c-MET扩增程度或影响克唑替尼的疗效:在高度扩增即c-MET/CEP7 比值>5 的患者中,口服克唑替尼250 mg每天2次,其有效率高达67%,显著高于中、低度扩增的0%和17%的有效率。这提示克唑替尼可能是中、高度c-MET扩增晚期NSCLC人群的潜在选择。2022 年最新NCCN指南推荐克唑替尼、卡马替尼及替泊替尼用于高水平的MET扩增。
本病例的特点之一:病理类型为肺黏液腺癌,是一种少见的特殊类型的肺腺癌,国外有文献报道其约占肺癌所有病理类型的0.25%[10-11]。两项回顾性研究总结了肺黏液腺癌的基因突变类型特点,认为KRAS突变最为常见,其突变率分别为76%和71%[12-13]。有研究发现,ALK重排的患者占总原发性肺黏液腺癌患者的34.2%;而对于一般的NSCLC患者来说,ALK重排仅占3%~8%;在肺腺癌患者中,其比例为13%。这说明了ALK重排现象在原发性肺黏液腺癌较一般肺腺癌更为常见[14]。本例患者术后第一次基因检测为少见的ALK融合突变,但患者因经济问题而选择术后辅助化疗,疾病进展后选择阿来替尼治疗,治疗过程中规律随访至2021年8月出现两肺及纵隔淋巴结转移,再次基因检测提示ALK融合合并c-MET扩增。尽管某些肿瘤患者最初对于TKI敏感,但最终会产生耐药性。ALK-TKI耐药机制包括ALK依赖性耐药和非ALK依赖性耐药,其中非ALK依赖性耐药机制最常见的为替代或旁路信号通路的激活,目前已知的旁路机制包括MET、EGFR、SRC和IGF1R的激活,在大约一半的病例中,对第二代ALK-TKI的耐药性是由于ALK激酶结构域中的继发性突变引起的[15]。此前已报道5%~20% EGFR-TKI耐药病例出现MET扩增,但MET扩增对于ALK-TKI耐药的作用机制尚未完全明确,基础研究表明在ALK阳性细胞系中表达ST7-MET可诱导对ALK-TKI的耐药,这种耐药又可被ALK/MET的双重抑制剂所逆转[16]。CHEN等[17]研究发现,在一小部分晚期NSCLC患者中,c-MET过度表达与ALK重排共存。以上研究提示获得性MET突变的患者可能从同时针对ALK/MET的靶向治疗中获益。
本例患者为青年女性,局部晚期肺黏液腺癌,4个周期含铂双药化疗失败且不良反应明显,肿块穿刺活检,NGS提示ALK(Exon19)-EML4(Exon21),予阿来替尼靶向治疗2个月后出现纵隔淋巴结及两肺转移,提示耐药,后再次行转移灶穿刺送检NGS提示MET扩增,合并ALK融合,予克唑替尼治疗,1个月后两肺转移病灶及纵隔肿大淋巴结基本完全吸收,疗效评价为完全缓解,用药期间未出现明显不良反应。
从上述病例及相关文献中我们发现,对于肺腺癌伴ALK阳性和c-MET扩增NSCLC患者,克唑替尼靶向治疗可能有效。当NSCLC经过一线靶向治疗后出现获得性c-MET扩增,仍可能从其他靶向药物治疗中获益。目前还需要更多研究来证实并探索其中可能存在的机制。
