微反应器在精细化工领域氧化反应中的应用进展
2022-09-01李绪根王建芝喻发全
李绪根,王建芝,刘 捷,林 笑,张 程,喻发全
(武汉工程大学化工与制药学院,湖北 武汉 430502)
精细化工在化工行业的地位十分重要,精细化学品种类多、专用性强、附加值高,广泛应用于各领域。随着绿色环保节能理念的提出,精细化工行业越来越注重可持续发展,绿色化工技术已成为精细化工行业实现节能减排、绿色安全生产的新趋势。
氧化反应是有机合成中最重要的化学反应之一,是杂原子引入和官能团转化的关键,被广泛应用于精细化学品的合成[1-2]。在精细化学品的合成过程中约50%以上的关键步骤是氧化反应过程,其中约90%以上是催化氧化反应过程[3]。例如,烃类选择性氧化可以得到许多大吨位的有机化工原料和小吨位的精细化学品;醇类选择性氧化可以得到重要的精细化工中间体[4-5]。因此,氧化反应是精细化学品合成不可或缺的步骤。但是传统间歇式反应器应用于氧化反应存在诸多问题:(1)氧化过程放热量大、升温速率快,使用的高锰酸钾等强氧化剂在加热、振荡及与酸反应时,易引起火灾和爆炸等;(2)在高温热重排反应中,反应温度越高,反应速率越快,反应时间越短,对反应过程传质、传热的控制就越差;(3)对反应过程的放热和混合速率的控制效果差,常出现局部过热现象,导致过度氧化;(4)无法连续长时间运行,严重限制了工业化生产[6-11]。因此,急需开发一种能提高氧化反应效率和安全性的新工艺、新设备[12-14]。
1989年出现了第一台微反应器,其应用潜力受到广泛关注。微反应器是直径为10~1 000 μm的管道式反应器,由混合器、换热器、反应器、控制器等组成[15-17]。与间歇式反应器相比,微反应器的优势在于:(1)反应系统是呈模块结构的并行系统,反应器尺寸小,操作性强,能最大程度减小事故危害程度;(2)微通道的比表面积可达10 000~50 000 m2·m-3,传质、传热效率高,反应速率在毫秒级,能避免因反应时间过长而产生不稳定的副产物;(3)换热效率极高,可以精确控制物料温度,有效避免局部过热;(4)由于反应器内的反应是连续流动反应,可以通过增加微通道的数量达到常规反应器的生产规模[18-27]。因此,微反应器可以实现大型反应器很难或不可能完成的化学反应[28-30]。
近几十年来,微反应器被广泛用于精细化学品的合成,并取得了长足进展。作者在此对微反应器在精细化工领域氧化反应中的应用进展进行综述,包括烷烃氧化、烯烃氧化、醇氧化、醛酮氧化、芳香族化合物氧化、胺氧化等,以期为微反应器的更广泛应用提供帮助。
1 烷烃氧化
烷烃被氧化后可得到醇、醛、酮和酸。烷烃氧化是生产有机化工产品和精细化学品的重要工业过程[31-32]。但是传统烷烃氧化过程存在传质及传热效果差、转化率低、产率低、反应条件较苛刻等缺点[33],微反应器的出现为烷烃氧化提供了一条新途径。
Willms等[34]开发了一种微反应器模块化设备,使用长度可变且可替换的毛细管(长100 m、内径1 mm)作为单个反应器,在一定流速、温度(75~165 ℃)和压力(25~100 bar)下,以液体异丁烷和氧气为原料制备过氧化氢叔丁醇(TBHP)。模块化结构微反应器解决了传统间歇式反应器无法连续生产、不适用反应条件苛刻且存在爆炸隐患工艺的问题,使得TBHP的制备过程可以在毛细管反应器中完成;在停留时间为4 h时,异丁烷转化率达到5%,TBHP 选择性为60%。
Hofmann等[35]将工业磷酸氧钒(VPO)催化剂填充至微反应器中,应用于正丁烷氧化制备马来酸酐(式1)。结果表明,当微反应器狭缝宽度为1.5 mm、反应温度为410 ℃、反应时间为48 h时,正丁烷转化率为88%,马来酸酐选择性为63%,而且在正丁烷入口体积分数高达4.5%时,微反应器仍可以实现几乎等温的操作;当微反应器狭缝宽度增至3.0 mm时,反应热显著增加,热点温差(热点值与盐浴温度420 ℃的差值)未超过298 ℃,较工业多管式反应器减小了约80%。证明了微反应器对于这种典型的高放热、非均相催化气相氧化反应具有较大的应用潜力。
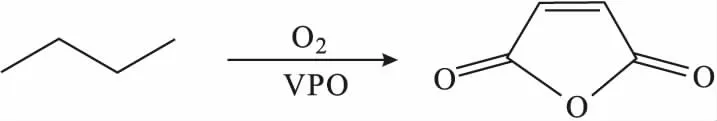
(1)
Pieber等[36]以加压空气为氧化剂、碳酸丙烯酯为绿色溶剂、三氯化铁为催化剂,在微反应器中进行气液连续流动氧化2-苄基吡啶制备2-芳酰基吡啶。在三氯化铁物质的量分数为5%、温度为200 ℃、停留时间为13 min时,2-苄基吡啶转化率为99%,2-芳酰基吡啶选择性为81%。该方法优势:(1)高温高压条件极大地增强了三氯化铁的催化作用,不需要大量的催化剂即可获得良好的催化效果;(2)实现了连续高效生产酮,反应时间从数小时显著缩短到数分钟;(3)加压空气代替高纯氧气作为氧化剂,降低了生产成本。
Gutmann等[37]以溴化钴为催化剂,以过氧化氢或空气代替高锰酸盐、铬酸、重铬酸钾或硝酸等作为氧化剂,在微反应器中氧化乙苯制备苯乙酮和苯乙酸。研究发现,过氧化氢氧化引发乙苯发生C-H 氧化,快速生成乙苯过氧化氢、苯乙酮等混合物;在反应温度为110~120 ℃、反应时间为6~7 min、压力为12 bar时,苯乙酮的选择性基本实现100%,产率为66%;当反应温度升至150 ℃、反应时间延长至16 min时,最终产物为苯乙酸,产率为71%。
2 烯烃氧化
烯烃在不同条件下氧化得到醇、醛、酮、酸和环氧化合物,其中环烯烃的氧化反应是在C=C键上加入一个氧原子,形成一个含氧原子的三环化合物。烯烃氧化是均相催化反应的重要工业过程,其中芳香基烯烃氧化产物是非常重要的有机合成中间体,被广泛应用于医药、染料、香料等领域[38-39]。
己二酸的传统合成工艺需两步氧化,即环己烷氧化得环己酮和环己醇的混合物,再经硝酸氧化得己二酸。该工艺虽然成本低,但使用硝酸作为氧化剂会产生大量氮氧化物(N2O)。Shang等[40]以环己烯和过氧化氢为原料,以Na2WO4·2H2O为催化剂,无溶剂条件下在填充床微反应器中合成己二酸(式2)。结果发现,添加适量硫酸可稳定过氧化氢,加速水解,并形成更活跃的氧化催化剂,己二酸产率在20 min内可达到50%,相比间歇式反应器,反应时间缩短了约96%。该方法也证实了微反应器在直接氧化反应中具有较大的发展潜力。
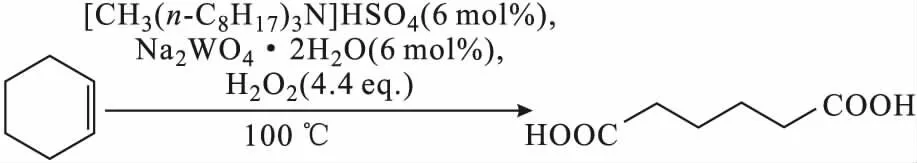
(2)
Ley课题组[41]利用不锈钢盘管(30 mL)微反应器,以(MeCN)2PdCl2(5 mol%)和CuCl2(5 mol%)为催化剂,以分子氧(20 bar)为氧化剂,开发了一种高效连续流氧化4-甲氧基苯乙烯合成4-甲氧基苯乙醛的方法(式3)。结果显示,在60 ℃、25 bar、停留时间为1 h的条件下,4-甲氧基苯乙烯转化率达83%,4-甲氧基苯乙醛产率达74%,且副产物少。
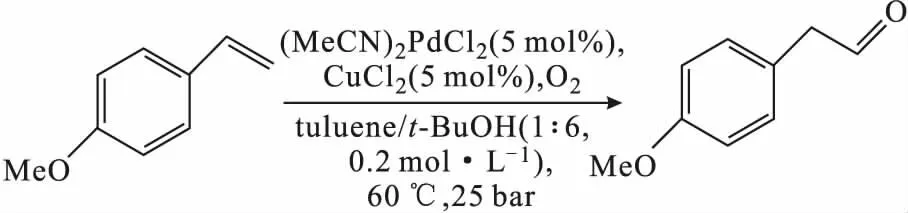
(3)
驱蛔素是一种天然的双环单萜烯,也是著名的驱虫化合物之一,具有抗疟、抗癌和杀线虫活性,也被用作有机合成中间体。然而,驱蛔素热稳定性差,且光化学效率随其浓度的增加而降低,从而阻碍了其大规模生产。Shvydkiv等[42]通过对工艺参数的优化,在膜微反应器中成功进行了α-萜烯的光氧化反应(式4),可合成选择性高达89%的驱蛔素,合成速率为2.5~3.2 mol·L-1·h-1。膜微反应器具有高效光透性的溶液薄膜,避免了大量含氧产品的生成,实现了潜在危险化学品的可控生产。

(4)
Park等[43]在两个连续流反应器中进行了单萜类化合物(α-蒎烯、β-蒎烯、δ-柠檬烯、α-萜烯)的光氧化反应。在聚醚醚酮(PEEK)树脂微反应器(内径0.5 mm,体积26 μL)中进行反应条件探索,在聚四氟乙烯(AF-2400)管式微反应器(内径0.6 mm,体积7.92 mL)中进行放大实验。发现以自然光代替钨丝灯、LED灯作为光源,β-蒎烯(0.5 mol·L-1)、亚甲基蓝(质量分数5%)与氧气合并,以分段流动状态通入PEEK树脂微反应器(图1),其日产量是间歇式反应器的270倍。

图1 在PEEK树脂微反应器中催化氧化β-蒎烯Fig.1 Catalytic oxidation of β-pinenein in PEEK resin microreactor
3 醇氧化
醇氧化在精细化工领域有着不可忽视的地位,其氧化产物醛或酮广泛应用于药物、涂料、食品添加剂等领域。但是醛、酮化学性质活泼,在合成过程中容易发生过度氧化生成酸进而发生酯化或羟醛缩合等副反应,使得醇氧化的大规模应用受到限制。微反应器可以精准调控停留时间,使得醇氧化的选择性大大提高,而且规模小、安全性高、可以强化传质及传热,在以分子氧和过氧化氢为氧化剂的液相氧化反应中得到广泛应用。
Vanoye等[44]以铜盐和2,2,6,6-四甲基哌啶氮氧化物(TEMPO)为共催化剂,利用微反应器催化氧化苯甲醇合成苯甲醛(图2)。在内径为1.6 mm、长2.6 m的PFA毛细管中,以乙腈为溶剂、Cu/TEMPO为催化剂,在室温和5 bar氧气的条件下,苯甲醇转化率在5 min内可达70%;同时还改进了以Cu(Ⅱ)为铜源的催化体系,在微反应器中实现了安全高效氧化苯甲醇。

图2 催化氧化苯甲醇合成苯甲醛Fig.2 Synthesis of benzaldehyde by catalytic oxidation of benzyl alcohol
微反应器的使用提高了苯甲醇的转化率,但是Cu/TEMPO催化剂的成本过高。因此,工业生产更青睐于使用廉价的均相催化剂(如金属溴化物)。Yue课题组[45]在聚四氟乙烯微反应器中进行了均相催化剂Co/Mn/Br 催化氧化苯甲醇合成苯甲醛(式5)。以乙酸为溶剂,在 150 ℃、5 bar空气条件下,苯甲醛产率在18 s内可达到85.6%;同时对气液两相在微反应器中的流动模型进行了探究:根据气泡的产生速度和长度,观察到湿润或脱湿的弹状流,其特征是气泡周围有完全或部分湿润的液膜;验证了在温度高于90 ℃时,湿段塞流和脱段塞流下产率基本没有差异。
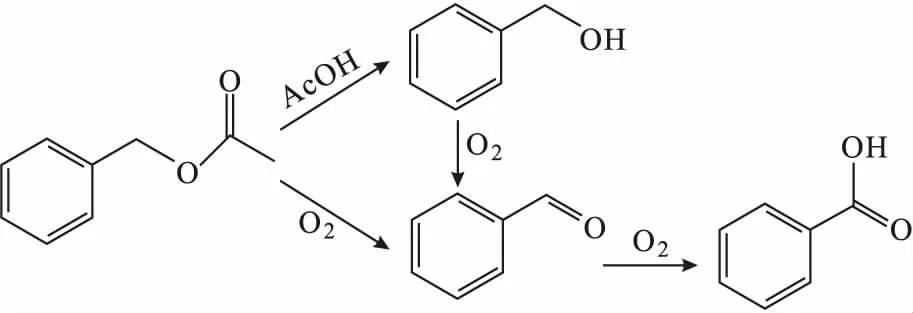
(5)
Swern氧化反应是用二甲基亚砜作氧化剂将醇氧化成醛或酮的反应,是将羟基转化成羰基的常用方法,在有机合成中被广泛应用。当反应温度高于-20 ℃时,中间体二甲基氯锍盐会发生部分分解,所以Swern氧化反应温度一般在-50~-70 ℃范围,但是间歇式反应器对温度控制不好便会有副产物产生[46-47]。
Zhu等[48]以草酰氯为活化剂,在连续流微反应器中通过Swern氧化反应氧化苯甲醇合成苯甲醛。先将二甲基亚砜和草酰氯经过T型混合器混合,再将混合后的溶液与苯甲醇经过Y型混合器混合后进入1.5 m长的微反应器。在甲醇、草酰氯和苯甲醇的物质的量比为4∶2∶1、二甲基亚砜流速为1.5 mL·min-1、反应温度为15 ℃、常压条件下,苯甲醛产率高达84.7%,选择性达98.5%。由于微反应器单位时间处理量小、换热高效,使得苯甲醇Swern氧化反应可在5~19 ℃下进行,为常温进行Swern氧化反应提供了新途径,且反应速率和安全性得以控制。
Kawaguchi等[49]利用三氟乙酸酐活化二甲基亚砜进行苯甲醇Swern氧化反应合成苯甲醛(式6)。先将二甲基亚砜与三氟乙酸酐混合,然后与苯甲醇混合,再用三乙胺处理,得到苯甲醛。在20 ℃、停留时间为2.4 s时,确保了高度不稳定的中间体在分解前可以非常快速地转移到下一个反应器,苯甲醇转化率高达97%,苯甲醛产率高达91%;继续扩大试验,在20 ℃下连续反应3 h,发现苯甲醇转化率和苯甲醛产率不变。

(6)
Cao等[50]在硅玻璃填充床微反应器(MPBR)中填充Au-Pd/TiO2催化剂,在无溶剂的情况下用纯氧氧化苯甲醇合成苯甲醛。结果表明,苯甲醇转化率随温度和氧气压力的升高而升高;而苯甲醛选择性随温度的升高而降低,随氧气压力的升高而升高。在120 ℃、5 bar氧气下,苯甲醇转化率达95%,苯甲醛选择性为78%。但是,氧气在高温条件下与有机蒸汽直接混合存在爆炸风险,从而限制了其工业化生产。Greene等[51]利用廉价的、耐高温高压的、有氧渗透性的聚四氟乙烯管作反应器,开发了一种“管壳式”膜微反应器,避免了有机蒸汽与氧气直接混合,但是苯甲醇在反应器中要停留约1 h才能被完全氧化,催化剂活性较低。
Wu等[52]将质量分数1%的Au-Pd/TiO2催化剂颗粒填入半渗透性聚四氟乙烯(AF-2400)管式微反应器的半渗透管中,研究了苯甲醇催化氧化合成苯甲醛。这种半渗透管式微反应器有气液两条通道,氧气在反应过程中可以连续渗透,使得催化剂床中的氧气浓度较氧气预饱和进料的非渗透反应器中的高2个数量级,进而提高苯甲醇转化率。
4 醛酮氧化
醛和酮是一类重要的有机化合物,在精细化工领域占据重要地位。但是醛不稳定,易被进一步氧化成羧酸;而酮难以被氧化,只有在强氧化条件下羧基两侧的键才断裂生成小分子羧酸。
Vanoye课题组[53-55]以Mn(Ⅱ)盐为催化剂,采用连续流微反应器,在室温、5 bar氧气条件下研究了2-乙基己醛催化氧化合成2-乙基己酸(式7)。结果发现,以0.01%Mn(Ⅱ)盐为催化剂、2%2-乙基己酸钠为添加剂、停留时间为6 min时,2-乙基己醛转化率达98%,2-乙基己酸选择性达98%。其工艺流程如图3所示。
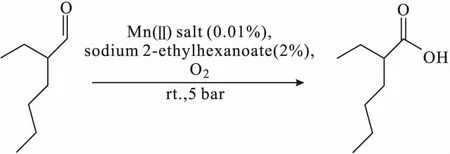
(7)
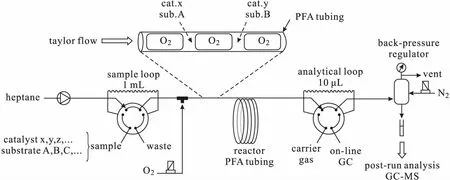
图3 室温下2-乙基己醛催化氧化合成2-乙基己酸的工艺流程Fig.3 Synthesis of 2-ethylhexanoic acid by catalytic oxidation of 2-ethylhexanal at room temperature
Hommes等[56]首次在聚四氟乙烯毛细管微反应器中以5-羟甲基糠醛(HMF)为原料、醋酸为溶剂、空气或纯氧为氧化剂、Co/Mn/Br为催化剂,均相催化氧化合成2,5-二甲酰呋喃(DFF)、5-甲酰呋喃甲酸(FFCA)和2,5-呋喃二甲酸(FDCA)(式8)。结果表明,以纯氧为气相的微反应器中,在150 ℃、5 bar氧气、停留时间为2.73 min时,HMF转化率为 99.2%,DFF、FFCA、FDCA 的产率分别为22.9%、46.7%、23.8%;总体选择性从常压下(需加入乙醛作为共氧化剂)的5%~15%提高到60%~94%,实现了微反应器高效合成FDCA。微反应器中传质限制少,可作为一种潜在的过程强化工具,但是,流动相中出现沉淀会导致毛细管道堵塞。

(8)
5 芳香族化合物氧化
氧化反应可以将芳香族化合物转化为醛、酮、酸、环氧化合物和过氧化合物等,是精细化工领域核心技术,用于生产中间体和特种精细化学品。由于芳香族化合物C-H的键能较大,氧化反应存在条件苛刻、能耗高、转化率低、选择性差和污染大等问题。微反应器为其提供了一条绿色安全新途径[57-58]。
Schmid课题组[59]以2-羟基联苯-3-单加氧酶(HbpA)为生物催化剂,同时添加甲酸脱氢酶(FDH)以确保辅助因子NADH的再生循环,在连续分段流管式微反应器(TiTR)中进行2-羟基联苯的酶催化氧化合成3-苯基邻苯二酚,合成速率可达14.5 g·L-1·h-1。
亚砜化合物是重要的医药、农药中间体,可通过选择性氧化得到,该方法虽然绿色安全,仍存在过度氧化的问题。在传统的间歇式反应器中,过氧化氢和苯硫醚需要3 min才能完全转化,产物中亚砜占82%,过氧化砜占15%。Noguchi等[60]在不锈钢毛细管微反应器(内径1 mm,体积730 mL)中,提前用一个T型混合器将30%过氧化氢和苯硫醚混合,在停留时间为2.12 s、未添加催化剂的情况下,亚砜产率可高达97%(式9)。

(9)
苯酚是医药、农药的重要中间体和生产原料,可由异丙烯过氧化氢工艺合成,但存在中间体热稳定性差、副反应多等问题[61]。Su课题组[62]以2,3-二氯-5,6-二氰基对苯醌(DDQ)为氧化剂、乙腈为溶剂,用蓝色LED灯作为环保光源,在毛细管微反应器中实现了苯转化为苯酚的连续流动光氧化。在室温、乙腈∶苯∶DDQ为12∶1∶1.5(物质的量比)、苯浓度为30 mmol·L-1、停留时间为60 min的最佳条件下,苯酚产率可达94%,选择性超过99%,较间歇式反应器光氧化显著提高,且反应时间显著缩短。
6 胺氧化
胺氧化可得到多种含氮化合物,如肟、亚胺、腈、酰胺、氧化胺和偶氮化合物等,含氮化合物是重要的精细化学品,在现代化学工业中应用广泛[63-64]。废气中的微量氧气会导致活性胺氧化降解,使得胺氧化效果不佳[65]。目前,关于胺氧化的报道不多[66]。
Jensen课题组[67]在螺旋通道的硅和耐热玻璃组成的微反应器(230 μL)中,以30%过氧化氢溶液为氧化剂,在不使用任何催化剂或其它试剂的情况下,研究了各种芳醛与仲胺的直接氧化酰胺化反应(式10)。结果表明,在80~110 ℃,芳醛可以在20~40 min内转化为酰胺,产率达到79%~92%。其反应装置如图4所示。该方法同样适用于无外消旋的手性氨基酸衍生物的酰化反应。

(10)

图4 芳醛与仲胺直接氧化酰胺化反应装置Fig.4 Experimental setup for direct oxidative amidation of aldehydes with secondary amines
Zhu课题组[68]开发了一种毛细管微反应器的连续工艺,将2-巯基苯并噻唑(MBT)溶解在过量的环己胺中,再与氧气在气液分段流动的毛细管微反应器(内径0.6 mm或2 mm,长度5~18 m)中进行反应,得到N-环己基-2-苯并噻唑次磺酰胺(CBS)(式11)。结果发现,以一水合乙酸铜[Cu(CH3COO)2·H2O]为均相催化剂时,反应时间从4 h缩短到3~5 min,产率为85%~87%;氧气的使用明显减少了过度氧化的副产物。
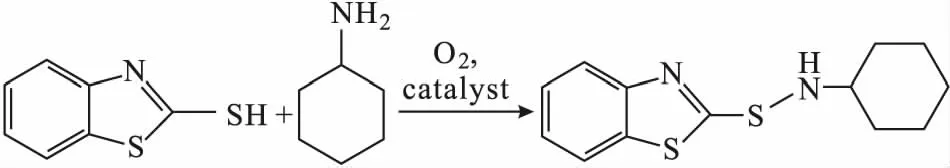
(11)
Baumeister等[69]在可以周期性变窄的不锈钢管式微反应器中,利用过氧化氢氧化N-甲基吗啉,并在二氧化碳催化下合成N-甲基吗啉氧化物(式12)。在反应温度为60 ℃、二氧化碳质量分数为1%、停留时间为13.9 min时,转化率高达98%,产率高达93.5%,反应时间较传统间歇式反应器(20 h)显著缩短。

(12)
7 氧化脱氢偶联
氧化脱氢偶联是指一个X-H键(X:碳或杂原子)与一个Y-H键(Y:碳或杂原子)直接结合构建新的X-Y键[70-71]。氧化脱氢反应一般在高温条件下进行,并且是放热反应[72],因此,传统氧化脱氢工艺受热力学限制,存在能耗高的缺点。
No⊇l课题组[73]在毛细管微反应器中实现了吲哚的Heck交叉脱氢偶联反应(式13),吲哚与2,2,2-三氟丙烯酸乙酯之间的偶联在10 min的停留时间内即可完成,得到纯度为82%的吲哚偶联产物。这是因为,气体和液体在毛细管道中分段流动,使得气相与液相的接触面积变大,高表面体积比有效防止了催化剂降解及管道堵塞;毛细管微反应器对传质和传热的高度控制使得反应时间从几小时缩短到几分钟。
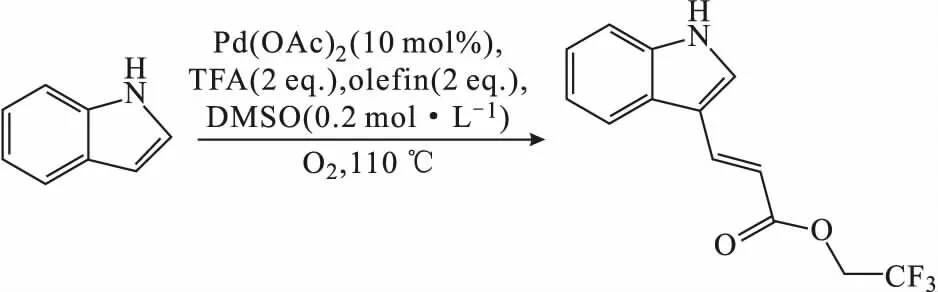
(13)
Nguyen等[74]和Cheng课题组[75]以聚乙烯醇(PVA)溶液为粘合剂将催化剂涂在金属-陶瓷复合基底上,研究了填充床微反应器中乙烷氧化脱氢合成乙烯(图5)。在420 ℃、1.0 atm氧气下,乙烷转化率达60%,乙烯选择性达85%;传统的固定床反应器需要约5倍体积才能达到与微反应器相同的产率。

图5 乙烷氧化脱氢合成乙烯示意图[75]Fig.5 Schematic diagram for synthesis of ethylene by oxidative dehydrogenation of ethane[75]
Zhou等[76]利用膜分散来提高萃取效率,以实现高效合成5-羟甲基糠醛(HMF)(式14)。将平均孔径为5 μm的微滤膜置于混合器和横流通道之间,使得分散相流体形成大量液滴,1 s内即可与连续相流体均匀混合,反应时间从传统搅拌反应器的60 min缩短到微反应器的4 min,HMF选择性更高,萃取效率接近100%,产率为93%,是传统反应器的1 000倍。
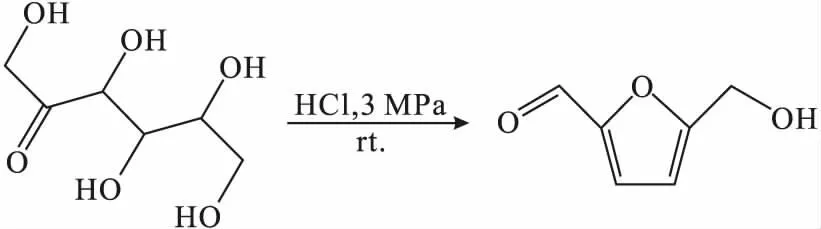
(14)
8 结语
微反应器应用于氧化反应,不仅可以提高反应的选择性,缩短反应时间,而且可以实现连续生产,在精细化工领域发展空间较大。微反应器中的氧化反应基本上以氧气或过氧化氢为氧化剂,可以减少副产物,是非常理想、经济、可持续发展的绿色反应。然而,微反应器技术仍面临许多困难和挑战,特别是对多相流动、微反应器通道内 “缩放效应”(包括入口效应、共轭传热、非均匀流动分布等)的探究相对较少;微反应器中氧化反应的动力学、热力学、流体力学等理论体系还未得到优化。
