K3Fe(CN)6增强钴镍基硒化物的电化学性能研究
2022-09-01张文哲钱苗苗罗刚吴春秦伟
张文哲,钱苗苗,罗刚,吴春,秦伟
(长沙理工大学材料科学与工程学院,湖南长沙 410114)
寻找并构建高效的能源储存器件,是目前新能源领域的研究热点[1-3]。超级电容作为一种介于常规电容器和二次电池之间的储能器件,具有长循环寿命、高功率密度、高安全性和效率等方面的优势,越来越受到相关研究者关注重视[4-5]。然而,超级电容器的能量密度远低于锂离子电池等二次电池,这大大限制了其在高能量密度需求领域的应用。如何在保持超级电容器长循环寿命等优势的前提下,提升超级电容器的能量密度是一个重要挑战[6]。
电极材料是决定超级电容器电化学性能的关键所在,寻找具有高比电容的电极材料是获得高能量密度超级电容器的一种重要途径[7]。受限于双电层电容机制,常规碳基电极材料的比电容普遍偏低[8]。因而,基于氧化还原反应机制的赝电容电极材料开始受到研究人员的广泛关注。过去几年,包括MnO2[9]、NiO[9]、CoO[10]等在内的具有不同形貌、结构的过渡金属氧化物及氢氧化物等,得到了广泛研究。然而,由于这些材料本征的导电率较低,导致其倍率特性及长循环稳定性并不理想,限制了其实际应用。
过渡金属硒化物具有较高导电性等优势,在包括锂离子电池在内的电化学储能器件领域得到了大量的应用。其作为超级电容器电极材料也开始得到了研究人员的关注[11-12]。由于Se 的电负性低于同族的O 和S,因而过渡金属硒化物的导电性一般高于相应的氧化物或硫化物。钴镍基最近几年得到了研究人员的广泛关注。济南大学原长洲课题组[13]利用溶剂热法制备了单分散金属相的H-NiCoSe2微球,当其用作超级电容器电极材料时,表现出极为优异的电化学特性,在3 A∙g−1电流密度下的比电容为750 F∙g−1。武汉理工大学的孙义民等[14]利用先水热后硒化的方法在碳布上生长了Ni0.34Co0.66Se2纳米棒并用作自支撑柔性超级电容器电极材料,相比NiCo2O4和NiCo2S4,其 所 制 备Ni0.34Co0.66Se2电 极 的比电容、循环稳定性等都得到了明显提升。
此外,有研究表明[15],除对电极材料进行设计外,在水系电解液中加入氧化还原添加剂也可以明显改善超级电容器的电化学特性。早在2005 年,日本大阪工业大学的I. Tanahashi 等人[16]发现,对于活性碳布电极,当在5.0 mol∙L−1的H2SO4电解液中添 加0.1 mol∙L−1的AgNO3,相 比 未 添 加AgNO3的电解液,其比电容增大3 倍以上,并指出这种提升来源于Ag+/Ag 氧化还原对的贡献。其后,研究人员陆续发现了多种可以提升超级电容器性能的氧化还原添加剂[17-20]。K3Fe(CN)6作为一种可以在同时中性、碱性环境中都可以稳定存在的物质,可以通过Fe(CN)63−/Fe(CN)64−的氧化还原反应,有效提升超级电容器的电化学特性[21]。台湾成功大学的Van Thanh Nguyen 等[22]研 究 表 明,当 使 用NiCo(CO3)(OH)2作为超级电容器正极材料,Fe2O3/rGO(reduced graphene oxide)作为负极材料构建非对称超级电容器,电解液中添加K3Fe(CN)6后其能量密度可达84.1 W∙h∙kg−1。
采用共沉淀法制备了钴镍基普鲁士蓝类似物,并经过硒化之后得到钴镍基金属硒化物。当其用作超级电容器电极材料时,相比未添加K3Fe(CN)6的电 解 液,在KOH(1 mol ∙L−1)+K3Fe(CN)6(0.02 mol∙L−1)电解液中,电容器的比电容得到了显著提升。
1 实验部分
1.1 材料制备
称取7.15 g 氯化镍溶于1 L 去离子水中,之后添加13.25 g 柠檬酸三钠,磁力搅拌待完全溶解后得到溶液A。同时,称取6.65 g 钴氰化钾溶于1 L去离子水中,搅拌均匀后得到溶液B。将溶液B 添加至溶液A 中,用保鲜膜覆盖并静置反应24 h,溶液变得悬浊后,以12 000 r∙min−1离心清洗15 min,然后分别使用去离子水和乙醇清洗三遍,并在80 ℃下干燥12 h,得到反应前驱样品(记作NCP)。
为了得到对应硒化物,在管式炉中N2气氛下对所得前驱样品进行硒化。首先称取一定量的NCP和硒粉,分别置于管式炉中的不同坩埚中,其中硒粉靠近进气端。然后进行热处理,其中升温速度为5 ℃∙min−1、温度为450 ℃,时间为2 h,之后自然降温至室温,最终得到样品(记作NCSe)。
1.2 材料表征及电化学性能测试
分别利用XRD 和SEM,对材料进行结构及微区形貌进行表征。利用EDX,分析元素的分布情况。
电极制备:将所得电极材料与导电剂乙炔黑、粘结剂PVDF 按照质量比8∶1∶1 进行混合,再添加一定量的NMP(N-甲基吡咯烷酮),在研钵中研磨均匀后涂覆到玻碳电极片上,然后置于100 ℃真空干燥箱中干燥12 h,得到工作电极。电极材料平均负载量约为3 mg∙cm−2。
电化学性能测试:在CHI760 电化学工作站上采用三电极体系进行性能测试,其中工作电极为所制备电极,对电极及参比电极分别为Pt和Hg/HgO,电解液分别为KOH(1 mol∙L−1)和KOH(1 mol∙L−1)+K3Fe(CN)6(0.02 mol∙L−1)。分别使用循环伏安法和恒流充放电,评估电极材料在不同电解液中的比电容。
2 结果与讨论
2.1 样品形貌结构表征

图1 NCP 前驱体和NCSe 样品的SEM 图Figure 1 SEM images of precursor NCP and NCSe
NCP 前驱体及NCSe 样品的SEM 图如图1 所示。从图1 可见:使用共沉淀法制备的前驱体NCP为均匀的立方体结构,立方体的边长大约300 nm,且表面光滑、无明显孔结构出现;在N2气氛下经硒化处理后得到的NCSe 样品依旧保持了良好的立方体结构,且立方体尺寸仍旧保持在300 nm 左右;相比纯未经硒化处理的样品,硒化后立方体的表面变得粗糙,明显表现出多孔结构。多孔结构的出现,有利于电解液的浸润,进而提升电极材料的电化学特性。
为了分析样品中元素的分布,使用X-射线能量色散谱仪表征了样品中元素情况,图2 为NCSe 样品中元素分布图及其EDX 扫描图。从图2 可以看出,样品中存在C、Ni、Co 和Se 元素,并且在样品中均匀分布,进一步证明了所制备样品的良好一致性。

图2 NCSe 样品中元素分布图及其EDX 扫描图Figure 2 SEM image,elemental mappings and EDX spectrum of NCSe
利用XRD 分析了样品的晶体结构,结果如图3所示。从图3 可以发现,硒化后样品的XRD 衍射峰相比之前发生了明显的改变。对于未经硒化处理的NCP,其所有衍射峰与Ni3(Co(CN)6)2·12H2O 的标准峰对应良好(PDF 卡片号89-3738),这也与文献[23]报道结果一致。硒化后,新出现的衍射峰分别为立方结构的CoSe2(PDF 卡片号09-0234)和六方晶系的NiSe(PDF 卡片号18-0887)。没有其他杂峰出现,表明没有其他新相出现,所制备的NCSe 主要由CoSe2和NiSe 组成。
2.2 电化学性能测试
利用三电极体系评估了所制备材料的超级电容器储能特性,其中参比电极和对电极分别为Hg/HgO 和Pt。在100 mV∙s−1扫 速 条 件 下,在KOH(1 mol∙L−1)+ K3Fe(CN)6(0.02 mol∙L−1)和KOH(1 mol∙L-1)电解液中分别测试电容器的循环伏安曲线,结果如图4 所示。从图4 可以发现:在两种不同的电解液中测得的循环伏安曲线的形状没有发生明显改变,两者均在0.38 和0.52 V 处出现了一对明显的氧化还原峰,对应电极材料的典型特征;两者测得的循环伏安曲线所围成的面积有明显的不同,添加了K3Fe(CN)6的面积远大于未添加的。

图3 NCP 和NCSe 的XRD 衍射图谱Figure 3 XRD patterns of NCP and NCSe
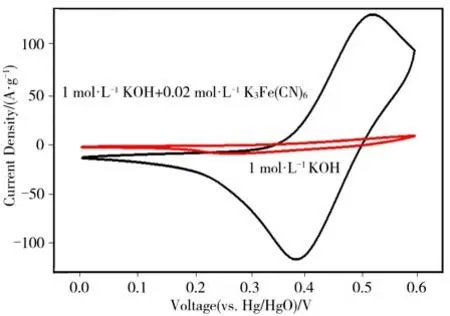
图4 NCSe 在KOH+K3Fe(CN)6和KOH 电解液中的循环伏安曲线Figure 4 CV curves of NCSe in KOH+K3Fe(CN)6 and KOH
图5 为在KOH+K3Fe(CN)6和KOH 电解液中不同扫速的循环伏安曲线。从图5 可见,随着扫描速度的增加,循环伏安曲线围成的面积明显增加,而CV 曲线形状并没有发生明显改变。
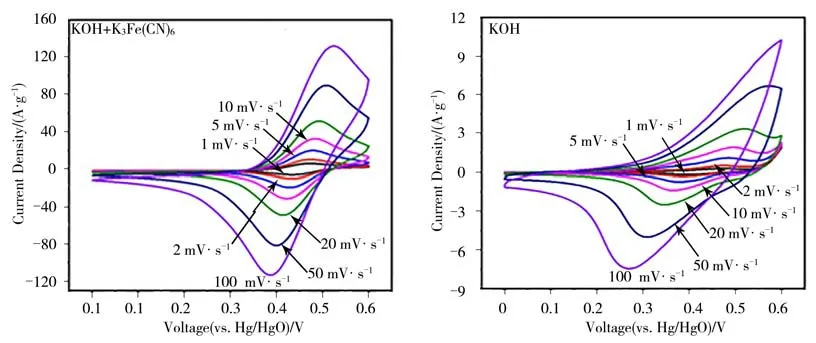
图5 不同扫速下NCSe 电极在KOH+K3Fe(CN)6和KOH 中的循环伏安曲线Figure 5 CV curves of NCSe in KOH+K3Fe(CN)6 and KOH at different scan rates

图6 NCSe 电极在KOH+K3Fe(CN)6和KOH 中扫速-比电容的关系曲线Figure 6 Scan rate-specific capacitance relation⁃ships of NCSe in different electrolytes
利用恒流充放电手段评估了所制备NCSe 的充放电特性,测试同样采用三电极体系进行,充放电测试所用的电流密度分别为2、5 和10 A∙g−1,其结果如图7 所示。从图7 中的对应放电曲线可以发现:在不同电解液中NCSe 电极均在0.4—0.5 V 电压窗口出现了明显的电压平台,与循环伏安曲线对应;相对于KOH 电解液,在KOH+K3Fe(CN)6中相同电流密度下的放电时间大大增加。
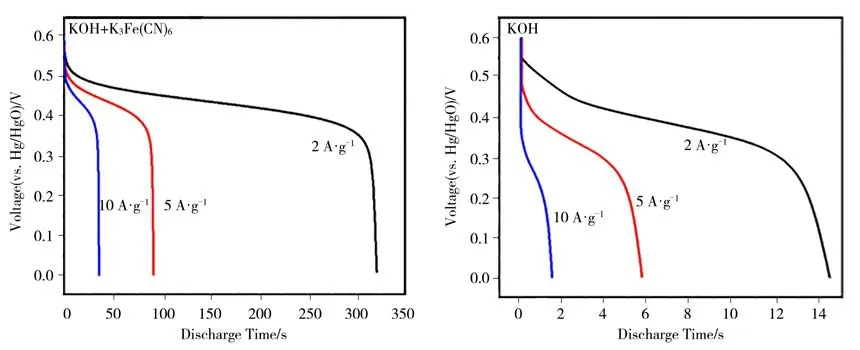
图7 不同电流密度下NCSe 电极在KOH+K3Fe(CN)6和KOH 中恒电流放电曲线Figure 7 Discharge profiles of NCSe in KOH+K3Fe(CN)6 and KOH at different current densities
利用公式,C=it/mΔV 分别计算不同电流密度对应的比电容,其中C 为比电容(F∙g−1),i、t、m 及∆V 分别为放电电流(mA)、放电时间(s)、电极中活性物质质量(mg)和充放电电压窗口(V),结果如图8 所示。从图8 可见:在2、5 及10 A∙g−1电流密度下,在KOH 电解液中的比电容分别为48.1、47.2 和24.4 F∙g−1,而在KOH+K3Fe(CN)6中,相应的比电容则分别高达1 070.1、765.7 和596.0 F∙g−1。循环伏安测试及恒流充放电测试结果均表明,电解液中添加氧化还原添加剂可以显著提升NCSe 电极材料的超级电容储能特性。

图8 NCSe 电极在不同电解液中的比电容-电流密度关系曲线Figure 8 Specific capacitance-current density relation⁃ships of NCSe in different electrolytes

图9 NCSe 在KOH+K3Fe(CN)6中长循环稳定性Figure 9 Long-term cycling stability of NCSe in KOH+K3Fe(CN)6
图9 为 在10 A ∙g−1电 流 密 度 下NCSe 电 极 在KOH+K3Fe(CN)6电解液中的长循环稳定性。从图9 可以看出,整个体系的循环稳定性并不特别理想。在前1500 次循环过程中,比电容出现了明显衰减,大约保持率为71%;随着循环次数的增加,比电容衰减程度有所缓解,5000 次循环后比电容保持率为58.2%。这可能是由于NCSe 的导电性并不理想,接下来可以尝试通过与石墨烯/碳管高导电性的材料构建复合材料体系,进一步提升其长循环稳定性。
3 结论
利用共沉淀法制备了钴镍基普鲁士蓝类似物前驱体,在管式炉中硒化得到了多孔钴镍金属硒化物(NCSe),同时研究了其作为超级电容器电极材料时的电化学储能特性。结果表明,当在1 mol∙L−1的KOH 电 解 液 中添 加0.02 mol∙L−1的K3Fe(CN)6氧化还原添加剂时,NCSe 的比电容相较未添加的得到 了 显 著 提 升,在1 mV ∙s−1扫 速 下 高 达1 156.5 F∙g−1,即便在50 和100 mV∙s−1大扫速下比电容依旧保持为433.1 和301.2 F∙g−1。该研究结果可以为研究高性能超级电容器提供一定的指导作用。
