维奈克拉联合小剂量阿柔比星、阿糖胞苷方案治疗老年急性髓系白血病的疗效观察*
2022-08-31王小蕊李文倩杨红艳
王小蕊,李文倩,杨红艳
(青海省人民医院 血液科,青海 西宁 810000)
老年急性髓系白血病(acute myeloid leukemia,AML)患者(年龄≥65 岁)因不良基因组特征频率高、合并基础疾病、免疫功能低下等对诱导化疗反应不佳[1]。常用的低强度诱导方案包括低甲基化剂阿扎胞苷、地西他滨、阿柔比星联合阿糖胞苷(aclarubicin and cytosine arabinoside,AA)等,该类方案治疗反应率低,为10%~50%,且不能治愈,中位总生存期不到1年[2-3]。临床迫切需要开发能够快速诱导高临床反应率、对老年AML 患者具有更好耐受性和持久反应的靶向疗法。
B 细胞淋巴瘤2(B cell lymphoma 2,Bcl-2)是线粒体凋亡途径的关键调节剂,在AML 母细胞的存活、繁殖中起重要作用[4]。2017年美国食品药品监督管理局批准Bcl-2 抑制剂维奈克拉上市;近期国外临床试验证明将维奈克拉疗法用于新诊断的AML 中,可获得明显临床益处;美国食品药品监督管理局也批准维奈克拉与低甲基化剂或低剂量阿糖胞苷联合用于新诊断的老年AML 患者[5-6]。
维奈克拉是口服Bcl-2 抑制剂,国外研究证实其在复发或难治性AML 患者中表现出单药临床活性和可耐受安全性[7]。2020年,维奈克拉在中国上市,国内较缺乏维奈克拉治疗老年AML 患者的临床研究数据,目前仅有王淡瑜等[8]报道应用维奈克拉联合阿扎胞苷治疗5 例老年AML 患者的回顾性研究,且国内尚未见维奈克拉联合小剂量AA 方案治疗老年AML 疗效的报道。鉴于此,笔者对上述问题开展研究,以便为国内维奈克拉治疗AML 提供参考。
1 资料与方法
1.1 一般资料
回顾性分析2017年2月—2020年12月在青海省人民医院治疗的83 例老年AML 患者的临床资料。其中,62 例采用小剂量AA 方案治疗作为对照组;21 例采用维奈克拉联合小剂量AA 方案治疗作为研究组。两组患者基本资料比较,差异均无统计学意义(P>0.05),具有可比性(见表1)。
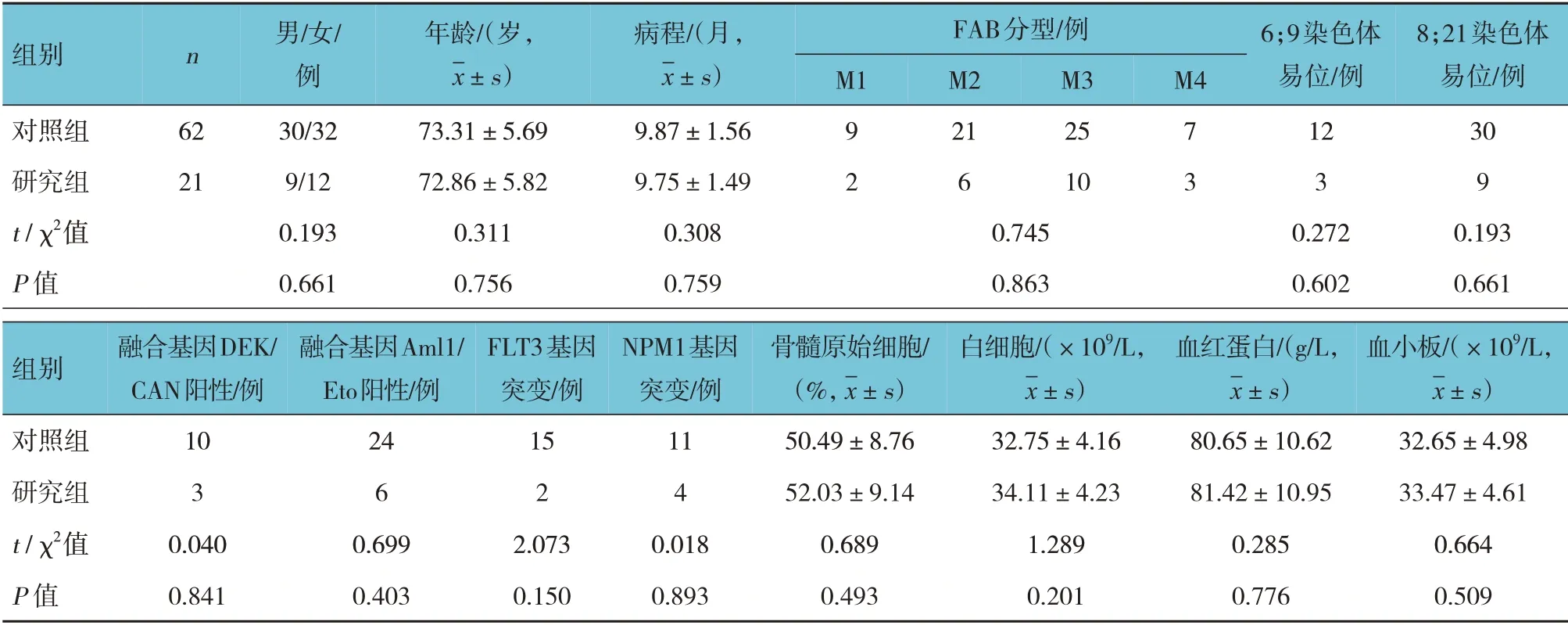
表1 两组患者临床资料比较
1.2 纳入与排除标准
1.2.1 纳入标准①符合《成人急性髓系白血病(非急性早幼粒细胞白血病)中国诊疗指南(2017年版)》[9]诊断标准;②年龄>65岁;③预计生存期>6 个月;④Karnofsky 功能状态评分>80 分;⑤初次治疗;⑥白细胞计数≤25×109/L;⑦临床资料完整。
1.2.2 排除标准①伴有传染性疾病、精神性疾病;②心肝肾等重要脏器功能障碍;③既往有药物滥用史、吸毒史;④伴有严重心脑血管、内科疾病;⑤对治疗药物过敏;⑥依从性差;⑦参与其他临床研究;⑧未完成治疗疗程;⑨随访资料不全。
1.3 方法
1.3.1 对照组患者给予小剂量AA 方案治疗:10 mg 阿柔比星(国药准字H10910093,深圳万乐药业有限公司)与250 mL 生理盐水混合均匀静脉滴注,1 次/d,连续用药5~7 d;25 mg 阿糖胞苷(意大利Actavis 公司,生产批号:0ND5241、0ND5221、0ND5131、0ND5041,规格:100 mg)皮下注射,1 次/12 h,连续用药10~14 d。若患者诱导后达到完全缓解(complete response,CR)或部分缓解(partial remission,PR),则继续采用原方案巩固1~2 疗程后观察效果。
1.3.2 研究组在对照组基础上口服维奈克拉(意大利Actavis 公司,生产批号:1142422、1148749、1142421,规格:100 mg),第1天100 mg,第2天200 mg,第3 天400 mg,第4 天及以后400 mg,1 次/d,1 个疗程28 d,持续用药至疾病进展或发生不可耐受毒性反应。
1.4 观察指标
1.4.1 近期疗效持续治疗28 d 后评价疗效,依据国际工作组2003年提出的AML 疗效标准[10],两组均于术前1 周评价新辅助治疗及全程新辅助治疗疗效,包括CR、PR,客观缓解率=(CR+PR)/总例数×100%。
1.4.2 酶联免疫吸附试验测定外周血p53 蛋白含量所有患者治疗前后空腹抽取静脉血液,3 000 r/min离心10 min,收集血清,采用酶联免疫吸附试验测定p53 蛋白含量,试剂盒购自上海西唐生物科技有限公司。
1.4.3 血液学不良反应及血制品输注情况统计两组治疗期间粒细胞缺乏时间、血小板计数<20×109/L时间、细胞输注量、血小板输注量。
1.4.4 非血液学不良反应参照美国国立肿瘤研究所抗癌药物急性与亚急性不良反应及分级标准[11],统计两组治疗期间感染、皮疹、胃肠道反应、肝肾功能损伤等情况。
1.4.5 近期生存情况所有患者治疗后门诊随访7 个月,1 次/月,统计随访期间癌因死亡情况,分析患者生存情况。
1.5 统计学方法
数据分析采用SPSS 18.0 统计软件。计量资料以均数±标准差(±s)表示,比较用t检验;计数资料以构成比或率(%)表示,比较用χ2检验;Kaplan-Meier 法绘制生存曲线,比较用Log-rank χ2检验。P<0.05 为差异有统计学意义。
2 结果
2.1 两组患者近期疗效比较
研究组与对照组客观缓解率比较,经χ2检验,差异有统计学意义(χ2=7.680,P=0.006),研究组客观缓解率高于对照组。见表2。
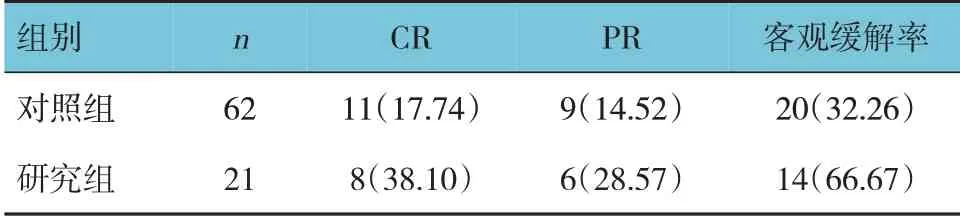
表2 两组患者近期疗效比较 例(%)
2.2 两组患者治疗前后外周血p53 蛋白含量的变化
对照组、研究组治疗前后p53 蛋白的差值分别为(52.81±7.97)ng/L 和(79.18±8.86)ng/L,经t检验,差异有统计学意义(t=12.739,P=0.000),研究组治疗前后p53 的差值高于对照组。
2.3 两组患者血液学不良反应及血制品输注情况比较
研究组与对照组的粒细胞缺乏时间、血小板计数<20×109/L 时间、细胞输注量、血小板输注量比较,经t检验,差异有统计学意义(P<0.05),研究组粒细胞缺乏时间、血小板计数<20×109/L 时间短于对照组,细胞输注量、血小板输注量少于对照组。见表3。
表3 两组患者血液学不良反应及血制品输注情况比较 (±s)

表3 两组患者血液学不良反应及血制品输注情况比较 (±s)
组别对照组研究组t 值P 值n 62 21粒细胞缺乏时间/d 14.84±2.17 13.31±2.05 2.913 0.005血小板计数<20×109/L时间/d 11.03±2.05 9.92±1.38 2.796 0.006细胞输注量/u 6.03±0.97 4.71±0.69 6.801 0.000血小板输注量/u 46.73±6.48 38.98±5.11 5.601 0.000
2.4 两组患者非血液学不良反应比较
两组患者感染、皮疹、肝功能损伤、胃肠道反应发生率比较,经χ2检验,差异均无统计学意义(P>0.05)。见表4。

表4 两组患者治疗期间非血液学不良反应发生情况比较 例(%)
2.5 患者近期生存情况
截止随访结束,研究组1 例死亡,对照组7 例死亡;两组患者总存活率比较,经Log-rank χ2检验,差异无统计学意义(χ2=0.762,P=0.383)。见图1。
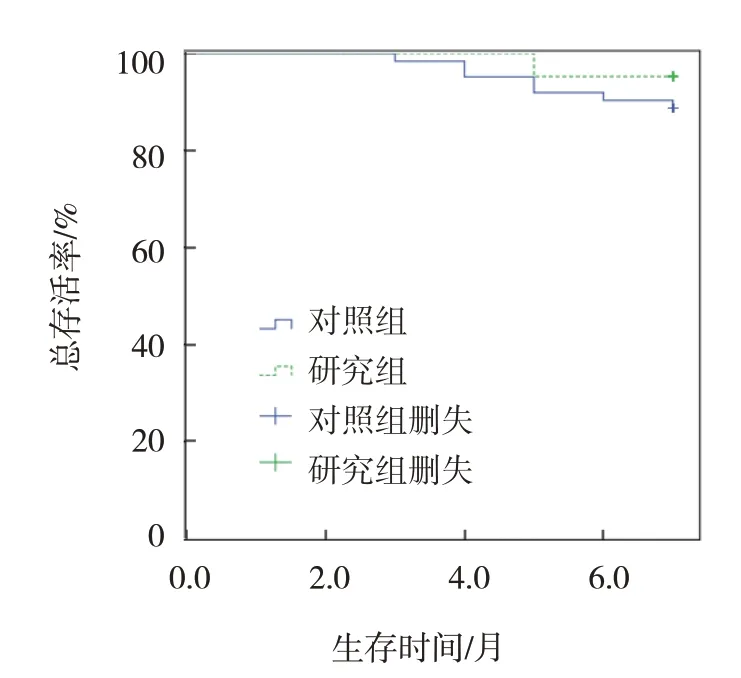
图1 两组患者Kaplan-Meier总生存曲线
3 讨论
AML 标准治愈性方案包括强化诱导化疗、巩固化疗及同种异体干细胞移植,但由于高龄、合并疾病等原因,老年AML 患者通常不适合标准化疗,多接受强度较低的低甲基化药物(阿扎胞苷或地西他滨)、低剂量阿糖胞苷治疗方案,预后不佳,且风险较高。有资料显示,年龄≥65 岁的初治AML 患者进行低甲基化药物治疗的缓解率甚至<30%,1年死亡风险较高[11]。老年AML 患者对一线治疗药物低剂量阿糖胞苷的缓解率同样较差,为11%~19%,中位生存时间≤6 个月[12]。随着医学水平不断发展,成人AML 治疗已逐渐转变为个性化治疗,适合白血病特征的靶向治疗已逐渐用于临床。AML 细胞依赖于Bcl-2 存活,Bcl-2 抑制剂维奈克拉联合低强度诱导方案用于AML(包括复发或难治性AML)可得到高缓解率,患者获益明显[13]。维奈克拉作为国内近期上市的新药,目前比较缺乏其在国内应用效果的临床数据,故笔者探讨了维奈克拉联合小剂量AA 方案治疗老年AML 的安全性和有效性,以便为维奈克拉在国内的临床应用提供依据。
维奈克拉是一种强效的选择性小分子Bcl-2 抑制剂,可直接与Bcl-2 结合,单药维奈克拉在AML中具有适度活性,可改变线粒体外膜通透性,活化半胱天冬酶,可能通过下调髓细胞白血病1 和诱导死亡蛋白NOXA 和PUMA 的表达,诱导依赖Bcl-2 生存的肿瘤细胞凋亡,促进化疗耐药性,并提高白血病祖细胞和原始细胞的存活率。ZHANG 等[14]将225 例年龄>70 岁初治AML 患者纳入研究,发现维奈克拉联合去甲基化药物组较去甲基化药物单药治疗组客观缓解率显著升高(66.7% VS 25.5%),但两组早期病死率接近(1.5% VS 3.4%)。DINARDO等[15]研究显示,维奈克拉联合阿扎胞苷(或地西他滨)治疗老年AML 患者的缓解率可达67%左右。本研究中,研究组客观缓解率(66.67%)高于对照组(32.26%),提示维奈克拉联合小剂量AA 方案治疗老年AML 疗效显著,与上述研究中维奈克拉治疗老年AML 的客观缓解率接近。研究组治疗前后p53的差值高于对照组,也印证了研究组疗效优于对照组。王淡瑜[8]等报道应用维奈克拉联合阿扎胞苷治疗5 例老年AML 均完全缓解,推测可能是研究对象过少有关。本研究中,研究组1 例死亡,对照组7 例死亡,两组患者总存活率无差异,与ZHANG等[14]研究结果类似,推测可能是观察时间短、样本量小所致。由于维奈克拉上市时间相对较短,目前维奈克拉治疗老年AML 的临床研究多为小样本量,后期可延长观察时间、扩大样本量进一步验证。研究组粒细胞缺乏时间、血小板计数<20×109/L 时间短于对照组,细胞输注量、血小板输注量低于对照组,说明维奈克拉联合小剂量AA 方案治疗老年AML 可获得相对较短的化疗后低细胞期,进而减少红细胞、血小板的输注,节约血液资源。
综上所述,维奈克拉联合小剂量AA 方案治疗老年AML 疗效显著,患者耐受性良好,可作为老年AML 患者治疗的新选择之一。维奈克拉单药治疗老年AML 易发生获得性耐药,联合治疗方案将是今后的研究热点。
