以震颤起病的成年散发型神经元核内包涵体病一例
2022-08-26刘振兴张术词王刚王耀振耿建红张绪美王炎强庞萌
刘振兴 张术词 王刚 王耀振 耿建红 张绪美 王炎强 庞萌
1 病例报告患者女,60岁,因“右上肢震颤20年,步态异常5年,足底麻木1年,意识障碍4h”于2021-10-19入作者医院。患者2001年出现右上肢不自主震颤,以姿势及动作性震颤为主。2016年出现步态异常,步态不稳,伴阵发性腹胀、反酸、便秘,于外院胃镜检查示慢性萎缩性胃炎。2019年右上肢震颤频率及幅度加重,右手持物不稳,出现双下肢震颤,多于静坐或下蹲时诱发,自觉记忆力下降,言语清晰度、流利度下降。2020年出现持续性足底麻木。2021-07-05就诊院脊椎外科,腰椎MRI示:L3-4、L4-5、L5-S1椎间盘突出,行腰椎间盘突出髓核切除+椎间骨cage融合+椎弓根螺钉内固定术治疗后腰痛明显缓解,足底麻木无改善。此次入院4 h前突发意识障碍,不识家人,胡言乱语,反应迟钝,双手不自主摸索。入院10 h后意识转清,不能回忆发生情景。既往高血压病史10年,规律应用降压药物治疗。否认糖尿病、冠心病、肝炎、结核病病史,无外伤史,无食物、药物过敏史,无烟酒、吸毒等不良嗜好。入院查体:体温:36.3℃,心率80次/min,呼吸16次/min,血压163/114 mmHg(1 mmHg=0.133 kPa),心肺腹未见异常,神经系统查体:意识模糊,构音障碍,远近记忆力、计算力、定向力下降,命名、听理解、阅读、书写、视空间能力和执行功能障碍,双侧瞳孔缩小,左∶右=2 mm∶2 mm,对光反射灵敏,无眼震,余脑神经检查正常。右上肢平举可见震颤,四肢肌力正常,双上肢肌张力(+++),双下肢肌张力(++),四肢腱反射(+),左侧Chaddock征阳性,右侧足底痛觉减退,双手轮替动作笨拙,双手指鼻试验、双下肢跟膝径试验欠稳准,闭目难立征阳性,直线行走步态不稳,脑膜刺激征阴性。额叶功能评定表(frontal assessment battery,FAB)评分11分,简易精神状态检查量表(mini-mental state examination,MMSE)评分19分。入院后完善相关辅助检查,总胆固醇7.72 mmol/L(2.86~5.98 mmol/L),三酰甘油1.91 mmol/L(0.45~1.69 mmol/L),低密度脂蛋白5.73 mmol/L(2.1~3.1 mmol/L),括号内数据为正常参考值范围;血常规、尿常规、粪便常规、肝功、肾功、空腹血糖、电解质、同型半胱氨酸、甲状腺功能及抗体未见异常。头颅MRI:弥散加权成像(DWI)序列:皮髓质交界区高信号(图1A、1B),T2 Flair序列:双侧对称弥漫的脑白质病变(图1C、1D)。脑电图示:安静状态下双侧枕区6~7 Hz低波幅θ活动,夹杂少量低波幅快波,左右对称,睁眼时枕区节律可抑制,背景节律偏慢、电压偏低。四肢肌电图示:双上肢正中神经腕管段损害、双下肢周围神经源性损害。右外踝上部10cm处皮肤病理活检:真皮层部分汗腺腺体细胞核内见弱嗜酸性透明包涵体样物(图2A);免疫组织化学标记可见包涵体呈p62阳性表达(图2B)、泛素蛋白阳性(图2C),符合神经元核内包涵体病在皮肤病理的改变特点。基因检测结果:NOTCH2NLC基因5′非翻译区RP-PCR扩增,色谱图呈现锯齿状逐步降低的峰图,提示存在GGC重复扩增突变(图3),DNA长度620 bp,重复155次(图4)。诊断神经元核内包涵体病。治疗及病情演变:入院即给降压、调脂、改善循环及营养神经等治疗。第2天患者出现持续性头痛、恶心、呕吐,给予对症治疗。8 d后患者好转出院,行走较前平稳,肢体震颤、足底麻木无明显改善。
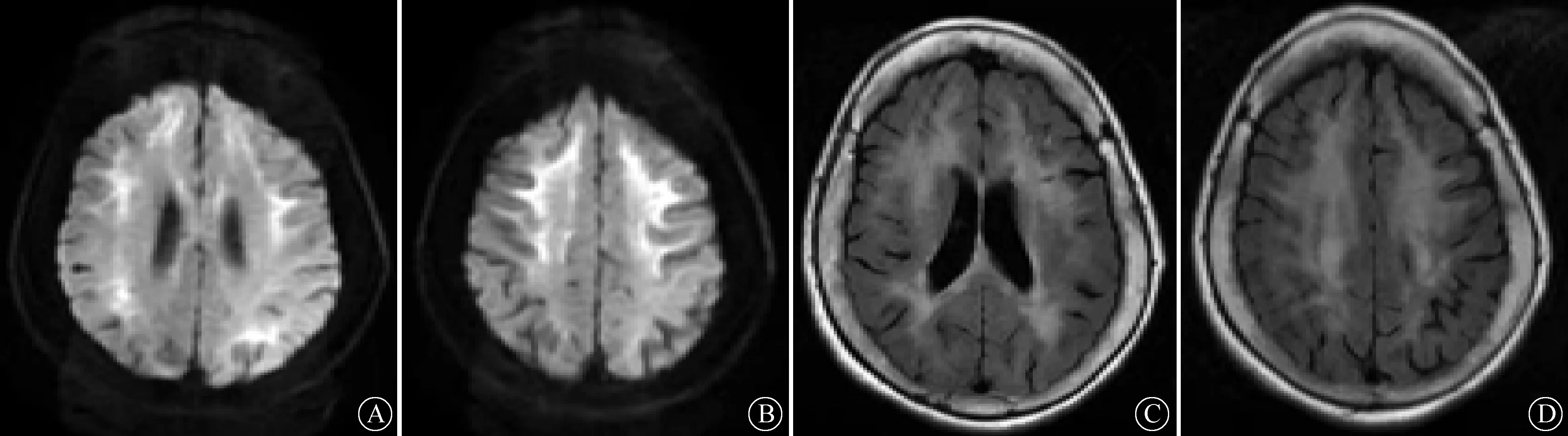
图1 患者头颅MRI(2021-10-20)显示双侧脑室旁及胼胝体压部(A)、额顶叶(B)皮髓质交界区,DWI高信号;双侧脑室旁(C)、额顶叶(D)白质,T2 Flair高信号
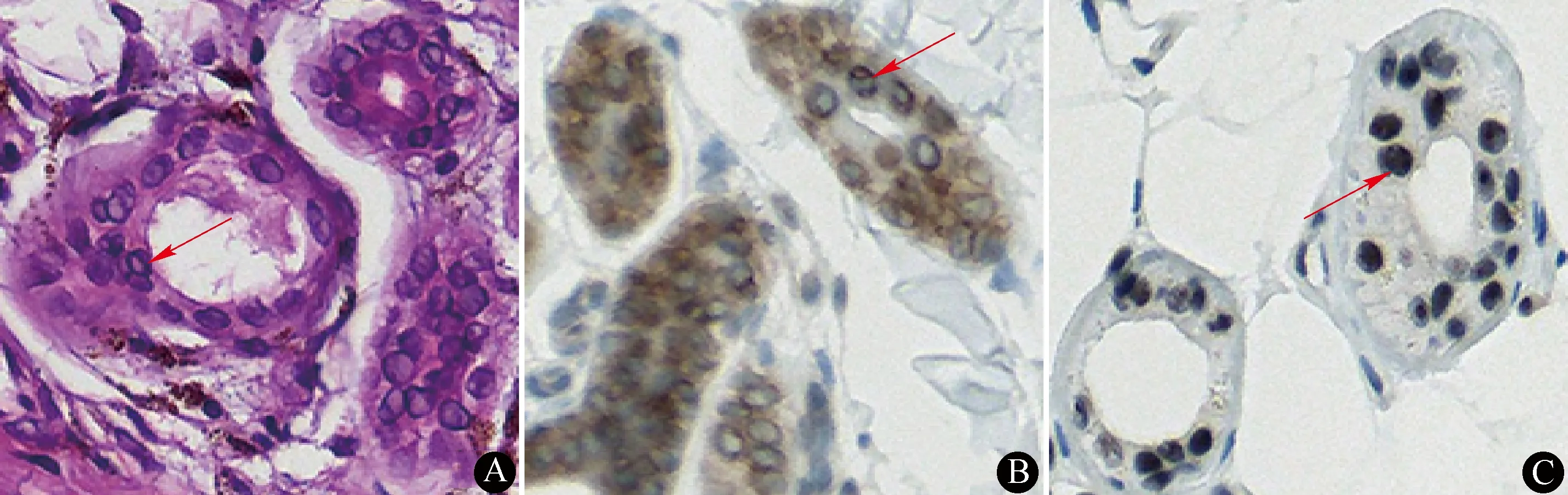
图2 患者皮肤活检病理图片:部分真皮层部分汗腺腺体细胞核内见透明嗜酸性包涵体,HE染色×200(箭头所示,A);部分汗腺细胞核内可见抗p-62阳性的包涵体,免疫组化×200(箭头所示,B);抗泛素蛋白阳性的包涵体,免疫组化×200(箭头所示,C)

图3 TP-PCR结果显示:NOTCH2NLC基因5′非翻译区GGC异常重复扩增

图4 PCR结果显示:GGC重复扩增次数155次〔≥60次即具有致病性;重复扩增次数=(DNA长度-154)/3〕
2 讨论神经元核内包涵体病(neuronal intranuclear inclusion disease,NIID)是一种罕见的多系统慢性进展性神经变性疾病,该病以其病理特征命名,由染色体1q21中NOTCH2NLC基因5′非翻译区的GGC重复序列扩增导致[1]上游非AUG启动翻译产生聚甘氨酸(poly-G)或聚丙氨酸(poly-A),从而诱导包涵体聚集和细胞毒性[2]。
NIID成年型分为散发型和家族型,临床以散发型多见,患者以痴呆为首发症状和主要临床表现,病程进展中常见意识障碍、感觉障碍、自主神经症状、精神异常行为、亚急性发作性脑病症状[3]等,少部分患者有共济失调、僵直、震颤和全身性惊厥。家族型NIID肢体无力型以肢体乏力为首发症状,自主神经功能障碍和远端感觉障碍明显,恶化较为缓慢;痴呆型主要表现为认知功能障碍,伴有轻微的周围、中枢及自主神经症状。既往报道亦有因反复发作的偏头痛、膀胱功能障碍、癫痫发作、脑卒中样发作、发作性小脑共济失调、反复发作的Miller-Fisher综合征以及眼肌麻痹和肌无力等起病的NIID患者[2],国内目前关于震颤为首发症状的NIID仅见1例报道[4]。依据Sone 等在2016年推荐的NIID的诊断流程[6],本病例报道患者系散发型,40岁以震颤起病,呈持续进展的单向病程,疾病迁延过程中临床表现有:(1)中枢神经系统受累:包括头痛、认知功能减退、发作性意识障碍、精神行为异常、步态不稳;(2)周围神经症状:肌电图提示多发周围神经损害;(3) 自主神经症状:包括腹胀、恶心呕吐、便秘,查体可见双侧瞳孔缩小。研究发现震颤可能仅仅是NIID的早期临床表现之一,随着病程的进展,临床症状逐渐出现,影像学特征逐渐明显。此类患者需长期随访[6]。
MRI检查在NIID诊断中不可或缺,DWI序列皮髓质交界处火焰样(曲线样、鸡冠花样、绸带样)高信号为NIID特征性表现,随病情进展从前向后广泛受累,仅局限在皮髓质交界,可能与U型纤维多发灶性海绵样变有关[7],是进一步采取皮肤活检明确诊断的首要条件[8]。T2WI序列脑皮层下白质区弥漫对称性、斑片状高信号灶,可能与脑白质区星形胶质细胞功能障碍有关[9],信号越广泛,提示病情越严重,影像科医生容易误认为急性脱髓鞘改变。另外NIID患者还可出现幕上脑室扩大、小脑萎缩、脑膜强化或皮层脑回样强化等影像学表现。本病例报道患者DWI序列双侧脑室旁、胼胝体压部、额顶叶皮髓质交界处出现弥散受限高信号,与NIID特征性影像学DWI序列皮髓质交界处火焰样高信号表现一致。
早期NIID主要通过尸检等途径发现神经元核内包涵体(neuronal intranuclear inclusion,NII),2011年,Sone等[10]发现皮肤汗腺细胞NII病理学特点与神经元NII一致,皮肤活检作为微创病理检查具有很高病理诊断价值,且p62和泛素免疫组化更易发现NII的存在,使NIID诊断率大大提高。近年来关于NIID基因学研究报道愈来愈多,成年型NIID均为杂合性突变导致的常染色体显性遗传,NOTCH2NLC基因5′UTR中的短串联重复序列GGC正常扩增上限低于40次,超过60次即具有致病性,且与临床表现复杂多样性相关[6]。本病例报道患者经皮肤病理活检确诊,完善基因检测发现NOTCH2NLC基因的5′UTR区域GGC突变重复扩增155次,明显超过正常正常扩增次数。
NIID因具有极大的临床异质性,特别是当一些患者表现出单一器官受累或单一症状时,很容易导致临床误诊或诊断不足,其中突发意识障碍、谵妄或精神症状、癫痫、卒中样发作、脑炎样表现等发作性脑病是成人NIID的一个重要且强有力的诊断指标。目前NIID 尚无特异性治疗方法,在患有发作性脑病的成年起病NIID患者中,使用皮质类固醇未观察到明确的效果,主要以对症治疗为主。
