市售双氯芬酸钠肠溶片探索性研究
2022-08-18巩峰贤齐衍超李子静杨丽蓉赵海鹏
巩峰贤 齐衍超 李子静 谭 颖 杨丽蓉 赵海鹏▲
1.潍坊市检验检测中心,山东潍坊 261200;2.山东医学高等专科学校,山东临沂 276000
双氯芬酸钠是邻氨基苯甲酸类非甾体抗炎药,通过抑制环氧合酶(COX)的活性,阻断花生四烯酸转化为前列腺素,从而达到解热、镇痛和抗炎的作用[1-2]。临床上用于急慢性风湿性关节炎或类风湿性关节炎等,也可用于痛经、感冒、头痛及肌肉痛等症状[3-5]。经文献检索,双氯芬酸钠是一类无定型化合物,解离常数pKa值(25℃)为3.8,药物的溶解度显示出pH依赖性,为BCSⅡ类药物(即低溶解度、高渗透性药物)[6]。由于双氯芬酸钠遇酸不稳定且对胃黏膜具有刺激性,它的口服制剂通常制成肠溶制剂,多数是通过片芯或微丸包肠衣的方式来降低药物的不良反应[7-8]。双氯芬酸钠肠溶片的原研厂为诺华制药有限公司,于1974年首次国际上市,国内于1986年首次上市,现收录于《中华人民共和国药典》(二部)[9]。
本研究通过采用法定标准检验以及针对不合格项目开展的探索性研究,结合统计学分析,旨在评价双氯芬酸钠肠溶片的整体质量,为该品种的安全监管和质量标准完善提供参考。
1 仪器与试药
1.1 仪器
Ultimate 3000型Thermo高效液相色谱仪;Agilent 708+850DS溶出自动取样系统(安捷伦科技有限公司);KQ-700VDE型超声波清洗器(昆山市超声仪器有限公司);XSE-205DU型电子天平(METTLER TOLEDO公司,);UV2450紫外可见分光光度计(日本岛津公司)。
1.2 试药
双氯芬酸钠对照品(中国食品药品检定研究院,批号:100334-201803,含量为100%),邻苯二甲酸二乙酯(Sigma-Aldrich,批号:1912500,含量为99.5%),甲醇(色谱纯),冰醋酸(国药集团化学试剂有限公司,浓度:99.5%),盐酸(国药集团化学试剂有限公司,浓度:36.5%),水为纯化水,其他试剂均为分析纯。
1.3 样品
本次抽检的双氯芬酸钠肠溶片共44批次,涉及生产企业14个,其规格均为25 mg,其中A企业为北京诺华制药有限公司。其肠溶包衣分为薄膜衣型肠溶衣24批次(占比54.5%)和糖衣型肠溶衣20批次(占比45.5%)两种。
2 溶出度的HPLC检测方法研究
参照《中华人民共和国药典》(二部)[9]“双氯芬酸钠肠溶片”项下的含量测定方法,重点对其专属性进行考察,建立了溶出度的HPLC检测方法。
2.1 色谱条件
色谱柱:Agilent ZORBAX Eclipse Plus C18色谱柱(4.6 mm×250 mm,5 μm),进样量:20μl,柱温:30℃,检测波长:276 nm,二极管阵列检测器,流动相:甲醇-4%冰醋酸溶液(70∶30),流速:1.0 ml/min。
2.2 溶液的制备
2.2.1 溶出介质制备 参照《中华人民共和国药典》(二部)[9]“双氯芬酸钠肠溶片” 溶出度项下磷酸盐缓冲液的制备方法。取0.1 mol/L盐酸溶液和0.2 mol/L磷酸钠溶液,按3∶1混合均匀,必要时用2 mol/L盐酸溶液或2 mol/L氢氧化钠溶液调节pH值至6.8。
2.2.2 对照品储备液配制 取双氯芬酸钠对照品约10 mg,精密称定,置于100 ml量瓶中,用磷酸盐缓冲液(pH 6.8)溶解并稀释至刻度,摇匀,作为对照品储备液。
2.2.3 供试品溶液制备 取A企业(批号:X1366)样品,按照《中华人民共和国药典》(二部)[9]“双氯芬酸钠肠溶片”溶出度项下测定,转速100 r/min,溶出介质体积为1000 ml,温度(37.0±0.5)℃,于45 min适量取样,用0.45μm微孔滤膜滤过,取续滤液作为供试品溶液。
2.2.4 空白辅料溶液制备 按照处方比例称取空白辅料(D企业提供),溶于1000 ml溶出介质,过滤,取续滤液即得。
2.3 专属性考察
2.3.1 系统适用性试验 取双氯芬酸钠对照品适量,用水制成l mg/ml的溶液,取适量该溶液,暴露于紫外光灯(254 nm)下照射15 min,取20 μl注入液相色谱仪,记录色谱图,在与主峰相对保留时间约0.8处出现一杂质峰,两者的分离度> 4.0。
2.3.2 空白辅料干扰试验 取溶出介质、空白辅料溶液、对照品溶液、供试品溶液,均照“2.1”项下色谱条件进样,记录色谱图(图1)。由图谱可知,主成分处无空白干扰峰;经二极管阵列检测器软件分析,对照品与样品主成分峰纯度均> 990,表明空白辅料对主成分的测定无干扰。

图1 空白辅料干扰试验色谱图
2.4 线性关系考察
取对照品储备液,用溶出介质分别稀释配制成含双氯芬酸钠2.7、5.3、13.3、26.7、53.4和106.7μg/ml的系列溶液。照“2.1”项下色谱条件分别进样测定,记录峰面积。以各对照品浓度为横坐标、峰面积为纵坐标,计算得线性方程为Y=44.192X-39.439,R2=0.9999,结果表明双氯芬酸钠在2.7~106.7μg/ml范围内,浓度与峰面积呈良好线性关系。
2.5 精密度考察
精密量取对照品溶液20μl,照“2.1”项下色谱条件连续进样6次,计算双氯芬酸钠峰面积的RSD值为0.12%,进样精密度良好。
2.6 溶液稳定性考察
取“2.2.3”项下的供试品溶液,室温条件下,分别于0、2、4、6、12、18、24 h进样,照“2.1”项下色谱条件,记录色谱图峰面积,计算双氯芬酸钠峰面积的RSD值为0.69%。结果表明供试品溶液在24 h内稳定。
2.7 样品溶出度测定
采用建立的HPLC法对14个生产企业44批次双氯芬酸钠肠溶片在45 min时的溶出度进行测定,并与原UV法结果进行比较,结果显示两类测定方法对应数值总体趋势基本一致。
3 结果分析
3.1 现行质量标准检验
双氯芬酸钠肠溶片执行《中华人民共和国药典》(二部)[9]标准,其标准项下检验项目包括性状、鉴别(HPLC鉴别及UV鉴别)、有关物质、溶出度、重量差异、含量测定等。其中对该药的质量控制以溶出度测定和含量测定为主。依据法定标准检验44批次样品,结果43批次符合规定,合格率为97.7%;1批次样品的不合格项目为溶出度检查项。检验中发现,溶出度测定方法采用紫外-可见分光光度,专属性不强,测定时易受辅料的干扰。
3.2 探索性研究
3.2.1 建立了溶出度的HPLC检测方法 参照《中华人民共和国药典》(二部)[9]该品种含量测定项的方法,建立了双氯芬酸钠肠溶片溶出度的HPLC检测方法,并重点对其专属性进行考察。以十八烷基硅烷键合硅胶为填充剂,检测波长为276 nm,以甲醇-4%冰醋酸溶液(70∶30)为流动相进行测定。采用建立的方法对14个生产企业的44批次双氯芬酸钠肠溶片溶出度进行测定(表1),结果显示,样品在45 min时溶出度数值与UV法测定数值总体趋势基本一致,但发现不合格品种(H厂家样品)两种方法的结果差异较大,可能因为辅料对UV法产生较大干扰,进一步表明HPLC方法更加适合该品种的溶出度检测。
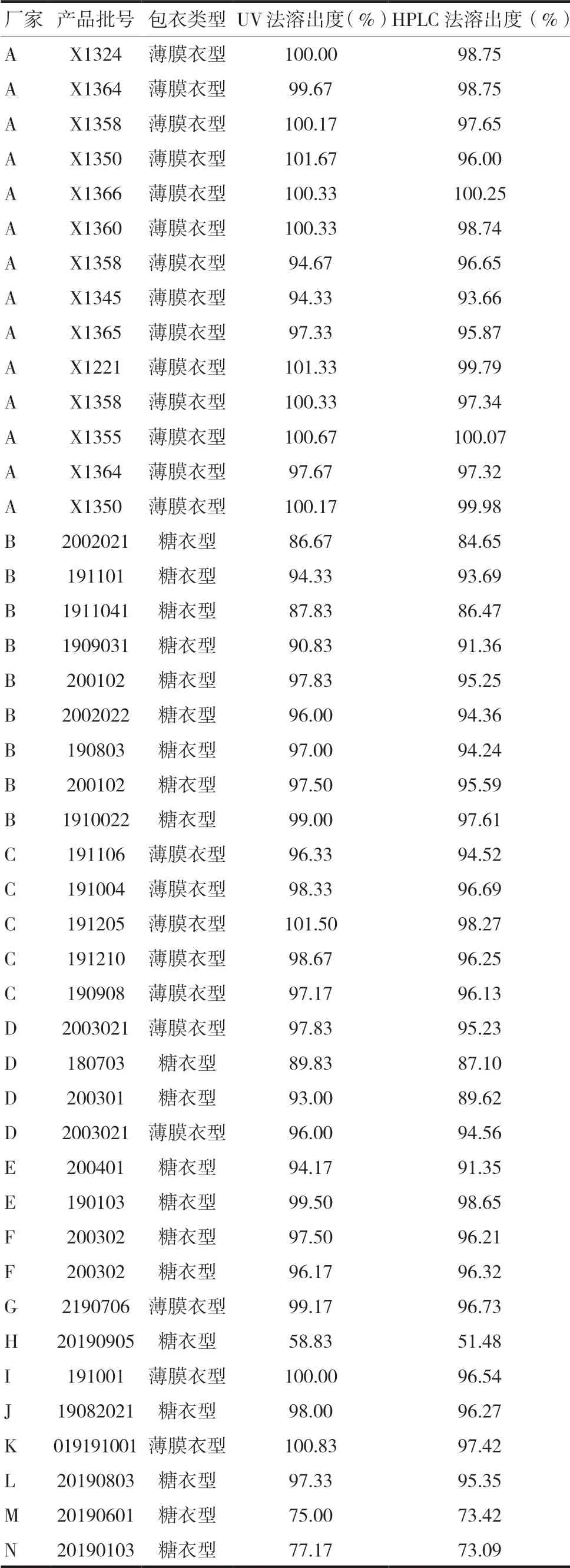
表1 各厂家溶出度HPLC法与UV法测定结果比较表
3.2.2 包衣工艺对溶出度的影响 依据法定标准对24批次薄膜衣型肠溶衣片和20批次糖衣型肠溶衣片的溶出度进行检验(图2),结果显示,薄膜衣型的肠溶片的平均溶出量高于糖衣型的平均溶出量,且薄膜衣型肠溶片的相对偏差较小,生产工艺较为稳定。
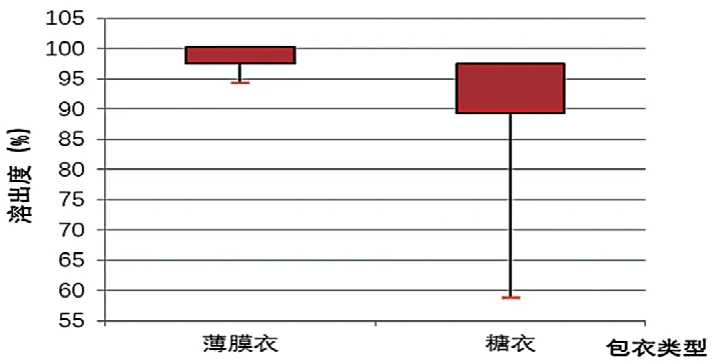
图2 不同包衣类型的双氯芬酸钠肠溶片溶出度箱线图
3.2.3 不同厂家双氯芬酸钠肠溶片f2相似因子比较 优质药品可在任何体内环境下都有一定的崩解、溶出或释放,即对任何体质的患者均有较高的生物利用度[10-11]。以原研企业(A企业)生产的双氯芬酸钠肠溶片为参比制剂,对其他厂家在45 min时的f2相似因子进行释放度的比较和评价。结果显示,13个厂家中只有6个厂家的f2相似因子>50.00,相似率仅为46%(表2)。通过比较不同包衣类型f2相似因子数值可知,薄膜衣型肠溶包衣的溶出性能明显优于糖衣型肠溶包衣片。
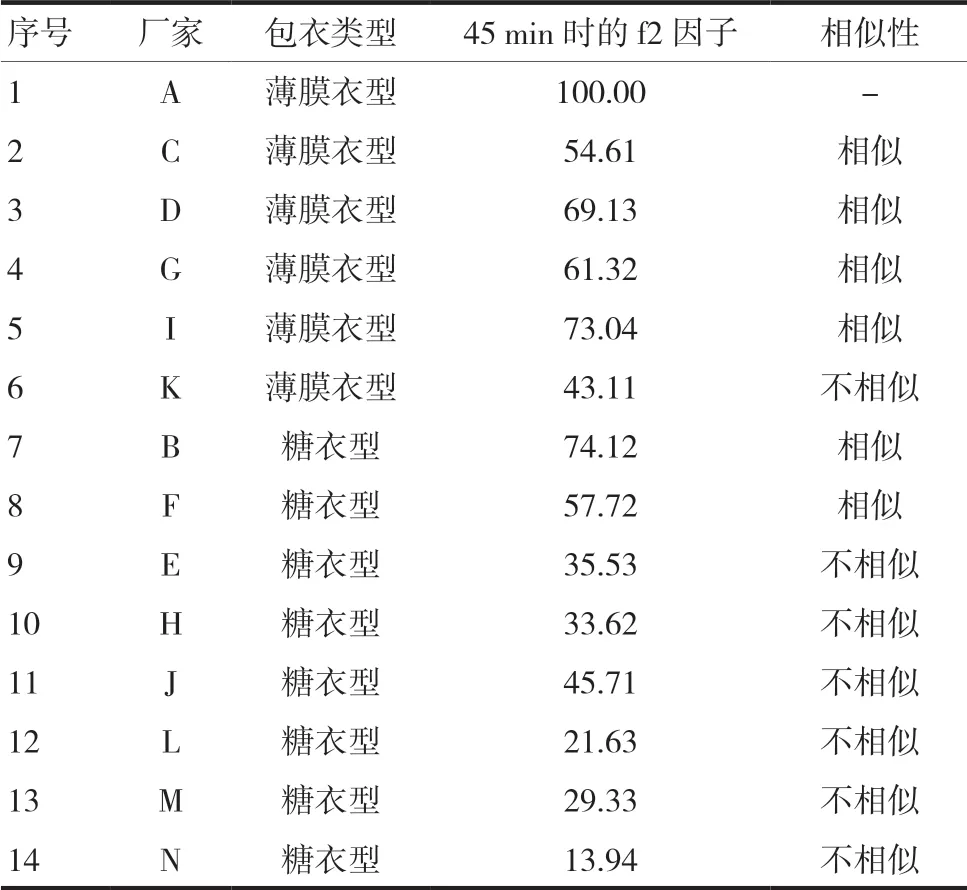
表2 14个厂家双氯芬酸钠肠溶片f2相似因子
4 讨论
4.1 针对双氯芬酸钠肠溶片制剂片芯处方与包衣过程对其溶出度的影响开展探索性研究
本研究通过采用法定检验与探索性研究相结合的方式,重点围绕影响双氯芬酸钠肠溶片质量的溶出度检查项目进行探索性研究,研究探讨该剂型片芯处方与包衣过程对其溶出度的影响。
文献报道,肠溶制剂的溶出行为常取决于肠溶包衣的溶解速率与片芯的溶出速率[12-13]。因肠溶包衣的溶解需要一定时间且不是一个均匀溶解的过程[14],故保证制剂肠溶包衣的溶解速率与片芯的溶出速率稳定是避免制剂批间不等效的有效手段。因此,双氯芬酸钠肠溶片的关键工艺参数为包衣过程与制剂片芯处方中各辅料组分的比例。通过查阅资料及对D企业的调研,双氯芬酸钠肠溶片片芯处方中一般都含有淀粉、糊精、微晶纤维素、羧甲淀粉钠、乙醇及硬脂酸镁等辅料,包衣处方中一般都含有蔗糖、邻苯二甲酸二乙酯、聚丙烯酸树脂、蓖麻油、聚山梨酯-80、滑石粉等辅料。肠溶片片芯一般生产工艺为:配料→粉碎过筛→制粒→干燥→整粒→总混→压片→片芯。包衣的一般程序为:片芯→隔离层→肠溶层(→粉衣层→糖衣层→色糖层)→打光→除湿。由于工业化生产时制剂处方固定,且其含量测定结果波动不大,提示导致样品体外溶出行为差异大的主要影响因素可能与关键步骤工艺的操控条件不当有关,例如素片处方(如崩解剂、助流剂、赋形剂等)、素片压片过程(如温湿度控制、压片机压力)、肠溶包衣过程(如包衣设备,包衣时间)等。
4.2 针对不合格项目开展探索性研究
双氯芬酸钠肠溶片的常见包衣材料为聚丙烯酸树脂,丙烯酸树脂物理化学性质稳定,不会与包衣药物发生相互作用,并且可以在指定条件下释放出被包裹的药物[15]。可以溶解丙烯酸树脂介质的pH值随共聚物中甲基丙烯酸含量的增高而降低,即包衣处方中含甲基丙烯酸比例越高,其对酸的耐受力越差[16]。研究发现,H厂家的样品在溶出度测定过程中,包衣未全部溶散,溶出度值明显偏低,且批内溶出度的RSD值较大。分析其原因可能是包衣材料选取不当、包衣增重过大或包衣工艺不稳定。
通过研究发现,国内只有少数厂家样品质量综合指标与原研厂接近,质量堪忧。建议督促国产企业进一步研究该产品的处方工艺及制剂工艺,不断提高产品溶出批间的重复性和批内均一性,提升产品质量。本研究建立了溶出度的HPLC检测方法,实现了与含量测定项检测方法的统一,专属性更强、效率更高,能更准确地反映该品种的溶出度结果。
