单孔腹腔镜及超声监测下子宫腺肌瘤微波消融术的临床效果
2022-08-10周丽娜孟焕然宋琳琳马亚楠杨彩虹
周丽娜,孟焕然,宋琳琳,马亚楠,杨彩虹
子宫腺肌瘤是指子宫肌层中出现子宫内膜呈局限性生长逐渐形成结节、团块,类似子宫肌壁间肌瘤样。主要表现为月经紊乱,经量增多、经期延长、继发性痛经进行性加重和不孕等,严重影响女性的生活质量[1]。子宫腺肌瘤治疗方法有药物及手术治疗,前者治疗周期长、副反应重、价格昂贵,患者接受度低。后者虽然可明显缓解患者的一般状况,但出血多,手术时间长,术后恢复慢;对于药物治疗失败且要求保留子宫的患者,需要更微创、有效且安全的治疗手段解除病痛[2]。近几年,超声引导下经皮微波消融术作为一种更新、更微创的介入治疗手段被引入,具有创伤性小、安全性高、操作简单等优势。而单孔腹腔镜及阴道超声监测下,更能够较好地选择穿刺路径,避免周围脏器损伤,把控消融范围。同时部分腺肌瘤病人合并盆腔粘连及巧囊,单孔腹腔镜监测下可有效地松解粘连并剥除囊肿,提高了手术的安全性[3]。本研究旨在探讨单孔腹腔镜及超声监测下子宫腺肌瘤微波消融术的临床效果。
1 资料与方法
1.1 一般资料:选取2019年10月至2021年10月就诊于宁夏医科大学总医院心脑血管病医院妇科,因子宫腺肌瘤行单孔腹腔镜及阴道超声监测下子宫的患者为观察组,对照组为超声监测下行子宫腺肌瘤微波消融术腺的患者,每组各44例。观察组年龄32~50岁,平均(41.50±3.51)岁;病程4个月~4年,平均(2.59±1.12)年;腺肌瘤直径4~12 cm,平均(6.74±1.35)cm。对照组年龄31~48岁,平均(39.0±5.31)岁;病程4个月~5年,平均(2.85±0.86)年;腺肌瘤直径4~13 cm,平均(6.95±1.04)cm。2组患者一般资料具有可比性(P>0.05)。纳入标准:①术前自愿选择手术方式,并签署手术同意书;②药物保守治疗失败,且坚决要求保留子宫;③患者有痛经,月经量大,贫血及自觉下腹部包块的症状[4]。排除标准:①怀疑妇科恶性肿瘤及急性盆腔炎症;②妊娠期及严重凝血功能异常的患者;③肾功能异常[4]。
1.2 仪器及方法
1.2.1 仪器及设备:采用奥林巴斯电子腹腔镜;采用女娲Resona8超声诊断仪,阴式探头 ;采用KY-2000型微波治疗仪(南京康友医疗科技有限公司),输出频率为2 450 MHz,输出功率为50~70 W。微波消融针规格为2.0 mm,冷循环液为冰冻生理盐水。造影剂是六氟化硫微泡。
1.2.2 术前准备:完善血常规、凝血全套及肝肾功能等术前检查,无明显手术禁忌证;术前口服聚乙二醇电解质散经口清洁灌肠,以免手术操作过程中肠管胀气影响手术;签署手术及麻醉同意书[5]。
1.2.3 手术方法:手术由经验丰富的主任医师、主治医师及超声科主任医师共同完成。单孔腹腔镜及阴道超声监测下子宫腺肌瘤微波消融术的方法为取膀胱截石位,全麻后消毒铺单,在超声造影指导下定位病灶,评估其大小、位置、范围及血供情况,单孔腹腔镜监测下,消融针选择最佳路径避开血管、肠管及膀胱进入到盆腔,若术中发现盆腔粘连,则先行粘连松解术,其次穿透子宫浆膜层进入子宫肌层及病灶内,全程由阴道超声监测[6]。开启微波治疗仪,60 W为输出功率,消融3 min后退针1 cm,病灶较大时持续消融3 min,由深到浅,逐步移动靶点,消融全过程由阴道超声监测,直至高回声到达预定消融边界且病灶组织逐渐气化时停止消融,沿针道退出消融针。同时需注意观察造影剂在消融区的变化情况,凝固坏死病灶常表现为无造影剂灌注[7]。而超声监测下子宫腺肌瘤微波消融术的方法为术中超声引导下先穿刺活检,然后进行腺肌瘤消融,手术操作方法与观察组相同,但全程仅有超声监测,通过超声确定病灶消融范围。
1.3 疗效评估:分析两种不同术式的子宫腺肌瘤微波消融术,术后3、6个月及1年复查阴道B超、CA125、血常规及口述评分法(VRS评分)评估痛经缓解程度等各项临床指标,进行组内与术前比较,组间比较,进一步分析两种不同术式的子宫腺肌瘤微波消融术术后患者子宫及腺肌瘤体积变化,痛经缓解情况、经量及贫血改善情况的差异性[7]。子宫体积V(cm3)=长×宽×高×0.523。病灶体积V(cm3)=长×宽×高×0.523[8]。痛经分级同时通过视觉模拟疼痛量表VAS评分:0分代表无痛经;1~3分代表轻度疼痛,伴腰酸,可以忍受;4~6分代表中度疼痛,经期疼痛明显,必要时需服用镇痛药物才能缓解,睡眠受影响;7~10分代表重度痛经,无法忍受,严重干扰睡眠及食欲。最后分析术后常见并发症发生情况及相应处理措施[9]。
1.4 统计学方法:采用SPSS 18.0统计软件,计量资料多组间比较采用方差分析,正态分布计量资料2组间比较采用t检验,计数资料采用χ2检验,以P<0.05 表示差异有统计学意义。
2 结果
2.1 2组患者术前术后子宫体积、腺肌瘤大小比较:观察组及对照组术前与术后3、6个月及1年的子宫及腺肌瘤体积相比差异有统计学意义(P<0.05),见表1至表2,图1(封三)。
2.2 2组患者术前、术后CA125及HGB水平:2组患者术前均有不同程度贫血,且肿瘤标记物CA125也升高,术后3、6个月及1年复查CA125后,2组均较术前明显下降(P<0.05)。术后复查血红蛋白2组均较术前明显升高(P<0.05),见表3至表4。
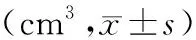
表1 2组患者术前、术后子宫体积比较
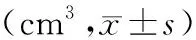
表2 2组患者术前、术后腺肌瘤大小比较
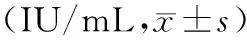
表3 2组患者术前、术后CA125比较
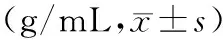
表4 2组患者术前、术后HGB比较
2.3 通过VAS评估痛经缓解情况:术后3、6个月及1年,2组患者痛经随着时间的延长明显较术前缓解(P<0.05),见表5。
2.4 2组术后并发症:观察组术后并发症15例(34.1%),对照组术后并发症19例(43.2%),2组比较差异无统计学意义(χ2=1.61,P>0.05)。

表5 2组通过VAS评估痛经缓解情况
3 讨论
子宫腺肌瘤是常见的妇科疾病,发病原因主要是由于子宫内膜腺体及间质异位到子宫肌层,随着月经周期的变化,在雌激素的作用下,子宫体积不均匀增大形成腺肌瘤[10],主要以月经量增多、继发性痛经进行性加重、月经周期紊乱、子宫增大、下腹包块等为主要临床表现,严重影响着女性的生活质量[11]。近几年,子宫腺肌瘤的发病率逐年提高,且发病年龄趋于年轻化,严重威胁到了女性的身心健康。目前对于该病的主要治疗方法有药物保守治疗与手术[12]。但是药物治疗周期较长且药物副反应重、价格昂贵,对于一些药物治疗效果差的患者,往往建议手术治疗。微创手术方式常常有保留子宫的腹腔镜下腺肌瘤病灶切除术或者根治性子宫全切术,但两种手术方式手术时间均较长,且术中出血多,腺肌瘤病灶易合并盆腔重度粘连,而松解粘连时易导致严重并发症。近几年,随着疾病的年轻化且越来越多女性要求保留子宫,超声阴道下微波消融术作为一种更微创、更经济、更简单的手术方式被广泛应用,其主要原理是微波所产生的热能量使病灶组织蛋白质变性,凝固坏死,最终被正常组织吸收或者排出[13]。
本研究主要是对两种术式,即单孔腹腔镜及超声监测下子宫腺肌瘤微波消融术与超声监测下子宫腺肌瘤微波消融术进行对比分析。观察组较对照组不同之处在于引入了单孔腹腔镜,这种经自然腔道的单孔腹腔镜监测更能有效地选择最佳的穿刺路径,从而较好地避开了血管、膀胱、肠管等脏器的损伤,若术中发现粘连及合并卵巢囊肿时可松解粘连带的同时剥除囊肿[14]。除此之外,腹腔镜及阴道超声监测下子宫腺肌瘤消融能严格避免对子宫内膜的损伤,把控消融范围,对于一些有生育要求的年轻患者而言是极大的福音[14]。本课题通过对比单孔腹腔镜及阴道超声监测下子宫腺肌瘤微波消融术与超声监测下子宫腺肌瘤消融术,分析比较术前及术后3、6个月及1年子宫体积、腺肌瘤体积及相关实验室指标、临床表现变化等,发现2组术后子宫体积及腺肌瘤明显缩小,且经量明显减少,贫血症状明显改善,痛经症状极大缓解,组内比较差异均有统计学意义(P<0.05)。而单孔腹腔镜及超声监测下子宫腺肌瘤微波消融术的最大优势在于全程可视化操作,术中及术后均未发现膀胱、肠管损伤,同时对于合并巧囊或者盆腔粘连的患者,术中可一并解决,相比单纯的超声监测下子宫腺肌瘤消融术,联合单孔腹腔镜监测占了更大的优势,病人也获益更多。2组常见的并发症如术后腹痛及阴道排液患者,考虑与子宫收缩及腺肌瘤组织凝固性坏死排出有关,腹痛发生在术后1~3 d,给予布洛芬止痛处理后明显缓解[8]。阴道异常排液常见于术后1~3周,考虑腺肌瘤组织凝固性坏死经阴道排出引起,偶伴有发热,以低热为主,给予补液、物理降温及阴道擦洗放药后明显缓解[10]。若术后出现高热,不能排除外感染可能时还需抗生素抗炎治疗。术后恶心、呕吐并发症少见,考虑与麻醉药物引起有关,给予胃复安缓解胃部不适。所以单孔腹腔镜及超声监测下子宫腺肌瘤微波消融术是一项安全性高、精准度高,更加微创、简单的诊疗技术,值得广泛推广。
