苏北灌河口多介质多环芳烃污染调查及生态风险分析
2022-08-06于英鹏蒋玉波
于英鹏,蒋玉波
(1.盐城师范学院, 城市与规划学院,江苏 盐城 224007;2.盐城师范学院, 苏北农业农村现代化研究院,江苏 盐城 224007;3.盐城师范学院, 盐城城乡融合发展研究院,江苏 盐城 224007)
多环芳烃(PAHs)是一类具有三致效应(致癌、致畸和致突变)的持久性有机化合物。PAHs广泛分布于环境中,对生态环境和人体健康具有严重危害性,其特殊的理化性质和三致效应,对生态系统造成危害的机理更复杂、作用更隐蔽、效应更持久,因而倍受学术界关注[1-2]。河口地区受海陆过程的交互影响,理化特征变化剧烈,环境过程复杂,具有较高的科学研究价值[3-5]。环境中的PAHs通过干湿沉降和径流等途径进入河口系统,对河口地区产生严重的影响和潜在危害。因此,在河口地区由PAHs所引起的环境与健康问题一直被广泛关注。
目前,关于苏北河口地区环境污染的报道越来越多,但受经济发展与区位因素的影响,相关科学研究对苏北小型河口地区的关注远低于其他地区[6-7]。近年来,关于苏北主要入海河道生态环境的研究虽有开展,但研究多关注重金属、无机盐及水体常规监测污染物的检测分析,而对多介质中PAHs的研究却少有报道[8-11]。因此,开展苏北灌河口典型介质中PAHs污染调查及生态风险评价具有重要的理论和实际意义,以期为江苏沿海大开发过程中的环境管理工作提供科学依据和数据支撑。
1 研究方法
1.1 研究区概况
灌河地处黄海中部(119°29′~120°17′E,34°18′~34°45′N),是苏北地区最大的入海潮汐河流。河口宽约350 m,深7~11 m,干流长约74.5 km,流域面积8 000 km2,年径流量约5×108m3。灌河口宽阔,呈喇叭状,潮汐差大。从2000年开始,灌河口地区以堆沟港镇、陈家港镇和燕尾港镇为中心,沿灌河两岸工业区迅速发展并形成相当规模,工业区主要以火力发电、石油化工和有机材料化工为主。此外,灌河口建有国家一类开放口岸——响水港,随着苏北沿海经济快速发展,港口货物吞吐量逐年增加。快速的工业化过程和进出港船舶污染物的排放给河口地区环境带来了极大压力。
1.2 采样时间
于2018年1, 7和11月在灌河口采集水样(包含水相和悬浮颗粒物)、沉积物、植被和生物样品。
1.3 样品采集
采样点位分布示意见图1。于1月(枯季)和7月(洪季)采集水样(枯季和洪季各采集3个样品)、光滩沉积物(枯季和洪季各采集3个样品);7月采集芦苇和互花米草及植株根系附近沉积物(各采集3个样品);7和11月采集螃蟹样品(毛蟹和无齿相手蟹共16个样品),总计37个样品。样品采集后快速运回实验室进行处理,沉积物冷冻保存,植物样品清洗干净,蟹类分雌雄去壳,取软组织冷冻风干保存。

图1 采样点位分布示意
1.4 样品处理
水相:将水样进行抽滤分离出水相和悬浮颗粒物,利用固相萃取(SPE)法对水相中PAHs进行吸附,利用二氯甲烷和乙酸乙酯(V∶V=1∶1)进行洗脱,洗脱液经氮吹后上机分析。
悬浮颗粒物:将冷冻风干后的滤膜剪碎,加入适量铜粉和石英砂并填装装于加速溶剂萃取仪(Dionex ASE300,美国赛默飞世尔科技有限公司)萃取池中,利用二氯甲烷和丙酮混合溶剂(V∶V=7∶3)进行萃取,萃取液经旋转蒸发浓缩至2~3 mL后过硅胶氧化铝层析柱净化(湿法填装,V∶V=2∶1),分别用15 mL正己烷和70 mL二氯甲烷和正己烷的混合溶剂(V∶V=3∶7)淋洗出烷烃和芳烃组分,含芳烃组分进行溶剂置换后定容至1 mL,进行气相色谱-质谱分析。
植株:将植物样品剪碎后称取2 g(干重)填入已净化滤纸筒,索氏抽提器回流提取24 h,萃取试剂为二氯甲烷和丙酮混合液(120 mL,V∶V=1∶1),水浴温度为70 ℃,萃取液净化与定容过程同悬浮颗粒物样品。
沉积物:称取3 g沉积物(干重)填入滤纸筒,索氏抽提器回流提取24 h,提取方法、萃取液净化与定容过程同植物样品。
蟹:取冷冻风干的蟹组织3 g置于滤纸筒,索氏抽提器回流提取24 h,提取方法、萃取液净化与定容过程同植物样品。
1.5 仪器及分析条件
1.5.1 仪器
选用气相色谱-质谱联用仪(GC-MS,7890A-5975C,美国Agilent 公司)对16种PAHs进行分析测试[萘(NA)、苊烯(ACL)、苊(AC)、芴(FL)、菲(PHE)、蒽(AN)、荧蒽(FA)、芘(PY)、苯并[a]蒽(BaA)、(CHR)、苯并[b]荧蒽(BbFA)、苯并[k]荧蒽(BkFA)、苯并[a]芘(BaP)、茚并[1, 2, 3-cd]芘(IP)、二苯并[a, h]蒽(DBahA)、苯并[g,h,i]苝(BghiP)]。DB-5聚硅氧烷聚合物色谱柱(30 m×0.25 mm×0.25μm,美国Agilent公司)。
1.5.2 气相色谱条件
色谱柱升温流程:色谱柱进样口温度55 ℃,保持2 min,按照20 ℃/min编程升温至280 ℃,再经过10 ℃/min上升到达310 ℃,持续5 min;载气纯度为高纯氦气(99.999%),流量:1 mL/min。
1.5.3 质谱条件
离子源:EI源;离子源温度:230 ℃;离子化能量:70 eV;扫描模式:离子模式(SIM);溶剂延迟3 min;传输线温度:280 ℃。
1.6 质量保证和质量控制
采样和分析过程中,加标空白、样品平行样和方法空白被用于质量保证(加标空白和方法空白实验各做2组,选10%样品做平行样实验)。加标空白实验回收率在74.7%~106.3%;每组平行样品的相对标准偏差(RSD)都保持在10%之内;方法空白实验未检测出目标污染物。方法检出限为0.07~0.12 ng/g。
2 结果与分析
2.1 水体中PAHs富集组成特征及生态风险分析
2.1.1 水体中PAHs富集特征
水体包含水相、悬浮颗粒物和沉积物。水相、悬浮颗粒物和沉积物中单体PAHs质量浓度和质量分数见表1。

表1 水相、悬浮颗粒物和沉积物中单体PAHs质量浓度和质量比
由表1可见,水相中总PAHs质量浓度范围为449~6 222 ng/L;悬浮颗粒物中总PAHs质量分数范围为131~6 644 ng/g;沉积物中总PAHs质量分数范围为147~1 840 ng/g。洪季水相PAHs质量浓度(1 698 ng/L)低于枯季(1 998 ng/L),这可能由于洪季上游来水量较大,对河口水体中污染物起到稀释的作用。悬浮颗粒物中PAHs质量分数均值在不同采样时期差异较大,枯季(2 987 ng/g)远高于洪季(630 ng/g),可能是由于洪季环境气温较高,光照使PAHs的降解过程比较强烈,另外洪季水中微生物及浮游植物生长和繁殖比较旺盛,对水体中PAHs的利用和降解较多,这些影响因素导致了洪季悬浮颗粒物中PAHs质量分数均值远低于枯季[12]。沉积物中PAHs质量分数均值同样呈现枯季(1 056 ng/g)高于洪季(558 ng/g)的特征。沉积物中PAHs质量分数均值在洪季和枯季的分布特征与水相和悬浮颗粒物相似。
2.1.2 水体中PAHs组成特征
通过不同环数单体PAHs质量浓度与16种PAHs(∑16PAHs)总的质量浓度比值可判断污染物来源。水相、悬浮颗粒物和沉积物中PAHs组成特征见图2(a)(b)(c)。
由图2(a)可见,枯季和洪季水相中PAHs主要以2+3环PAHs为主(平均占比分别为60.3%,60.4%),洪季水相中4环PAHs占比(36%)略高于枯季(35.7%),5+6环PAHs占比表现为枯季(4.0%)略高于洪季(3.6%),枯季和洪季PAHs组成特征总体上差异不大,说明水相中PAHs来源相对稳定。
由图2(b)可见,枯季和洪季悬浮颗粒物中PAHs仍然是2+3环PAHs为主(平均占比分别为46.5%,41.3%),相较于水相有所降低。4环PAHs占比枯季略高于洪季(枯季为38.1%,洪季为36.3%),而5+6环PAHs占比洪季高于枯季(洪季为22.4%,枯季为15.4%)。
沉积物中PAHs主要来源于上覆水体及颗粒物沉降,组成特征大体上与水相和悬浮颗粒物相似。由图2(c)可见,枯季沉积物中2+3环PAHs平均占比高于洪季,而4环,5+6环PAHs平均占比为洪季高于枯季。研究表明,环境中2+3环低环数PAHs主要来源于石油类产品(特别是精炼油产品)和化石燃料的不完全燃烧(低至中等温度燃烧),而4环,5+6环高环数PAHs来源于化石燃料的高温燃烧与裂解[13]。从研究区水相、悬浮颗粒物和沉积物中PAHs组成特征可大致推断工业区化石燃料不完全燃烧过程,港口往来船舶石油类泄漏是研究区各介质中PAHs主要输入源。
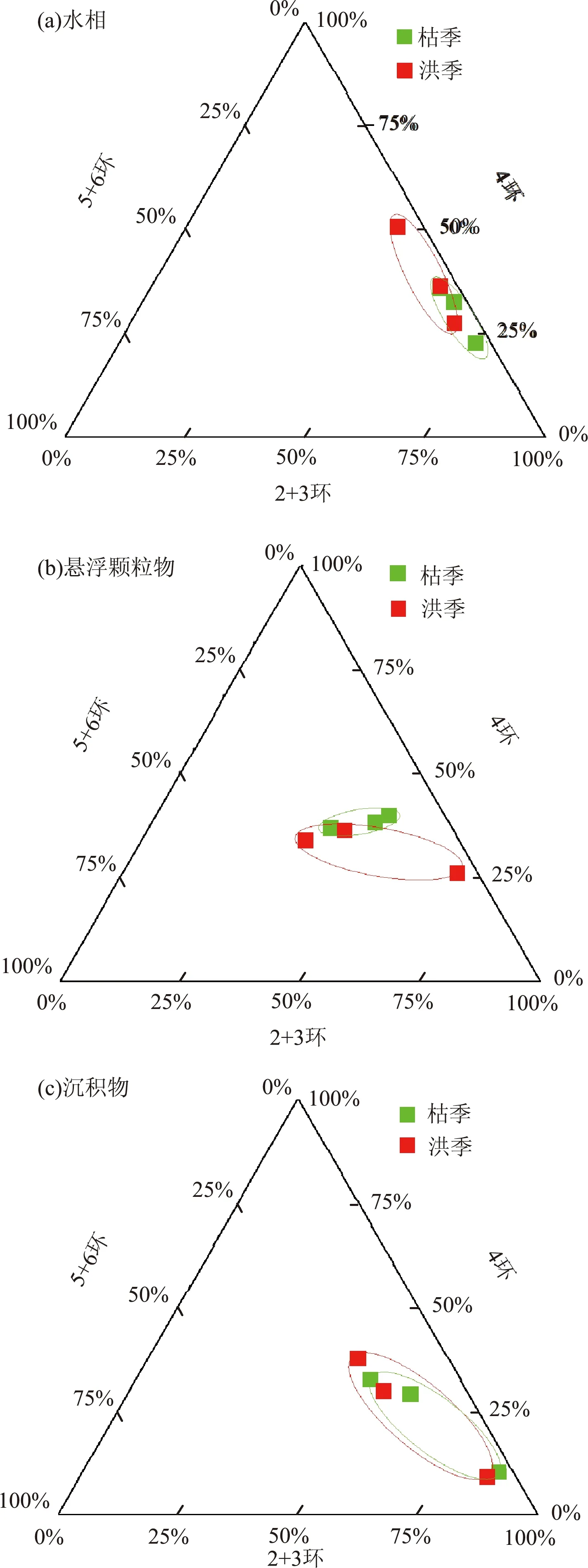
图2 水相、悬浮颗粒物和沉积物中PAHs组成特征
2.1.3 水体中PAHs生态风险分析
水生生物可摄入水环境中PAHs并通过食物链逐级富集放大,最终影响人类的健康。国外学者和国际生物学组织制定了评价水生生物暴露水体的生态安全标准[14-15]。研究区水相中PAHs质量浓度与美国环保署(US EPA)推荐水质量标准比较见表2。由表2可见,枯季水相中BaA、CHR、B[b+k]FA和IP质量浓度高于US EPA推荐水质量标准;洪季水相中,除NA、AN、BaP质量浓度高于枯季,AC质量浓度在洪季和枯季相等外,其他单体PAH质量浓度均低于枯季,但洪季水相中BaA、CHR和B[b+k]FA质量浓度同样高于US EPA标准。因此,建议加强河口区污染物的排放监管及监测工作。

表2 水生生物暴露于水体的安全食用标准 mg/L
Long等[16]和Chapman等[17]基于不同PAHs浓度对生物的影响实验,利用风险评价低值(ER-L或ISQV-L)和风险评价高值(ER-M或ISQV-H)进行生态风险评价。ER-L和ER-M代表浓度分布在第10个百分位值和第50个百分位值的生物影响范围的低值和高值;ISQV-L表示低于该值对生物无不利影响,ISQV-H表示超出此值可能对生物具有严重的影响。
悬浮颗粒物和沉积物中PAHs与基于生物影响实验的环境质量标准对比见表3。由表3可见,枯季悬浮颗粒物中AC、FL、PHE和AN质量分数均超过了ER-L值和ISQV-L值,但低于其ER-M和ISQV-H值;洪季悬浮颗粒物中FL质量分数超过其ER-L值和ISQV-L值。此外,对B[b+k]FA这种没有最低安全值的PAHs化合物来说,环境中只要存在就可能对水生生物产生不利影响。可见灌河口悬浮颗粒物中PAHs的生态风险在枯季时需引起重视。沉积物是环境中PAHs最主要的储库,当环境条件改变时又是主要的释放源,其对生物乃至人体均会造成风险。枯季沉积物中FL和PHE质量分数高于其ER-L值和ISQV-L值,其他单体PAH的质量分数均较低;洪季沉积物中只有FL的质量分数高于其ER-L值和ISQV-L值,因此需重点关注沉积物中FL和PHE对生物的影响,加强对环境及生物影响较大的单体PAHs的监测与研究。
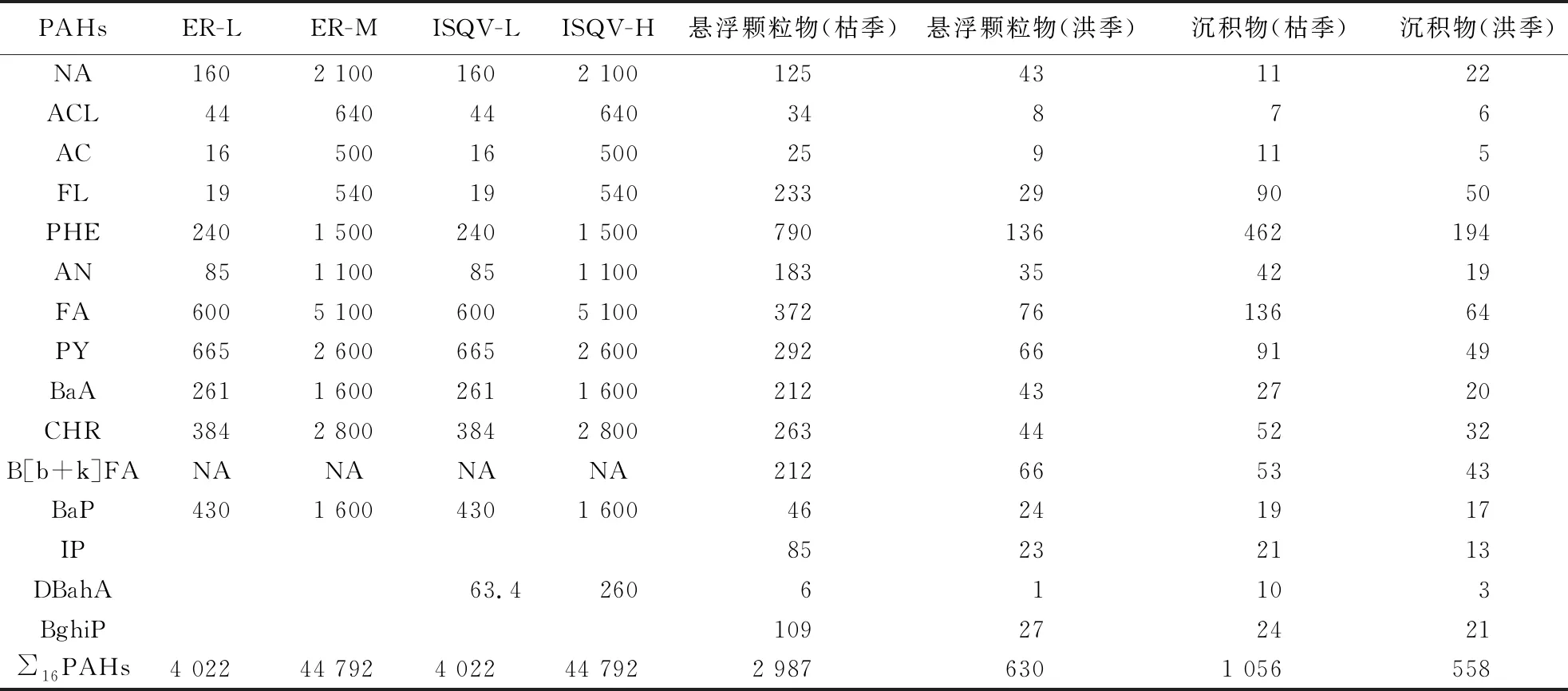
表3 悬浮颗粒物和沉积物中PAHs与基于生物影响实验的环境质量标准对比① ng/g(干重)
2.2 生物体中PAHs富集及组成特征
2.2.1 植株与沉积物中PAHs富集及组成特征
河口光滩沉积物中PAHs质量分数均值为43.5 ng/g,远低于有芦苇和互花米草覆盖的沉积物中PAHs质量分数(152.4和125.7 ng/g)。不同覆盖情况下沉积物中PAHs富集水平可能受控于沉积物中有机碳含量,而芦苇和互花米草的落叶效应使沉积物中有机碳含量高于光滩[18]。互花米草根系沉积物中PAHs质量分数均值为63.7 ng/g,芦苇根系沉积物中PAHs质量分数均值为104.96 ng/g,均低于有芦苇和互花米草覆盖的表层沉积物,说明植物根系可能从沉积物中利用一部分PAHs,此外根系附近细菌可能对沉积物中PAHs起到降解作用。芦苇和互花米草植株内PAHs质量分数(139.6和84.8 ng/g)介于表层沉积物和根系沉积物之间。3环(PHE)和4环(FA、PY和CHR)PAHs是表层沉积物和植株中PAHs的主要成分;而芦苇和互花米草中中低环数(2+3环、4环)PAHs质量分数要高于芦苇和互花米草根系沉积物中PAHs质量分数,以PHE尤为明显;根系组织可能通过蒸腾作用富集PHE和FA[2]。
植株及沉积物中PAHs组成特征见图3。
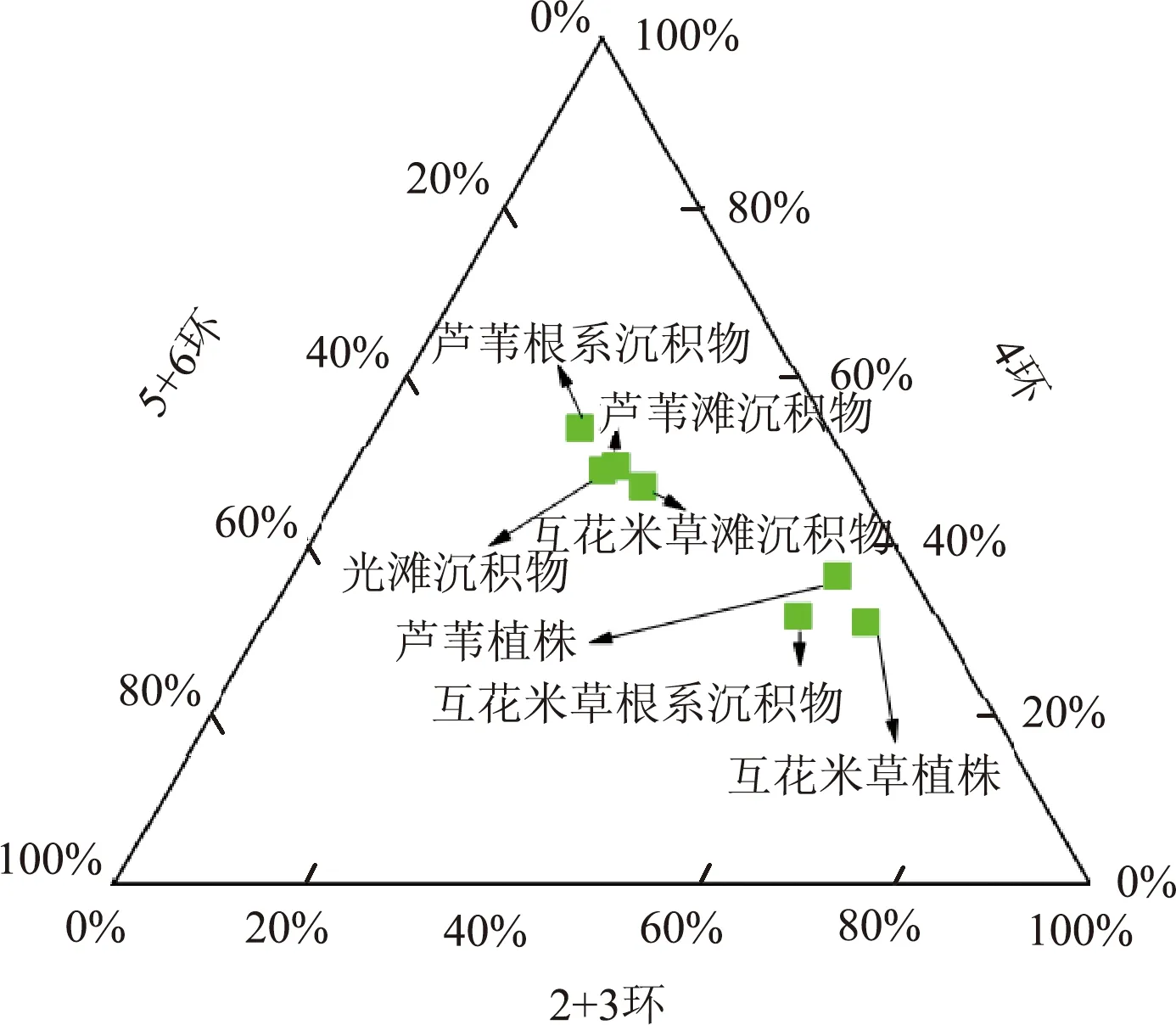
图3 植株及沉积物中PAHs组成特征
由图3可见,芦苇根系、芦苇滩、光滩和互花米草滩沉积物中PAHs组成相似;而芦苇植株、互花米草根系沉积物和互花米草植株中PAHs组成相似。具体表现为2+3环PAHs在互花米草植株(62.1%)、芦苇(56.2%)和互花米草根系沉积物(54.6%)中的占比很高,这与相应沉积物中的分布特征相反,说明芦苇和互花米草对低环数PAHs的吸附可能不是从沉积物中获取,而通过其他方式如植株叶片对大气中低环数PAHs的吸附。沉积物中的PAHs主要以4环为主,其中在芦苇根系、芦苇滩、光滩和互花米草滩沉积物的占比分别为53.9%,48.5%,48.3%和47.3%。芦苇根系和互花米草根系沉积物中PAHs的组成差异较大,可能由于二者对大气和沉积物PAHs的吸附和代谢转化存在差异[6]。
2.2.2 蟹体内PAHs富集及组成特征
河口同种蟹体内PAHs质量分数差别不大。7月雌无齿相手蟹体内PAHs质量分数(72.4 ng/g)高于雄无齿相手蟹(54.2 ng/g);7月雌毛蟹体内PAHs质量分数(58.1 ng/g)高于雄毛蟹(47.2 ng/g)。11月雌雄蟹体内PAHs质量分数远高于7月份,且呈现出雄蟹PAHs质量分数(无齿相手蟹:128.5 ng/g,毛蟹:97.0 ng/g)高于雌蟹(无齿相手蟹:65.4 ng/g,毛蟹:83.6 ng/g)。分析原因为7月为蟹的生长期,而11月为其成熟期,雄蟹成熟期体内脂含量远高于生长期,推测脂含量影响其PAHs富集[19]。
不同月份蟹体内PAHs组成特征也存在差异。雌雄蟹体内PAHs组成特征见图4。由图4可见,7月无齿相手蟹和毛蟹体内更易富集低环数的PAHs,表现出2+3环PAHs平均占比(75.3%)高于11月(67.9%);11月无齿相手蟹和毛蟹体内富集的4环PAHs平均占比(29.1%)高于7月(23.7%),而5+6环PAHs平均占比11月(3.0%)高于7月(1.0%)。研究区蟹类更易富集低环数PAHs,这可能与蟹类的饮食方式及体内PAHs的代谢过程有关,或者存在通过上覆水体直接获取溶解度较高的低环数PAHs的可能性[19]。
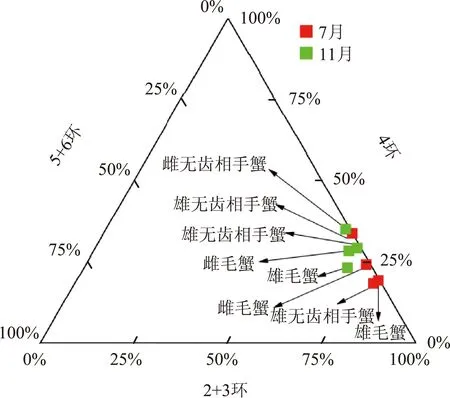
图4 雌雄蟹体内PAHs组成特征
3 结论
(1)2018年苏北灌河口水相、悬浮颗粒物和沉积物中PAHs均值为枯季(1 998 ng/L,2 987 ng/g, 1 056 ng/g)高于洪季(1 698 ng/L,630 ng/g, 558 ng/g)。水相、悬浮颗粒物和沉积物中均以2+3环PAHs为主,其次为4环PAHs,最后为5+6环PAHs。不同环数PAHs组成特征说明河口区污染物主要来源于工业区化石燃料不完全燃烧排放和港口船舶石油类泄漏。水相中BaA、CHR、B[b+k]FA质量浓度高于US EPA推荐水质量标准,而悬浮颗粒物和沉积物中FL和PHE对水生生物可能存在不利影响。
(2)芦苇和互花米草覆盖的沉积物中PAHs质量分数高于光滩,落叶效应影响下沉积物中有机碳含量可能是影响PAHs富集的主要因素;芦苇和互花米草根系附近细菌对沉积物中PAHs可能起到降解作用;芦苇根系和互花米草根系部沉积物中PAHs的组成差异较大,可能由于芦苇和互花米草对大气和沉积物PAHs的吸附和代谢转化存在差异。
(3)不同月份蟹体内PAHs质量分数差异较大,成熟期(11月)雌雄蟹体内PAHs平均质量分数远高于生长期(7月)。蟹体内更易富集低环数(2+3环)PAHs,这可能与蟹的饮食方式及其对PAHs的代谢过程有关,或者存在通过上覆水体直接获取低环数PAHs的可能。
