不同药物对高危型HPV持续感染及宫颈癌前病变合并高危型HPV感染的临床疗效对比研究
2022-08-05唐宇星张诗敏周莹莹
唐宇星,王 敏*,张诗敏,王 佩,丁 伟,曾 志,周莹莹
0 引言
子宫颈癌是一种常见的妇科恶性肿瘤,其发病率及致死率排在所有妇科恶性肿瘤的第4位[1-2]。我国每年新增宫颈癌约有14万例,其中死亡约3.7万例[3]。人乳头瘤病毒(Human papillomavirus,HPV)感染和宫颈癌、宫颈病变的发生有密切的关联。有研究表明,高危型HPV持续感染是宫颈癌发生的独立危险因素,90%以上子宫颈癌患者都存在高危型HPV感染[4]。从HPV慢性持续感染进展为子宫颈癌大约需要10~20年的时间,因此,有效控制HPV的感染尤其是高危型HPV持续感染将大大降低子宫颈癌的发生率,具有重要的临床意义。
目前,临床上用于治疗子宫颈HPV感染的药物有许多种类,但尚无针对HPV感染的专一特效药,这些药物大多数是通过增强阴道局部或全身的免疫力以期达到清除HPV的目的,疗效是否确切还有待于更多的研究来验证。
红色诺卡氏菌是具有细胞毒活性及免疫促进作用的一种微生物,红色诺卡氏菌细胞壁骨架(Nocardia rubrum cell wall cytoskeleton,Nr-CWS)是从红色诺卡氏菌中提取的一种细胞壁骨架成分,是一种非特异性免疫调节剂[5]。外用Nr-CWS对清除HPV感染及逆转子宫颈上皮内病变也具有一定疗效。保妇康栓和重组人干扰素α-2b栓是目前临床上比较常见的用于治疗高危型HPV感染的药物。研究表明,二者在清除HPV感染、逆转HPV相关子宫颈病变方面也具有一定疗效,但研究结果间存在差异,疗效有待于进一步验证。
本文旨在通过此前瞻性研究,对比不同药物对高危型HPV持续感染及子宫颈癌前病变合并高危型HPV感染的临床疗效,以期为今后的临床用药选择提供依据。
1 资料与方法
1.1 病例选择 前瞻性收集2018年9月至2020年1月,就诊于中国医科大学附属盛京医院,符合入组标准的高危型HPV持续感染及子宫颈癌前病变同时合并高危型HPV感染的患者163例。按照受试患者的意愿分配至Nr-CWS组、保妇康栓组、干扰素组和空白对照组。Nr-CWS组给予外用Nr-CWS阴道上药,保妇康栓组给予保妇康栓阴道上药,干扰素组给予重组人干扰素α-2b栓阴道上药,空白对照组不给予任何特殊处置,仅定期随访。分别于完成治疗后的1、4、8、12个月行随访检查,每次随访需进行的内容包括HPV分型检测、液基薄层细胞检查(Fluid based thin-layer cytological test,TCT)及不良反应情况,必要时行阴道镜下检查及宫颈活组织检查。所有患者在用药过程中、用药后及随访过程中未见明显不良反应发生,部分患者未定期随访,随访完整的受试者共120例,Nr-CWS组30例,保妇康栓组30例,干扰素组30例,空白对照组30例。本研究通过中国医科大学附属盛京医院伦理审批,伦理编号:2017PS015K。
1.1.1 入组标准 ①自愿参加本项研究,愿意并且保证按照方案的要求予以合作者;②年龄21~65岁,有性生活的女性,同意参加研究期间进行有效避孕,并在治疗期间禁止性生活者;③确诊为宫颈高危型HPV持续感染12个月及以上者,或低级别鳞状上皮内病变(Low-grade squamous intraepithelial lesion,LSIL)伴高危型HPV感染者,或高级别鳞状上皮内病变(High-grade squamous intraepithelial lesion,HSIL)治疗后/子宫颈癌术后3个月后伴高危型HPV感染者,经阴道镜和宫颈活检确诊为非HSIL和子宫颈癌者。
1.1.2 排除标准 ①妊娠期或哺乳期的妇女;②宫颈癌及宫颈癌术后或HSIL术后再次复发者;③严重心、肺、肝和肾脏疾病的患者;④有免疫系统疾病或恶性肿瘤的患者;⑤3个月内使用过激素、免疫抑制剂或其他作用于免疫系统的药物治疗者;⑥滴虫、霉菌、细菌性阴道病的患者;⑦ 2周内或正在接受经阴道给药治疗的患者;⑧对试验药物过敏的患者。
1.1.3 退出标准 ①试验者要求退出;②发生严重不良事件;③试验者怀孕;④有证据表明试验者疾病进展。
1.2 分组及治疗方案
1.2.1 治疗方案 Nr-CWS组:月经干净后第2~3天开始用药,每次用药2瓶,隔日阴道给药1次,连续给药10次为1个疗程。保妇康栓组:月经干净后第2~3天开始用药,每晚2粒,每个月用药16 d,使用3个月。干扰素组:月经干净后第2~3天开始用药,1次1粒,隔天1次,使用3个月。空白对照组:不给予药物,仅定期随诊复查。
1.2.2 月经期所有的用药都要停用,用药期间避免性生活和盆浴,停药后至随访结束前性生活要使用避孕套。分别于完成治疗后的1、4、8、12个月行随访检查,每次随访需进行的内容包括HPV分型检测、TCT及不良事件情况,必要时行阴道镜下检查及宫颈活组织检查。
1.2.3 检测方法 ①TCT:应用TBS分级诊断标准:未见上皮内病变或恶性细胞(Negative for intraepitheial lesion or malignancy,NILM)、无明确诊断意义的不典型鳞状细胞(Atypical squamous cell of undetermined significance,ASC-US)、不能排除高级别鳞状上皮内病变不典型鳞状细胞(Atypical squamous cells-cannot exclude HIS,ASC-H:)、LSIL、HSIL、鳞状细胞癌、非典型腺细胞(Atypical glandular cells,AGC)、原位癌(Adenocarcinoma in situ,AIS)和腺癌。②HPV分型检测:采用PCR核酸杂交法进行HPV分型检测。③阴道镜及病理组织学检查:阴道镜下观察受试者的宫颈情况。需要行阴道镜检查患者:HPV16或18阳性者;高危型HPV阳性且TCT为ASC-US者;高危型HPV阳性持续1年者;TCT为ASC-H、LSIL、HSIL、AGC或AIS者。根据阴道镜检查结果决定是否行宫颈活检,所取组织使用标准病理组织学标准处理和结果判读。
1.3 疗效判定标准
1.3.1 HPV的疗效判定 转阴:HPV转阴;显效:HPV感染的类型数目比用药前减少;无效:HPV感染的类型无变化。总有效=转阴+显效。
1.3.2 TCT的疗效判定 有效:异常TCT的级别较用药前降低或转为正常;无效:异常TCT的结果无变化或较用药前级别升高或正常TCT变为异常。
1.3.3 阴道镜疗效判定 根据2019年ASCCP阴道镜诊断标准可诊断为:正常或良性病变;LSIL;HSIL;癌。病变程度逐级递增。根据阴道镜检查结果,必要时行宫颈活检。逆转:病理结果较用药前级别降低或转为正常;进展:病理结果较用药前级别升高;无进展:病理结果较用药前无变化。
1.3.4 宫颈组织病理结果疗效判定 病理结果可分为:慢性宫颈炎;LSIL;HSIL;癌。病变程度逐级递增。逆转:病理结果较用药前级别降低或转为正常;进展:病理结果较用药前级别升高;无进展:病理结果较用药前无变化。
1.4 统计学分析 使用SPSS 21.0统计学软件进行统计学分析,计量资料分析使用单因素方差分析,计数资料分析使用卡方检验或者Fisher确切概率法(频数<5),等级资料分析使用非参数检验(Kruskal-Wallis H检验),P<0.05为差异有统计学意义。
2 结果
2.1 各组患者临床资料比较 各组间平均年龄及平均高危型HPV初始感染个数差异均无统计学意义(P>0.05),见表1。四组病例各组间初始感染类别情况(见表2)及用药前TCT结果比较(见表3)差异均无统计学意义(P>0.05)。四组资料具有可比性。

表2 四组患者初始感染类别情况
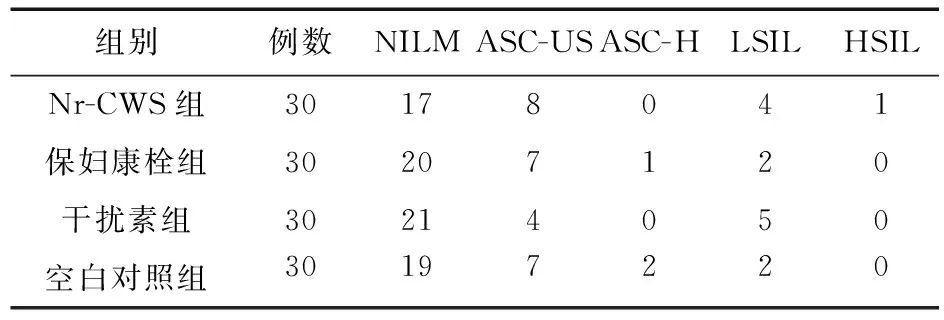
表3 四组患者用药前TCT结果比较
2.2 疗效比较
2.2.1 HPV转归情况比较 ①停药后1个月的HPV转归情况比较。停药后1个月,Nr-CWS组的转阴率及总有效率均高于保妇康栓组及空白对照组,差异有统计学意义(P<0.05)。Nr-CWS组转阴率高于干扰素组,差异有统计学差异(P<0.05),但总有效率差异无统计学意义(P>0.05)。除Nr-CWS组外的其余3组的转阴率及总有效率分别相比,差异无统计学意义(P>0.05),见表4。
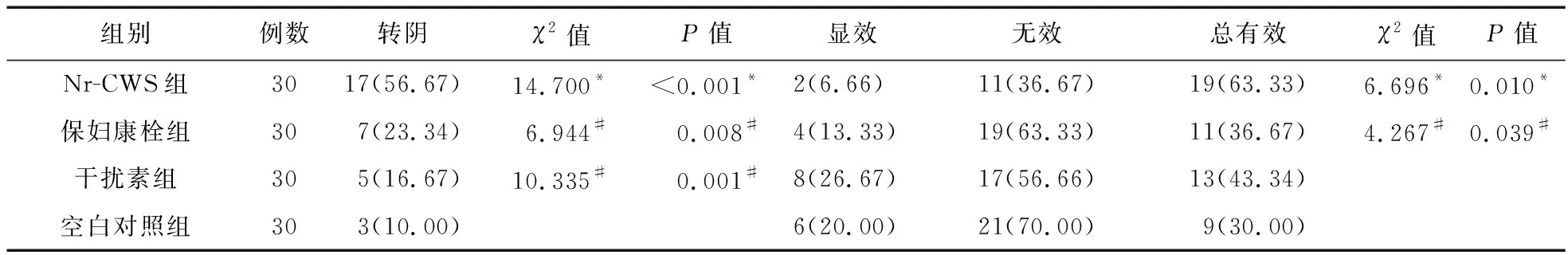
表4 四组患者停药1个月后HPV转归情况比较[例(%)]
②停药后4个月的HPV转归情况比较。停药后4个月,Nr-CWS组的转阴率高于其余3组,除保妇康栓组外,差异有统计学意义(P<0.05)。Nr-CWS组的总有效率高于保妇康栓组、干扰素组及空白对照组,但仅与空白对照组相比,差异有统计学意义(P<0.05)。除Nr-CWS组外,其余3组患者的转阴率及总有效率分别相比,差异无统计学意义(P>0.05),见表5。
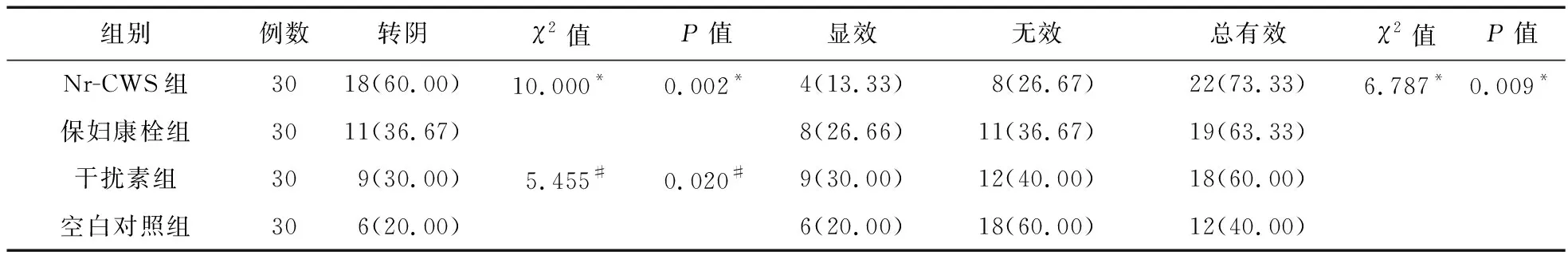
表5 四组患者停药4个月后HPV转归情况比较[例(%)]
③停药后8个月的HPV转归情况比较。停药后8个月,Nr-CWS组的转阴率及总有效率略高于保妇康栓组及干扰素组,但差异无统计学意义(P>0.05)。Nr-CWS组的转阴率及总有效率高于空白对照组,差异有统计学意义(P<0.05)。保妇康栓组和干扰素组的总有效率均高于空白对照组,差异均有统计学意义(P<0.05),见表6。
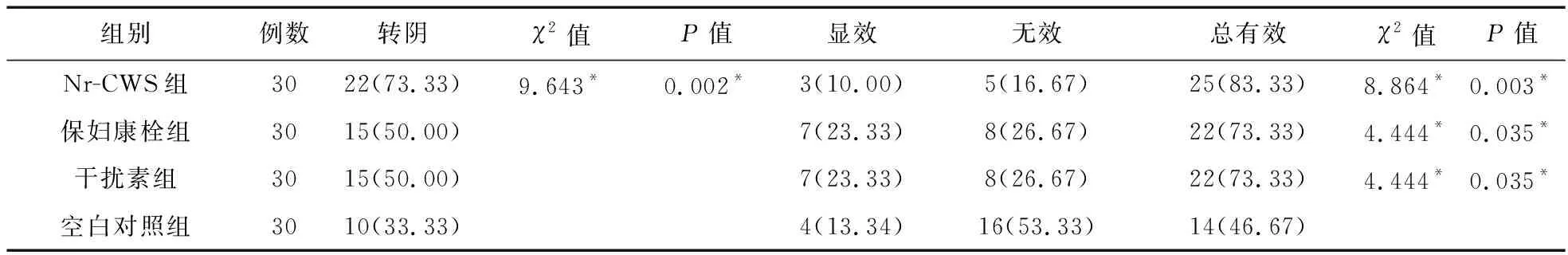
表6 四组患者停药8个月后HPV转归情况比较[例(%)]
④停药后12个月的HPV转归情况比较。停药后12个月,各组间转阴率及总有效率比较,结果与停药后8个月的随访结果一致,见表7。
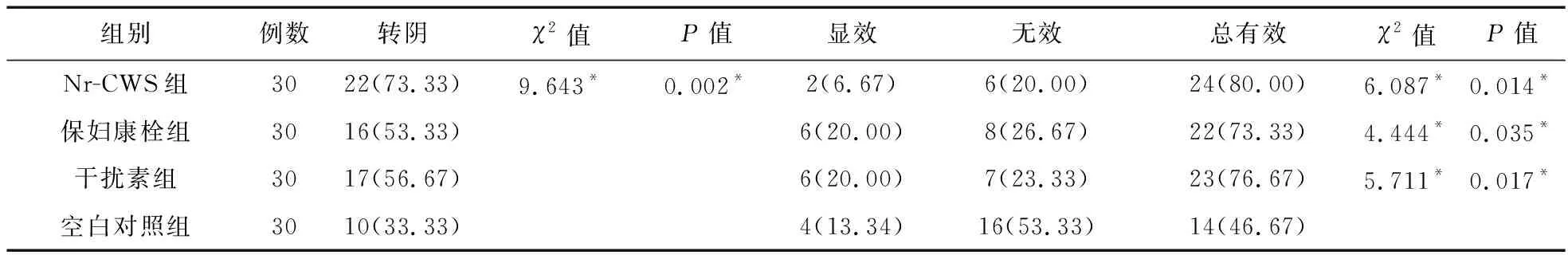
表7 四组患者停药12个月后HPV转归情况比较[例(%)]
2.2.2 TCT转归情况比较 停药后的1、4、8、12个月,分别行TCT检测,Nr-CWS组TCT转归情况的有效率略高于其他3组,但差异均无统计学意义(P>0.05),见表8~表11。
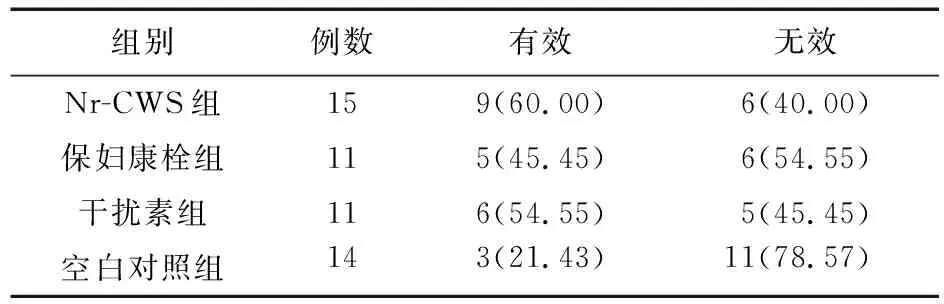
表8 四组患者停药1个月后TCT转归情况比较[例(%)]
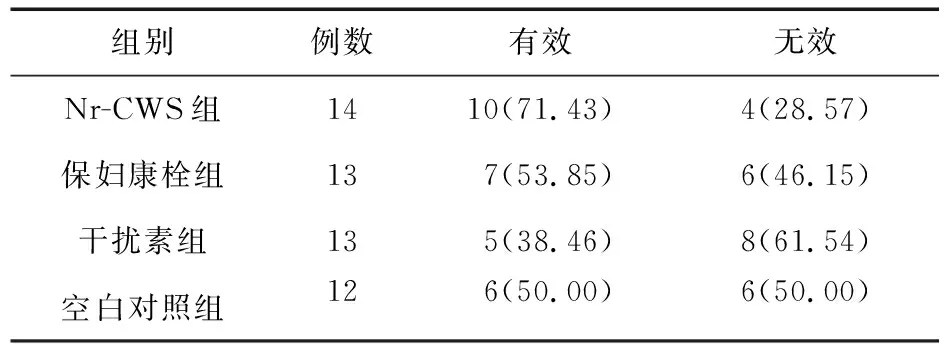
表9 四组患者停药4个月后TCT转归情况比较[例(%)]
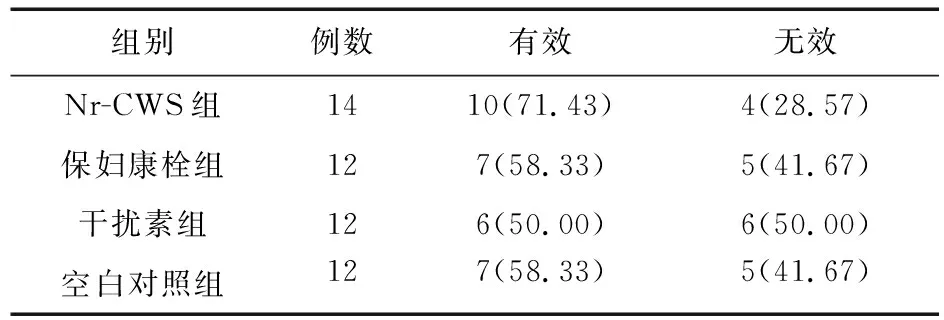
表10 四组患者停药8个月后TCT转归情况比较[例(%)]
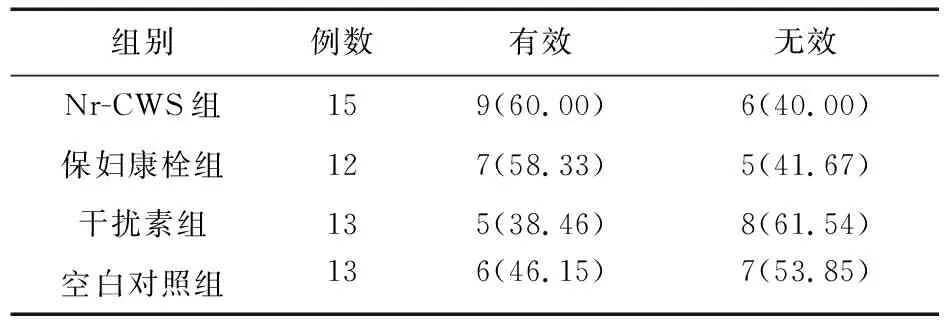
表11 四组患者停药12个月后TCT转归情况比较[例(%)]
2.2.3 阴道镜转归情况比较 共有79例于用药后行阴道镜检查。组间比较差异均无统计学意义(P>0.05)。见表12。
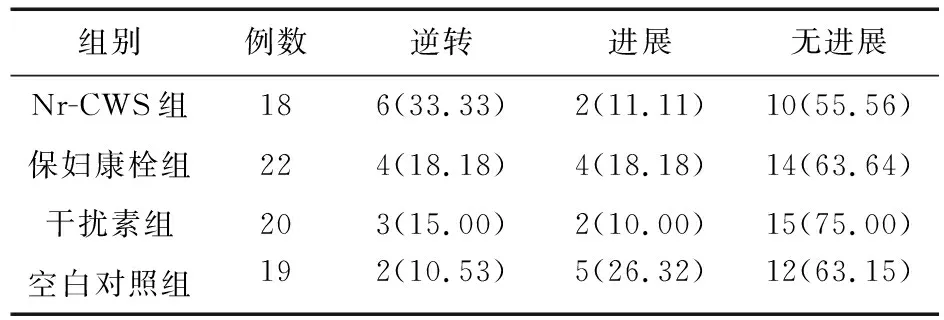
表12 四组患者用药后阴道镜转归情况比较[例(%)]
2.2.4 病理转归情况比较 高危型HPV感染合并LSIL并且用药后行病理组织学检查共29例。Nr-CWS组的逆转率为60.00%,空白对照组的逆转率为20.00%,其余两组的逆转率均为42.86%。组间比较差异均无统计学意义(P>0.05),见表13。
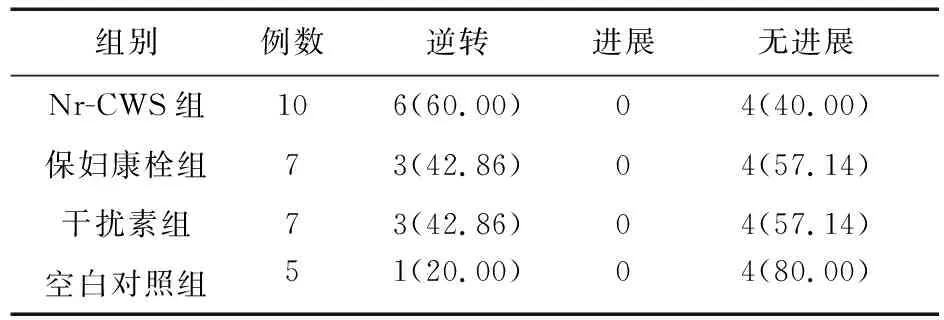
表13 四组中高危型HPV感染合并LSIL患者用药后LSIL转归情况比较[例(%)]
2.2.5 不良反应发生情况 药物治疗过程中,部分患者出现了轻度的不良反应,组间差异均无统计学意义(P>0.05),见表14。
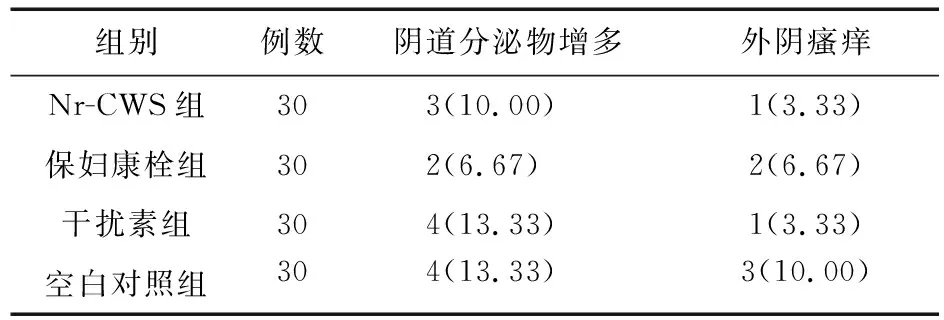
表14 四组患者用药后不良反应比较
3 讨论
HPV是一种微小无包膜的环状双链 DNA病毒[6],目前分离出将近200种HPV亚型,其中有约40种HPV亚型在女性的生殖道中发现[7]。根据病毒致病力不同,可将HPV分为低危型及高危型,高危型HPV持续感染是导致子宫颈上皮内病变及子宫颈癌的主要原因[8-9],其中16、18型与子宫颈癌的发生密切相关[10]。HPV持续感染过程中,病毒DNA可以整合到人类宿主细胞基因组中,可引起 E6和E7基因的过度表达,从而抑制 P53、pRb等基因活性[11],使细胞分化异常,进而抑制细胞凋亡。两者相互协同,促使细胞发生恶性转化[12]。毛炎红等[13]发现,HPV16的 E6和hTERT蛋白高度表达可能促进子宫颈病变的发生。因此,高危HPV与人类宿主细胞基因组的整合是一个关键点。整合前处于病毒感染阶段,整合后开始子宫颈病变。因此,在整合前尽早清除高危HPV持续感染是预防子宫颈癌的关键。
目前,临床上尚无针对HPV感染的专一特效药物,抗HPV感染的药物治疗仍处于研发探索阶段。常见的主要有免疫增强剂(如干扰素)、抗代谢药物(如5-氟尿嘧啶)、乳酸杆菌制剂以及中药(如保妇康栓)等。目前临床上最常用的药物是保妇康栓和重组人干扰素α-2b栓。保妇康栓是一种中药栓剂,主要由莪术油和冰片组成,具有一定的抗HPV病毒感染的效果,对高危型HPV感染者的转阴率为30%~90%[14],各研究结果间存在一定的差异。有研究发现,保妇康栓可能通过抑制HPV16中E6、E7的基因表达来达到抑制肿瘤的作用[15]。本研究中,保妇康栓治疗HPV感染的总有效率为73.33%,高于空白对照组。干扰素是一种具有免疫调节作用的蛋白质,能诱导靶细胞产生抗病毒蛋白来达到抑制病毒的作用[16]。有研究表明,干扰素不仅能清除HPV感染,在逆转HPV相关子宫颈病变方面也有显著疗效[17]。重组人干扰素α-2b是临床中比较常用的干扰素类型,其可参与调节机体的免疫机制,通过诱导一系列因素干扰病毒复制而达到抗病毒效果[18]。本研究中,重组人干扰素α-2b栓治疗HPV感染的总有效率为73.33%,高于空白对照组。保妇康栓组和重组人干扰素α-2b栓治疗HPV感染的转阴率及总有效率相近,两组的总有效率均高于空白对照组。两者都可以作为治疗HPV感染的一种选择。
Nr-CWS是一种新型的非特异性的免疫调节剂。Tao等[19]发现,Nr-CWS可能通过增加CD8+T细胞应答而具有免疫增强治疗作用。Meng等[20]也证实了Nr-CWS可以显著促进CIK、DC和NK细胞的生长,特别是由于其通过诱导凋亡而具有强大的抗肿瘤活性。Nr-CWS能提高子宫颈局部的免疫功能,促进细胞因子的大量分泌,进而诱导细胞凋亡,促进子宫颈组织的修复,从而达到清除子宫颈HPV感染及逆转子宫颈病变的作用。目前临床上对外用Nr-CWS的研究并不多,大多数是基于小样本量的研究。潘梅钦等[21]研究发现,外用Nr-CWS治疗后,HPV的转阴率可以达到66.6%,可以有效清除子宫颈HPV感染。李欢梓等[22]研究发现,外用Nr-CWS治疗后,HPV的转阴率为65.7%,对宫颈HPV亚临床感染有一定的清除作用。本研究显示,外用Nr-CWS治疗后,HPV的转阴率为73.3%,总有效率为83.3%。本研究与其他研究的结果不完全一致,可能因为本项研究为前瞻性研究,入组的病例有限,且随访周期长,失访率高。本研究还发现,外用Nr-CWS治疗HPV感染的转阴率和总有效率略高于保妇康栓及重组人干扰素α-2b栓,但差异无统计学意义,而与空白对照组相比差异有统计学意义,表明外用Nr-CWS也可能成为一种治疗HPV感染更好的选择。
本研究中,部分患者LSIL同时合并高危型HPV感染,且4组LSIL的逆转率比较差异无统计学意义,但Nr-CWS组LSIL逆转率高于其他3组。因样本量过少,尚不能得出准确的结论,需要进一步扩大样本量来加以验证。本研究的120例受试者中,共12例HSIL治疗后合并高危型HPV感染,1例子宫颈癌术后合并高危型HPV感染,治疗后,Nr-CW组的转阴率高于其他3组,但因样本量过少,并未行统计学分析。此研究结果可能会为预防术后潜在的HPV残留感染提供一种新的选择。
Nr-CWS临床使用的时间比较短,其疗效需进一步扩大样本量来加以验证。目前已经开展全国多中心临床试验,我院为参与单位,以期通过大样本数据观察Nr-CWS的临床疗效。保妇康栓和重组人干扰素α-2b栓虽为临床常用药,尚缺乏确切的证据证明二者的疗效。本研究通过分析比较3种药物及空白对照组对HPV感染的疗效,以期为高危型HPV持续感染的药物治疗选择提供参考依据。
