铁碳复合材料催化电Fenton处理抗生素废水的效果和机理研究*
2022-08-03李方舟陈梓慧夏建新陈慧英
徐 进,李方舟,陈梓慧,海 浩,夏建新,陈慧英,姚 硕,邢 璇
(1. 中央民族大学 生命与环境科学学院,北京 100081; 2. 中国节能环保集团有限公司,北京 100035)
0 引 言
抗生素类药物因被广泛应用于医疗、畜牧业和水产养殖业,并通过人类和兽类的排泄物,污水处理厂[1-3]和医院以及畜牧养殖场[4-5]的废水等途径进入到环境,污染地表水和饮用水,诱导环境中耐药性致病菌的出现,进而严重危害人类身体健康[6]。电化学氧化技术因操作简单,工艺条件温和,无二次污染,反应活性高,逐渐成为抗生素废水处理中可行性最高的技术。在电化学技术中, BDD(boron-doped diamond,BDD)电极因具有电化学窗口宽、背景电流低、抗腐蚀性强、化学性能稳定等诸多优点在电化学氧化系统中得到广泛应用[7]。在以BDD为阳极,碳毡(carbon felt,CF)为阴极的电化学氧化系统中,BDD阳极产生·OH,进攻阳极附近的有机物来降解水中有机污染物。CF阴极可在原位生成H2O2,在 Fe2+存在的条件下,H2O2被催化分解产生大量·OH,形成 Fenton 反应,进一步强化系统去污能力。但是,传统的均相催化反应中存在Fe2+与H2O2总量不匹配的问题。反应初期Fe2+被大量集中加入,而H2O2则随着反应时间逐渐生成,过量Fe2+的会消耗·OH,降低系统的反应效率,同时也不利于后续催化反应的进行[8]。如何确保系统中 Fe2+和 H2O2生成量相匹配,使是电化学耦合氧化系统效能提升有待解决的问题。本研究采用浸泡烧结法,将Fe2+负载在多孔活性炭表面,制备能够缓释Fe2+的铁碳复合材料,使反应过程中Fe2+逐渐释放,拟解决Fe2+量和H2O2生成量不匹配的问题,并对反应的作用机理进行分析。
1 实 验
1.1 试剂与仪器
磺胺二甲基嘧啶(sulfamethazine,SMT,纯度>99%)购自北京索莱宝科技有限公司;无水硫酸钠(分析纯)购自天津福晨化学试剂厂;硫酸亚铁,醋酸钠,盐酸羟胺,活性炭和1-10一水菲啰啉均为分析纯,购自国药集团化学试剂有限公司。
BDD电极购自德国CONDIAS GmbH公司;碳毡电极购自天津碳素厂;直流稳压稳流电源(DH1765-1)购自北京大华无线电仪器厂;管式炉(GSL-1100X)购自合肥科晶材料科技有限公司;X射线衍射仪(XD-DI)产自日本岛津公司;扫描电子显微镜(sigma300)产自德国卡尔蔡司公司;高效液相色谱(LC-20A)产自日本岛津公司,色谱柱为安捷伦SB-C18(4.6 mm×250 mm×5 μm)型;紫外可见分光光度计(V-750)产自日本JASCO公司。
1.2 铁碳复合材料的制备
在三颈烧瓶中将2 g活性炭浸泡至200 mL浓度为0.025 mol/L的FeSO4溶液中2 h,溶液中持续通氮气以隔绝氧气。所得材料用蒸馏水洗涤3次,乙醇洗涤两次,放入真空干燥箱,在60 ℃下干燥4 h。干燥后将材料取出,置于管式炉中200 ℃通氮气加热2 h得到Fe@C复合材料。
1.3 材料表征
使用扫描电子显微镜(scanning electron microscopy,SEM,sigma300,德国卡尔蔡司公司)观察材料的表面形态。使用X射线衍射分析仪(X-ray diffraction,XRD,XD-DI,日本岛津公司)分析材料晶体结构,测试条件:管电压为36 kV,管电流为30 mA,扫描速度为4°/min,2θ= 20°~80°。
1.4 电化学氧化实验
电化学氧化实验阳极BDD电极,阴极为CF电极,两电极板平行放置,间距约1 cm,电极板面积均为1.25 cm2。电解液为30 mg/L的SMT添加0.1 mil/L的Na2SO4作为支持电解质,电解液体积为400 mL,外加电流60 mA,温度为(23±1)℃,电解时间6 h,pH值为3,用H2SO4和NaOH调节溶液pH,Fe@C复合材料投加量为0~0.2 g。电催化氧化实验过程中通过磁力搅拌使溶液充分混合均匀,转速为15 r/s。
1.5 溶液中铁离子浓度测定
本研究采用邻菲啰啉分光光度法对电催化氧化过程中溶液中不同价态的铁离子浓度进行测定。
1.6 污染物降解中间产物测定
采用高效液相色谱串联四级杆飞行时间质谱技术(HPLC-Q-TOF-MS/MS)对降解过程中产生的中间产物进行定性分析。色谱柱为美国Waters Symmetry-18C液相色谱柱(4.6 mm×150 mm×3.5 μm),质谱仪为德国Bruker MicrOTOF-QII型。流动相采用溶剂A(0.1%甲酸和99.9%去离子水)和溶剂B(甲醇)组成,流速为0.5 mL/L。以溶剂B浓度表示的梯度为:0~15 min,20%;15~23 min,线性增加到90%;23~24 min,保持在90%;24~30 min,线性下降到20%。采用电喷雾电离源(electrospray ionization,ESI)在正模式下进行质谱分析。质谱参数如下:范围50~1 000 m/z;离子喷雾电压为3 500 V;雾化气为0.08 MPa;干燥气温为180 ℃;干气体流速为8.0 L/min;碰撞能量为150 Vpp。使用Bruker Compass Data Analysis 4.1软件进行统计数据处理。
1.7 量子化学计算
利用Gaussian 09软件和密度泛函理论(density functional theory,DFT)在B3LYP/6-31+g(d,p)水平下优化SMT的几何结构,并计算SMT分子中各原子的福井函数与电子云密度,结合两个值的大小判断SMT分子中的反应活性位点。
2 结果与讨论
2.1 材料性能表征
Fe@C复合材料的XRD谱图如图1所示。图中37.7°,43.9°,49.7°处出现了FeSO4的特征峰,说明FeSO4成功负载到了活性炭上。同时,出现了两处Fe2(SO4)3·9H2O的峰,这可能是材料在制备和保存过程中被氧化的结果。
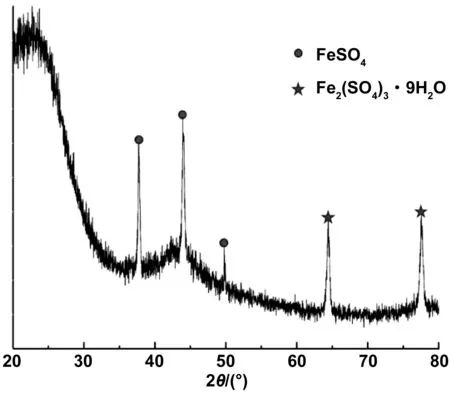
图1 Fe@C复合材料的XRD谱图Fig 1 XRD image of Fe@C composite material
Fe@C复合材料的表面形貌结构是影响其催化效率的重要因素,实验所用Fe@C复合材料的SEM图如图2所示。从图中可以看出,Fe@C复合材料表面出现了纳米颗粒,颗粒分布均匀无团簇,增加了与污染物的接触面积,大大提高了反应速率。此外,活性炭中丰富的多孔结构有利于纳米颗粒生长,在碳基体的保护下,纳米颗粒的氧化速率受到抑制。且制备的Fe@C复合材料具有良好的吸附能力,能将溶液中的污染物主动吸引到其表面,而不是被动地等待与污染物接触,提高了原位还原[9]的效率。

图2 Fe@C复合材料的SEM谱图Fig 2 SEM images of Fe@C composite material
2.2 SMT降解效果分析
在电催化氧化降解SMT的实验中,向BDD-CF系统中分别添加0.02,0.1和0.2 g的Fe@C材料,其余实验条件保持一致,对不同电解条件下SMT的降解效果进行探究。结果如图3(a)所示。当溶液中投加不同量的Fe@C材料时,电解6 h后,投加量为0.1和0.2 g Fe@C材料的系统能够完全去除SMT,而投加0.02 g Fe@C复合材料的条件下,SMT在溶液中仍有10%的剩余,降解效率随投加量的增大而提高,表明Fe@C复合材料在溶液中起到了催化有机污染物降解的作用。同时,加入0.2 g制备好的Fe@C材料进行单纯吸附实验,可以发现单独吸附有一定的效果,但通电条件下,电Fenton氧化作用是污染物去除的主要机制。
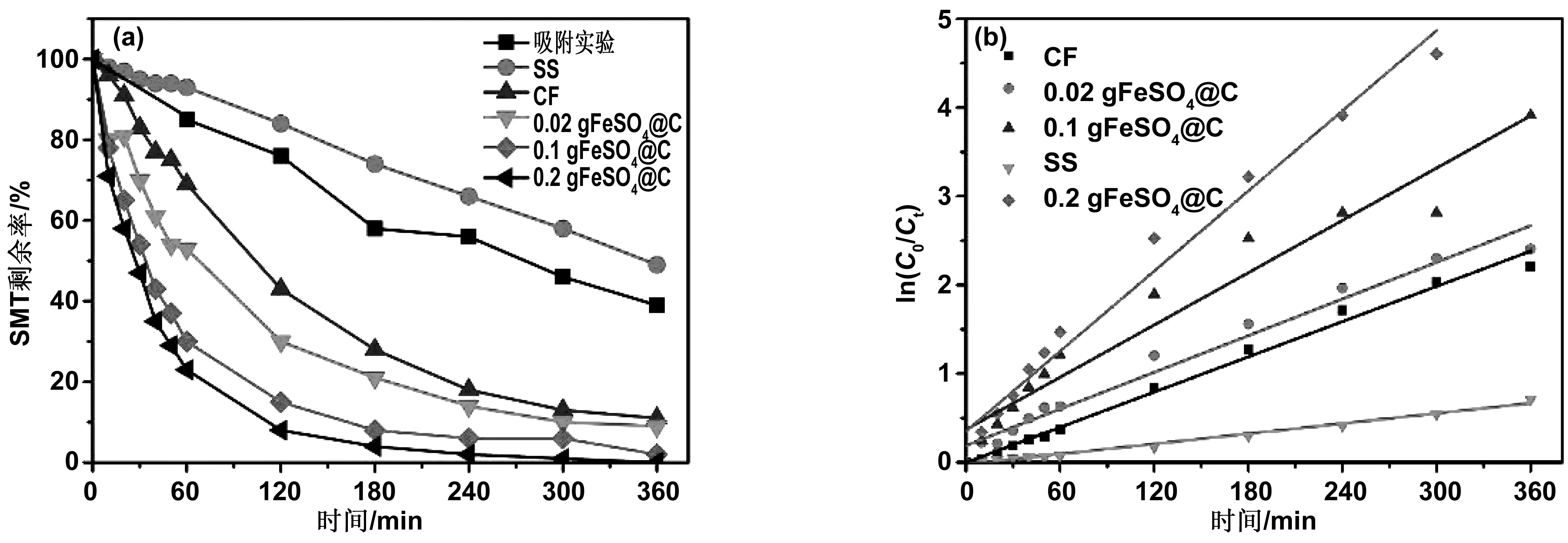
图3 Fe@C投加量对SMT降解效率的影响(a)及拟一级动力学拟合模型(b)Fig 3 The effect of Fe@C dosage on SMT degradation(a) and pseudo-first-order kinetic model (b)
对SMT的降解过程进行动力学拟合,如式(1)和图3(b)所示:
(1)
动力学拟合结果表明,SMT的降解遵循拟一级动力学方程,表明BDD-CF体系中SMT的氧化降解也处于传质扩散控制之下。随着反应时间的进行,SMT去除效率变缓,主要是由于快速反应使得材料发生了钝化[10],当溶液中Fe@C复合材料投加量分别为0.02,0.1和0.2 g时,kSMT值分别为0.007,0.010和0.015 min-1,降解速率逐渐增大,均高于未投加材料的系统。
2.3 溶液中铁离子浓度变化探究
在BDD-CF降解SMT的系统中,为了探究铁离子在反应过程中起到的重要作用,通过紫外分光光度法对投加了Fe@C材料的溶液电解过程中Fe2+和总铁的含量进行了测定,结果如图4所示。结果表明,Fe2+和总铁的含量在电催化氧化过程中表现出上升的趋势,并随电催化时间的增加而逐渐趋于平缓,溶液中的总铁主要是以Fe2+的形式存在,且投加量越多溶液中铁离子浓度越大,这主要是因为Fe@C复合材料在电催化过程中向溶液中缓释铁离子,并参与反应。结合图1可以看出,当Fe@C复合材料投加量为0.02 g时,催化位点不足限制了Fe2+和电子的产生,从而使其催化降解效率明显低于投加量为0.1和0.2 g时的催化降解效率[9]。虽然较高的投加量会提供更多的接触面积和催化位点,但过高的投加量并不会使SMT降解效率一直提升,由于Fe@C复合材料利用不足,过量的投加量也导致单位去除能力的持续下降。
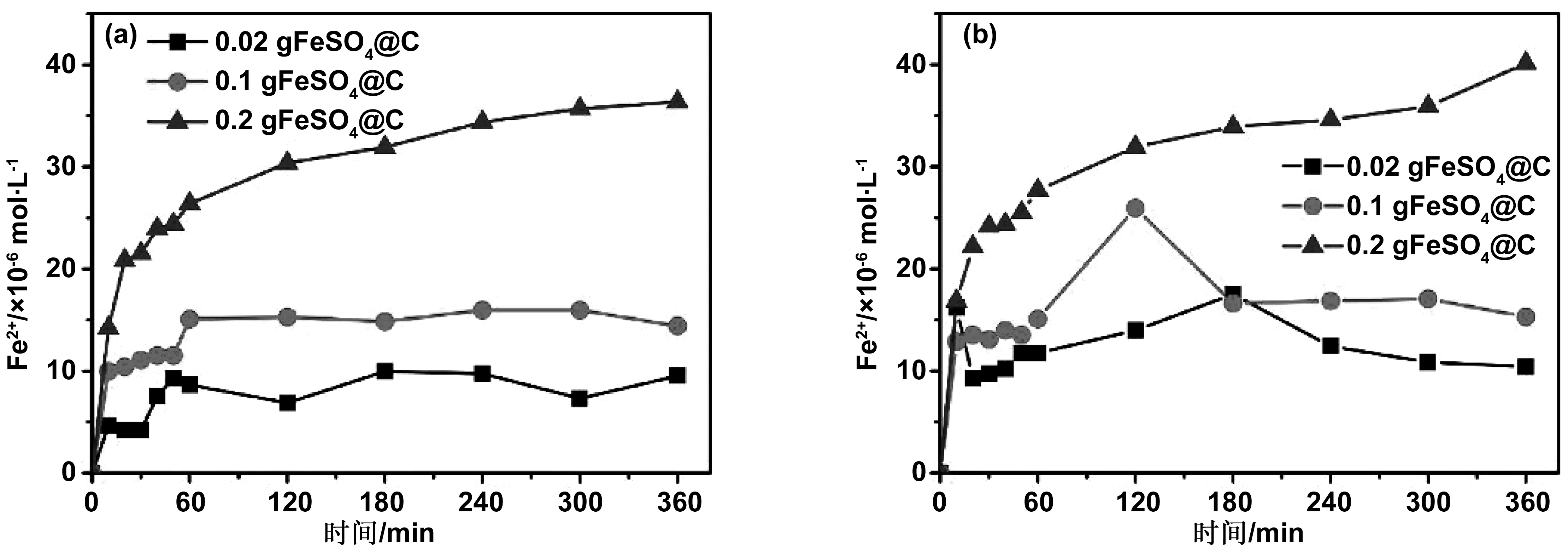
图4 溶液中总铁(a)与Fe2+(b)的浓度随电解时间的变化趋势Fig 4 The trend of total iron(a) and Fe2+ (b) concentration with electrolysis time in solution
溶液中铁离子浓度含量测定结果表明,制备的Fe@C复合材料能够在溶液中缓释Fe2+,使体系中的Fe2+始终维持在一定浓度,从而与H2O2的生成形成较好的匹配关系,可以持续高效催化阴极的电芬顿反应来产生·OH降解磺胺二甲基嘧啶,解决了传统电芬顿系统中存在的Fe2+与H2O2总量不匹配的问题。
2.4 量子化学计算
使用Gaussian 09软件在B3LYP/6-31+g(d,p)水平下优化SMT的几何结构,如图5所示。
福井函数的左导数、右导数和左右导数的平均值分别对应亲电、亲核和自由基反应[11],即:
(2)
(3)
(4)
式中:qk(N)、qk(N+1)、qk(N-1)分别代表体系在原始状态(N电子)、结合一个电子状态(N+1电子)和电离掉一个电子状态(N-1电子)下的电子云密度。计算qk(N)、qk(N+1)、qk(N-1)时,体系的几何结构保持不变。计算结果如表1所示。
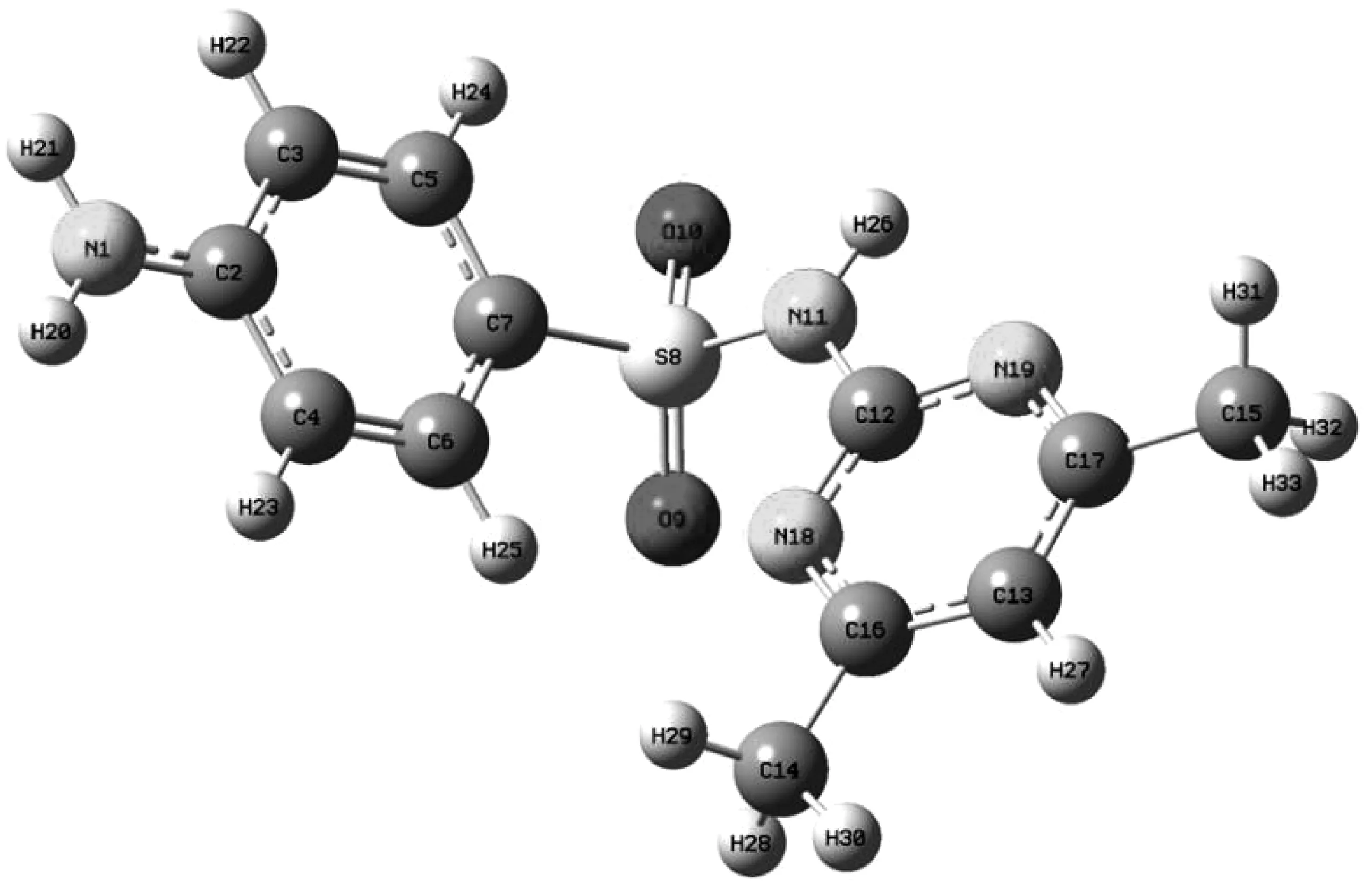
图5 采用Gaussian在B3LYP/6-31+G(d,p)水平优化后的SMT构象Fig 5 SMX conformation optimized by Gaussian at the B3LYP/6-31+ G (d, p)
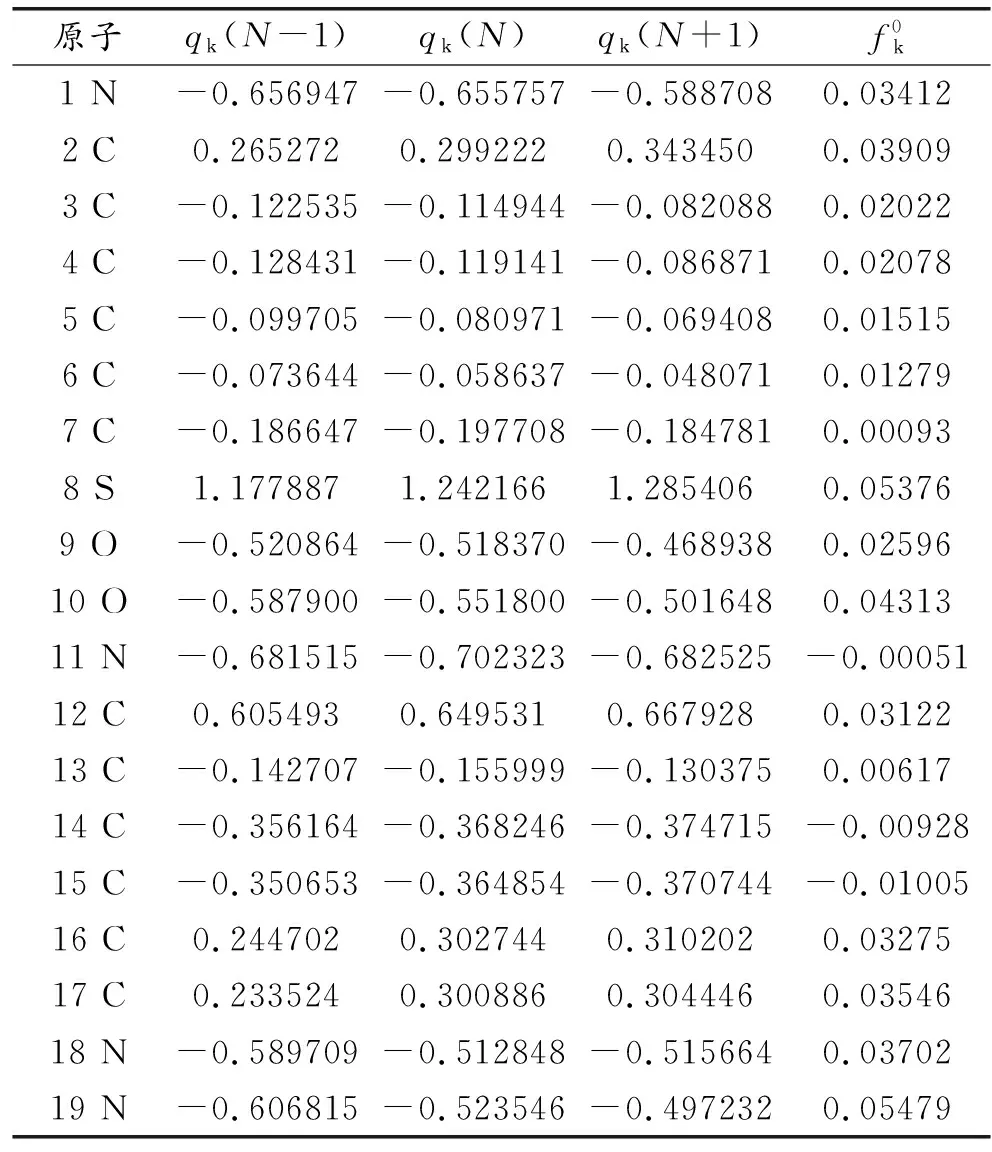
表1 SMT分子各原子电荷分布及福井函数
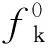
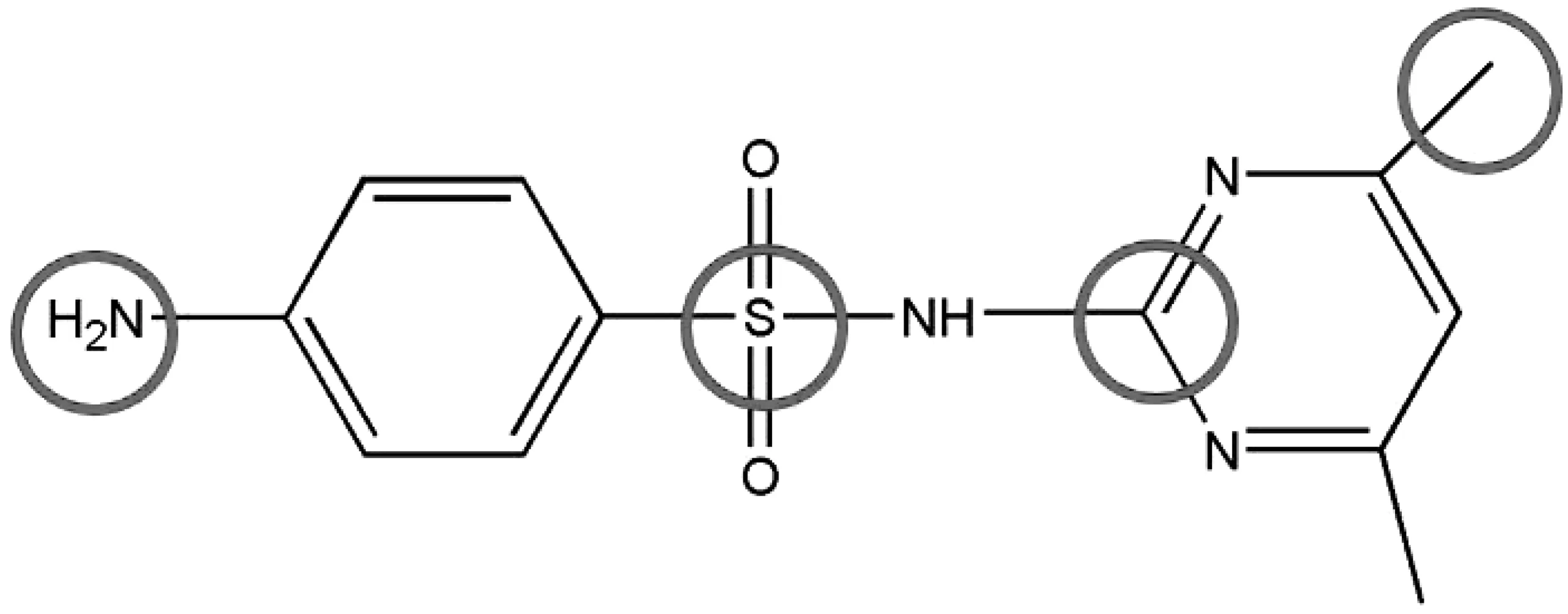
图6 SMT分子中可能的反应活性位点Fig 6 Possible active sites identified by Fukui index and cloud density
2.5 LC-MS测定结果
通过超高效液相色谱串联高分辨质谱仪对SMT降解过程中中间产物进行测定,测定结果如表2所示。
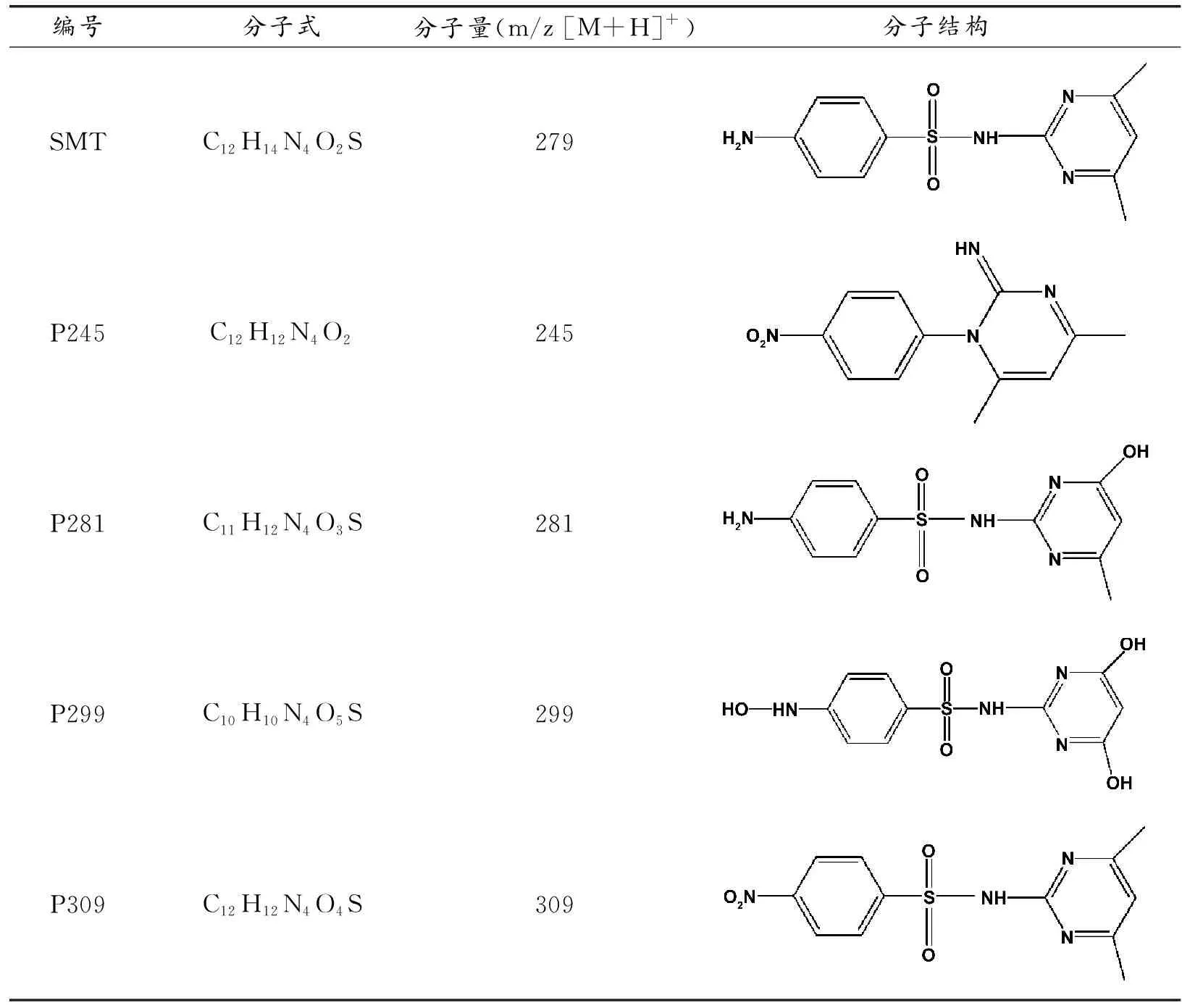
表2 通过LC-MS分析得到的中间产物Table 2 The intermediate product obtained by LC-MS analysis
2.6 降解路径探究
通过量子化学计算结果和液质联用结果相结合,推出SMT可能的降解路径,其中检测出的物质用P表示,实验中未检出而是通过以往研究得来的物质用S表示并加以虚线,结果如图7所示。共推测出两种氧化途径的降解机制:(Ⅰ)苯胺部分的逐步氧化和磺胺键(S-N)的裂解及(Ⅱ)嘧啶环中的N-C键受到·OH的攻击发生氧化反应以及磺胺键(S-N)的裂解。
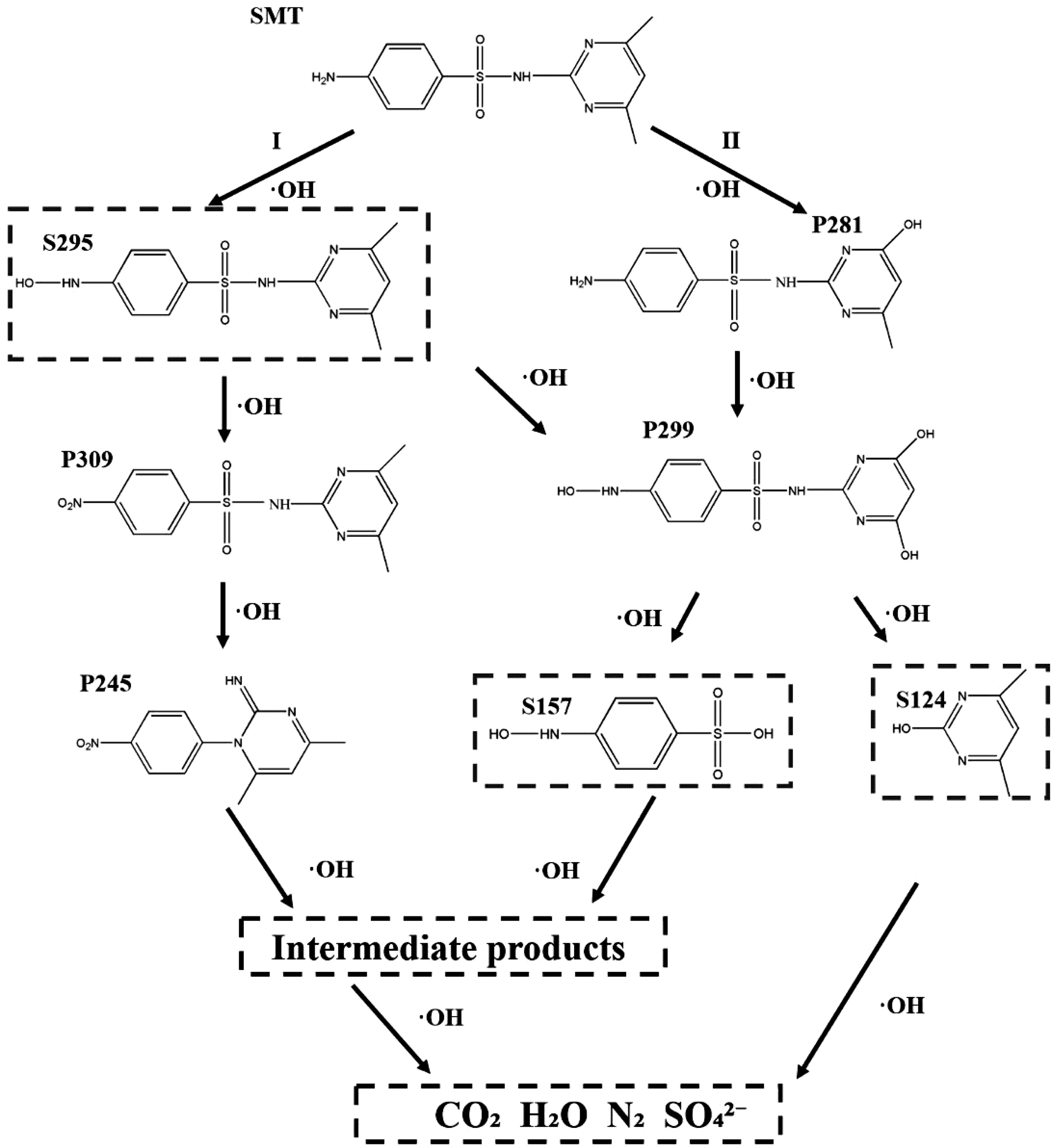
图7 SMT降解路径机理图Fig 7 Mechanism of SMT degradation pathway
结果表明,本研究中检测到的大部分有机化合物是由·OH攻击SMT形成的。降解路径主要有两条,路径一主要是由于苯胺部分的逐步氧化和磺胺键(S-N)的裂解。首先,SMT的苯胺部分在·OH的攻击下逐步形成SMT-硝基衍生物S295和P309[12-14],这与DFT计算结果相一致,即具有较高函数值和较高电子云密度的N1原子具有较高反应活性。之后,具有较高f0(0.05376)的S8在·OH的作用下发生S-N的断裂以及分子结构的重排,生成产物P245[15]。路径二主要是由于嘧啶环中的N-C键受到·OH的攻击发生氧化反应以及磺胺键(S-N)的裂解。首先,嘧啶环上发生氧化反应导致甲基羟基化从而生成产物P281和P299,P299也可经过第一步中产生的S295通过甲基羟基化而产生,之后发生S-N的断裂产生S157和S124。此外,在一些研究中,这些中间产物在氧化作用下还会生成一些短链脂肪族羧酸等小分子物质[16],最终在·OH的持续氧化作用下矿化为CO2和H2O。
3 结 论
(1)采用浸泡烧结法制备出铁碳复合材料,XRD和SEM谱图显示FeSO4颗粒成功负载至活性炭表面,且在活性炭表面分布均匀无团簇,增大了反应的接触面积,促进了反应的进行。
(2)在BDD-CF电化学氧化系统中,投加铁碳复合材料的系统与未投加的系统相比,SMT去除效率明显提高,且当投加量为0.2 g Fe@C时SMT在6 h内达到完全去除,经过拟合后,系统中SMT的降解遵循拟一级动力学方程。
(3)Fe@C复合材料能够在溶液中缓释Fe2+,使溶液中Fe2+始终维持在一定浓度,与H2O2的生成形成较好的匹配关系,解决了传统电芬顿系统中存在的Fe2+与H2O2总量不匹配的问题。
(4)基于量子化学计算和HPLC-Q-TOF-MS/MS中间产物分析确定了SMT分子中活性位点,推测出两种氧化途径的降解机制:(Ⅰ)苯胺部分逐步氧化和磺胺键(S-N)的裂解及(Ⅱ)嘧啶环中的N-C键受到·OH的攻击发生氧化反应以及磺胺键(S-N)的裂解。
