FOLFOX4化疗方案联合康艾注射液对原发性肝癌患者血清AFP、CEA和CA19-9水平及免疫功能的影响
2022-07-12付先锋晏燕郭红飞
付先锋 晏燕 郭红飞

【摘要】 目的:探討FOLFOX4化疗方案联合康艾注射液对原发性肝癌(PHC)患者血清甲胎蛋白(AFP)、癌胚抗原(CEA)和糖类抗原19-9(CA19-9)水平及免疫功能的影响。方法:选择2019年
6月-2021年5月于江西中医药大学附属医院治疗的86例PHC患者,按随机数字表法将其分为两组,各43例。对照组采用FOLFOX4化疗方案治疗,观察组采用FOLFOX4化疗方案、康艾注射液治疗,两组均治疗3个疗程。比较两组肿瘤标志物、免疫功能及不良反应。结果:治疗3个疗程后,两组AFP、CEA及CA19-9水平均低于治疗前,且观察组均低于对照组,差异均有统计学意义(P<0.05)。治疗3个疗程后,对照组CD4+、CD4+/CD8+均低于治疗前,CD8+高于治疗前,观察组CD4+、CD4+/CD8+均高于对照组,CD8+低于对照组,差异均有统计学意义(P<0.05);观察组治疗3个疗程后CD4+、CD8+、CD4+/CD8+与治疗前比较,差异均无统计学意义(P>0.05)。观察组血小板减少、白细胞减少、胃肠道反应发生率均低于对照组,差异均有统计学意义(P<0.05)。结论:PHC患者采用FOLFOX4化疗方案联合康艾注射液治疗是安全可行的,有利于降低血清AFP、CEA及CA19-9水平,减轻单纯化疗治疗对患者免疫功能的损伤,有利于控制病情进展,并可减少不良反应的发生。
【关键词】 原发性肝癌 康艾注射液 甲胎蛋白 癌胚抗原 糖类抗原19-9 免疫功能
Effects of FOLFOX4 Chemotherapy Combined with Kang’ai Injection on Serum AFP, CEA and CA19-9 Levels and Immune Function in Patients with Primary Hepatic Carcinoma/FU Xianfeng, YAN Yan, GUO Hongfei. //Medical Innovation of China, 2022, 19(18): 0-014
[Abstract] Objective: To investigate the effects of FOLFOX4 chemotherapy combined with Kang’ai Injection on serum alpha fetoprotein (AFP), carcinoembryonic antigen (CEA), carbohydrate antigen 19-9 (CA19-9)
and immune function in patients with primary hepatic carcinoma (PHC). Method: A total of 86 PHC patients treated in Affiliated Hospital of Jiangxi University of Traditional Chinese Medicine from June 2019 to May 2021 were selected and divided into two groups according to random number table method, 43 cases in each group. The control group was treated with FOLFOX4 chemotherapy regimen, and the observation group was treated with FOLFOX4 chemotherapy regimen and Kang’ai Injection, two groups were treated for 3 courses. Tumor markers, immune function and adverse reactions were compared between two groups. Result: After 3 courses of treatment, the levels of AFP, CEA and CA19-9 in two groups were lower than before, and the observation group were lower than the control group, the differences were statistically significant (P<0.05). After 3 courses of treatment, the CD4+ and CD4+/CD8+ in the control group were lower than those before treatment, while CD8+ was higher than that before treatment, and the CD4+ and CD4+/CD8+ in the observation group were higher than those in the control group, while the CD8+ was lower than that in the control group, the differences were statistically significant (P<0.05). There were no significant differences in the CD4+, CD8+, CD4+/CD8+ in the observation group after 3 courses of treatment were compared with those before treatment (P>0.05). The incidences of thrombocytopenia, leukopenia and gastrointestinal reactions in the observation group were lower than those in the control group, with statistical significance (P<0.05). Conclusion: FOLFOX4 chemotherapy combined with Kang’ai Injection is safe and feasible for PHC patients, which is beneficial to reduce the levels of AFP, CEA and CA19-9 in serum, reduce the damage of immune function caused by chemotherapy alone, control the progression of the disease and reduce the occurrence of adverse reactions.
[Key words] Primary hepatic carcinoma Kang’ai Injection Alpha fetoprotein Carcinoembryonic antigen Carbohydrate antigen 19-9 Immune function
First-author’s address: Affiliated Hospital of Jiangxi University of Traditional Chinese Medicine, Nanchang 330006, China
doi:10.3969/j.issn.1674-4985.2022.18.003
原发性肝癌(PHC)属于消化系统恶性肿瘤,PHC的治疗方法主要包括放化疗、手术及肝动脉化疗栓塞等,多数PHC患者确诊时已处于中晚期,错失根治性手术治疗机会,多选择化疗[1-2]。化疗能延长PHC患者生存时间,抑制病情进展,但化疗药物毒副作用较多,会对患者免疫功能造成一定影响[3-4]。康艾注射液属于复方中药注射剂,具有增强机体免疫功能及益气扶正等作用,已在PHC、直肠癌、肺癌等恶性肿瘤治疗中不断应用,也被用于各种原因所致的白细胞降低及减少症治疗中[5-6]。鉴于此,本研究将探讨FOLFOX4化疗方案联合康艾注射液对PHC患者血清甲胎蛋白(AFP)、癌胚抗原(CEA)和糖类抗原19-9(CA19-9)水平及免疫功能的影响。现报道如下。
1 资料与方法
1.1 一般资料 选择2019年6月-2021年5月于江西中医药大学附属医院治疗的86例PHC患者。(1)纳入标准:①PHC诊断标准参照《原发性肝癌诊疗规范》[7],且经细胞学或病理学检查证实;②预计生存期≥6个月;③卡氏(KPS)评分≥60分;④能耐受化疗、康艾注射液治疗。(2)排除标准:①合并免疫系统疾病;②重要脏器功能损伤;③患有精神疾病,行为异常;④存在出血倾向或消化道出血。按随机数字表法将其分为对照组和观察组,各43例。本研究已经医院医学伦理委员会批准,患者及家属均知情同意并签署知情同意书。
1.2 方法 对照组采用FOLFOX4化疗方案治疗。静脉滴注奥沙利铂(生产厂家:Sanofi-Aventis France,批准文号:注册证号H20171064,规格:50 mg)
85 mg/m2,第1天;亚叶酸钙[生产厂家:山东凤凰制药股份有限公司,批准文号:国药准字H20055197,规格:100 mg(以亚叶酸计)]200 mg/m2,第1~2天;5-氟尿嘧啶[生产厂家:海南卓泰制药有限公司,批准文号:国药准字H20051626,规格:0.25 g(按氟尿嘧啶计)]400 mg/m2,第1~2天。4周为一疗程,治疗3个疗程。观察组采用FOLFOX4化疗方案、康艾注射液治疗,FOLFOX4化疗方案同对照组;静脉滴注康艾注射液(生产厂家:长白山制药股份有限公司,批准文号:国药准字Z20026868,规格:20 mL/支)40 mL+5%葡萄糖注射液(生产厂家:杭州民生药业股份有限公司,批准文号:国药准字H33021630,规格:500 mL︰25 g)250 mL,4周为一疗程,治疗3个疗程。
1.3 观察指标与评定标准 (1)肿瘤标志物。采集两组空腹静脉血,采用电化学发光免疫分析法测定AFP、CEA、CA19-9水平,检测试剂盒由罗氏公司提供,两次测定时间分别为治疗前、治疗3个疗程后。(2)免疫功能。采集兩组空腹静脉血,采用FACSCalibur流式细胞仪(美国BD公司)及配套试剂测定CD4+、CD8+,计算CD4+/CD8+,两次测定时间分别为治疗前、治疗3个疗程后。(3)不良反应,包括血小板减少、白细胞减少、胃肠道反应等。
1.4 统计学处理 采用SPSS 22.0软件对所得数据进行统计分析,计量资料用(x±s)表示,组间比较采用独立样本t检验,组内比较采用配对t检验;计数资料以率(%)表示,比较采用字2检验。以P<0.05为差异有统计学意义。
2 结果
2.1 一般资料 观察组,男27例,女16例;年龄41~78岁,平均(57.91±5.20)岁;体重指数
(BMI)18~29 kg/m2,平均(24.18±1.13)kg/m2;临床分期:Ⅱ期10例,Ⅲ期16例,Ⅳ期17例。对照组,男25例,女18例;年龄40~76岁,平均(58.21±5.13)岁;BMI 18~28.5 kg/m2,平均(24.12±1.07)kg/m2;临床分期:Ⅱ期10例,Ⅲ期19例,Ⅳ期14例。两组一般资料相比,差异均无统计学意义(P>0.05),具有可比性。
2.2 AFP、CEA及CA19-9水平 治疗前,两组AFP、CEA及CA19-9水平比较,差异均无统计学意义(P>0.05);治疗3个疗程后,两组AFP、CEA及CA19-9水平均低于治疗前,且观察组均低于对照组,差异均有统计学意义(P<0.05)。见表1。
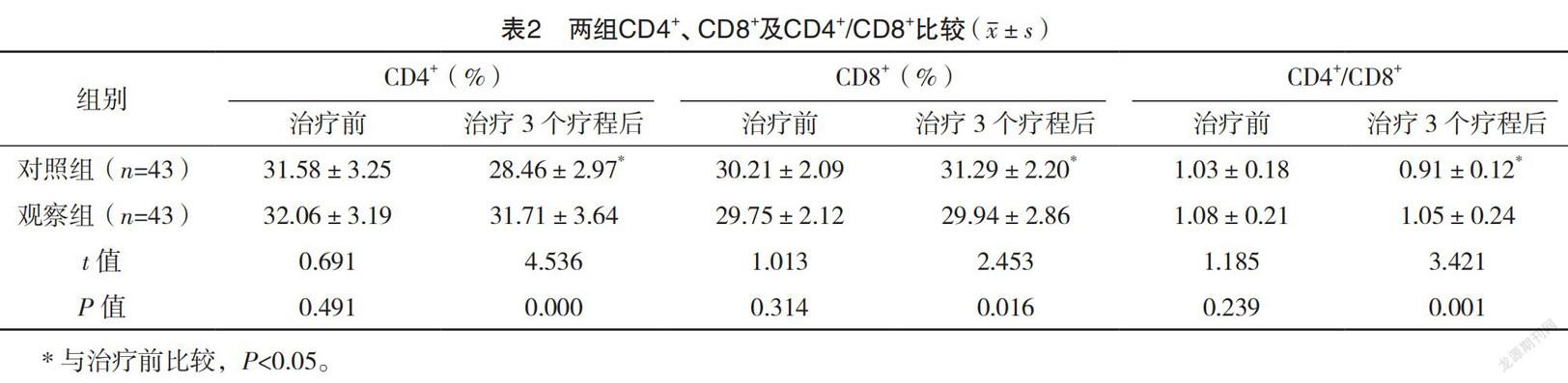
2.3 CD4+、CD8+及CD4+/CD8+ 治疗前,两组CD4+、CD8+、CD4+/CD8+比较,差异均无统计学意义(P>0.05);治疗3个疗程后,对照组CD4+、CD4+/CD8+均低于治疗前,CD8+高于治疗前,观察组CD4+、CD4+/CD8+均高于对照组,CD8+低于对照组,差异均有统计学意义(P<0.05);观察组治疗3个疗程后CD4+、CD8+、CD4+/CD8+与治疗前比较,差异均无统计学意义(P>0.05)。见表2。
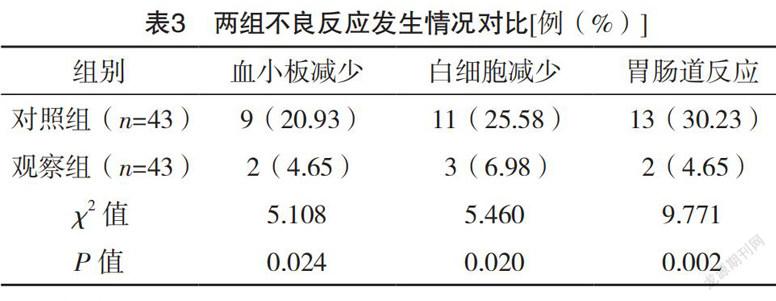
2.4 不良反应 观察组血小板减少、白细胞减少、胃肠道反应发生率均低于对照组(P<0.05),见表3。
3 讨论
PHC发病机制尚未完全明晰,临床认为与环境、肝硬化、病毒性肝炎等具有密切联系[8]。外科手术为治疗PHC的优选方法,但针对无法进行手术切除的PHC患者,化疗为重要治疗方法之一。近年来随着奥沙利铂等新型化疗药物的研发应用,FOLFOX4化疗方案已成为治疗PHC常用的姑息性治疗措施,有利于杀伤肿瘤细胞,缩小肿瘤体积,抑制肿瘤生长,改善患者临床症状,延长生存期[9-10]。
中医学认为,PHC归属于“积聚”“癥瘕”范畴,嗜酒过度、七情内伤、感受湿热邪毒及长期饮食不节等,使机体阴阳失衡、防御功能不足,进而诱发PHC[11-12]。康艾注射液是一种中成药,是由人参提取物、黄芪提取物与苦参素配伍精制而成,具有清热解毒、益气扶正之功[13]。黄芪味甘,微温,利水消肿、补气升阳;人参气味特异,味微苦且甘,主补五脏,安精神、除邪气、大补元气;苦参素即氧化苦参碱,利尿、清热燥湿[14-15]。经现代药理证实,康艾注射液具有调节免疫系统的作用,有利于对癌细胞生长进行抑制,发挥抗肿瘤效果,同时可提高化疗敏感性,减轻化疗所致的相关症状,改善患者生存质量,有效控制病情[16]。经研究发现,化疗易导致患者免疫功能紊乱,导致细胞免疫功能下降,T淋巴细胞亚群在机体抗肿瘤免疫反应中发挥重要作用[17-18]。AFP、CEA及CA19-9等血清肿瘤标志物在PHC诊断中具有重要价值,由肿瘤组织产生并释放入血,通过测定AFP、CEA及CA19-9水平能为PHC的诊断及治疗效果的评估提供参考[19-20]。本研究结果显示,治疗3个疗程后,两组AFP、CEA及CA19-9水平均低于治疗前,且观察组均低于对照组(P<0.05);治疗3个疗程后,对照组CD4+、CD4+/CD8+均低于治疗前,CD8+高于治疗前,观察组CD4+、CD4+/CD8+均高于对照组,CD8+低于对照组,差异均有统计学意义(P<0.05);观察组治疗3个疗程后CD4+、CD8+、CD4+/CD8+与治疗前比较,差异均无统计学意义(P>0.05)。观察组血小板减少、白细胞减少、胃肠道反应发生率均低于对照组(P<0.05)。提示于FOLFOX4化疗方案治疗基础上辅以康艾注射液治疗,有利于降低AFP、CEA及CA19-9水平,控制肿瘤进展,减轻单纯FOLFOX4化疗方案治疗对患者免疫功能的损伤,减少不良反应的发生。
综上所述,FOLFOX4化疗方案联合康艾注射液用于PHC治疗中安全、有效,有利于降低AFP、CEA及CA19-9水平,调节患者免疫功能,减少不良反应的发生,提高PHC治疗效果。
参考文献
[1]胡官强,张晓斌,赵新汉,等.老年原发性肝癌晚期联合化疗的临床研究[J].现代消化及介入诊疗,2018,23(2):173-175.
[2]李健,羅祖炎,俞文强,等.雷替曲塞介入治疗不可切除原发性肝癌的疗效及安全性分析[J].肿瘤学杂志,2018,24(5):484-486.
[3]付烊,赵旭,刘亚琪,等.数据挖掘BLQ复方中药联合化疗治疗原发性肝癌的临床观察[J].中华中医药杂志,2018,33(11):5249-5252.
[4]李巍,董晓彤,傅华,等.含奥沙利铂化疗方案联合热疗治疗原发性肝癌的临床治疗效果研究[J].中国现代医学杂志,2018,28(1):125-128.
[5]王红兵,蒲志忠,邓彬,等.康艾注射液对乳腺癌组织中PI3k/akt通路和CD、NK细胞的影响[J].世界中医药,2018,13(5):1156-1159,1163.
[6]刘增利,汪晓军.康艾注射液降低乙肝相关性肝癌介入术后不良反应效果观察[J].北京中医药,2018,37(11):1092-1094.
[7]中华人民共和国卫生和计划生育委员会医政医管局.原发性肝癌诊疗规范(2017年版)[J].中华消化外科杂志,2017,16(7):705-720.
[8]邴浩,王薇,李异玲.中国东北地区汉族人群PNPLA3 rs738409及TM6SF2 rs58542926基因多态性与原发性肝癌的相关性[J].中华肝脏病杂志,2021,29(2):156-162.
[9]陈嵩,吴志强,庄文权,等.经肝动脉栓塞术联合FOLFOX4方案持续动脉灌注化疗治疗肝细胞癌合并门静脉癌栓15例近期临床疗效评价[J].介入放射学杂志,2019,28(4):328-333.
[10]贺小军,杨振宇,杜锡林,等.FOLFOX4化疗方案联合免疫治疗在中晚期肝癌中的应用价值(附2例报告)[J].现代肿瘤医学,2019,27(14):2518-2523.
[11]赵艳莉,千维娜,吴召利.自拟扶正解毒消积方联合替吉奥胶囊治疗中晚期原发性肝癌疗效观察[J].现代中西医结合杂志,2018,27(9):926-928,933.
[12]赵延军,单宇鹏.复方斑蝥胶囊对原发性肝癌患者介入治疗后细胞免疫功能的影响[J].陕西中医,2018,39(1):77-79,134.
[13]于霞,蒋丽丽,朱卫华.康艾注射液联合FOLFOX化疗方案治疗结直肠癌的临床研究[J].癌症进展,2018,16(5):650-653.
[14]朱诗聪,王鹤玲,徐娅,等.康艾注射液联合PP方案治疗脾肺气虚型晚期肺腺癌患者的临床研究[J].医药导报,2020,39(4):572-576.
[15]伍晓慧,张英,侯炜,等.康艾注射液联合一线含铂化疗治疗晚期非小细胞肺癌的随机对照多中心临床试验[J].中国新药杂志,2018,27(6):662-667.
[16]许恩健,陆国军.康艾注射液联合伊立替康和卡铂治疗广泛期小细胞肺癌的临床研究[J].现代药物与临床,2018,33(10):2651-2654.
[17]郑操,张荣胜,潘勇,等.金龙胶囊与介入治疗原发性肝癌的疗效及对T淋巴细胞亚群、肿瘤免疫因子的影响[J].现代消化及介入诊疗,2018,23(4):506-509.
[18]金灵莉,杜致远,卢光新,等.原发性肝癌介入治疗联合沙利度胺对VEGF、bFGF水平及红细胞免疫功能、T淋巴细胞亚群水平的影响[J].广西医科大学学报,2019,36(3):431-434.
[19]王春玲,叶加润.腹部超声联合甲胎蛋白在原发性肝癌患者中的诊断效果及临床治疗指导价值研究[J].中国医学创新,2018,15(30):105-109.
[20]崔琦,董延娥,霍云龙,等.多种血清肿瘤标记物联合检测在原发性肝癌临床诊断中的价值[J].现代肿瘤医学,2019,27(18):3267-3270.
(收稿日期:2021-11-30) (本文编辑:程旭然)
