镍/氧化铝加氢催化剂的制备及性能研究
2022-07-11杨文龙卢雁飞南芷钰李宇航李世松王春雷张东升
杨文龙,程 鹏,卢雁飞,南芷钰,李宇航,李世松,王春雷,舒 畅,张东升
(1.河北工业大学化工学院,天津 300130;2.中海油天津化工研究设计院有限公司;3.中国石油大学)
新戊二醇(Neopentyl glycol,简称NPG),化学名为2,2-二甲基-1,3-丙二醇,分子式为C5H12O2。NPG特殊的新戊基结构使其衍生产品具有优良的化学稳定性、耐腐蚀性及抗水解性,广泛应用于合成聚酯树脂、润滑油、增塑剂、阻聚剂、医药、农药等[1-7]。据统计[8],2020年中国NPG消费量为30万t,2021年已达42.5 万t。而且,随着中国经济的快速发展,未来几年NPG需求量还将持续增长。
通常,NPG 工业化生产路线有两条,即卤代丙醇路线[9-10]和异丁醛路线[11-19]。卤代丙醇路线以2,2-二甲基-3-氯代丙醇为起始原料,经环醚化和碱解生成NPG。但该路线因原料紧缺,产量较少,故已被淘汰。异丁醛路线是目前主流合成工艺,即以异丁醛和甲醛为起始原料,经碱催化缩合生成中间体2,2-二甲基-3-羟基丙醛(俗称羟基新戊醛,简称HPA),再还原生成NPG。因HPA 被还原的方法有甲醛歧化和催化加氢,故工艺上又细分为歧化法[13-15]、缩合加氢法[16-19]两种。
目前,缩合加氢工艺中常见的加氢催化剂有贵金属系[18,20]催化剂、镍系[16,21]和铜系催化剂[22-23]。为改善加氢工艺,研究者不断优化催化剂体系。例如,李吉明等[18]以钯碳为加氢催化剂,研究了不同反应条件对HPA加氢合成NPG反应的影响,适宜的加氢工艺条件为:反应温度为95 ℃、反应压力为4 MPa、反应时间为4 h,此时NPG 收率为94.6%、选择性为94.7%。SCHALAPSKI 等[21]以脂肪醇为溶剂,镍为催化剂,催化HPA 加氢反应,反应温度为130 ℃、反应压力为8 MPa、液时空速为0.9 h-1时,HPA转化率为98%、NPG 选择性为98%。EISENACHER等[22]制备了钡和锰为活化剂的铬酸铜催化剂,用于HPA 加氢反应,反应温度为155 ℃、反应压力为80 kPa、液 时 空 速 为0.57 h-1时,HPA 转 化 率 为99.8%、NPG 选择性为98.6%,但是铬会造成一定的环境污染。总之,对于加氢催化剂来说,贵金属催化剂生产成本较高,不利于工业化生产;铜系催化剂,如铬酸铜等,会造成环境污染;镍系催化剂活性较低,且需要较高的反应温度和压力。因此,开发适用反应条件温和、低温低压、低成本的催化剂反应体系,仍然是今后重点研究的内容之一。基于此,本文以常规的共沉淀法和浸渍法制备了镍系催化剂Ni/Al2O3,并重点考察了其催化羟基新戊醛加氢制备新戊二醇的反应性能。
1 实验部分
1.1 原料与仪器
无水乙醇、1,4-二氧六环、2,2-二甲基-3-羟基丙醛、新戊二醇、氧化铝、六水合硝酸镍、九水合硝酸铝、氢氧化钠,均为AR。商用催化剂(共沉淀法制备的Ni/Al2O3催化剂)。
Thermo Trace 1310 ISQ 气相色谱-质谱联用仪;安捷伦7890B 型色谱;D/max-2500 X 射线衍射仪;ASAP 2020 型物理吸附仪;ZSX Primus Ⅱ全自动扫描型X射线荧光光谱仪;ASAP 2420 全自动静态化学吸附仪;Optima5300DV 电感耦合等离子体发射光谱仪。
1.2 催化剂的制备及表征
实验采用共沉淀法制备了20%Ni/Al2O3、40%Ni/Al2O3催化剂,采用浸渍法制备了20%Ni/Al2O3催化剂,制备过程简述如下。
共沉淀法[24]:首先,按催化剂负载量要求称取Ni(NO3)2·6H2O、Al(NO3)3·9H2O,配制为1 mol/L 硝酸盐溶液备用,称取一定量的氢氧化钠,配制1.1 mol/L的NaOH 溶液;其次,在2 L 的三口烧瓶中加入100 mL去离子水,硝酸盐溶液和NaOH 溶液同时滴入三口烧瓶中,搅拌速率控制在300 r/min,滴加速率为3 mL/min,反应温度为40 ℃,滴定过程中需严格控制pH 保持在7~8;反应完全后,浆液在40 ℃下继续搅拌老化4 h;老化完成后抽滤,用1 L的去离子水多次洗涤滤饼,洗涤后的催化剂自然干燥24 h,在120 ℃鼓风干燥12 h;最后,将催化剂放入马弗炉中,升温速率为1 ℃/min,在550 ℃下焙烧3 h;冷却至室温后,得到Ni/Al2O3催化剂。
浸渍法[25]:测定载体的吸水率,将载体γ-Al2O3等体积浸渍一定浓度的硝酸镍溶液,浸渍6 h后置于干燥箱中,120 ℃下干燥12 h,干燥后在550 ℃下焙烧3 h,制得Ni/Al2O3催化剂。
采用D/max-2500 型X 射线衍射仪进行XRD 测试,扫描角度为5~80°、扫描速度为10(°)/min。采用ASAP 2020型物理吸附仪测定催化剂比表面积及孔结构,样品测定前在150 ℃下抽真空活化4 h,以液氮为吸附介质,-196 ℃下进行测试。X 射线荧光光谱图在ZSX Primus Ⅱ全自动扫描型X射线荧光光谱仪上测得。氢气程序升温还原(H2-TPR)在ASAP 2420 全自动静态化学吸附仪上进行,催化剂用量为150~200 mg、粒度为180~250µm,样品置于氩气环境在350 ℃下预处理1 h后降至室温,切换气体为10% H2/Ar 进行程序升温还原,由室温升至900 ℃,升温速率为15 ℃/min。CO 脉冲吸附同样在ASAP 2420 全自动静态化学吸附仪上进行,测试催化剂Ni表面CO吸附能力,催化剂经过原位还原后,在He气氛下冷却至室温,之后进行CO脉冲吸附,脉冲采用10% CO/He 混合气,直至检测到的CO 峰面积不再变化。采用Optima5300DV 电感耦合等离子体发射光谱仪(ICP-AES)确定反应后溶液中催化剂金属离子含量,确定是否有镍离子流失。
首句透露了诗人失偶的痛苦而点到即止,立即援引荀息、屈平典故,转向对丈夫节行的表彰,体现出作者的深明大义。当然,商景兰不可能将全部的心绪都反映在这首广为传诵、具有公众性的悼亡诗中,但诗中欲语还休、隐隐透出的怨意,已经奠定了她后半生诗作的感情基调。
1.3 催化剂的评价
在固定床反应器上对制备的3种催化剂进行性能评价。反应装置简图如图1所示。典型操作过程如下:将30 mL 375~850µm的加氢催化剂装入固定床反应器恒温区,其余部分用相同粒径的瓷球装填;通入氮气试漏,确保气密性良好后,依次通入氮气和氢气置换;置换后开启加热,程序升温还原催化剂;还原完成后,待催化剂床层升至预设温度和压力后,泵入HPA 溶液进行加氢反应,反应过程中每隔1 h进行取样分析。

图1 固定床反应装置简图Fig.1 A sketch of fixed bed reactor
1.4 产物的计算及分析
采用安捷伦7890B 型色谱对加氢原料及加氢产物进行定量分析,FFAP 色谱柱(60 m×0.32 mm×0.25µm),氢火焰(FID)检测器。色谱操作条件:载气为氮气,检测器温度为350 ℃,气化室温度为250 ℃;柱温采用程序升温:起始温度为50 ℃,以10 ℃/min升至230 ℃,保持3 min。采用内标法进行定量,二氧六环为内标物。
HPA的转化率为:
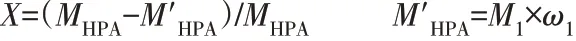
NPG的收率为:
NPG的选择性为:
式中:MHPA为原料中HPA 的质量,g;M′HPA为反应后溶液中HPA的质量,g;M1为反应后溶液的总质量,g;ω1为反应后溶液中HPA的质量分数;MNPG为反应前原料中NPG 的总质量,g;ωNPG为反应后NPG 的质量分数;X为HPA的转化率;Y为NPG的收率;S为NPG的选择性。
2 催化剂表征
2.1 XRF结果
通过XRF 对不同镍催化剂中的元素组成及含量进行测定,表征结果如表1 所示。并将实际结果与理论结果对比,可以看出自制的3 种催化剂中的实际镍含量与理论镍含量基本保持一致;商用催化剂NiO含量较高。
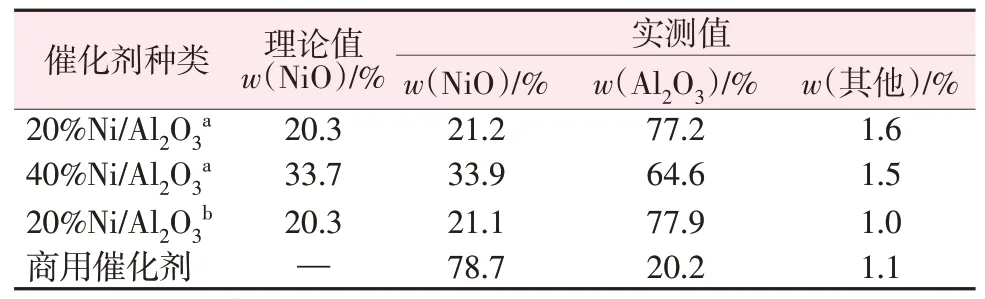
表1 不同镍催化剂的XRF结果Table 1 XRF results of different nickel catalysts
2.2 BET结果
为探究不同制备方法制备的镍系催化剂比表面积及孔结构的差别及其对HPA加氢性能的影响,对4种催化剂进行BET测试,测试结果如表2所示。由表2 可知,共沉淀法制得的催化剂比表面积随着镍负载量的增大呈减小趋势,这可能是由于催化剂活性组分中镍含量越高,载体Al2O3含量会越少,载体所能提供的有效表面积就会越少;共沉淀法制得的20%Ni/Al2O3催化剂比表面积最大,其次是浸渍法制得的20%Ni/Al2O3催化剂[26-27],商用催化剂比表面积最小;孔容和孔径越小,反应过程中受内扩散的影响就会越大,浸渍法制得的20%Ni/Al2O3催化剂孔径和孔容都是4 种催化剂中最大的。综上所述,浸渍法制得的20%Ni/Al2O3催化剂比表面积、孔容和孔径均相对较大,反应活性可能会高。
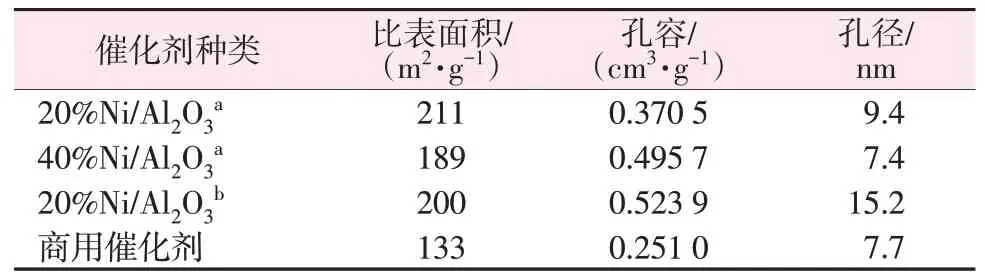
表2 不同镍催化剂的BET结果Table 2 BET results of different nickel catalysts
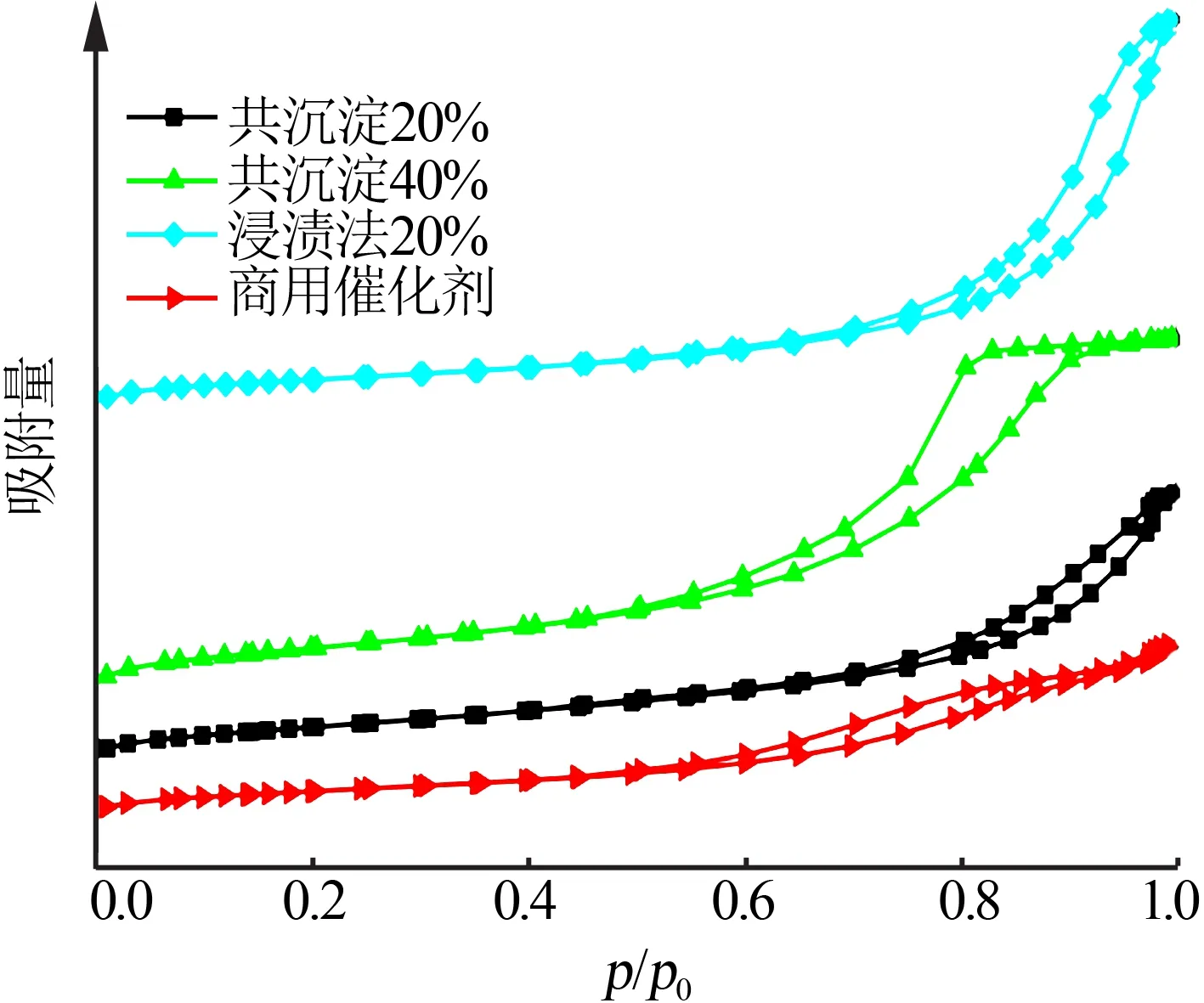
图2 不同镍催化剂的吸脱附等温线Fig.2 Adsorption and desorption isotherms of different nickel catalysts
2.3 XRD与H2-TPR结果
4 种催化剂的XRD 结果与H2-TPR 结果分别如图3 和图4 所示。主峰位于2θ=37.3°、45.5°和67.3°分别对应立方γ-Al2O3(311)、(400)和(440)晶面的衍射峰[28]。共沉淀法40%Ni/Al2O3、浸渍法20%Ni/Al2O3和商用催化剂在37.3°、43.4°和63°都存在明显的NiO 的特征峰。而共沉淀法制得的20%Ni/Al2O3在37.3°有明显的NiO 的特征峰,而43.4°、63°的特征峰几乎没有,结合H2-TPR 结果表明NiO 结晶到γ-Al2O3载体的面心立方氧上填充部分空隙形成了NiAl2O4。

图3 不同镍催化剂的XRD图Fig.3 XRD patterns of different nickel catalysts

图4 不同镍催化剂的H2-TPR图Fig.4 H2-TPR diagrams of different nickel catalysts
NiAl2O4尖晶石的峰不容易被分辨出来,NiAl2O4在2θ=45°时有特征峰,靠近γ-Al2O3在45.5°的特征峰。2θ=66.5°的峰接近2θ=67.3°的γ-Al2O3特征峰和2θ=65.5°的NiAl2O4特征峰,结合H2-TPR 结果可证明4 种催化剂中均存在有缺陷的NiAl2O4尖晶石相[29]。NiAl2O4尖晶石的其他特征衍射峰出现在37.3°附近,这种尖晶石结构很稳定,能防止微晶的聚集,保持NiO 高分散状态和催化剂的热稳定性。除NiAl2O4尖晶石外,还存在NiAl10O16(2θ=37.59、45.45、45.64°),NiAl26O40(2θ=45.47、66.44、66.98°),NiAl32O49(2θ=37.41、37.72、45.43°)以及Ni2Al18O29(2θ=37.59、45.62、66.87°)[30]。
不同镍催化剂的H2-TPR 图中,位于350、520、650、800 ℃的还原峰所对应的Ni物种分别为无定形NiO、晶型NiO、NiAl2O4和NiAlxOy(x>2)。
共沉淀法20%Ni/Al2O3催化剂还原峰主要分布在350 ℃、620~630 ℃以及750~790 ℃,与文献[31]结果一致。对于第一个还原峰,在低镍负载下,最低的还原峰(350 ℃)非常微弱,为相变过程并发生部分NiO 还原。当催化剂的镍含量较高时,则会出现较大的重叠峰(500~520 ℃、620~630 ℃、750~790 ℃),通常被确定为一个峰,高温峰可归因于非晶态铝酸镍晶格中Ni2+的还原。共沉淀法40%Ni/Al2O3和浸渍法20%Ni/Al2O3的还原峰如上所述为一个大的还原峰,还原温度为550 ℃时,催化剂中的全部NiO及部分铝酸镍被还原,而共沉淀法制备的20%Ni/Al2O3催化剂,只有无定形的NiO 被还原。商用催化剂是还原之后加钝化剂的产品,因此还原温度相对较低。
据文献报道,Ni2+负载量较低时,Ni2+优先占据Al2O3中四面体的空位,Ni2+物种主要以NiAl2O4尖晶石相存在。Ni2+负载量较高时,Ni2+会同时占据Al2O3的四面体空位和八面体空位,形成NiO 相[32-33]。因此,对比共沉淀法制备的20%Ni/Al2O3和40%Ni/Al2O3催化剂,可以发现镍负载量的增加有助于易还原镍物种的生成,提高催化剂的还原度[34],证实了共沉淀法40%Ni/Al2O3催化剂中NiAl2O4尖晶石占比低于20%Ni/Al2O3。
2.4 CO脉冲吸附结果
对不同镍催化剂进行CO 脉冲吸附测试来计算活性金属分散度,表3为不同催化剂的金属分散度。由表3可知,共沉淀法制备的Ni/Al2O3催化剂随着镍含量的增加,金属分散度减小。浸渍法制备的20%Ni/Al2O3催化剂累积吸附量较高,金属分散性较好。
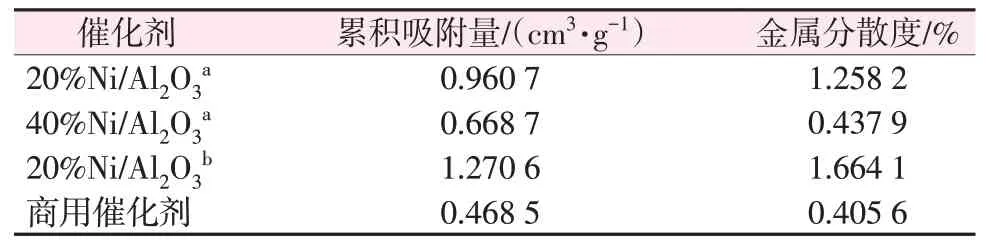
表3 不同镍催化剂的金属分散度Table 3 Metal dispersion of different nickel catalysts
2.5 加氢反应液ICP结果
取加氢反应后的溶液进行ICP 测试,测定溶液中镍金属离子的浓度。4 种催化剂反应后溶液的ICP结果如表4所示。由表4可知,共沉淀法20%Ni/Al2O3催化剂反应后的溶液中镍离子含量略高于共沉淀法40%Ni/Al2O3反应液中的镍离子含量。结合催化剂XRD 和H2-TPR 表征结果,推测该结果可能的原因为共沉淀法20%Ni/Al2O3催化剂中体相NiO高度分散且晶粒较小,该镍组分与载体间作用力较小[35],故反应过程中其可能与副产物(如原料HPA中含有少量甲酸)反应,造成少量镍流失。4种催化剂的反应液中镍离子质量分数均小于1×10-6,表明镍催化剂适用于HPA加氢反应体系,不存在严重的镍流失问题。
3 催化剂评价结果及讨论
在固定床反应器上对3 种自制的Ni/Al2O3及商用催化剂进行评价,质量分数为10%的HPA乙醇溶液为加氢原料。进料前使用N2-H2混合气对催化剂进行还原,升温速率为15 ℃/h,升温至550 ℃,稳定4 h。还原完成后,调节所需温度、压力等参数,开始进料。通过改变反应温度、反应压力、氢醛比、液时空速等参数,探究催化剂的反应性能,并筛选出最佳加氢合成NPG的工艺条件。
3.1 反应温度对NPG合成的影响
在反应压力为3 MPa、液时空速为1 h-1、氢醛比为10的条件下,反应温度对HPA加氢的影响如图5所示。由图5可知,在所考察的温度范围内,HPA转化率随温度的升高而增加,当温度超过103 ℃时,HPA转化率趋于稳定,由于HPA可分解为甲醛和异丁醛及HPA 缩聚生成羟基特戊酸新戊二醇单酯(1115酯),导致NPG的选择性大幅度降低。综合考虑,HPA加氢制备NPG适宜反应温度为103 ℃。
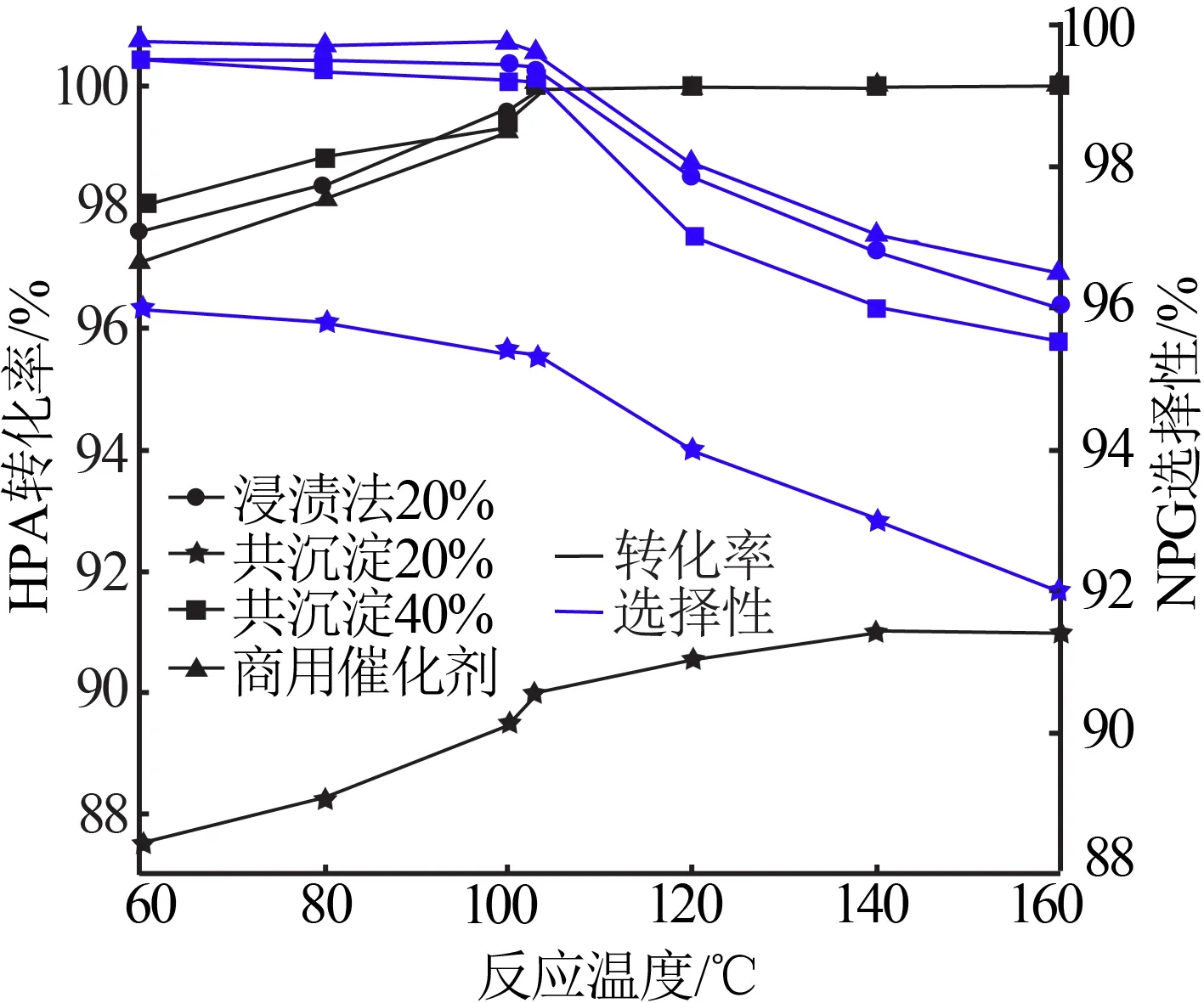
图5 不同反应温度对HPA加氢反应的影响Fig.5 Effect of different reaction temperature on HPA hydrogenation reaction
3.2 反应压力对NPG合成的影响
在反应温度为103 ℃、液时空速为1 h-1、氢醛比为10的情况下,考察了不同反应压力对HPA加氢反应的影响,实验结果如图6所示。由图6可知,当反应压力小于3 MPa 时,HPA 的转化率随压力的增加而增加,当压力大于3 MPa时,NPG的选择性有下降趋势。当反应压力小于3 MPa时,提高压力,氢气的分压也随之变大,HPA转化率也随之增加。对于浸渍法20%Ni/Al2O3、共沉淀法40%Ni/Al2O3及商用催化剂,当反应压力大于3 MPa 时,HPA 转化率为100%,且保持不变,NPG选择性在反应压力为1~5 MPa时波动较小。综合考虑,HPA加氢制备NPG适宜反应压力为3 MPa。
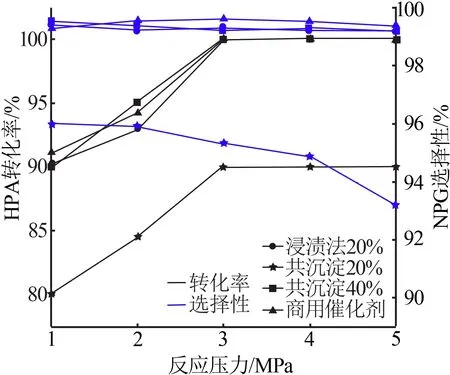
图6 不同反应压力对HPA加氢反应的影响Fig.6 Effect of different reaction pressure on HPA hydrogenation reaction
3.3 氢醛比对NPG合成的影响
在反应温度为103 ℃、液时空速为1 h-1、反应压力为3 MPa 时,考察了不同氢醛比对HPA 加氢反应的影响,结果如图7所示。由图7可知,随着氢醛比的增大,HPA 转化率略有提高,NPG 的选择性波动较小。这是由于HPA 加氢反应存在气-液-固三相间的动态平衡,首先气液混合反应物需扩散到催化剂活性中心,然后进一步反应。因此,增加氢气流量,有利于突破内扩散控制,反应效果更好。氢气过量还可以抑制结焦反应,有利于提高催化剂稳定性。但氢气量过大,会导致循环气负荷高,增加能耗。综合考虑,HPA加氢制备NPG适宜氢醛比为10。
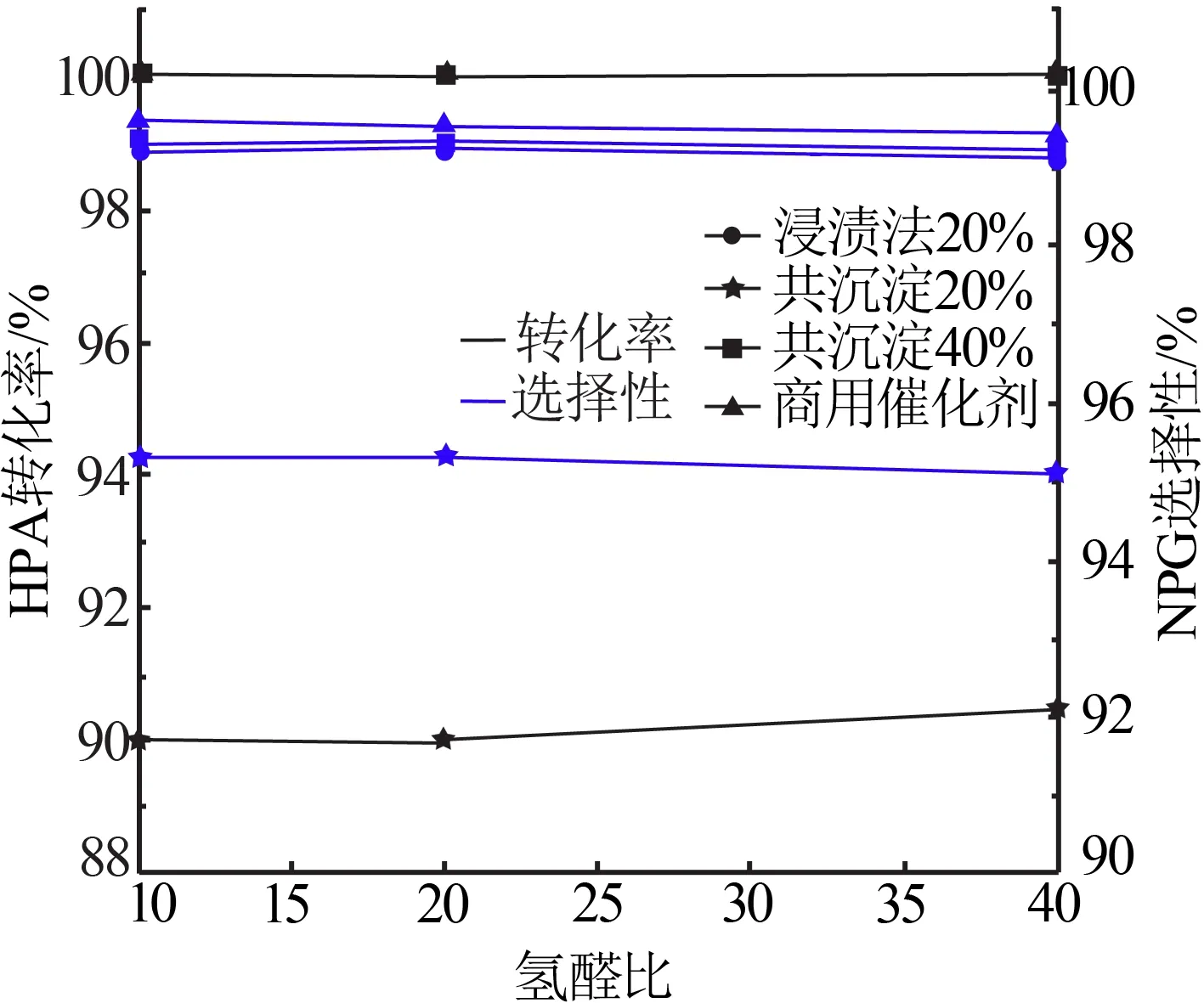
图7 不同氢醛比对HPA加氢反应影响Fig.7 Effect of different hydrogen to aldehyde ratio on HPA hydrogenation reaction
3.4 液时空速对NPG合成的影响
在反应温度为103 ℃、反应压力为3 MPa、氢醛比为10的情况下,考察了不同液时空速对HPA加氢反应的影响,结果如图8所示。由图8可知,HPA转化率随液时空速的增加而降低;当液时空速小于1 h-1时,HPA 转化率为100%,NPG 选择性基本不变(>99%);当液时空速大于1 h-1时,HPA 的转化率明显下降,NPG 选择性基本不变。液时空速较大会导致HPA 与催化剂接触不充分,降低HPA 转化率,液时空速较小又会造成经济损失。因此,综合考虑产品收率以及催化剂床层处理量,HPA加氢制备NPG适宜液时空速为1 h-1。
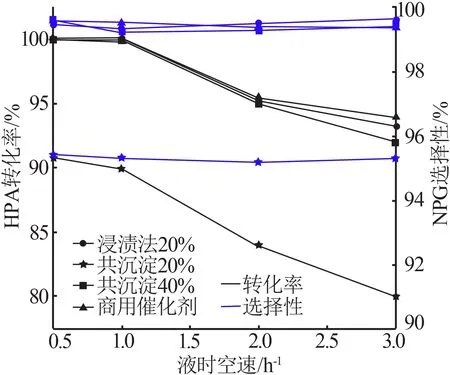
图8 不同液时空速对HPA加氢反应的影响Fig.8 Effect of different liquid space-time velocities on HPA hydrogenation reaction
通过对HPA加氢工艺条件的优化,HPA加氢制备NPG较优的工艺条件为:反应温度为103 ℃、反应压力为3 MPa、液时空速为1 h-1、氢醛比为10。由浸渍法制备的20%Ni/Al2O3催化剂和共沉淀法制备的40%Ni/Al2O3催化剂加氢性能与商用催化剂相当,HPA转化率为100%、NPG选择性为99.3%。共沉淀法制备的20%Ni/Al2O3加氢性能相对较差,HPA 转化率为95.2%、NPG选择性仅为84%。分析其催化性能较差的原因:共沉淀法制备的20%Ni/Al2O3催化剂孔容较小,反应过程中受内扩散影响大;根据H2-TPR结果,550 ℃还原温度下,该催化剂中仅体相的NiO被还原,活性组分数量相对较少,且体相NiO与载体之间的作用力较小,易造成部分镍离子流失,故催化活性较差。
3.5 催化剂稳定性实验考察
对催化剂稳定性进行评价,反应结果见图9。浸渍法相对于共沉淀法操作简单,考虑到经济性和工业化要求,选择反应效果较优的催化剂为浸渍法制备的20%Ni/Al2O3催化剂。反应条件为:反应温度为103 ℃、反应压力为3 MPa、液时空速为1 h-1、氢醛比为10。由图9看出,浸渍法制备的20%Ni/Al2O3催化剂在1 000 h 的长周期评价过程中,HPA 转化率(>99%)和NPG选择性(>99%)基本稳定。
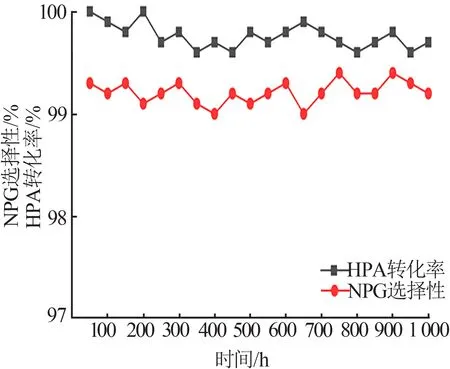
图9 浸渍法20%Ni/Al2O3催化剂稳定性评价Fig.9 Stability evaluation of 20%Ni/Al2O3 catalyst by impregnation method
3.6 催化剂评价结果对比
将浸渍法制备的20%Ni/Al2O3催化剂评价结果与文献中其他镍系催化剂、铜系催化剂及贵金属催化剂评价结果进行对比(见表5),20%Ni/Al2O3对于HPA 加氢反应所需反应温度及反应压力均相对较低,且HPA可以完全转化,NPG选择性也相对较高。铜系催化剂催化HPA加氢反应,HPA转化率及NPG选择性相对较低;镍催化剂成本与贵金属催化剂相比,成本相对较低。综上所述,该催化剂适用于条件温和、低温、低压且成本低廉的催化剂反应体系。
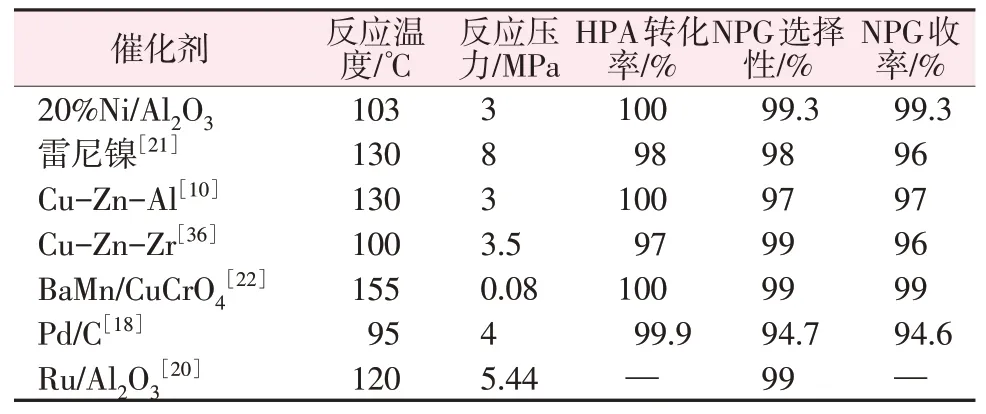
表5 不同催化剂反应条件与催化性能对比Table 5 Comparison of reaction conditions and catalytic performance of different catalysts
4 结论
基于羟基新戊醛合成新戊二醇反应,以非贵金属Ni为催化活性组分,采用共沉淀法和浸渍法制备了Ni/Al2O3催化剂。催化剂表征结果表明,浸渍法20%Ni/Al2O3催化剂比表面积较大,金属分散性好,且催化剂中的镍物种易被还原,其反应性能良好。催化剂评价结果表明,浸渍法20%Ni/Al2O3和共沉淀法40%Ni/Al2O3催化剂催化效果与商用催化剂相当,而共沉淀法制备的20%Ni/Al2O3催化剂催化效果相对较差。在相对较温和的反应条件下,即反应温度为103 ℃、压力为3 MPa、空速为1 h-1、氢醛比为10的条件下,浸渍法制备的20%Ni/Al2O3催化剂催化HPA加氢反应,HPA转化率为100%、NPG选择性为99.3%。浸渍法相对于共沉淀法操作简单,考虑到经济性和工业化要求,反应效果较优的催化剂为浸渍法制备的20%Ni/Al2O3催化剂。对催化剂进行长周期评价,结果表明催化剂性能稳定,容易实现工业化。
