基于分组注意力残差网络的锥束XLCT成像
2022-07-04周仲兴郭司琪贾梦宇
周仲兴,郭司琪,贾梦宇,张 林,吴 越
基于分组注意力残差网络的锥束XLCT成像
周仲兴1, 2,郭司琪1, 2,贾梦宇1, 2,张 林2,吴 越2
(1. 天津大学精密仪器与光电子工程学院,天津 300072;2. 天津市生物医学检测技术与仪器重点实验室,天津300072)
锥束X射线磷光断层成像(cone-beam X-ray luminescence computed tomography,CB-XLCT)作为一种新兴的混合成像技术可同时获得解剖结构信息和功能代谢信息,在疾病的早期诊断和靶向治疗上具有广泛发展前景.然而,由于锥束XLCT成像过程中的高度不适定性,重建结果的空间分辨率较低.针对该问题,提出了一种基于分组注意力残差网络的锥束XLCT定量磷光分布重建方法.该方法采用注意力机制优化光子密度特征通道的权重系数,并结合近似域约束损失函数,从而改善残差网络的特征表达过程,提高图像重建精度和模型稳健性.结果表明:所提出的方法在仿真实验中可清晰分辨并重建出靶心距离为7mm的双目标体,位置误差(LE)约为0.37mm,戴斯相似性指数(Dice)达到了84%.在仿体实验中,LE约为0.48mm,Dice达到了79%.因此,分组注意力残差网络方法能够有效在定位精度、空间分辨率、稳健性等多方面提高图像重建质量.
锥束XLCT;深度学习;分组注意力;图像重建
X射线激发传感和光学分子传感是利用两种不同的相互作用方式和传感方法激发生物组织中的纳米分子探针,并对信号发射位置进行检测和定位的成像技术.基于X射线的激发传感技术在近十年时间内发展迅速,为深入开展组织生理学及病理生理学研究奠定了基础[1].X射线作为探针激发源的优势在于穿透性强并且具有广泛的生物医学成像场景.但X射线成像通常基于光电效应,峰值衰减在keV能量范围内,分子敏感性较低[2].相比而言,光学分子传感成像提供了优越的分子灵敏度.目前,随着探测器和传感器在探测范围和光子灵敏度等方面的不断发展,提高了光学传感器件在信号检测、采集方面的能力,为X射线在分子成像领域的应用奠定了基础[3].
为进一步提高分子敏感性,X射线磷光断层成像(X-ray luminescence computed tomography,XLCT)作为一种混合成像模态,通过使用传统X射线的组织感知力和光学分子成像的对比能力,在深度外显率和空间分辨率方面呈现出潜在优势[4].该技术通过X射线激发生物组织体内的磷光探针产生可见光或近红外,而后利用光敏探测器接收光学信号,最后通过图像重建方法恢复出测量组织中磷光探针空间分布.目前,XLCT成像系统根据激发模式的不同主要分为窄束XLCT和锥束XLCT,两类系统具有不同的硬件设计和成像性能[5].窄束XLCT通常基于有限视角成像技术,需要按照特定的顺序激发X射线并获取测量结果,具有一定的采样复杂度.锥束XLCT基于全域激发可实现快速测量,因此在X射线利用率与数据采集模式上具有较大优势.然而,由于XLCT成像过程中的高度不适定性,重建图像质量相对较低.此外,锥束XLCT缺乏窄束XLCT中的X射线位置信息,进一步加剧了成像目标重建难度.目前,锥束XLCT成像仍存在空间分辨率不佳、重建精度受限等问题,从而限制了其面向高质量快速组织体成像的应用[6].因此,进一步研究锥束XLCT图像质量的改善方法对于活体生物和生化过程的无创成像至关重要.
目前,用于改善锥束XLCT成像不适定性的重建方法可分为两类:一类为基于光学传输方程构建代数迭代的传统重建方法,以得到测量值与估计值之间的最佳匹配,如L1正则化、L2正则化方法等[7].该类算法通常具有严谨的数学理论支撑,并能得到稳定且有效的解.然而,这类方法过度依赖于逆向问题求解模型的设计,且不同成像样本也面临反复调节参数以优化重建结果的问题,重建效果受主观因素影响较大,图像重建质量受限[8].另一类方法为深度学习重建方法,其核心思想为通过大型数据集学习逆问题的未知解,建立更符合实际环境的非线性模型.与传统方法相比,深度学习方可有效避免研究学者将精力放在特征提取上,解决了人工提取特征不完整的问题[9].此外,随着近年来大数据时代的到来及人工智能技术的发展,深度学习技术在光学分子成像领域发展如火如荼.如Gao等[10]提出了基于多层感知机的生物发光断层成像(bioluminescence tomography,BLT)逆问题模拟方法,采用神经网络拟合组织表面光子密度与组织体内发光源之间的非线性关系,实验结果表明该方法显著提高了BLT在活体肿瘤中的重建质量.Lun等[11]使用残差网络(ResNet)实现了多个投影角度下的聚焦X射线磷光断层成像,有效验证了深度学习方法应用于窄束XLCT重建的可行性.综上所述,传统方法通常存在模型精度误差,且由于逆问题的严重病态性导致求解不稳定,图像重建的空间分辨率和量化度较差.深度学习方法发展迅速,具有广泛的应用潜力,但对于不同类型的光学成像技术需设计出符合实际需求的个性化网络.
因此,为进一步改善锥束XLCT图像重建质量,本文基于深度学习框架的自适应参数学习特性,构建了一种用于锥束XLCT定量磷光分布的分组注意力残差网络重建方法,该方法仅需通过简单的训练、优化,便可得到成像物体表面光子密度与内部磷光探针浓度分布间的非线性映射.
具体来说,该方法通过在残差网络中融合注意力机制,实现从锥束XLCT光学信号中高效学习到有助于目标光源重建的有效特征表示,快速逼近成像过程中的近红外光传播函数.此外,本文将磷光探针的浓度分布范围作为锥束XLCT的先验知识集成到网络的损失函数中,使得从训练数据中学习的模型符合可接受的领域规则,增强网络模型的鲁棒性.最后通过仿真实验及仿体实验验证了本文方法的可行性和有效性.
1 理论方法
1.1 成像模型
一般来说,锥束X射线激发发光在生物组织 中的传播可以描述为3个过程:X射线在生物组织 体内的传播模型、X射线激发磷光纳米粒子产生近 红外光子模型以及近红外光子在生物组织体内的传播模型.
首先,高能X射线源发射锥形X射线束并穿透生物组织.根据朗伯比尔定律,X射线在组织体内的传播模型[12]为
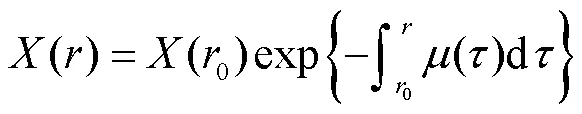
其次,深埋在成像物体内的磷光探针与X射线相互作用,受激产生的近红外光强度为

最后,近红外光与组织体发生吸收、散射等相互作用后的能量变化可以用辐射传输方程(radiative transfer equation,RTE)描述[13].由于RTE方程求解较为复杂,光在高散射弱吸收组织中的传输过程通常近似为扩散方程(diffusion equation,DE)来表示,即
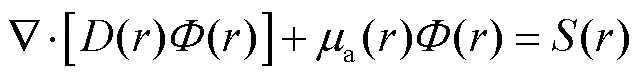
根据微分方程理论,求解扩散方程需具备合适的边界条件.本文采用罗宾边界条件进行补充[14],即
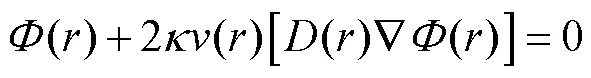
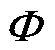

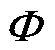
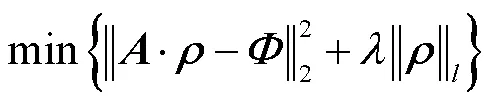
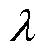
1.2 基于分组注意力残差网络的锥束XLCT重建 方法
1.2.1 分组注意力残差网络
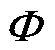
鉴于本文需对多个不同投影特征通道间的依赖关系进行重要性解析.因此本文使用简洁而有效的通道注意力机制(channel attention,CA)作为信息增强模块[20],并根据锥束XLCT图像重建特点,对注意力机制的作用域按照锥束XLCT测量模式进行设计和优化,进一步处理RB单元中卷积模块的输出.如图1(c)所示,CA作用于特征图时,首先输入维度为××的特征图(为特征图的高度,为特征图的宽度,为特征图的通道数),之后以两种不同的池化形式充分提取通道信息,将各通道表示为最大池化特征和平均池化特征,得到两个大小为1×1×的一维通道描述矢量.其次,将两个一维矢量传入卷积核数分别为/(为通道缩减率)和、卷积核大小为 1×1的两层卷积层,学习各通道的依赖程度,分别生成两个大小为1×1×的通道注意力特征向量.最后将向量对应元素求和,使用Sigmoid激活函数生成数值介于0~1之间的通道注意力权重.将通道注意力权重值逐一加权到原特征通道上,根据依赖程度的不同更新各通道的特征权重,实现自适应特征细化,增强特征的可分辨性,加权图大小与原输入特征图大小保持一致.此外,本文采用基于多头输入的分组卷积[21]提取注意力信息,有效降低计算复杂度并扩大通道注意力范围,学习更为丰富的信息表示.如图1(b)所示,将通道注意力的单输入按通道维度方向进行平均拆分,形成多组并行的4个输入后分别进行CA操作.最后,将处理后的分组特征按照通道维度连接(concatenate).此外,由于分组设计会带来各组间信息孤立问题[22],本文在通道维度连接后引入卷积尺寸为1×1的卷积操作,避免引入过多参数的同时促进组间信息流通与组内信息融合.最后,将分组CA模块嵌入RB中构成RB+CA单元.与RB单元共同作为分组注意力残差网络中的基本单元(图1(b)).因此,RB+CA单元可在网络训练过程中实现对隐含在特征空间不同感知野范围下的锥束XLCT光子密度信息进行综合挖掘,获得各层次下对重建结果具有关键性影响的特征通道并进行优选,从而实现对于锥束XLCT四角度投影测量结果中有效部分的自动注意.

图1 网络结构图及通道注意力模块
如图1(a)所示,分组注意力残差网络主要由3个部分组成.首先将每个成像样本在4个投影角度下所测量的光子密度信息作为网络输入,依次通过残差基本单元RB及RB+CA组合基本单元,由浅至深进行特征提取并捕获关键信息通道.其次,从第2组RB单元开始,由于降维卷积的使用,特征图每经过一组RB单元,图像大小减半,通道数为之前的2倍.最后,在一系列的特征提取后,连接1层用于缓解过拟合的全局池化层和1层用于生成重建仿体内各个节点处磷光分布的全连接层.因本文所用仿体剖分后的节点数为9446个,因此全连接层所连接神经元数量为9446.基于上述对于分组注意力残差网络的描述,本文通过此架构以网络的形式将给定数据集转换为具有一系列网络参数的非线性映射并动态学习映射内各项参数,完成从锥束XLCT测量光子信息中识别及提取有效特征表示并最终实现磷光探针分布重建的过程.
1.2.2 领域知识损失函数
为使得模型在弱信号、高噪声的情况下也能产生良好的重建性能,提高模型的泛化能力及鲁棒性,本文采用领域知识损失函数作为网络训练过程中的损失函数[23],其主要原理为在TensorFlow库中的平滑平均绝对误差(Huber loss)基础上引入近似域约束损失函数,即将结果变量的定量范围(磷光探针的浓度值分布范围)作为自适应领域知识,将其结合到深度前馈神经网络的训练损失函数中,与Huber loss共同作用于网络的权值参数更新过程.领域知识损失函数计算公式为

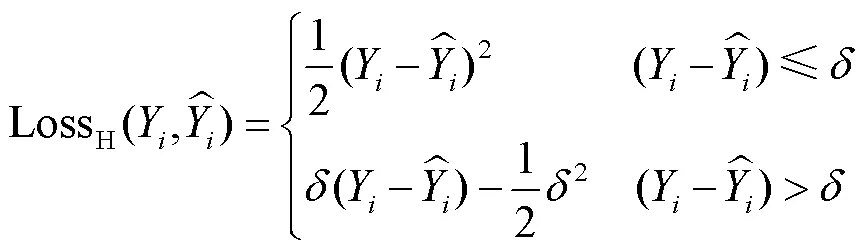
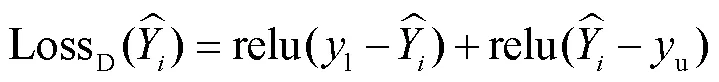
1.2.3 数据准备与网络训练
通过计算机仿真模拟实际实验获取训练及测试数据集.本文采用由南加州大学与UCLA医学院联合开发的标准数字鼠模型[24]制作实验所用仿体,该标准数字鼠横断面的最大直径约为33mm,总长度大约为87.2mm.由于此标准数字鼠的结构较为复杂,因此本文在此基础上对数字鼠模型进行一定的简化处理,即仅研究躯干部分的几个主要器官区域,例如心脏、肺部、肝脏、肾脏等.
如图2所示,本文设计了一个高为30mm、半径为15mm的空心圆柱,并将数字鼠躯干简化部分嵌入圆柱体成像腔内,构建数字鼠躯干仿体.另外,在数字鼠躯干仿体与空心圆柱的缝隙区域,其光学参数被设定为与肌肉组织相同[25-26].采用有限元剖分软件COMSOLTM将模型离散为9446个节点与51594个四面体.随着血液循环,磷光纳米探针通常会在肝脏肿瘤中积聚.因此,在仿真实验中,本文以肝脏区域的200个随机点作为光源中心,构造半径为1.5~2.5mm,高为1mm的圆柱形光源.接下来,将单光源进行两两组合,使得双光源位置中心距离在7~9mm内随机变化.共构建18850组双目标数据集.仿体内光源区域磷光探针浓度随机设置为1~3mg/mL,仿体内非光源区域磷光探针浓度设置为0,根据上述双光源特征进行锥束XLCT前向仿真.其中,仿体内不同器官光学特性参数如表1所示.
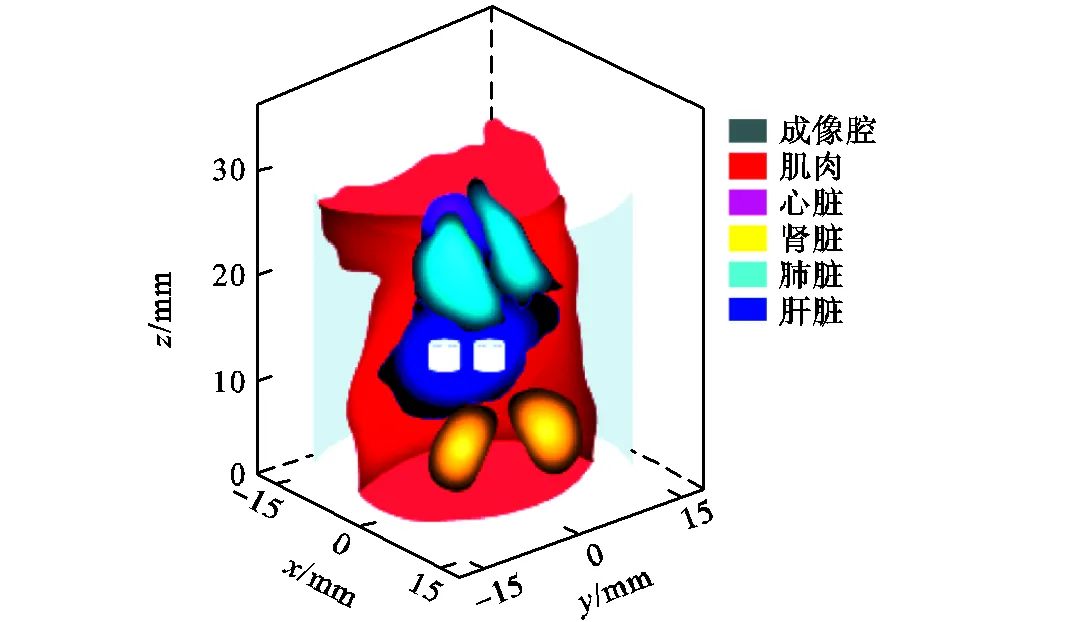
图2 数字鼠仿体
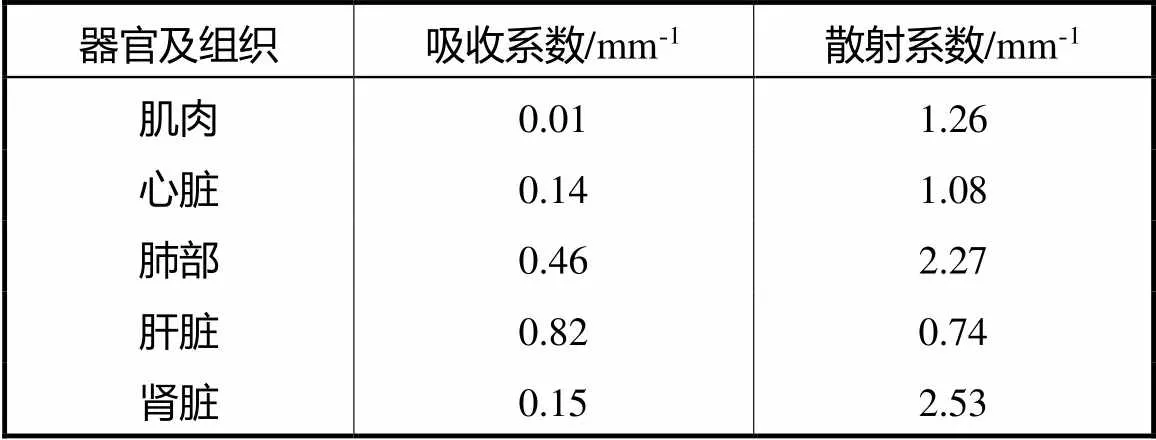
表1 不同器官光学特性参数
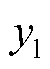
实验硬件平台采用Intel(R)Xeon(R)CPU E5-2650 v4 @2.20GHz处理器,NVIDIA GTX 1070 Ti显卡(可使用CUDA加速模块),深度学习框架采用基于Python的TensorFLow开源框架,Python版本为3.6.2,Tensorflow版本为2.3.0.
2 实验结果与分析
2.1 评价指标
为了对图像重建结果做出客观公正的评价,本文实验采用位置误差(location error,LE)[27]、均方误差(mean square error,MSE)[28]、戴斯相似性指数Dice[29]进行定量分析,计算公式如下.
LE用于评估图像内光源位置准确度.LE值越小,表明重建目标体的几何中心与真实目标体的几何中心差异越小,其表达式为

MSE用于评估图像重建精度.MSE越小,表明重建的图像更接近真实图像.MSE的表达式为


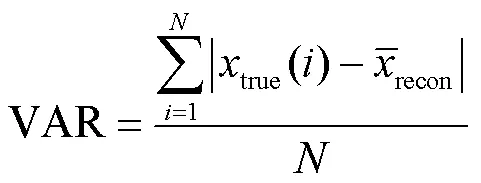
Dice用于衡量重建图像与真实图像的相似度.当Dice为100%时,表示相同的图像.其表达式为
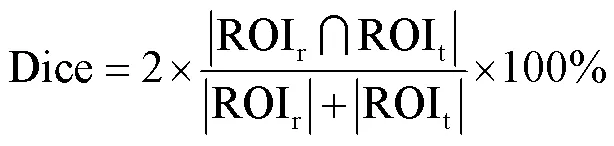
2.2 仿真实验
2.2.1 不同靶心距下重建性能比较
实验将设置7mm和9mm两种靶心距测试不同方法重建精度,两种情况对应的双光源的位置中心坐标分别为(-5mm,0,14.5mm)、(2mm,0,14.5mm)和(-4mm,0,14.5mm)、(5mm,0,14.5mm).双目标体半径均为2.5mm,磷光探针的真实浓度为1mg/mL.图3 ART方法、ISPR-ART方法、Tikhonov方法、ResNet18方法、分组注意力残差方法在=14.5mm切片处重建结果的二维截面图.其中,黑色圆圈代表真实的纳米发光目标所在区域,红色区域代表重建的纳米发光目标,目标体颜色越红,表示重建得到的节点处磷光探针浓度值越高.从图3中可以看出,传统方法中的ART、Tikhonov几乎无法清晰分辨双目标体,重建效果较差.ISPR-ART通过将可行性区域进行迭代收缩,基本上可以重建出目标体的浓度及位置,明显改善了图像重建质量.但在靶心距为7mm时,ISPR-ART出现了一定的目标黏连,即使在靶心距为9mm仍无法有效分离双目标体.
相比3种传统方法,ResNet18及分组注意力残差网络方法对于相邻靶目标的参数恢复准确度有了较大提升,能够明显区分双目标体并重建出其位置及浓度,同时在视觉上保持了一个较好的目标形状.然而,ResNet18模型在靶心距为7mm时出现了一侧目标重建区域明显偏离真实目标区域的情况,很大程度上是由于ResNet18模型仅使用残差单元无法充分聚焦局部关键特征,因此在重建质量方面的性能受限,对于复杂双目标的模型收敛结果不如分组注意力残差网络.
图4为不同靶心距下各方法在=0mm处的浓度曲线.可以看出,无论在何种靶心距时,传统方法中仅ISPR-ART可以基本恢复出双磷光靶体浓度,但在非目标靶体区域的重建浓度与真实浓度误差较大.其次,分组注意力残差网络的预测浓度值明显优于ResNet18网络重建结果,与真实浓度间差异较小.另外,本文提出的方法重建结果始终保持在合理的浓度约束范围之内,充分验证了本文在损失函数中加入近似域约束将重建结果限制在定量范围的有效性,具有更为稳定的重建性能.
由表2可得,传统方法中的ART算法、Tikhonov方法各项指标相对较低.两种深度学习方法与传统方法相比,可以得到较为理想的定量指标结果.在靶心距为7mm和9mm两种情况下,采用分组注意力残差网络方法重建位置误差最小,LE分别为0.37mm和0.30mm,均小于0.38mm,明显优于传统重建方法和ResNet18.这说明分组注意力残差方法可以在保证获得复杂分类特征的同时,提高了细节特征提取能力,同时这也是其他算法无法比拟的优势.
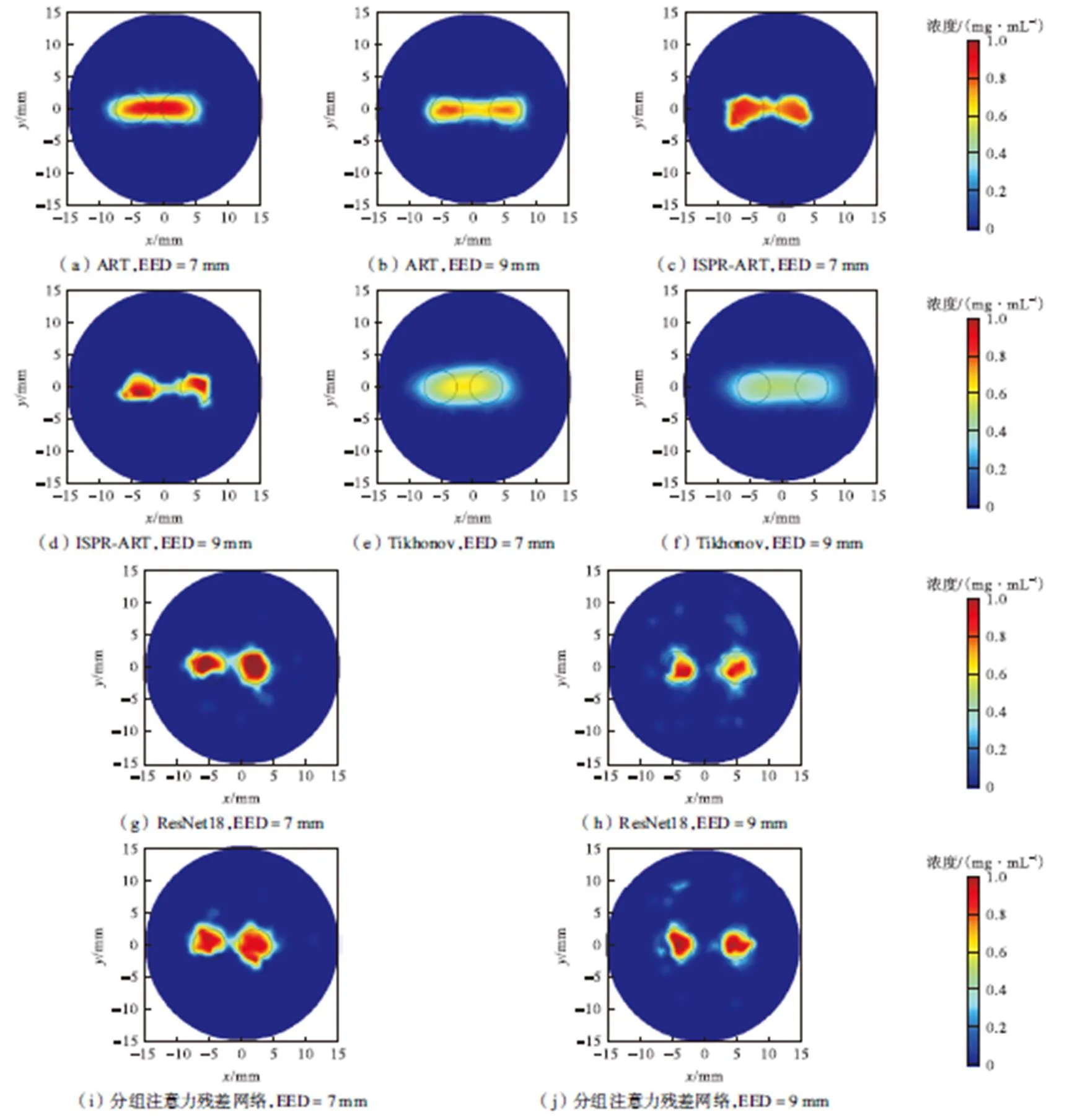
图3 不同靶心距双目标重建结果剖面图(z=14.5mm)
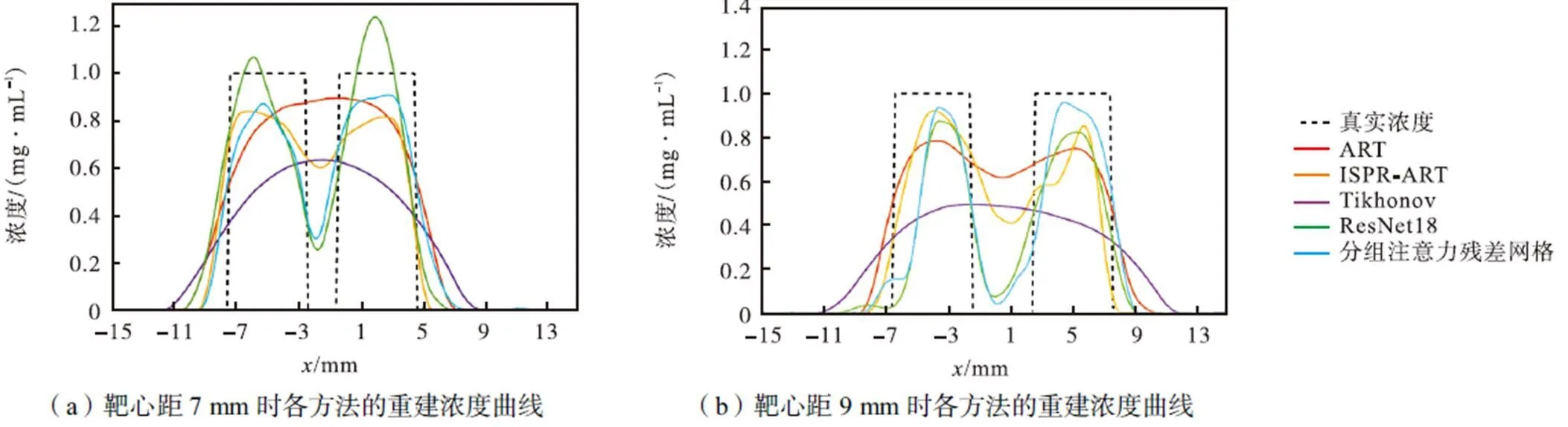
图4 不同靶心距各方法的重建浓度曲线比较
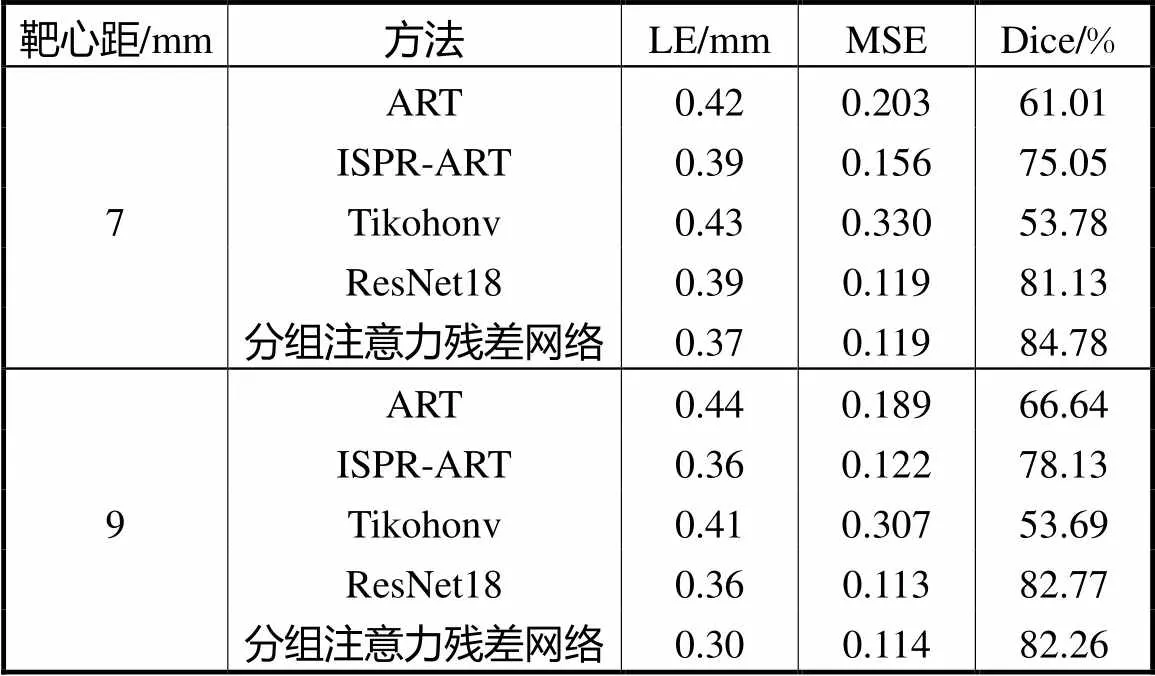
表2 不同靶心距各方法量化重建结果
2.2.2 不同噪声水平下重建性能比较
为评估本文方法在不同信噪比环境下的鲁棒性,本组实验分别在信噪比(SNR)为30dB、40dB、50dB 3种噪声水平下测试,靶心距为9mm,目标体半径从2.5mm缩小至2.0mm,加大重建难度,光源的真实浓度为1mg/mL.双目标的中心坐标分别为(4mm,0,14.5mm)和(5mm,0,14.5mm).图5为不同信噪比下ResNet18及分组注意力残差网络在=14.5mm切片处重建得到的二维截面图,图6为信噪比为30dB时两种深度学习方法的重建浓度曲线比较.结合图5的定量重建结果及图6的各方法重建浓度曲线可以得出:在靶目标尺寸缩小的情况下,ResNet18网络重建结果出现浓度预测值与真实浓度值偏差过大、不能均匀预测左侧和右侧目标体的浓度等结果,磷光浓度分布重建能力较弱;而集成了注意力模块的残差网络,重建目标的大小、浓度分布也更加均匀,对半径为2.0mm的目标依然可以得到清晰的磷光分布图像.

图5 不同信噪比各方法重建结果剖面图(z=14.5mm)
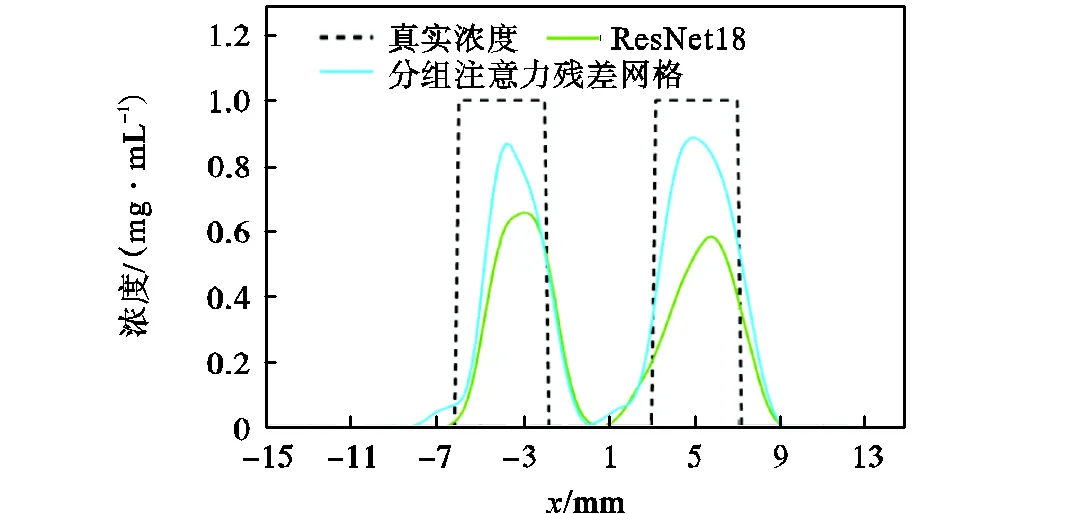
图6 信噪比为30dB时重建浓度曲线比较
表3展示了不同信噪比环境下两种深度学习方法的量化重建结果,可以得出,尽管随着噪声的增加会使得重建问题的病态性加重,但两种深度学习算法的定量重建结果如LE、MSE等仍相对稳定,进一步突出了模型的鲁棒性.其中,分组注意力残差网络的位置误差相比于ResNet18网络下降了约0.04mm,Dice提升了4%左右.由此可见,单一的堆叠残差基本单元并不能较为有效地提升模型性能,在ResNet18主干网络的基础上加入分组注意力模块增强了模型对于目标的感知能力,尤其是小目标体的磷光探针浓度分布恢复上.此外,将此组实验结果与图3中半径为2.5mm的目标重建实验对比也可以得出,目标体尺寸越大,位置定位越准确,浓度恢复程度越高.
仿真实验表明,分组注意力残差方法能够有效分辨距离较近的靶目标.与ResNet18网络重建结果相比,该方法增强了对于小目标的感知能力,可以更为精确地恢复出磷光探针的空间分布,具有更好的指标量化结果.此外,与传统方法相比,该方法在定位精度、空间分辨率、稳健性等多方面显著提高了双目标光源成像质量.

表3 不同噪声水平各方法量化重建结果
2.3 仿体实验
为进一步验证本文方法的有效性和稳健性,本文设计了一种圆柱形聚甲醛仿体(如图7所示),该仿体的直径为20mm,高为40mm,仿体对于近红外光子的吸收系数为0.0072mm-1,散射系数约为0.72mm-1.使用注射器将由1%的脂肪乳、2%的琼脂以及Gd2O2S:Eu3+配置而成的2mg/mL目标溶液置入外径为5mm的试管中,溶液深度为5mm.将试管嵌入仿体内,以仿体底面圆心为坐标原点,双目标仿体中心位置坐标分别为(-4.5mm,0,27.5mm)和(5.5mm,0,27.5mm).成像系统采用锥束XLCT成像系统.X射线源的工作电压为50kV,工作电流为1mA.CCD相机作为光学检测仪器用于测量仿体在0°(初始位置设为0°)、90°、180°、270° 4个投影角度下的表面光子密度信息,用于后续的图像重建.每次扫描CCD相机的曝光时间设置为2s,增益为260.

图7 仿体结构示意
图8为分别采用ART、ISPR-ART、Tikhonov、ResNet18、分组注意力残差网络在=27.5mm处的重建剖面图.图9为仿体实验各方法重建浓度曲线比较,结合二者可以看出,3种传统重建算法在4个投影角度下的重建图像对实验环境中的测量噪声敏感,重建目标边界模糊,无法准确定位目标体位置及恢复目标体浓度,且浓度预测值相较于正确浓度存在较大差距.此外,因仿体实验所用目标体尺寸较大,所以在浓度恢复上两类残差模型都表现出了相对良好的重建精度,但ResNet18出现了双目标重建区域明显超出真实光源区域的情况.
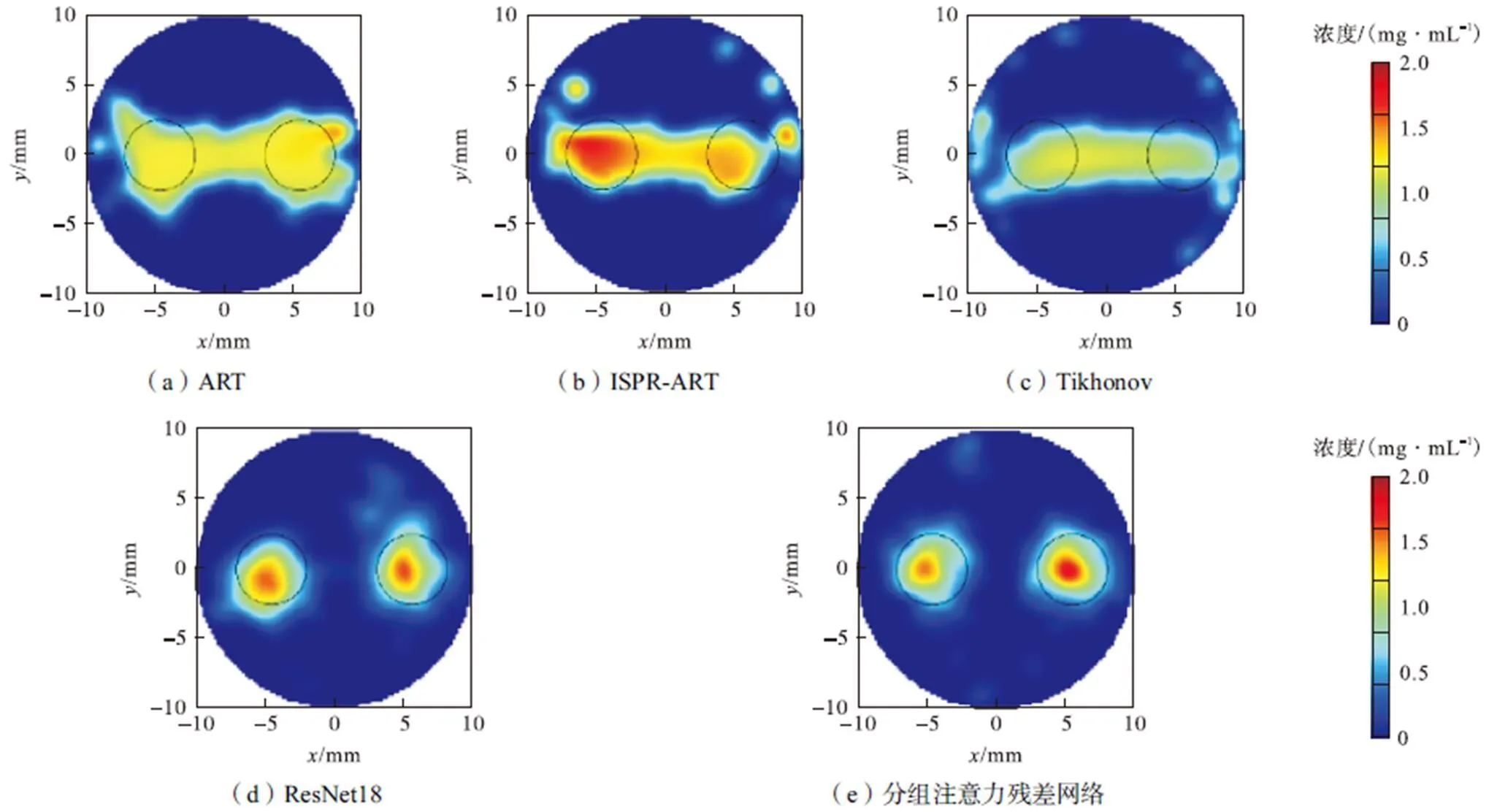
图8 仿体实验各方法重建结果剖面图(z=27.5mm)
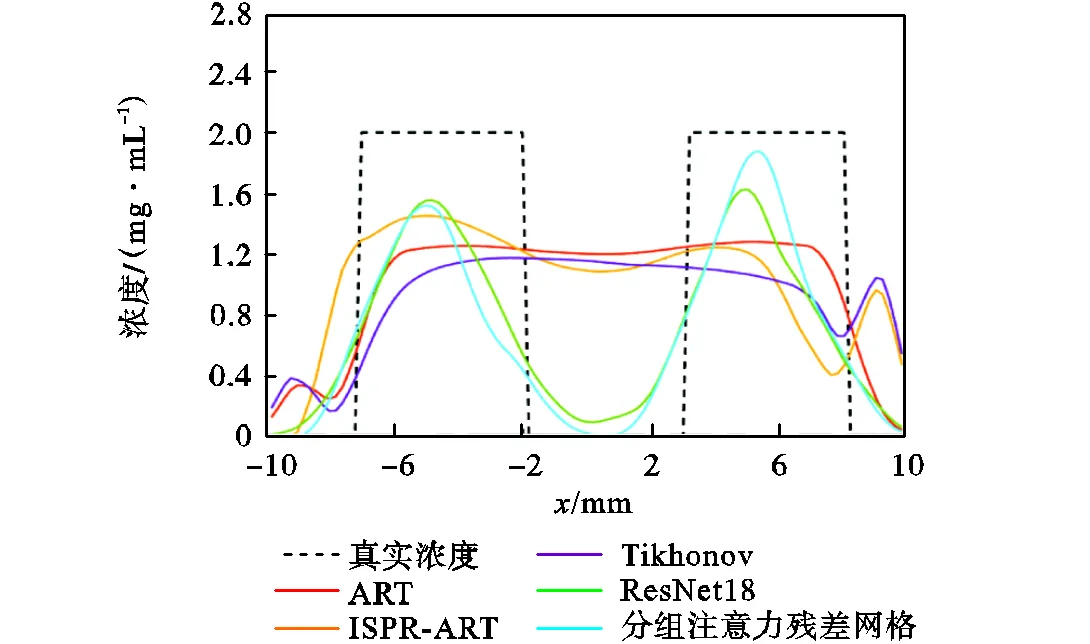
图9 仿体实验各方法重建浓度曲线比较
结合表4可知,相较于ResNet18,分组注意力残差方法重建光源中心更接近光源中心,其LE为0.48mm,明显小于ResNet18的0.52mm.此外,混合了分组注意力机制的残差网络重建信号对比度明显,MSE、Dice等量化指标相比ResNet18均有一定的改善,更好地反映了目标准确收敛的特性.
仿体实验结果表明,相较于其他重建方法,分组注意力残差网络在恢复目标体的中心位置、相似度上具有非常大的优势.面对实际实验中不确定的噪声,LE低至0.48mm且Dice仍能保持在79%的水平以上,验证了本文所提出方法的泛化能力以及稳健性.

表4 仿体实验量化重建结果
3 结 语
本文针对锥束XLCT图像空间分辨率不高、传统模型过度依赖于辐射传输方程的问题,提出了一种基于分组注意力残差网络的重建策略.相较于传统残差网络ResNet18而言,该网络可实现跨通道维度的有效特征识别及关键信息捕捉,作为一种高效的信息增强机制改善学习过程并提升网络表达能力,为解决逆问题提供了一种更为精确的重建方法.结果表明,本文提出的方法在双目标数字鼠仿真实验中,可清晰分辨半径为2.0mm的小目标体,LE均小于0.37mm,Dice可达到82%左右,且在不同噪声水平下重建结果较为稳定.综上所述,本文方法相较于其他方法而言,可以精确、稳健地重建出目标体的形状、大小、位置及浓度,具有优异的图像重建性能.
虽然本文提出的重建方法在一定程度上提高了锥束XLCT的图像质量.但是,新的方法也面临着新的挑战.在未来将关注以下挑战:首先,在网络的架构设计方面.现阶段网络可实现双目标光源重建任务,考虑到未来临床研究中肿瘤等病变部位数量及位置的不确定性、测量误差及环境干扰等问题.因此从实际应用角度出发,未来将基于分组注意力残差方法设计锥束XLCT多目标成像方案,进一步证明本文方法的有效性.同时,对于复杂目标的重建研究也将有助于探索精细化的模型体系及加速收敛的优化技巧,提高解决重建任务的能力.另外,在数据集的构建方法上.现阶段数据集无法穷尽所有目标状态,即不同的成像对象需要根据相应的轮廓建立不同的训练数据集,但真实人体内病变目标具有不同的大小和形状,较难获得足够数量的病灶数据,且仿真数据与实验数据之间差异不可忽略.未来将采用从具有已知光学特性的病灶几何形状创建训练数据对,真实数据用于评估的数据集构建策略,缩小仿真数据和实验数据之间的差异性.最后,基于锥束XLCT成像在提高肿瘤检测精度方面的临床应用价值.未来将基于本文方法开展大量生物分布成像研究如小鼠原位胶质瘤实验.通过在体实验发现问题、解决问题,推动锥束XLCT在肿瘤早期检测中的发展.
[1] Bradley W G. History of medical imaging[J]. Proceed-ings of the American Philosophical Society,2008,152(3):349-361.
[2] Ginat D T,Gupta R. Advances in computed tomography imaging technology[J]. Annual Review of Biomedical Engineering,2014,16(1):431-453.
[3] Jaffer F A. Molecular imaging in the clinical arena[J]. JAMA,2005,293(7):855-862.
[4] Pratx G,Carpenter C M,Sun C,et al. Tomographic molecular imaging of X-ray-excitable nanoparticles[J]. Optics Letters,2010,35(20):3345-3347.
[5] 束月霞,赵丽丽,蒋皆恢,等. X射线发光光学断层成像的研究进展[J]. 科学通报,2017,62(33):3838-3850.
Shu Yuexia,Zhao Lili,Jiang Jiehui,et al. Research progress of X-ray luminescence optical tomography[J]. Science Bulletin,2017,62(33):3838-3850(in Chi-nese).
[6] Chen D,Zhu S,Yi H,et al. Cone beam X-ray lumi-nescence computed tomography:A feasibility study[J]. Medical Physics,2013,40(3):031111.
[7] Zhao J,Guo H,Yu J,et al. A robust elastic net-l112 reconstruction method for X-ray luminescence computed tomography[J]. Physics in Medicine and Biology,2021,66(19):195005.
[8] Arridge S R,Schotland J C. Optical tomography:Forward and inverse problems[J]. Inverse Problems,2009,25(12):1541-1548.
[9] Lucas A,Iliadis M,Molina R,et al. Using deep neural networks for inverse problems in imaging:Beyond ana-lytical methods[J]. IEEE Signal Processing Magazine,2018,35(1):20-36.
[10] Gao Y,Wang K,An Y,et al. Nonmodel-based bioluminescence tomography using a machine-learning reconstruction strategy[J]. Optica,2018,5(11):1451-1454.
[11] Lun M C,Cong W,Arifuzzaman M,et al. Focused X-ray luminescence imaging system for small animals based on a rotary gantry[J]. Journal of Biomedical Op-tics,2021,26(3):036004.
[12] 王正坤,王 鹏,徐昊昊. CT系统成像原理[J]. 信息记录材料,2018,19(2):86-88.
Wang Zhengkun,Wang Peng,Xu Haohao. Imaging principle of CT system[J]. Information Recording Mate-rials,2018,19(2):86-88(in Chinese).
[13] 徐可欣,高 峰,赵会娟. 生物医学光子学[M]. 北京:科学出版社,2011.
Xu Kexin,Gao Feng,Zhao Huijuan. Biomedical Photonics[M]. Beijing:Science Press,2011(in Chi-nese).
[14] Klose A D,Larsen E W. Light transport in biological tissue based on the simplified spherical harmonics equa-tions[J]. Journal of Computational Physics,2006,220(1):441-470.
[15] Zhang Y,Lun M C,Li C,et al. Method for improving the spatial resolution of narrow X-ray beam based X-ray luminescence computed tomography imaging[J]. Journal of Biomedical Optics,2019,24(8):1-11.
[16] 董 芳,侯榆青,余景景,等. 结合区域收缩和贪婪策略的荧光分子断层成像[J]. 激光与光电子学进展,2016,53(1):175-181.
Dong Fang,Hou Yuqing,Yu Jingjing,et al. Fluores-cence molecular tomography combined with region con-traction and greedy strategy[J]. Progress in Laser and Optoelectronics,2016,53(1):175-181(in Chinese).
[17] Zhang G,Liu F,Liu J,et al. Cone beam X-ray lumi-nescence computed tomography based on Bayesian method[J]. IEEE Transactions on Medical Imaging,2017,36(1):225-235.
[18] He K,Zhang X,Ren S,et al. Deep residual learning for image recognition[C]// 2016 IEEE Conference on Computer Vision and Pattern Recognition(CVPR). Las Vegas,USA,2016:770-778.
[19] He K,Zhang X,Ren S,et al. Identity mappings in deep residual networks[C]// European Conference on Computer Vision. Amsterdam,the Netherlands,2016:630-645.
[20] Woo S,Park J,Lee J Y,et al. CBAM:Convolutional block attention module[C]// European Conference on Computer Vision,Glasgow. Munich,Germany,2018:3-19.
[21] Krizhevsky A,Sutskever I,Hinton G. ImageNet classi-fication with deep convolutional neural networks[J]. Communications of the ACM,2017,60(6):84-90.
[22] Zhang T,Qi G,Xiao B,et al. Interleaved group con-volutions for deep neural networks[C]// International Conference on Computer Vision. Venice,Italy,2017:4373-4382.
[23] Muralidhar N,Islam M R,Marwah M,et al. Incorporating prior domain knowledge into deep neural networks[C]// 2018 IEEE International Conference on Big Data. Seattle,USA,2018:36-45.
[24] Dogdas B,Stout D,Chatziioannou A F,et al. Digimouse:A 3D whole body mouse atlas from CT and cryosection data[J]. Physics in Medicine and Biology,2007,52(3):577-587.
[25] Liu X,Liao Q,Wang H. Fast X-ray luminescence com-puted tomography imaging[J]. IEEE Transactions on Bio-medical Engineering,2014,61(6):1621-1627.
[26] 侯榆青,贾 涛,易黄建,等. 基于改进谱投影梯度算法的X射线发光断层成像[J]. 光学精密工程,2017,25(1):42-49.
Hou Yuqing,Jia Tao,Yi Huangjian,et al. X-ray lumi-nescence tomography based on improved spectral projection gradient algorithm[J]. Optical Precision Engineer-ing,2017,25(1):42-49(in Chinese).
[27] Gao P,Rong J,Pu H,et al. Sparse view cone beam X-ray luminescence tomography based on truncated singular value decomposition[J]. Optics Express,2018,26(18):23233-23250.
[28] Feng J,Sun Q,Li Z,et al. Back-propagation neural network based reconstruction algorithm for diffuse optical tomography[J]. Journal of Biomedical Optics,2018,24(5):1-12.
[29] Zhang W,Zhu D,Lun M,et al. Multiple pinhole collimator based X-ray luminescence computed tomography[J]. Biomedical Optics Express,2016,7(7):2506.
A Group Attention Residual Network for Image Reconstruction in Cone-Beam XLCT
Zhou Zhongxing1, 2,Guo Siqi1, 2,Jia Mengyu1, 2,Zhang Lin2,Wu Yue2
(1. School of Precision Instruments and Optoelectronics Engineering,Tianjin 300072,China;2. Tianjin Key Laboratory of Biomedical Detection Technology and Instrument,Tianjin 300072,China)
Cone-beam X-ray luminescence computed tomography(CB-XLCT)is an emerging hybrid imaging modality that can simultaneously obtain both anatomical structure information and functional metabolism information,providing good prospects for the early diagnosis and targeted treatment of diseases. However,CB-XLCT generally suffers from high ill-posedness during image reconstruction,severely deteriorating the spatial resolution. To solve this problem,a quantitative phosphorescence distribution reconstruction method for CB-XLCT based on a group attention residual network is proposed. In this method,the attention module is used to optimize the weight of each photon density feature channel,which is combined with the approximate domain constraint loss function to improve the feature expression process and enhance the reconstruction accuracy and model robustness. Results show that the proposed method can clearly distinguish and reconstruct two targets with the target center distance of 7mm,yielding approximately 0.37mm location error(LE)and 84% Dice similarity index in the simulation experiment. In the phantom experiment,the LE is approximately 0.48mm,and the Dice reaches 79%. Therefore,the group attention residual network method can effectively improve the quality of image reconstruction in LE,spatial resolution,and robustness.
cone-beam X-ray luminescence computed tomography(CB-XLCT);deep learning;group attention;image reconstruction
TK448.21
A
0493-2137(2022)10-1082-11
10.11784/tdxbz202108051
2021-08-21;
2021-12-23.
周仲兴(1979— ),男,博士,副教授.
周仲兴,zhouzhongxing@tju.edu.cn.
国家自然科学基金资助项目(81971656,62175183);天津市自然科学基金资助项目(19JCYBJC28600).
the National Natural Science Foundation of China(No. 81971656,No. 62175183),the Natural Science Foundation of Tianjin,China(No. 19JCYBJC28600).
(责任编辑:孙立华)
