血清D-D、VEGF 水平与多囊卵巢综合征不孕女性IVF-ET 后妊娠丢失的相关性
2022-06-30王婧彦王宁波于晓娜
王婧彦,王宁波,于晓娜
(郑州大学第三附属医院生殖医学科,河南 郑州 450003)
作为重要的辅助生殖技术,体外受精-胚胎移植(In vitro fertilization-embryo transfer,IVF-ET)可满足多囊卵巢综合征 (Polycystic ovary syndrome,PCOS)不孕症女性一线治疗失败后妊娠的愿望,广泛应用于临床不孕症的治疗中[1]。 但王海燕等[2]研究发现, 不孕症患者IVF-ET 后受性激素水平、促性腺激素用量等因素影响,妊娠丢失风险较高。 因此寻找与PCOS 不孕症患者IVF-ET 后妊娠丢失有关的指标,可为预测妊娠丢失提供客观依据,并可为预防IVF-ET 后妊娠丢失提供新的治疗靶点。D-二聚体(D-Dimer,D-D)为交联纤维蛋白降解产物,为机体高凝状态的特异性标志物,而高凝状态可引起蜕膜与绒毛血管微血栓形成, 进而影响胎盘功能[3]。 血管内皮生长因子(Vascular endothelial growth factor,VEGF)是细胞产生的信号蛋白,不仅能刺激血管内皮细胞增殖,也可诱发钙离子内流,刺激内皮细胞磷脂C 活性,进而促进血管形成、维持血管功能,对胎盘功能具有保护作用[4]。 结合DD、VEGF 对胎盘功能的作用机制,推测二者可能与PCOS 不孕症患者IVF-ET 后妊娠丢失有关。 鉴于此, 本研究就血清D-D、VEGF 水平与PCOS 不孕症患者IVF-ET 后妊娠丢失的关系作以下分析。
1 对象与方法
1.1 研究对象 回顾性分析2018年10月至2020年8月郑州大学第三附属医院接受IVF-ET 后发生妊娠丢失的62 例PCOS 不孕症患者资料, 并将其纳入丢失组;将同期医院接受IVF-ET 后未发生妊娠丢失的62 例PCOS 不孕症患者资料, 纳入未丢失组。 纳入标准:(1)PCOS 及不孕症均符合《多囊卵巢综合征中国诊疗指南》[5]中相关诊断;(2)全部患者均接受IVF-ET,且妊娠2 周时测定血人绒毛膜促性腺激素 (Human chorionic gonadotropin,HCG)提示生化妊娠;(3)病历资料完整。 排除标准:(1)男方或女方存在染色体异常;(2)存在凝血功能异常;(3)合并甲状腺功能减退或亢进;(4)合并子宫畸形、子宫肌瘤、输卵管积水等其他妇科疾病;(5)合并慢性消耗性疾病或严重感染;(6)合并自身免疫性疾病;(7)患者有吸烟、大量饮酒、药物依赖等不良嗜好。 两组基线资料比较差异无统计学意义(P>0.05),有可比性。 见表1。
1.2 研究方法
1.2.1 基线资料收集 查阅患者病历资料, 详细记录患者年龄、母亲PCOS 史(有、无)、妊娠前体重指数(Body Mass Index,BMI)、不 孕年 限、周 期 类 型(冻胚移植、鲜胚移植)、移植胚胎发育时间(卵裂胚:取卵后第3 天胚胎;囊胚:取卵后第5~6 天胚胎)、移植日子宫内膜厚度(经超声检查测定)。
1.2.2 实验室指标检测 全部患者于移植前(移植日)采集空腹静脉血5 mL,离心分离15 min,半径10 cm,转速4000 r/min:(1)性激素水平:使用全自动化学发光免疫分析系统(瑞士罗氏,型号:Cobas 8000)测 定 患 者 血 清 睾 酮(Testosterone,T)、孕 酮(Progesterone,P)、黄体生成素(Luteinizing hormone,LH)、雌二醇(Estradiol,E2)、卵泡刺激素(Follicle stimulating hormone,FSH)、催乳素(Prolactin,PRL)水平;(2)胰岛素抵抗(Insulin resistance,IR):用化学发光法测定空腹胰岛素 (试剂盒购自深圳市亚辉龙生物科技),用葡萄糖氧化酶法测定空腹血糖(试剂盒购自上海博湖生物科技), 计算胰岛素抵抗指数(Homeostasis model assessment-IR,HOMAIR)=空腹胰岛素×空腹血糖/22.5;(3)D-D、VEGF:采用酶联免疫吸附法测定血清D-D、VEGF 水平,试剂盒购自武汉菲恩生物。
1.3 妊娠丢失判定 依据欧洲人类生殖和胚胎学协会[6]制定的标准:移植胚胎后2~3 周行超声检查未见孕囊,且HCG 呈阴性;或妊娠28 周前因胎儿异常人工终止妊娠及自然流产者。
1.4 统计学方法 用SPSS 25.0 统计学软件处理数据, 用Shapiro-Wilk 正态分布检验计量资料正态性,±s 表示符合正态分布计量资料, 组间比较行独立样本t 检验;偏态分布计量资料用[M(P25,P75)]表示,组间比较用Mann-Whitney U 检验;n(%)表示计数资料,用χ2检验;用logistic 回归分析检验各因素对PCOS 不孕症患者IVF-ET 后妊娠丢失的影响;用GraphPad Prism 8.0 软件绘制各因素影响PCOS 不孕症患者IVF-ET 后妊娠丢失的森林图;绘制ROC 曲线,并计算曲线下面积(AUC),分析D-D、VEGF 水平对PCOS 不孕症患者IVF-ET后妊娠丢失的预测价值,AUC<0.5 无价值,0.5≤AUC <0.7 价 值 较 低,0.7 <AUC ≤0.9 价 值 中 等,AUC>0.9 价值高;P<0.05 为差异有统计学意义。
2 结果
2.1 基线资料、实验室指标比较 丢失组患者移植前LH、FSH、VEGF 水平低于未丢失组,HOMA-IR、D-D 水平高于未丢失组,差异有统计学意义(P<0.05);组间其他资料比较差异无统计学意义(P>0.05)。见表1。
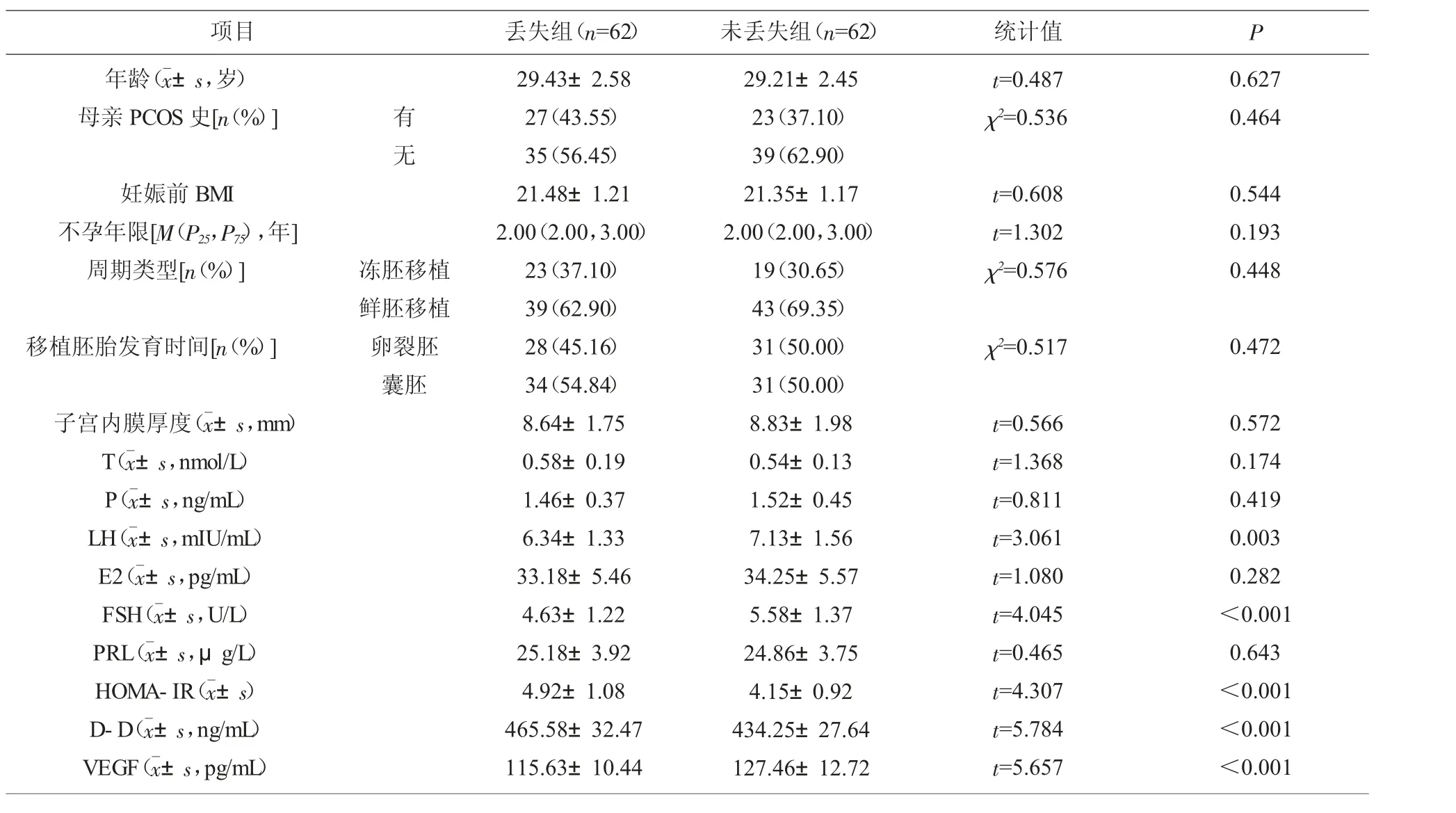
表1 基线资料、实验室指标比较
2.2 各因素影响PCOS 不孕症患者IVF-ET 后妊娠丢失的回归分析 将POCS 不孕症患者IVF-ET后妊娠丢失作为因变量(1=妊娠丢失,0=未妊娠丢失), 将结果2.1 中差异有统计学意义的变量纳入作为自变量(均为连续变量),经单项logistics 回归分析后,P<0.1,为符合条件的因素,行多项logistics回归分析结果显示, 移植前血清LH、FSH、VEGF水平高是PCOS 不孕症患者IVF-ET 后妊娠丢失的保护因素(OR<1,P<0.05),HOMA-IR、D-D 水平高是其危险因素(OR>1,P<0.05)。 见表2、见图1。

表2 各因素影响PCOS 不孕症患者IVF-ET 后妊娠丢失的回归分析

图1 各因素影响PCOS 不孕症患者IVF-ET 后妊娠丢失的森林图
2.3 血清D-D、VEGF 对PCOS 不孕症患者IVFET 后妊娠丢失的预测价值 将PCOS 不孕症患者IVF-ET 后妊娠丢失作为状态变量 (1=妊娠丢失,0=未妊娠丢失),将D-D、VEGF 及联合检测作为检验变量,绘制ROC 曲线,见图2。结果显示,D-D、VEGF 及二者联合预测PCOS 不孕症患者IVF-ET后妊娠丢失的AUC>0.7,具有一定的预测价值,见表3。

表3 血清D-D、VEGF 对PCOS 不孕症患者IVF-ET 后妊娠丢失的预测价值
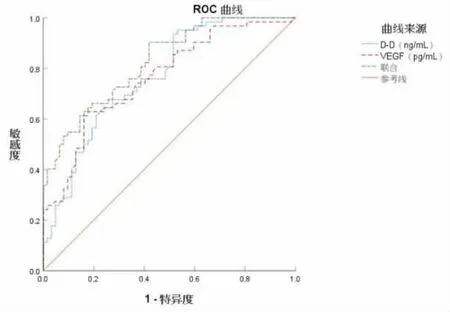
图2 血清D-D、VEGF 预测PCOS 不孕症患者IVF-ET 后妊娠丢失的ROC 曲线
3 讨论
妊娠丢失是PCOS 不孕症患者IVF-ET 后常见并发症,包括早期流产、因胎儿异常人工流产及胎死宫内等,不仅会影响患者妊娠结局,也会增加患者心理、经济负担,不利于患者身心健康[7]。 杨霞等[8]研究表明,IVF-ET 后妊娠丢失发生风险可达33.21%,且可能与患者年龄、既往流产史等因素有关。 因此寻找与PCOS 不孕症患者IVF-ET 后妊娠丢失有关的指标,并采取相应的预防措施,对改善患者妊娠结局尤为重要。
LH 为糖蛋白类促性腺激素, 对卵泡成熟、黄体生成均有促进作用,而LH 水平偏低易影响卵泡成熟度,进而影响精卵结合,导致妊娠丢失的发生[9]。 FSH 为垂体分泌的糖蛋白激素,其水平降低可影响优质卵泡的形成, 进而增加妊娠丢失风险[10]。HOMA-IR 是反映机体胰岛素抵抗程度的指标,而胰岛素抵抗水平越高, 越易影响纤溶酶原激活物抑制剂活性,进而促进胎盘血栓形成,引起妊娠丢失[11]。 目前临床多采用激素补充治疗联合IVFET 改善患者妊娠结局, 但LH、FSH 水平受PCOS不孕症患者年龄、检测时间等因素影响,而胰岛素抵抗与多种代谢疾病有关,在预测PCOS 不孕症患者IVF-ET 后妊娠丢失的临床应用中存在一定局限。
D-D 是凝血酶作用于纤维蛋白原, 引起纤溶系统激活后,由r 链将2 个D 片段接连而形成的,是反映机体纤溶活性的指标,研究指出,机体高凝状态易增加胎儿生长受限、 剖宫产等不良妊娠结局[12]。 VEGF 是血管形成的关键,可通过结合血管内皮细胞表面特异性受体,发挥效应,已被证实与胎盘组织低氧、缺血等改变密切相关[13]。 而胎盘血管、功能可影响母胎之间的营养、血液交换,胎盘血管损伤、功能障碍会造成胎儿发育不良,影响妊娠结局[14]。 结合D-D、VEGF 的作用机制,推测二者可能与PCOS 不孕症患者IVF-ET 妊娠丢失有关。 本研究发现,PCOS 不孕症患者IVF-ET 后妊娠丢失受移植前血清D-D、VEGF 水平的影响。 分析原因在于,D-D 水平升高提示机体凝血功能增强,可导致纤维蛋白原在子宫局部组织沉积, 促使绒毛血管、 蜕膜血管微血栓形成, 进而导致胎盘功能障碍。 而胎盘功能障碍会影响胚胎获取氧气与营养物质,导致胎胚停止发育、胎盘早剥等风险,引起妊娠丢失的发生[15]。D-D 水平升高也会对血管内皮细胞造成损伤,促使血小板大量活化、聚集,引起组织缺氧、脂肪代谢亢进,进而影响胚胎发育,增加妊娠丢失风险[16]。 尤其在临床妊娠受精后第6~7 d 着床时期, 子宫内膜短时间内可允许胚胎植入,若此时D-D 水平升高,易形成局部梗死灶,增加早期流产风险[17]。 VEGF 水平升高可增加微血管通透性,促进胎盘内皮细胞内葡萄糖转运,为毛细血管芽延伸提供基础, 进而为胎儿的生长发育提供营养供给,有利于降低妊娠丢失风险[18]。 Xie H等[19]研究表明,VEGF 可增加胞质内钙离子浓度,调节体内鸟苷酸环化酶、腺苷酸环化酶等代谢,进而增加胎盘组织血流量, 保证胚胎发育过程中充足的血流供应,进而减少妊娠丢失的发生。
最后本研究经绘制ROC 曲线, 结果显示,DD、VEGF 及二者联合预测PCOS 不孕症患者IVFET 后妊娠丢失的AUC>0.7,具有一定的预测价值;且当各指标cut-off 值分别取448.750 ng/mL、120.350 pg/mL 时,可获得最佳预测价值。这进一步说明血清D-D、VEGF 水平与PCOS 不孕症患者IVF-ET 后妊娠丢失密切相关。因此临床应在IVFET 前检测PCOS 不孕症患者血清D-D、VEGF 水平。针对D-D、VEGF 水平异常的患者,应尽早采取相应的治疗措施,如低分子肝素、戊聚糖钠、香豆素类等抗凝治疗, 或可联合中药制剂改善患者DD、VEGF 水平,但使用抗凝药物时应注意抗凝药物的使用剂量,避免药物过量引起PCOS 不孕症患者临床妊娠后发生自发性出血。
综上所述,PCOS 不孕症患者IVF-ET 后妊娠丢失可能与移植前血清D-D、VEGF 水平有关,临床应早期对二者水平进行测定, 并采取有效的治疗措施, 改善患者D-D、VEGF 水平, 有利于减少IVF-ET 后妊娠丢失的发生。 本研究也存在一定局限性,如仅纳入了PCOS 不孕症患者,未对其他类型、病因的不孕症进行分析,且本研究为回顾性的单中心研究, 纳入的患者均为符合入选标准的对象,未将同期所有患者进行研究,可能会导致研究结果产生一定偏倚, 未来仍需要进行前瞻性队列研究及大样本量研究。
