心脏瓣膜置换术后肺部感染的因素分析及预防护理对策
2022-06-29王永莉吴丽娜
王永莉,宁 园,吴丽娜
心脏瓣膜属于人体心脏重要组成结构,其出现功能或者解剖改变时会损害心脏功能,引发心脏疾病,最高发的是风湿热引起的瓣膜损害,近些年人口老龄化趋势的加重,导致老年退行性瓣膜疾病发生率提高[1]。目前心脏瓣膜置换术是治疗心脏瓣膜病的主要方式,手术过程中需要建立体外循环,加上手术影响,会损害到膈肌、胸壁、气道等结构,漫长的手术、过多的侵入性操作以及植入人工瓣膜,使术后感染风险增加[2],其中并发肺部感染的概率可达到15%左右[3]。肺部感染的出现首先增加医疗费用并延长治疗时间,其次对手术效果带来影响,最后影响术后恢复,因此积极防治术后肺部感染非常重要。本研究旨在分析心脏瓣膜置换术后肺部感染的危险因素,制定对应的预防护理对策。现报告如下。
1 资料与方法
1.1 一般资料 选择2017年8月—2021年7月在本院接受心脏瓣膜置换术的190例病人为研究对象。纳入标准:①符合《瓣膜性心脏病》(2012年版)疾病诊断标准[4];②存在心脏瓣膜置换术适应证;③临床各项检查资料完整,病史清晰;④无其他严重内外科疾病。排除标准:①年龄80岁以上;②最近1个月患有全身感染性疾病或者肺部感染疾病;③合并精神疾病、老年痴呆。190例病人术中采取全身麻醉下气管插管,手术中进行低温体外循环。190例病人中男100例,女90例;年龄18~71(42.63±10.15)岁;心功能分级Ⅱ级78例,Ⅲ级89例,Ⅳ级23例;疾病类型:风湿性心脏病156例,先天性心脏病31例,心脏退行性病变3例。
1.2 研究方法 采取回顾性研究法,收集、整理并统计分析190例病人的临床资料,成立课题组,由课题组专家制定心脏瓣膜置换术病人治疗调查表,选择3名具有5年工作经验的护士,开展培训工作,2名负责收集病人资料,包括性别(男、女)、年龄(18~50岁、>50岁)、吸烟(是、否)、合并基础疾病(是、否)、气管切开(是、否)、留置胃管(是、否)、再次插管(是、否)、二次开胸止血(是、否)、反复吸痰(是、否)、呼吸机使用时间(>10 h、≤10 h)。
1.3 观察指标 评估病人术后肺部感染情况,肺部感染诊断标准参考《临床肺部感染病学》[5]:①肺部叩诊显示浊音(或听诊闻及干湿啰音);②肺部X线检查显示进行性浸润,或者有新浸润,出现空洞和胸腔积液。满足上述2个条件的同时,符合下列2个标准之一:①呼吸道分泌物或血液培养出致病菌,连续3 d培养出同种菌株算阳性;②痰液特性改变,或有新浓痰出现。
统计190例病人中术后肺部感染的例数和未感染例数。针对已发生肺部感染的病例实施细菌鉴定,即术后关注病人呼吸道体征症状,出现湿啰音、发热、咳痰以及咳嗽表现,温水漱口,反复深呼吸,将气管深处痰液用力咳出,取标本置于无菌培养瓶中,0.5 h内送检。检验过程:标本接种在巧克力平板中,保存在37 ℃、5%二氧化碳(CO2)的培养箱中,共48 h,再利用全自动细菌鉴定仪鉴定分离病原菌。
采取单因素、多因素Logistic回归分析法,分析心脏瓣膜置换术后肺部感染的危险因素。

2 结果
2.1 单因素分析 单因素分析结果显示:合并基础疾病、留置胃管、反复吸痰、呼吸机使用时间>10 h是心脏瓣膜置换术后肺部感染的危险因素(P<0.05)。

表1 心脏瓣膜置换术后肺部感染影响因素的单因素分析 单位:例
2.2 多因素Logistic回归分析 将单因素分析中差异有统计学意义的变量纳入Logistic中进行多因素回归分析。多因素分析结果显示,合并基础疾病、留置胃管、反复吸痰、呼吸机使用时间>10 h是心脏瓣膜置换术后肺部感染的危险因素(P<0.05)。见表2、表3。

表2 变量赋值情况
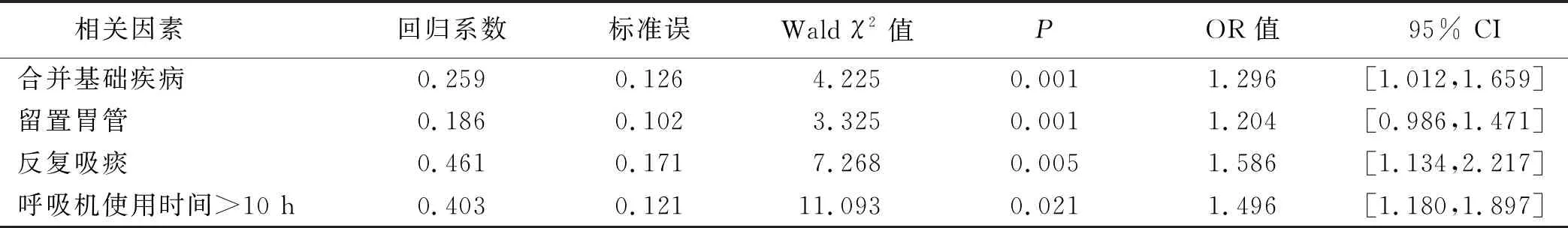
表3 心脏瓣膜置换术后肺部感染影响因素的多因素Logistic回归分析
3 讨论
心脏瓣膜置换术属于心胸外科比较常见的一种大型手术,这类手术术后的并发症比较多,如肺不张、肺炎、肺部感染等,其中肺部感染发生率较高,原因在于疾病本身以及手术破坏了呼吸系统免疫、防御机制,引发感染[6-9]。本研究190例心脏瓣膜置换术病人术后发生肺部感染70例,一旦确诊后需要查明病原菌,再采取针对性的抗菌治疗。
肺部感染会严重影响术后恢复,延长住院时间,需要积极预防,在制定预防措施前需要先了解引起术后肺部感染的原因。本研究结果显示,合并基础疾病、留置胃管、反复吸痰、呼吸机使用时间>10 h是心脏瓣膜置换术后肺部感染的危险因素。①合并基础疾病。高血压、糖尿病、慢性支气管炎等是心脏瓣膜置换术病人比较常见的合并症[10-11]。研究显示,合并基础疾病的病人与未合并基础疾病的病人相比,肺部感染率高出30倍左右[12],原因在于基础疾病的存在会损害宿主防御功能,加上术后病人需要在重症监护室(ICU)接受一段时间的治疗,与普通病房相比,感染风险进一步增加,此外耐药菌耐药程度明显[13]。②留置胃管。留置胃管时间过长会导致胃内细菌逆行转移到口咽部,并完成定植,随后进入下呼吸道,引发肺部感染。③反复吸痰。反复多次的吸痰操作对呼吸系统的纤毛、黏膜系统造成巨大损伤,感染风险随之增加。④呼吸机使用时间>10 h。呼吸机的管路中存在的细菌,会随着喷射形成的气溶胶或者污染的冷凝水进入到病人气道中[14],引发感染。另有研究表示,病人年龄越大,感染风险越高,人工气道的建立也会增加感染风险[15]。总之,心脏瓣膜置换术病人术后肺部感染的危险因素较多,积极预防才是关键。
心脏瓣膜置换术后肺部感染的预防护理对策总结如下。①做好术前准备工作:针对基础疾病开展积极的对症治疗干预,使病人自身免疫力在术前尽量提高,同时普及疾病相关知识,教会病人有效咳嗽、排痰。②规范使用呼吸机:使用呼吸机期间注意病人动脉血气变化,结合检测结果,调整呼吸机参数,满足病人实际需求,预防低氧血症[16],缩短呼吸机使用时间。③人工气道管理:做好气道湿化工作,在恰当的吸痰时机吸痰,呼吸机管路正常情况下更换频率是每周1次,雾化器、湿化罐中的灭菌注射用水,满24 h要立即更换,并清洗消毒灭菌[17-19]。病情允许的前提下取半卧位,促进肺膨胀,预防胃内容物反流,定时帮助病人翻身叩背,坚持胸部体疗,促进痰液排出。④口腔护理:结合病情选择口腔护理液,行气管插管的病人,需要双人完成口腔冲洗工作,将气囊充足,头部偏向一侧,寸带松开,其中一人一手扶住插管,一手冲洗,另外一人进行低位吸引操作[20-23],相互配合。⑤无菌操作:严格控制探视人数与时间,探视人员需要做好防护,遵守探视制度,60岁以上的老年人,做好重点保护,强化基础营养支持,室内温湿度适宜,减少侵入性操作[24-27]。
总之,导致心脏瓣膜置换术病人术后发生肺部感染的危险因素主要包括较多的基础疾病、留置胃管操作、反复吸痰操作、长时间使用呼吸机,针对性做好预防护理措施可预防肺部感染发生,改善病人预后。
