肢端肥大症性心肌病伴垂体瘤的多学科团队协作诊治一例
2022-06-22徐怡琼包程蓉裘佳培卫永旭郑思畅
钱 扬 徐怡琼 包程蓉 裘佳培 卫永旭 郑思畅 庄 蕾 罗 艳
1 临床资料患者男,52岁,因“活动后胸闷1月余”于2019年11月20日收治于上海交通大学医学院附属瑞金医院(简称瑞金医院)。患者为体力工作者,于1个月前逐渐出现活动后胸闷不适,不伴胸痛,无头晕、黑矇,症状反复无好转,严重时曾出现夜间阵发性呼吸困难,至当地医院就诊。心脏彩色多普勒超声(简称心超)检查结果示:二尖瓣前后叶对合错位致中重度关闭不全,三尖瓣轻度关闭不全,左心房、左心室及右心房明显增大,射血分数(EF)为33%。心电图检查结果示:窦性心动过速,频发室性早搏,建议手术治疗。患者为求进一步诊治至瑞金医院心血管外科就诊,拟诊“二尖瓣关闭不全”收治入院。入院后体格检查示:下颌稍突出,四肢远端关节粗大,双足宽大,全身肤色较深。追问病史,患者否认高血压、糖尿病、心肌梗死、脑梗死、高血脂、COPD、哮喘、肝和肾功能不全,以及甲状腺、肾上腺相关的慢性病史;否认头痛、视野缺损。自诉手足较同龄人粗大,未予干预,既往无心脏病病史及外伤史,否认家族病史。完善体格检查示:神志清,精神可,心率96次/min,血压115/58 mmHg(1 mmHg=0.133 kPa),呼吸15次/min,脉搏70次/min;双肺呼吸音粗,未闻及明显的干湿性啰音;心律齐,心界扩大,二尖瓣区可闻及收缩期2/6级吹风样杂音;双下肢无水肿及静脉曲张。请内分泌科会诊,建议完善相关检查,结果提示:胰岛素样生长因子630 ng/mL;脑利尿钠肽(BNP)1 903 pg/mL;TG 1.89 mmol/L;NSE 23.31 ng/mL;血皮质醇(早上8时)8.11 μg/dL,血皮质醇(凌晨0时)1.94 μg/dL,血皮质醇(下午4时)2.81 μg/dL,促肾上腺皮质激素(ACTH)41.45 pg/mL,尿游离皮质醇63.03 μg/24 h,尿皮质醇5.73 μg/dL;甲状腺功能三项,血、尿及粪常规,肝、肾功能及电解质,凝血功能,心肌肌钙蛋白及急诊CRP,ESR,生长激素及性激素等均无异常。患者入院检查提示多巴酚丁胺激发试验阳性。胸部X线摄片检查示:两肺纹理增多、稍粗、模糊,心脏增大,主动脉迂曲。胸部薄层CT平扫检查示:两肺下叶少许条索影,心包少许积液。心电图检查示:室性早搏,左心室高电压。心超检查示:左心增大伴重度二尖瓣关闭不全,心功能不全,轻度三尖瓣关闭不全,肺动脉高压[肺动脉压(PA)49 mmHg)],少量心包积液,EF为28%。心脏增强MRI检查示:室间隔心肌中层少许纤维化,左心增大,心功能不全,中度二尖瓣关闭不全,心包积液。冠状动脉造影(CAG)检查未见明显异常。头颅CT检查示:双脑室周腔隙灶。垂体增强MRI检查示:垂体左侧翼占位,大小约10.7 mm×10.4 mm,拟诊垂体腺瘤。副鼻窦横断位+冠状位CT重建平扫检查示:垂体形态饱满,右侧鞍底下陷伴结节状软组织密度影,鼻中隔左偏,右下鼻甲黏膜略增厚。腹部超声检查未见异常。结合患者的症状、体征、实验室及影像学检查结果,明确诊断为垂体微腺瘤,肢端肥大症,心肌病,中度二尖瓣关闭不全,慢性心功能不全(NYHA分级Ⅲ级),腔隙性脑梗死,鼻中隔左偏。
因患者垂体瘤有神经外科手术适应证,且心功能不全几近衰竭,急需手术治疗,遂组织相关科室进行MDT病例讨论,以明确手术适应证,即患者垂体瘤切除术和心脏瓣膜置换术的先后顺序,并制订具体的术前准备和围手术期管理方案。
2 术前MDT诊疗经过
2.1 神经外科意见 患者垂体微腺瘤诊断明确,心脏的病变与垂体微腺瘤相关,有确切的手术适应证。垂体瘤手术须考虑到术后出血等并发症。若先行心脏手术,术后所服用抗凝药物,会增加神经外科手术的难度和术后并发症的发生风险。
2.2 心血管外科意见 患者目前诊断为心脏瓣膜病,心功能NYHA分级Ⅲ级,心血管外科手术适应证明确。结合患者实验室检查结果及神经外科会诊意见,考虑垂体瘤为诱发心脏病变的主要原因,若先行心脏瓣膜置换术,术后心脏瓣膜病变及心肌病变复发可能性大,且瓣膜术后抗凝治疗会影响神经外科手术效果。此外,患者入院检查示多巴酚丁胺激发试验阳性,提示患者对正性肌力药物敏感,故麻醉手术风险仍较大。建议先行垂体瘤切除术,待生长激素(GH)降至正常水平后再行心脏瓣膜置换术(置换机械瓣);或可先行心脏瓣膜置换术(置换生物瓣),术后短时间服用抗凝药物,待可停药且手术完成半年后再行垂体瘤切除术。
2.3 内分泌科意见 生长抑素有导致心律失常及胆总管结石的风险。若先行心脏瓣膜置换术并予以生长抑素抑制GH,期间出现心律失常及胆总管病变的概率较高;若先行垂体瘤切除术可避免上述情况。如术后GH水平无明显下降,可短期内予以生长抑素辅助治疗。
2.4 麻醉科意见 患者左心室射血分数(LVEF)数值较低,考虑术中发生心力衰竭的风险较大,建议先行心脏瓣膜置换术;若需先行垂体瘤切除术,需加强围手术期心功能管理,并充分告知患者及其家属术中可能发生心力衰竭的风险。
2.5 MDT意见 综合上述各科医师讨论意见,拟提供两个备选方案。方案一:先行经鼻腔垂体瘤切除术,术后将患者送至ICU加强心功能监护,并视术后患者GH水平,必要时短期予以醋酸奥曲肽微球辅助治疗,待GH基本降至正常范围后转至心血管外科行心脏瓣膜置换术(置换机械瓣)。垂体瘤围手术期存在一定的心力衰竭风险。方案二:先行心脏瓣膜置换术(置换生物瓣),术后予以抗凝3个月并予醋酸奥曲肽微球控制GH水平,术后半年再行垂体瘤切除术。醋酸奥曲肽微球治疗控制GH期间存在心律失常和胆道病变发生的风险,且存在生物瓣置换术后10~20年瓣膜失功能需再次换瓣的问题。经过与患者及其家属的详细沟通后,决定启用方案二。
3 心脏手术情况于2019年12月5日行二尖瓣置换术(MVR),予置换生物瓣。患者术前常规禁食、禁饮,入手术室后监测生命体征,开放外周静脉,行左侧桡动脉穿刺置管,监测有创动脉血压。予静脉推注1%丙泊酚150 mg、舒芬太尼20 μg、罗库溴铵50 mg、地塞米松5 mg行麻醉诱导。在可视喉镜辅助下行气管插管及容量控制机械通气(VCV),设置呼吸机机械参数: FiO2为85%,氧流量为1.5 L/min、潮气量(VT)为6~10 mL/kg、呼吸频率 12~16次/min、吸呼比为1∶1.5,维持呼气末二氧化碳(petCO2)为35~45 mmHg。经患者右颈内静脉穿刺并置漂浮导管测肺动脉楔压(PAWP),动态监测混合动脉血氧饱和度(SCVO2)、心指数(CI)、右心室射血分数(RVEF)、舒张末容积(EDV)、中心静脉压力(CVP)、PA等。经口置入食道超声。术中麻醉维持方式为静脉-吸入复合麻醉,泵注顺式阿曲库铵2 μg/(kg·min)、瑞芬太尼0.15 μg/(kg·min),吸入地氟烷并维持0.8~1.2的最低肺泡有效浓度(MAC)。术中视具体情况予血管活性药物维持血流动力学稳定,监测麻醉深度,维持Narcotrend指数数值为37~45,体温为36~37 ℃,血红蛋白值>80 g/L、红细胞压积(Hct)>25%,pH值为7.35~7.45,碱剩余(BE)-2~+2,电解质基本维持在正常范围。术中见二尖瓣中重度关闭不全,切除前瓣,保留后瓣,测瓣后植入27#Edward生物瓣,手术顺利,术中二尖瓣病理学检查提示纤维组织增生伴胶原化、黏液变性。术中采用自体血回输,全程补液量为1 350 mL,尿量为750 mL。术后予患者静脉自控镇痛(PCIA)泵镇痛,配比为100 μg舒芬太尼、5 mg布托啡诺,背景输注速度为2 mL/h,单次剂量为1 mL,锁定时间为20 min,总容量为100 mL。
4 心脏术后辅助治疗方案患者术后带管回心血管外科ICU,于手术当晚顺利拔除气管导管。术后予抗凝、抗感染、维持内环境稳定等综合治疗。术后1周一般情况稳定,予出院。出院后1周拆线,予口服华法林2.5 mg、2粒/d,泮托拉唑肠溶片40 mg、1粒/d,治疗3个月;呋塞米20 mg、1粒/d,螺内酯20 mg、1粒/d,治疗1个月;倍他乐克缓释片47.5 mg、1粒/d, 长期口服;托伐普坦40 mg、1粒/d。抗凝及辅助治疗3个月后,嘱患者赴神经外科门诊就诊。
5 垂体瘤手术及围手术期情况心脏术后,患者未能按时复诊。于2020年4月14日,因“阵发性头痛1月”再次收入瑞金医院神经外科,拟行“经鼻腔-蝶窦垂体瘤切除术”。患者华法林停药7 d,自诉间断有视野缺损的症状。完善术前检查及术前准备,于2020年4月16日在全身麻醉下行神经内镜经鼻腔-蝶窦垂体病损切除术。患者入手术室后,予常规心电监测,开放外周静脉,经桡动脉穿刺监测有创血压。予静脉推注1%丙泊酚70 mg、舒芬太尼20 μg、顺式阿曲库铵15 mg、地塞米松5 mg行麻醉诱导,3 min后在可视喉镜辅助下行气管插管及VCV,并经口置入食道超声。术中经食道超声心动图(TEE)见二尖瓣瓣膜处可疑血栓形成(图1),与患者家属、外科医师及ICU医师沟通后决定继续手术。术中麻醉维持方式为静脉-吸入复合麻醉,泵注顺式阿曲库铵2 μg/(kg·min)、瑞芬太尼0.15 μg/(kg·min),1.1MAC地氟烷吸入维持。术中视具体情况予血管活性药物维持血流动力学稳定,并动态监测血气分析等指标。术中出血量为100 mL,补液量1 750 mL,尿量200 mL。手术过程顺利,术后入麻醉后监测治疗室(PACU),TEE实时监测患者血栓状态及心脏收缩情况,均较术前无明显变化。术中切除的垂体肿物病理学检查提示垂体腺瘤(稀疏颗粒性生长激素细胞腺瘤);补充特殊检查,结果示:肿瘤细胞核旁纤维小体(AE1/AE3)呈阳性,SYN(+),CgA(+),Pit-1(+),GH(±),肿瘤增殖指标(Ki67)阳性比例为1%,网状纤维染色示网状支架断裂。后拔除气管导管转入外科重症监护病房(SICU)进一步诊治,2 d后转回神经外科病房。术后第3天患者突发气促,坐位可减轻,复查BNP 35 000 pg/mL、肌钙蛋白0.47 ng/mL;心电图检查示: ST-T改变。诊断为心力衰竭,予吸氧、限制液体入量、利尿、扩血管、抗感染等对症支持治疗后好转。患者术后出现一过性甲状腺功能减退,予对症治疗后症状有所缓解。其他内分泌指标均恢复至正常水平,且患者外观肢端肥大症状明显改善。患者出院后予口服左甲状腺素钠片12.5 μg、1粒/d;氢化可的松片10 mg、0.5粒/次,2次/d;呋塞米1粒/d;螺内酯1粒/次,2次/d;华法林1粒/d。表1所示为患者围手术期不同时间点心超检查数值详情。
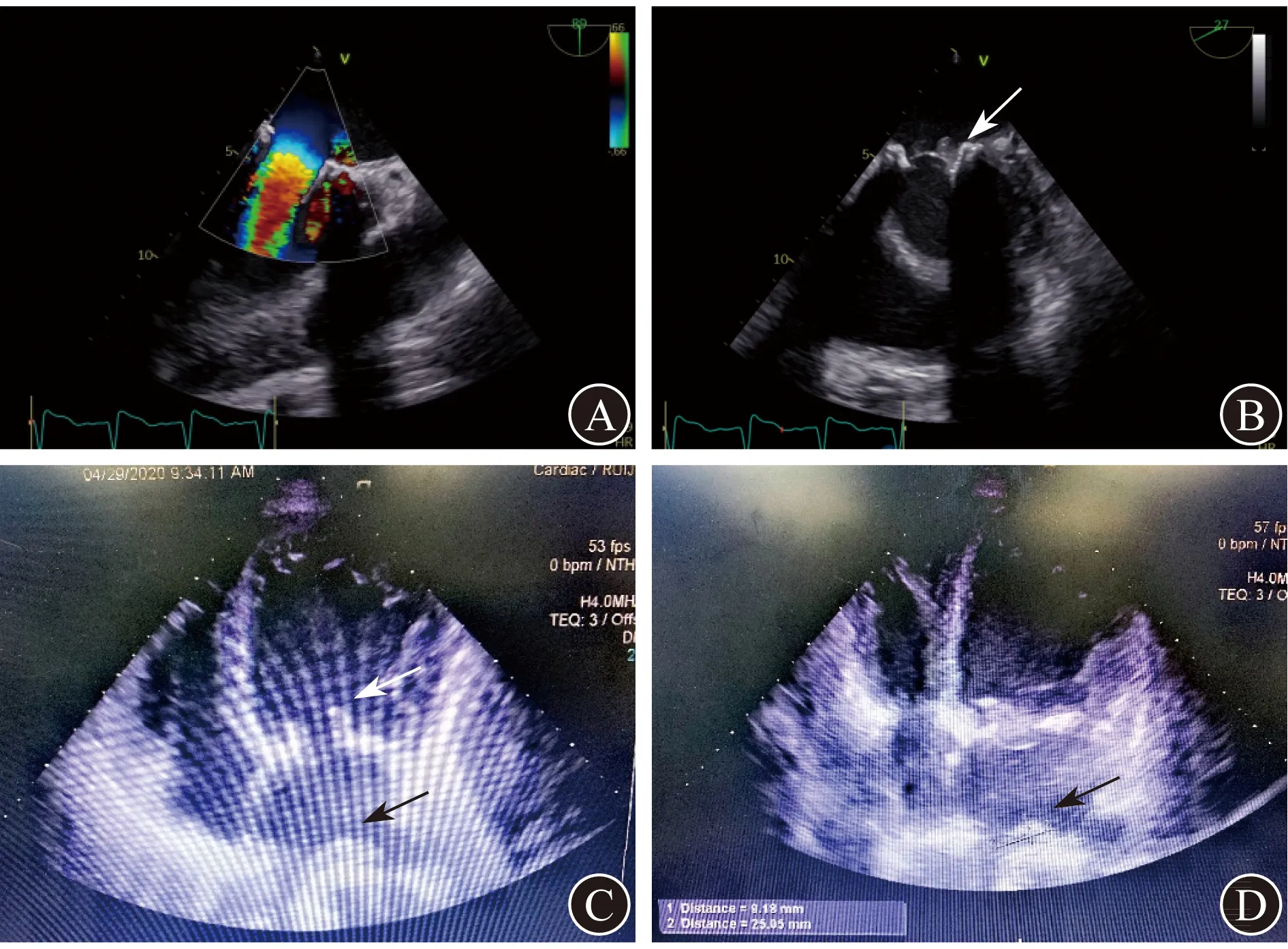
A 二尖瓣生物瓣活动正常、功能良好 B 二尖瓣生物瓣血栓形成(白色箭头所指) C 二尖瓣和左心房血栓形成(黑色箭头所指为心房附壁血栓) D 左心房血栓测量(黑色箭头所指为心房附壁血栓)
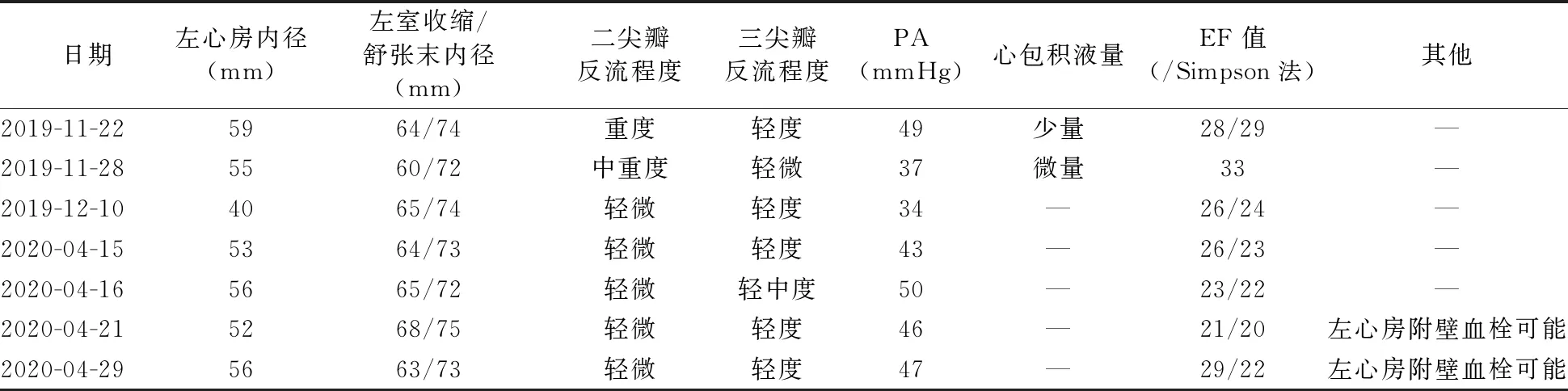
表1 患者心超检查指标数值详情
6 讨 论肢端肥大症性心肌病是内分泌科疾病,因GH水平升高导致患者出现肢端肥大症状,影响心肌,诱发心脏病变[1]。随着病程的延长,心脏病变的概率会逐渐增加,其诊断主要依靠心超所示的心脏结构和功能异常[2]。心脏MRI诊断肢端肥大症性心肌病也较为灵敏,可显示心肌纤维化、心肌灌注减少、水肿及区域心肌运动不协调等影像学表现[3]。心肌病是肢端肥大症患者最常见、最严重的并发症[4],起病多隐匿。本例患者症状、体征更为罕见,首发症状即为失代偿性心力衰竭。
这类患者多因垂体瘤起病,需择期行垂体瘤切除术。文献[5]综述分析了2017年一项针对65例GH型垂体瘤合并心肌病患者的研究,结果显示在行垂体瘤切除术后,患者的心脏结构及功能较术前显著改善。因此,对于部分心脏病变较轻的肢端肥大症性心肌病患者,只需进行垂体瘤切除术即可逆转心脏病变。但对于心脏病变较为严重的患者,多有行心脏瓣膜置换手术的适应证。有研究[6]建议,对于伴有心脏扩大、心排量减少、频发室性心律失常及失代偿性心力衰竭的肢端肥大症性心肌病患者,先行择期心脏瓣膜置换术,再行择期垂体瘤手术。而无论先行何种手术,患者皆有较高的出血风险。本例患者先行择期二尖瓣置换术,选用生物瓣,即考虑到生物瓣膜置换术后无需终身抗凝治疗,可降低患者数月后行垂体瘤手术时的围手术期出血风险。矛盾的是,外科手术本身的围手术期血栓形成风险是高危的。本例患者在垂体瘤术中行TEE检查时,发现二尖瓣存在可疑血栓,术后心超检查结果也证实心房甚至心室内血栓形成。这可能与患者术前未遵循医嘱直接停用华法林有关,也可能与神经外科手术本身存在血栓形成高风险有关,或与患者心脏术后未能有效监测INR也存在一定关系。由于患者未能提供当地医院凝血功能检查结果,因此,本例患者血栓形成的原因无法明确,极有可能是上述因素综合作用的结果。这也启示本MDT团队医师:对于心脏手术后需接受神经外科手术的患者,应更积极地行抗凝治疗并监测抗凝治疗效果,以减少可能发生的出血及血栓事件。对于常规服用华法林的患者,应于术前停用华法林,予以低分子肝素桥接,并复测INR,当INR<1.5时再行神经外科手术,这样可以在一定程度上减少围手术期出血风险。
本例患者的心脏手术顺利,在随后的垂体瘤手术中出现了一次心力衰竭的急性发作,这可能与患者垂体瘤术后激素水平波动(表现为术后的甲状腺功能减退)有关,也可能与术后潜在的感染和未严格控制出入液量有关。结合本例患者围手术期不同时间点心超检查结果,尽管其在心脏手术后心脏功能有所恢复,但患者的心脏仍处于慢性心力衰竭的代偿期,长久以来垂体瘤对于心脏的影响并未能在短期(3个月)内缓解。这种复杂的病情,需要麻醉科、神经外科等相关人员制订更周密的围手术期治疗方案,以保障患者安全。
综上,通过MDT诊治,以及与患者及其家属的充分沟通,医师与医师、医师与患者就疾病的诊治流程达成共识,对治疗所产生的效果及可能发生的风险进行综合评估,结合应用新项目和新技术,制订了全方位的诊疗方案,为促进患者早日康复保驾护航。
