Ni改性SAPO-11分子筛择形催化2-甲基萘烷基化制2,6-二甲基萘
2022-06-22冯刚文志辉周建林邵松刘清华张荣斌
冯刚,文志辉,周建林,邵松,刘清华,张荣斌
(南昌大学 化学学院,南昌 330031)
2,6-二甲基萘(2,6-DMN)是一种高端聚酯单体,其氧化为2,6-萘二甲酸后,与乙二醇缩合可以制得一种性能优良的聚酯材料聚萘二甲酸乙二醇酯(PEN)[1-4].PEN与聚对苯二甲酸乙二醇酯(PET)相比,PEN有更高的强度、更优异的热性能、更好的阻气性以及更强的化学稳定性和耐辐射性能等,广泛应用于电子元件、仪器仪表、绝缘材料、航天航空材料等[5-7].但是2,6-DMN制备技术不够成熟,致使其成本高、价格昂贵,导致PEN不能大规模进入市场.
过去几十年中,人们提出了很多种制备2,6-DMN的方法,但分子筛催化2-MN和甲醇一步法反应过程简单,原料来源广泛,因而被认为是最合理的技术路线[8-9].然而2-MN烷基化的产物十分复杂,仅二甲基萘就有10种,并且沸点非常接近,尤其是2,6-DMN和2,7-DMN的沸点只差0.3 ℃,分离提纯难度大,关键的挑战是要提高2,6-DMN的选择性和2,6-/2,7-DMN的比值.需要通过调节分子筛的酸性和孔道结构来修饰催化剂从而提高目标产物的选择性[10].
SAPO-n系列分子筛具有丰富的结构,已经成为一类重要的分子筛材料,在分离[11-12]、气体吸附[13]、催化[14]等领域有着广泛的应用.SAPO-11分子筛作为SAPO-n家族中的重要一员,具有温和的酸性和适中的孔隙结构,以及具有椭圆形十元环的孔道结构,孔径为0.39 nm×0.64 nm[15],被认为是加氢异构和加氢脱氧生产生物柴油等反应的优选催化剂[16-17].由于其特有的孔道结构,SAPO-11分子筛也被用于催化萘和甲醇烷基化制2,6-DMN的反应中.文献研究了不同硅含量的SAPO-11分子筛[18]、酸处理后的SAPO-11分子筛[19]和不同模板剂种类及不同含量的SAPO-11分子筛[9]对萘和甲醇烷基化的影响,发现SiO2与Al2O3物质的量之比为0.2合成的SAPO-11分子筛在反应6 h后,2,6-DMN的选择性可达到48.2%,2,6-/2,7-DMN比值为1.72[18];4 mol/L HCl处理后的SAPO-11分子筛反应6 h后,2,6-DMN的选择性为48.7%,2,6-/2,7-DMN的比值为1.81[19];由二正丙胺(DPA)合成的SAPO-11分子筛(nDPA/nAl2O3=1.2)在反应8 h后,2,6-/2,7-DMN比值为1.96[9].LIU等人[8]研究了不同方法合成的SAPO-11分子筛对萘与甲醇烷基化的影响,发现微波法合成的SAPO-11分子筛在反应4 h后,2,6-DMN的选择性可达到32.4%,2,6-/2,7-DMN比值为1.93.学者用不同方法改性SAPO-11分子筛催化剂有效提高烷基化的催化效率[20-21],如ZHANG等人[20]研究了PdO负载改性多种分子筛催化2-MN和甲醇烷基化的影响,发现PdO负载改性的SAPO-11分子筛在反应9 h后,2,6-DMN的选择性为28.0%,2,6-/2,7-DMN比值为1.50左右.Ni和Pt,Pd具有相似的性质,而通过金属Ni改性SAPO-11分子筛催化该反应报道较少.采用金属Ni改性对分子筛的理化性质有一定影响.首先,金属Ni形成的NiO会覆盖表面酸位点,抑制表面异构化反应的发生而提高选择性.其次,在硝酸镍浸渍改性SAPO-11分子筛的过程中,有部分金属Ni会进入分子筛的孔道内,对分子筛的孔径起到了一定的修饰作用.最后,除了分子筛本身的Lewis酸位点外,Ni/SAPO-11提供了更多的Ni2+物种,已知Ni2+物种是电子对的受体,充当L酸位点.Ni为非贵金属,价格便宜,而Pt,Pd为贵金属,价格昂贵.本文拟将活性金属Ni采用浸渍法负载到SAPO-11分子筛上,并用于催化2-MN和甲醇烷基化反应.
1 实验部分
1.1 试剂与仪器
硅溶胶(40%(质量分数)SiO2,山东豪耀新材料有限公司),拟薄水铝石(70%(质量分数),山东允能催化技术有限公司),磷酸(85%(质量分数),西陇科学股份有限公司),二正丙胺(分析纯,国药集团化学试剂有限公司),硝酸镍(分析纯,成都艾科达化学试剂有限公司),甲醇(分析纯,西陇科学股份有限公司),1,3,5-三甲苯(分析纯,国药集团化学试剂有限公司),2-甲基萘(97%(质量分数),国药集团化学试剂有限公司),上述试剂都未经进一步纯化,去离子水为自制.
在北京普析仪器有限责任公司XD-3型X射线衍射仪进行了XRD分析;通过Micromeritics公司ASAP2020型比表面积分析仪测得所有催化剂的比表面积和孔径等参数;使用Micromeritics公司AutoChem-2920型化学吸附仪测定催化剂的NH3-TPD曲线;使用日本Hitachi-4800型场发射扫描电子显微镜观察样品的形貌.
1.2 SAPO-11分子筛催化剂的制备
采用水热合成法制备SAPO-11分子筛.按照nAl2O3∶nDPA(二正丙胺)∶nP2O5∶nSiO2∶nH2O=10∶10∶10∶0.2∶43原料配比,将原料按水、磷酸、拟薄水铝石、二正丙胺、硅溶胶的顺序加入后搅拌均匀,放入含有聚四氟乙烯内衬的反应釜,在200 ℃下晶化24 h,晶化完成后进行抽滤、洗涤、干燥,最后在600 ℃马弗炉中煅烧4 h得到SAPO-11分子筛.
用分析天平称取一定量的Ni(NO3)2·6H2O固体,依次配制质量分数1%,2%,3%,4%的硝酸镍溶液.采用等体积浸渍法将金属镍负载到SAPO-11分子筛上,在105 ℃干燥12 h后,在600 ℃下煅烧2 h得到不同量Ni负载的催化剂,对应命名为1%Ni/SAPO-11,2%Ni/SAPO-11,3%Ni/SAPO-11,4%Ni/SAPO-11.
1.3 烷基化实验
2-MN和甲醇的烷基化反应在固定床反应器中进行,取2 g 20~40目的催化剂置于反应管中,两端用石英砂填充.反应前,将催化剂在N2气氛(20 mL/min)下500 ℃吹扫2 h,再冷却至反应温度(400 ℃).将反应原料2-MN、甲醇、均三甲苯依次按物质的量比1∶5∶3.5均匀混合,然后用微量计量泵以重时空速0.5 h-1(2-MN)泵入反应管.产物经过冷凝后收集,采用氢火焰离子化检测器(FID)的气相色谱进行分析.
1.4 产物分析
使用山东鲁南瑞虹有限公司SP7890 Plus气相色谱进行分析,载气为N2,色谱柱为Supelco公司的Beta-DEX-120型毛细柱(60 m×0.25 mm×0.25 μm),进样口温度为280 ℃,检测器温度为300 ℃,色谱柱采用程序升温,160 ℃保持36 min后以10 ℃/min的升温速率升到190 ℃并保持45 min.
通过2-MN的转化率X,2,6-DMN的选择性S和2,6-/2,7-DMN的比来评价SAPO-11分子筛催化剂的活性.计算公式如下:
其中,n0,n分别代表原料和产物中2-MN的物质的量,n2,6-DMN,∑nDMN分别代表产物中2,6-DMN和产物中所有DMN的物质的量.
2,6-/2,7-DMN的比为产物中2,6-DMN和2,7-DMN物质的量之比.
2 结果和讨论
2.1 催化剂表征

图1是SAPO-11分子筛及负载不同量Ni的SAPO-11分子筛催化剂的XRD谱图.从图1可以看出,水热法合成的SAPO-11分子筛样品在2θ=8.1°,9.6°,13.2°,15.8°,20.3~23.4°处的特征峰表明所合成的SAPO-11具有明显的AEL拓扑结构,并且和SAPO-11标准PDF卡片相符(PDF#41-0023).硝酸镍溶液浸渍后的SAPO-11分子筛,特征峰无明显变化,也没有出现其他杂峰,说明负载金属Ni不会破坏分子筛本身的结构也不会生成新的杂相.在2θ=37°和43°没有出现NiO的特征峰,可能是因为金属Ni颗粒均匀分散在催化剂表面或者Ni的负载量太小了.
图2是APO-11分子筛和2%Ni/SAPO-11分子筛的SEM图,SAPO-11分子筛颗粒大小比较均匀,形状为10 μm左右的球形,改性后的SAPO-11分子筛保持原有的形貌,说明浸渍Ni(NO3)2后并不会破坏分子筛的形貌.

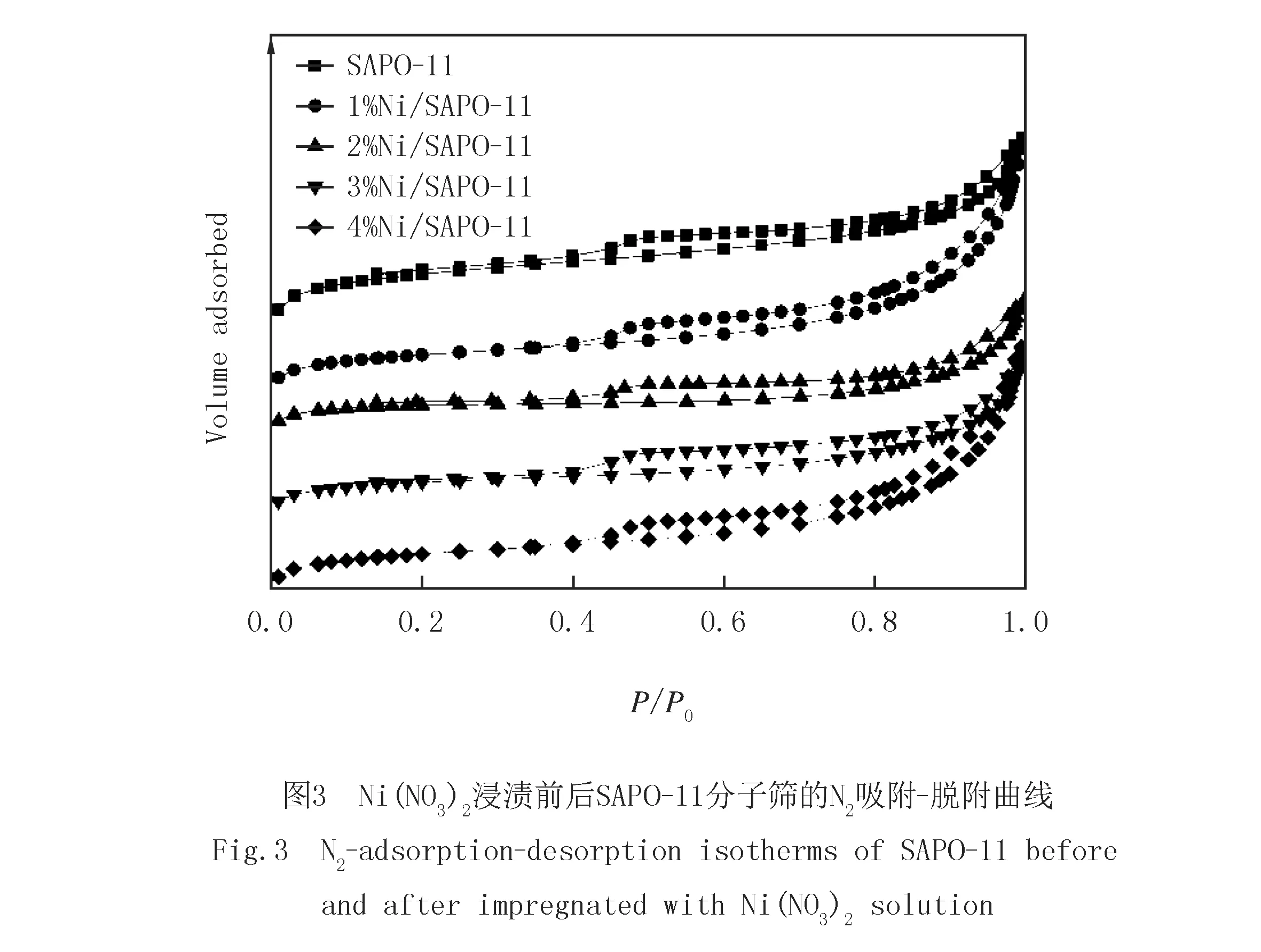
为了研究SAPO-11分子筛改性前后的结构变化,用N2吸附-脱附测定了SAPO-11分子筛的孔结构和比表面积.图3是改性前后SAPO-11分子筛的N2吸附-脱附等温线图.表1是改性前后SAPO-11分子筛的孔道结构和比表面积等.根据IUPAC气体吸附等温线的分类标准,改性前后的SAPO-11分子筛的吸附等温线是典型的第IV型,这种曲线类型在较高的相对压力下存在一个明显的回滞环,可能是由于沸石颗粒聚集产生了间隙,说明该分子筛存在介孔结构.
由表1可知,随着金属Ni负载量的增加,比表面积呈现一个下降的趋势,微孔面积和微孔体积都在减小.这一现象可能有3种解释:一是可能由于镍颗粒负载在SAPO-11分子筛的表面,堵塞了部分微孔,并且随着负载Ni含量的增加,堵塞效应越大,降低幅度更大.二是SAPO-11分子筛对水比较敏感,水分子可能会破坏分子筛的骨架结构,一些Al-O键可能由于溶剂水的侵蚀而断裂,这些断裂的Al-O键堵塞了部分微孔.三是SAPO-11分子筛中能量较高的缺陷部位更容易受到溶剂的侵蚀而断裂,从而产生一些固体碎片,碎片会沉积微孔的入口,使得微孔比表面积和体积都减小[22].

表1 Ni(NO3)2改性前后SAPO-11的比表面积和孔体积
SAPO-11分子筛催化剂表面酸性的强度分布和含量对2-MN烷基化有显著影响.为了研究Ni浸渍改性后对SAPO-11分子筛酸强度和酸量的影响,用NH3-TPD测试了催化剂的酸强度和酸量.酸强度由氨解吸峰值温度确定,酸量由TPD曲线下的面积来估计.图4为浸渍Ni(NO3)2前后SAPO-11分子筛催化剂的NH3-TPD图,由图4可知,SAPO-11分子筛在200 ℃左右有一个弱酸位点的解析峰,在250 ℃时有一个肩峰.浸渍Ni(NO3)2以后,SAPO-11分子筛的弱酸的酸量明显减小,且弱酸位点的解析峰随着负载量的增加逐渐向低温区偏移,说明弱酸位点的酸强在逐渐减弱.SAPO-11分子筛酸量减小的原因可能是因为负载金属后,分子筛表面的一些酸位点被NiO覆盖导致[22-23].
2.2 Ni改性SAPO-11分子筛催化2-MN和甲醇烷基化

分别测试了本体和负载量为1%,2%,3%和4%的SAPO-11分子筛的催化活性(图5).结果表明本体SAPO-11分子筛具有最高的初始转化率,反应1 h后转化率可达到41%,随着Ni的负载量增加,转化率逐渐降低.由于在SAPO-11分子筛催化剂上,甲醇可以发生很多副反应转化为各种烃类,进而又与萘环进行烷基化反应逐渐形成多环芳烃,产生的多环芳烃会堵塞孔道,增大反应物和产物的扩散阻力[24-25].用Ni(NO3)2浸渍改性后的SAPO-11分子筛表面无择形性的酸位点被覆盖,酸量降低,尤其是弱酸量降低,抑制了多环芳烃的生成,因此2-MN的转化率随着硝酸镍浸渍量的增加而降低.尽管负载金属Ni之后活性降低了,但是改性后的催化剂表现出更高的稳定性,失活速率较慢,本体分子筛则快速失活.可能是改性后表面异构化减少,使得积碳量减少,提高了催化剂的稳定性.

除负载4%Ni的催化剂外,其余催化剂随着反应时间增加,选择性逐渐升高.4%Ni/SAPO-11分子筛的选择性随时间增加而降低,可能是因为负载量较大,NiO颗粒堵塞了部分孔道,随着反应的进行伴有积碳生成从而进一步堵塞孔道,2,6-DMN扩散阻力加大,导致DMN的反应发生在外表面,所以2,6-DMN选择性降低.实验结果表明,2%Ni/SAPO-11分子筛的选择性一直保持最高,反应7 h后,选择性能达到46%,远高于2,6-DMN的热力学平衡值12%.2%Ni/SAPO-11分子筛催化剂有高选择性可能是如下几种原因:(1)通过负载金属Ni到SAPO-11分子筛载体上,表面部分无择形性的酸位点被覆盖,表面异构化减少使得选择性上升;(2)在10种DMN中,2,6-DMN有相对较小分子动力学直径,随着反应时间增加,反应产生的积碳覆盖在催化剂表面和堵塞在分子筛孔道,使得其较容易从催化剂中扩散,而其他体积较大的DMN难以扩散;(3)对2-MN来说,6位碳原子比7位碳原子具有更高的电子云密度[26],根据轨道理论,电子取代反应如芳烃烷基化,具有最高电子密度的碳原子既有最高的活性,所以在没有空间位阻的情况下,更容易生成2,6-DMN,SAPO-11分子筛的酸性温和,能够有效抑制2,6-DMN进一步异构化.
2,6-/2,7-DMN的比值是分离这两种异构体难易程度的重要指标.如果该比值小于0.70,那么这两种二甲基萘很难分离,如果比值大于1.40,则较易分离[9].所有SAPO-11分子筛催化剂催化后的产物该比值均大于1.40,远远高于该比值的热力学平衡值(1.00).除4%Ni/SAPO-11分子筛外,其他催化剂的该比值都随着反应时间增加而增加,且都大于本体的2,6-/2,7-DMN比.4%Ni/SAPO-11分子筛反应的前3 h,该比值缓慢上升,4 h后迅速下降,可能是因为负载量过多导致堵塞分子筛孔道,且随着反应进行伴随积碳生成,进一步堵塞孔道,导致其选择性和2,6-/2,7-DMN比值下降.其中2%Ni/SAPO-11分子筛催化剂的比值,可随反应时间增大到2.04.可能是因为负载Ni以后,异构化减少,2,6-DMN的选择性上升.随着反应的进行,产生了积碳覆盖在表面和堵塞在孔道中,使得酸性中心进一步被覆盖,产生碳正离子的活性降低,更容易进攻具有电子密度更高的6位,导致2,6-/2,7-DMN逐渐增大.
3 结 论
SAPO-11分子筛的孔道结构和酸性是影响2-MN和甲醇烷基化的主要因素.可以通过负载金属来调节分子筛的孔道结构和酸性,适中的孔径能够有效从产物中筛分出2,6-DMN,温和的酸性能有效减少异构化,从而提高目标产物的选择性.但是负载金属的比例需要适当,因为2,6-DMN的生成需要一定量的强酸位点参与.改性后的SAPO-11分子筛催化剂转化率比SAPO-11低,但是催化剂稳定性得以提高,失活速率更慢.改性后的分子筛的选择性和2,6-/2,7-DMN比值均有不同程度的升高.其中,2%Ni/SAPO-11在反应7 h后,选择性能够达到46%,2,6-/2,7-DMN比值能够达到2.04.
