术前超声在预测困难的腹腔镜胆囊切除术中的价值
2022-06-16叶学忠程小菊
叶学忠 程小菊 邾 磊 周 觅
安徽省无为市人民医院普外一科(无为 238300)
腹腔镜胆囊切除术(laparoscopic cholecystectomy, LC)是以胆囊结石为主的胆囊良性病变手术切除的“金标准”。它具有小切口、术后疼痛轻、恢复快的优点。但LC手术也有术中大出血、术中胆管损伤、中转进腹手术的风险。手术有难易程度之别。能否术前准确预测LC手术的难易,选择合适的手术方式和预防措施,从而预防并降低LC手术的并发症,一直是肝胆外科研究的重点。国内学者探讨了导致困难LC的影响因素,有的对LC难度建立模型进行预测[1-2]。超声检查获取的有关胆囊大小、胆囊壁厚度、黏膜面情况、胆汁透声情况、结石大小、有无颈部结石嵌顿等指标,诊断符合率达 99.7%[3]。可以反映胆囊疾病的严重程度,为术前评估胆囊疾病情况,预测手术难易提供参考。顾建萍等[4]通过对有无胆囊颈部结石等情况建立了判别LC难度的公式。本文回顾性分析了2018年1月—2020年8月期间安徽省无为市人民医院普外一科同一治疗组行LC手术的胆囊病例257例,探讨超声检测在LC术前评估中的作用。尝试通过多因素分析获得评估LC难度的有关独立危险因素,从而更简洁更直观地评估困难LC,降低腹腔镜手术风险。
1 资料与方法
1.1 临床资料
收集安徽省无为市人民医院普外一科同一治疗组在2018年1月—2020年8月期间行LC手术切除的病人共257例,其中男76例,女181例,年龄25~88岁,平均年龄(55.50±13.37)岁。所有病例术前检查均排除合并有胆囊肿瘤、肝内外胆管结石疾病。手术时间计算从腹腔镜进腹开始,分离胆囊周围粘连,解剖胆囊三角,胆囊床完整剥离胆囊,胆囊标本自剑突下切口取出为止。
1.2 术前超声检查方法
257例除急诊患者外,其余患者超声检查前均禁食8 h以上,以保证患者胆囊内胆汁充盈良好,并减少胃肠道气体的干扰。常规检查包括肝胆胰脾脏器,通常患者采取仰卧位,超声检查对胆囊和三管(胆囊管、胆总管、肝总管)作纵、横、斜位检测,必要时作左侧卧位和膝胸卧位检查。超声检测获取的数据包括:①胆囊的形态、大小和位置:胆囊大小的标准是取胆囊最大切面的横径和纵径,其投影面积 (横径×纵径)大于50 cm2被视为胆囊过大;②胆囊壁的厚度:以胆囊壁厚度>4 mm 作为胆囊壁增厚的衡量指标[5];③胆囊黏膜面的粗糙程度;④胆囊内胆汁透声情况;⑤胆囊息肉、胆囊结石的大小和数量;⑥胆囊颈部的情况,有无颈部结石嵌顿,同时观察三管(胆总管、胆囊管、肝总管)有无结石、有无嵌顿和梗阻;⑦胆囊周围有无积液。
1.3 LC手术方法
手术过程采用电子腹腔镜手术系统,按标准腹腔镜胆囊切除手术方法进行手术操作手术,术中麻醉采用气管插管或喉罩插管全身麻醉,LC手术中CO2气腹压力一般维持在12 mmHg。绝大多数病例常规行三孔法切除胆囊,有3例困难胆囊病例行四孔法切除胆囊。胆囊切除标本均进行病理检查,并与超声检查结果进行对照。
1.4 统计学分析
采用SPSS 26.0软件进行统计分析, 术前超声检查获取的参数与临床病例资料的关系采用χ2检验、多因素分析采用Logistic回归模型。P<0.05表示差异有统计学意义。
2 结 果
2.1 一般情况
LC手术成功共计254例,中转开腹有3例。257例胆囊LC手术的平均手术时间为(49.16±17.82)min,最短30 min,最长220 min。257例平均出血量(34.49±6.47)mL,最少5 mL,最多超过100 mL。全部257例病人无死亡病例,术中无胆管损伤,术后无并发症,均痊愈出院。
计算标准手术的平均时间为60 min,并将其称为标准手术时间。将88例手术时间超过60 min、术中出血≥100 mL、术中放置引流管、术中中转进腹手术等情况列为手术困难组。以手术时间等于或低于60 min、术中出血<100 mL、未放置引流管的有169例,列为手术容易组。
257例患者术前超声检查,胆囊结石患者252例,胆囊息肉样病变患者17例,其中:(1) 胆囊大小正常患者190例,大小>50 cm2者67例;(2) 胆囊壁的厚度≤4 mm者174例,厚度>4 mm者83例;(3)胆囊的黏膜面光滑者71例,黏膜面粗糙者186例;(4)胆囊内胆汁透声尚可者159例,透声差者98例;(5)胆囊结石最大直径≤2 cm者160例,最大直径>2 cm者97例;(6)胆囊颈部结石嵌顿者34例。
2.2 单因素分析
将257例患者术前超声参数和手术难易组进行单因素分析(见表1)显示:胆囊大小>50 cm2、胆囊壁厚度>4 mm、胆囊内胆汁透声差、胆囊结石最大直径>2 cm、胆囊颈部结石嵌顿,是LC难度的危险因素。
2.3 多因素Logistic多元回归分析
将手术时间超过60 min、术中出血≥100 mL、术中放置引流管、术中中转进腹手术等情况定义困难LC,为因变量。是赋值为“1”,否赋值为“0”。以胆囊大小>50 cm2、胆囊壁厚度>4 mm、胆囊内胆汁透声差、胆囊结石最大直径>2 cm、胆囊颈部结石嵌顿为自变量(见表2)。进一步Logistic多因素分析表明(见表3):胆囊大小、胆囊壁厚度、胆囊结石最大直径、胆囊颈部结石嵌顿等4项超声检测指标是困难LC的独立危险因素,此4项为预测LC难易程度的胆囊超声检测的危险因素。
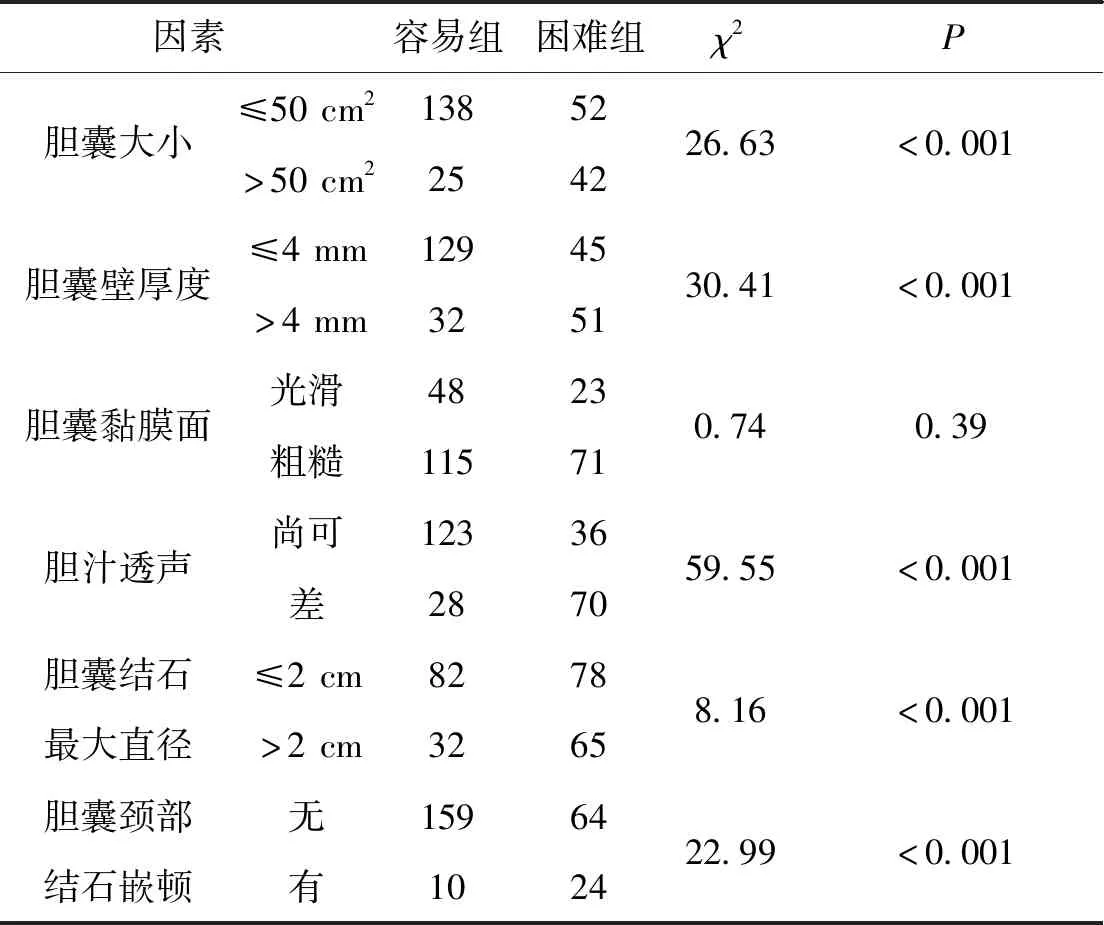
表1 257例术前超声参数与LC手术难易统计及单因素分析表

表2 自变量赋值情况

表3 困难LC的术前超声指标相关危险因素Logistic多元回归分析
由表2知,胆囊大小>50 cm2、胆囊壁厚度>4 mm、胆囊结石最大直径>2 cm、胆囊颈部结石嵌顿,经Logistic多元回归分析,P<0.05,差异均有统计学意义,为困难LC的预测因素。
3 讨 论
腹腔镜胆囊切除术以其手术切口小、创伤小、术后疼痛轻、恢复快的优点,现已成为胆囊良性疾病治疗的“金标准”。但LC也存在一定的不安全因素。在腹腔镜胆囊切除过程中需要解剖胆囊三角,明确胆总管、肝总管和胆囊管三管的位置,而胆囊炎症、解剖变异会增加手术的难度,并且会导致胆管损伤的可能性[6]。困难LC手术同样会增加中转开腹发生率,使术后并发症的发生风险大大升高,同时术中出血量增加、住院时间延长[7]。本文选取手术时间、术中出血≥100 mL、术中是否放置了引流管、是否中转进腹手术具体反映LC手术难度。Alponant等[8]认为手术时间是评价手术难度的良好指标,指出如分离胆囊三角超过30分钟没有进展应视为困难胆囊,因而手术时间是手术难度评估的可靠参考指标,至于术中出血量和手术并发症则更是困难LC的直接结果。
术前预判患者的手术风险以及术中精细化操作,能够降低术中并发症发生[9]。因为术前使用腹部B超、CT、磁共振胰胆管造影能准确评估患者胆囊炎症的程度、周围炎症及三管情况。而腹部超声检查有费用低廉、操作方便的优点,检查迅速可重复,而且可以在一定程度上反映出胆囊疾病的相关状况,如胆囊的大小,胆囊壁的厚度,胆囊内结石数量和大小,胆囊内胆汁透声情况,胆囊黏膜粗糙程度,这些检测指标与LC手术的难易度情况密切相关。此外,超声影像可以检测发现胆囊穿孔、合并肝内外胆管结石和梗阻,合并胰腺炎,肝硬化门脉高压,这些对明确LC手术禁忌症也有明显优势。
术前B超发现胆囊大小,可以反映胆囊炎症程度,评估LC手术难易。刘林勋等对80例LC中转进腹手术的分析后认为,胆囊大小是困难LC中转开腹的危险因素[10]。本研究257例患者中胆囊大小异常者67例,困难手术者42例单因素分析χ2=26.63,P<0.001,Logistic多元回归分析,Waldχ2=13.87,P=0.002,说明胆囊的大小与LC难易程度密切相关,是独立危险因素。这和国内宋宏巨[11]等的结论相符。当胆囊急性炎症时,胆囊内压力增高,渗出增多,胆囊体积增大。肿大的胆囊会有不同程度地存在胆囊三角区及胆囊周围组织的粘连,胆囊浆膜层的水肿,同时也存在胆囊周围组织不同程度的水肿。在胆囊急性炎症病程48小时内,胆囊及周围组织以水肿为主,组织粘连较轻,胆囊浆膜层易于分离,胆囊Calot’s三角粘连较轻,因而手术难度相应较低[12]。而当炎症病程超过72小时时,胆囊三角水肿增厚,组织粘连程度增加,此时解剖胆囊三角、显露分离胆囊管和胆囊血管均变得困难,手术操作时间变长且易引起肝外胆管、胆囊动脉的误伤,易出现术后并发症,也增加了中转开腹的发生率。目前共识,急性胆囊炎病程超过72小时,给予保守抗感染治疗,待症状消失后再进行手术[13]。因此临床可以通过超声检测发现胆囊的大小、水肿程度来筛选、选择LC手术病例。
术前超声可以检测胆囊壁厚度,胆囊壁的厚度可以在一定程度上反映胆囊炎症或纤维化情况。Ficms 等[14]研究结果显示术前超声中胆囊壁增厚是预测困难LC较精确的指标,其敏感度为69%,特异度96.5%,精确度92.5%。本研究发现,胆囊壁厚度与LC难易度呈正相关。本研究中胆囊壁厚度>4 mm的病例有83例,其中手术困难者有51例,单因素分析χ2=30.41,P<0.001,Logistic多元回归分析,Waldχ2=32.45,P=0.001,这说明胆囊壁的厚度是LC难易程度的独立危险因素。胆囊壁厚度与胆囊的炎症反应息息相关,当胆囊炎症反应加重时,胆囊壁的厚度随之增加,厚度>4 mm时,术中发现胆囊周围炎症粘连,解剖层次不清,手术难度增加,强行解剖分离胆囊,手术误伤的可能性增大[15]。
本研究显示,当患者胆囊内结石直径>2 cm时,LC手术会造成腔镜下解剖胆囊三角区操作空间狭小,从而使手术时间延长,手术难度增加,也增加了手术误伤的可能性。在胆囊颈部结石直径>2 cm时会引起胆囊颈部嵌顿、水肿,会波及肝外胆管,使胆囊三角区域粘连,解剖不清[16]。此外,结石直径过大也会影响胆囊从腹腔取出,延长手术时间。本研究257例患者中胆囊内结石直径>2 cm者有97例,手术困难者有65例,单因素分析χ2=8.16,P=0.005,Logistic多元回归分析,Waldχ2= 3.95,P= 0.047,说明术前超声发现胆囊结石最大直径>2 cm是LC手术难易的独立危险因素。这与曹葆强等的研究相一致[13]。
胆囊颈部结石嵌顿是造成LC手术困难的最常见原因之一[17]。本研究有34例患者术前超声检查发现有胆囊颈部结石嵌顿,手术困难者有24例。单因素分析χ2=22.99,P<0.001,Logistic多元回归分析,Waldχ2=12.13,P=0.005,说明术前超声胆囊颈部结石嵌顿是LC难易的独立危险因素。胆囊颈部结石嵌顿时会引起胆汁排出受阻,胆囊内内压增高,胆囊壁炎症加重,胆囊壁的炎性渗出会引起胆囊周围粘连,胆囊三角区域正常解剖结构会发生变形,使胆囊管、胆总管、肝总管三管辨认困难,这些病理变化大大增加了LC的难度,也大大增加了中转开腹,手术操作时误伤胆总管的可能性。因此,术前B超检查评估胆囊颈部结石嵌顿情况,在LC手术操作中尽量减少术中副损伤,预防术后并发症的出现,降低中转开腹手术的概率[18-19]。
胆囊内胆汁透声情况和胆囊黏膜面是否粗糙均为胆囊不同炎症程度的声像图改变。正常胆囊一般黏膜面均是光滑的,当胆囊内因结石导致炎症加重时胆囊内渗出越多,超声影像表现胆囊黏膜面越粗糙。但胆囊黏膜面情况与LC手术难易程度无关。有学者利用胆囊异常回声、胆囊黏膜面粗糙、胆汁透声差、胆囊收缩功能差超声影像指标间接推断胆囊和Calot’s三角粘连,其敏感性和特异性均一般。本临床研究对257例LC手术患者术前B超检测的胆囊黏膜面情况分析,胆囊黏膜光滑的病例有71例,LC手术困难者有23例,胆囊黏膜面粗糙的病例有186例,LC手术困难者有71例,单因素对比分析显示,χ2=0.74,P=0.39,P>0.05,差异无显著性,无统计学意义,说明术前B超检测的胆囊黏膜粗糙程度不是与LC难易程度相关的危险因素。同时超声检测可以显示胆囊内胆汁透声情况,胆囊内胆汁透声的好坏可以间接反映胆囊内环境的情况,当术前超声显示胆囊内胆汁透声好,说明胆囊内结构清晰;术前超声显示胆囊内胆汁透声越差说明胆囊内胆汁粘稠度越高。胆囊内胆汁粘稠度有时也反映LC手术难度。本临床研究对257例患者术前B超检测胆囊内胆汁透声情况分析,术前B超检测胆囊内胆汁透声尚可的病例有159例,LC手术困难者有36例,术前B超检测胆囊内胆汁透声差的病例有98例,LC手术困难者有70例,单因素对比分析χ2=59.55,P<0.001;但Logistic多元回归分析Waldχ2=0.200,P=0.655。单因素对比分析说明胆囊内胆汁透声情况与LC手术难度相关,但Logistic多元回归分析显示胆囊内胆汁透声差并不是导致LC困难的胆囊超声检测指标的危险因素。
诚然LC手术成功与否亦与术者的经验、操作能力、腹腔镜设备先进程度有关。但术前临床病例的选择,手术适应症的把握在一定程度上更为至关重要。本研究发现通过术前超声影像,了解胆囊的大小、胆囊壁厚度、胆囊结石最大直径>2 cm、胆囊颈部有无结石嵌顿这四项指标,术前就可以对LC手术难度进行准确预测,预判LC手术的风险,降低因预估不足带来的手术并发症的发生。
