氮化钛在燃料电池氧还原反应中的研究进展*
2022-06-02汤木娥刘舒钥梁平娟王春媛
汤木娥,周 易,刘舒钥,梁平娟,王春媛,邢 安,张 均
(1.重庆科技学院 冶金与材料工程学院,重庆 401331;2.重庆科技学院 化学化工学院,重庆 401331)
0 引 言
随着世界能源需求总量的持续增长,加快了石油、天然气等化石能源开发利用的步伐,也相继引发全球变暖、环境污染、资源短缺等一系列世界级难题,发展可再生清洁型能源迫在眉睫[1-2]。燃料电池作为最具前景的能源转换技术之一,具有能量转化效率高、环境友好等优点,备受研究者青睐[3-4]。氧还原反应(ORR)是燃料电池阴极重要的电极反应,往往涉及复杂的四电子反应,高度依赖于资源稀缺、价格昂贵、动力学效应迟滞的贵金属铂(Pt),极大限制了燃料电池商业化应用的进程[5-6]。此外,Pt/C作为最常用的催化剂,碳在燃料电池运行下的热力学不稳定,易发生碳载体腐蚀,引发铂纳米粒子(Pt NPs)脱落、迁移、溶解和聚集,导致电化学活性比表面积(ECSA)的退化,并在长时间运行后催化性能和耐久性的急剧退化[7-8]。因此,研制具有低成本、高催化活性、优越稳定性的ORR催化剂是燃料电池技术商业化中极富挑战性的课题。
近年来,过渡金属氮化物由于具有良好导电性、耐久性、抗腐蚀性能,在开发高度耐用的燃料电池载体方面取得了重大进展。作为目前国内外研究学者报道最多的过渡金属氮化物,氮化钛(TiN)中金属-氮键通常会引起金属晶格膨胀和金属能带收缩,使其在费米能级附近维持较高的态密度,表现出出色的导电性和耐腐蚀性以及类似贵金属的潜在催化性能[9-10]。相比金属-氧键,TiN中金属-氮键更倾向于向表面吸附氧分子供给电子。研究表明,可控制备具有良好形貌和结构特征的TiN纳米材料,或在其晶格内掺杂具有富d电子态元素,TiN基催化剂在电催化活性和稳定性方面已经表现出优于商业Pt/C催化剂的潜力。因此,本文基于当前国内外最新研究成果,探讨TiN材料最新的制备方法,综述其作为燃料电池阴极ORR催化剂载体和催化剂时的最新研究进展,并展望其在ORR领域中的应用前景,为设计和发展实用型催化剂材料指明方向。
1 氮化钛材料的制备
TiN属于典型的过渡金属氮化物,具有面心立方晶体结构,其晶格常数为0.4238 nm。TiN晶体结构中离子键、金属键和共价键共存,禁带宽度大约在3.35~3.45 eV,使其表现出高熔点、高硬度、高导热性、化学稳定性等优点。由于Ti-3d轨道与N-2p轨道未完全杂化,N的p轨道能级低于费米能级,自由电子将在Ti d轨道上迁移,使其表现出与Pt、Au、Ag等类似的电子属性。此外,研究发现,TiN材料的(200)晶面(图1)具有活跃的ORR催化活性[11],是ORR催化剂和催化剂载体中极具前景的候选材料之一。
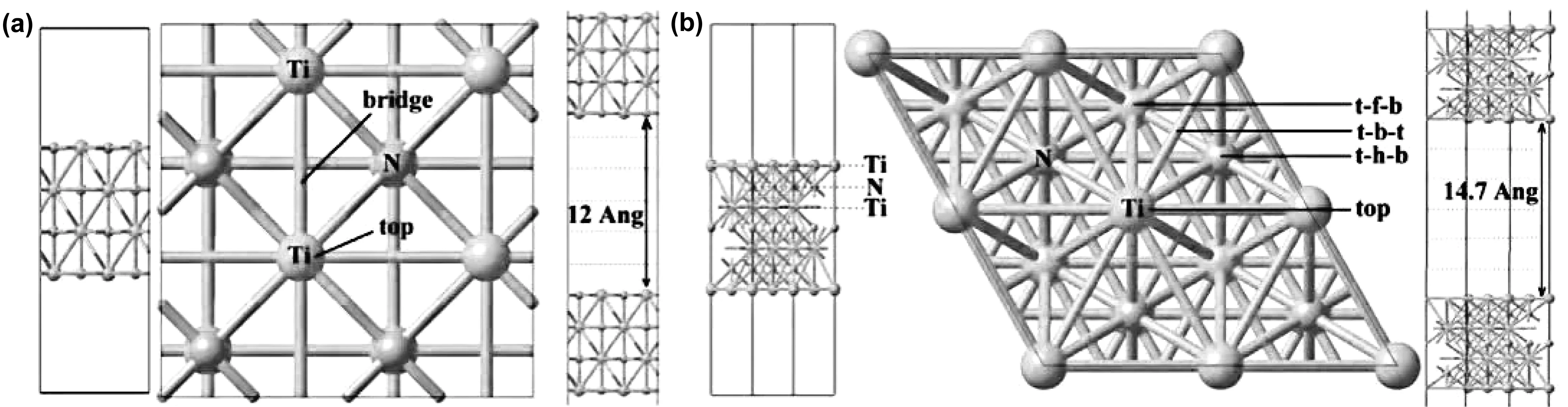
图1 TiN(111)有两个顶部和桥式活性位点(a)和TiN(111)4个顶部(b),(t-b-t),(t-h-b)和(t-f-b)是氧吸附位点[11]
1.1 溶胶-凝胶法
溶胶-凝胶法是制备TiN纳米材料常用的方法之一,将含Ti化合物溶解于水或有机介质中,通过水解、缩合反应,经溶胶凝胶化过程制备含钛氧化物,最后经热处理工艺制备TiN。Kumta等[12]以钛酸异丙酯、乙腈、肼为原料首先合成TiN前驱体,并在N2与NH3作用下800 ℃煅烧即可制备粒径约为10~20 nm,比表面积高达250 m2/g的TiN NPs。Esposito等[13]以四氯化钛为钛源,在N2保护下750 ℃煅烧制备粒径约为14 nm,比表面积高达212 m2/g的TiN NPs。基于溶胶-凝胶法制备的TiN材料通常具有分散均匀、粒径分布宽、比表面积大、纯度高等优点,但该方法也存在原料成本高、对人体危害大等缺点,限制了该工艺的推广。
1.2 溶剂热法
溶剂热法是一种制备TiN材料的新型方法,即首先通过水热反应合成二氧化钛(TiO2)前驱体,然后以NH3为还原剂,经高温煅烧制备TiN材料。Liu等[14]以钛酸四丁酯为钛源,通过水热反应先制备TiO2,并在NH3氛围下经热处理工艺制备具有三维海胆状结构的TiN材料,其平均尺寸为280 nm(图2(a))。Cui等[15]将乙醇酸钛与水在80 ℃回流3 h制备的纳米多孔TiO2与氰胺混合,在NH3氛围下经两步高温煅烧即可制备比表面积约为70 m2/g,孔径为14 nm的介孔TiN材料(图2(b))。Zhang等[16]将碳布(CC)浸入含钛正丁醇(TBT)和乙醇的混合溶液中,经400 ℃退火后分散于丙酮、浓盐酸和TBT的混合溶液中,在200 ℃下水热反应以制备TiO2/CC,并在NH3中900 ℃煅烧制备纳米线状TiN与CC的复合材料(TiN/CC)(图2(c, d))。Hou[17]等以钛酸四丁酯、异丙醇、甘油为原料,通过水热反应合成TiO2,并在NH3氛围中800 ℃煅烧,制备菊花状、粒径约为2 μm的TiN材料(图2(e))。综上所述,溶剂热法合成纳米TiN具有如下优点:(1)NH3不仅可作为还原剂还可充当氮源;(2)通过调控反应前驱体的含量、反应温度、煅烧时间等参数可制备具有不同形貌特征和孔结构的TiN;(3)转化率高。其缺点在于工艺流程耗时长,反应温度高,TiN的形貌结构规整度较差。
1.3 溶盐法
熔盐法是利用低熔点的熔盐作为反应介质,在原子级环境下完成整个反应,经热处理后即可获得TiN。Ding等[18]以TiO2和金属镁粉(Mg)为原料,在500~1100 ℃、N2保护下烧结1~7 h即可制备尺寸为5~30 nm,比表面积为93.09 m2/g的纳米TiN(图2(f)),该团队还探索了TiO2与Mg的摩尔比、反应时间以及温度对TiN生长的影响。Gogotsi等[19]利用氟化盐熔融法,将氟化钾、氟化锂和氟化钠的混合物在550 ℃氩气中热处理30 min,成功将Ti4AlN3MAX相前驱体中的Al去除,得到二维层状结构的Ti4N3材料。熔盐法制备TiN具有操作简便,反应时间短,晶体形貌好,物相纯度高以及盐易分离等优点。但某些熔盐挥发可能会污染和腐蚀炉体,在环保、节能角度有待提高。

图2 (a)三维TiN的SEM图像[14];(b)介孔TiN球的制备示意图[15];(c)TiN/CC的制备示意图和(d)TiN/CC纳米线的SEM图[16];(e)菊花状TiN的SEM图像[17];(f)熔盐法合成TiN粉末的示意图[18]
2 氮化钛在阴极氧还原反应中的应用
2.1 基于氮化钛的铂基催化剂
碳载铂催化剂是燃料电池ORR中最常用的催化剂。与因碳载体腐蚀而致使催化剂活性和稳定性急剧衰减相比[20],具有良好形貌和纳米结构的先进TiN材料,不仅可提高铂利用率、增强金属-载体间相互作用、促进质量/电荷转移和增强耐腐蚀性,在增强催化剂活性和稳定性方面备受关注。
2.1.1 氮化钛载铂催化剂
众所周知,形貌和微观结构是影响TiN电催化性能的重要因素。中空/介孔结构由于具有高比表面积、中空大孔结构、孔结构高度规整、孔径均匀且可调变,不仅有利于活性组分在其表面的有效负载和高度分散,还能缩短反应物/产物在其内部的扩散传质路径,增加电解质溶液和电极材料的接触面积,提高活性位点充分暴露在燃料电池三相反应界面的概率,可极大提高燃料电池电极的活性和耐久性[26]。Pan等[27]报道了具有中空、多孔结构的 TiN纳米管(NTs)作为ORR催化剂载体(图3(a、b))。归因于TiN NTs表面富含台阶和缺陷,可重新捕获、成核Pt原子,从而使TiN NTs载体上Pt NPs的脱落和聚集得到抑制,经过12 000次加速耐久性循环试验后,ECSA保持其初始值的77%。Jin等[28]通过静电纺丝和两步热处理工艺合成了TiN 纳米纤维(TNFs)(图3(c)),经加速应力测试后Pt/TNFs催化剂表现出较高的电化学稳定性。Shin等[29]制备了多孔TiN NTs(图3(d、e)),TiN NTs的电导率为球形TiN NPs的30倍。此外,Pt/TiN NTs[30]、介孔PtAg/TiN[31]也具有优异的ORR活性与稳定性。
通过对Pt表面电子结构的调控,改变Pt d带中心位置,从而引起催化剂表面化学吸附特性的改变是获得优越ORR性能的途径之一。Wu等[32]在一维中空TiN上负载具有高度开放纳米框架结构(NFs)的Pt3Cu,TiN将向Pt3Cu NFs转移电子,并调控Pt活性原子的配位结构,削弱Pt-O/OH的结合能。Lee等[33]采用浸渍法在TiN表面沉积单原子Pt,鉴于TiN中氮空位具有稳定单原子Pt的能力,Pt和TiN载体间强烈的相互作用有助于维持Pt处于还原态,该催化剂对ORR、甲酸氧化反应和甲醇氧化反应均表现出良好的电催化性能。研究发现CO2、CO和H更倾向于吸附在Pt顶部位点,而OH和O更倾向于吸附在Ti顶部位点。当CO与OH在Pt-TiN(100)表面发生共吸附时,OH的存在将削弱催化剂对CO的吸附,OH和H的共吸附也将削弱CO在Pt-TiN上的吸附,因此Pt/TiN催化剂在酸碱条件下表现出优异的抗CO中毒效应[34-35]。TiN载体还通过向Pt NPs转移电子从而引起Pt NPs具有更多还原态并降低Pt d带中心,吸附的氧分子更易与Ti位点结合,因而减轻了催化剂表面中毒并提高催化剂稳定性[36]。密度泛函理论计算表明相比碳载Pt催化剂,TiN载Pt催化剂具有更高的耐久性[37]。研究发现TiN、石墨和石墨烯分别向吸附Pt转移0.3、0.1和0.1静电荷量,Pt和Ti间强相互作用,促使单个Pt原子在TiN上的结合强度是碳载体的2.4~4.6倍。在投影态密度中Ti 5d与N 2p分别发生上移与下降,表明Ti位点将提供电荷,而N位点将接收电荷。此外,吸附在TiN和石墨烯上的Pt d带中心分别为-1.91 eV和-0.97 eV,因此Pt在TiN上的稳定性优于石墨烯(图3(f-h))。

图3 (a)TiN NTs的TEM图像,插图为其选取电子衍射图和(b)在(a)中标记区域的放大TEM图像[27];(c)TiN TNFs的SEM图[28];(d)支架状TiN NTs和(e)Pt/TiN NTs的HR-TEM图像[29];(f)和(g)为TiN、石墨烯上Pt 5d态的投影态密度,(h)Pt在TiN与石墨烯上吸附时的电荷密度差异[37]
2.1.2 过渡金属掺杂氮化钛载铂催化剂
通过在TiN中掺杂过渡金属与Pt形成Pt-M合金,使Pt d带中心位置下降,并改变含氧中间物与催化剂间的吸附特性,是提高ORR本征催化活性的有效策略。同时,金属与N原子间会形成具有较高金属键能的M≡N,赋予TiN基催化剂高稳定性[38]。Pan等[39]通过水热法和氨化法合成了钴(Co)掺杂TiN(Ti0.9Co0.1N NPs)作为Pt基催化剂载体,Co掺杂将增加Pt(0)含量,且Ti0.9Co0.1N载体向Pt转移电子,增强了Pt与Ti0.9Co0.1N载体间的强相互作用。因此在酸性条件下Pt/Ti0.9Co0.1N催化剂具有优异的ORR性能。
通常,特殊孔结构具有高比表面积,可实现Pt的均匀分散,提高Pt利用率,进而增加参与ORR活性位点数量,增强ORR性能。如铌(Nb)掺杂介孔TiN(Ti0.5Nb0.5N)载Pt催化剂在酸性和碱性介质中的半波电位分别为0.94、0.9 V,优于Pt/C催化剂[40]。Tian[41]等成功制备了镍(Ni)掺杂TiN载Pt催化剂(Pt/Ti0.9Ni0.1N NTs)催化剂(图4(a、b))。循环15 000次后,质量活性仍为Pt/C的3.2倍。同时,Cui等[42]在铬(Cr)掺杂介孔Ti0.5Cr0.5N上负载了结构有序的Fe3Pt NPs(Fe3Pt/Ti0.5Cr0.5N)。在酸性条件下经5 000次循环后,催化剂活性仅损失9.7%。此外,Liao等[43]通过脉冲沉积法,在Ni掺杂TiN(TiNiN NPs)上沉积超薄Pt层,结果表明,TiNiN@Pt在酸性条件下半波电位为893 mV,经10 000圈稳定性测试后,保持了原ECSA的79%。
2.1.3 氮化钛/碳复合载铂催化剂
尽管TiN作为Pt基催化剂载体可显著提升催化剂电催化活性和稳定性,但TiN NPs或其介孔结构中存在大量晶界和缺陷,可能会降低催化剂电导率和电子传输效率[44]。鉴于碳材料独特的多孔结构和高导电性,研究人员往往将TiN与碳材料组成复合载体来增强催化剂ORR性能[45]。
Zhang等[46]首次构建了二维层状介孔双过渡金属氮化物与石墨烯载Pt(Pt/TMNs/G)材料。他们发现Pt/Ti0.5Cr0.5N/G在酸性、碱性条件下的半波电位分别为0.84、0.91 V,且经5 000次循环伏安测试后,半波电位仅分别负移14、10 mV(图4(c-e))。Liao等[47]在氮掺杂碳纳米管(N-CNTs)负载Ti0.9Cu0.1N NPs上沉积超薄Pt层制备新型氮化物载低Pt催化剂(Ti0.9-Cu0.1N@Pt/NCNTs)。该催化剂的质量活性是商业Pt/C的5倍,且经10 000次循环伏安测试后,性能几乎没有衰减。此外,Zhang等[48]采用静电自组装法和氨化法首次构建了新型中空介孔氮掺杂石墨烯(N-G)包裹介孔TiN NPs(@M-TiN/N-G)复合材料(图4(f-h))。在酸性、碱性条件下@M-TiN/N-G(5)/Pt(13.5)具有优异的ORR性能且测试10000 s后电流密度仅分别衰减15.6%、2.3%。这些氮化钛/碳复合载铂催化剂活性优越的原因是由于石墨烯具有大比表面积和二维平面结构的优势,不仅可有效负载、分散金属,还可调变催化剂结构。同时,石墨烯具有良好的导电性,可与负载的金属或金属化合物形成很强的电子协同作用,能调控催化活性组分的电子特性,增强其催化功能。
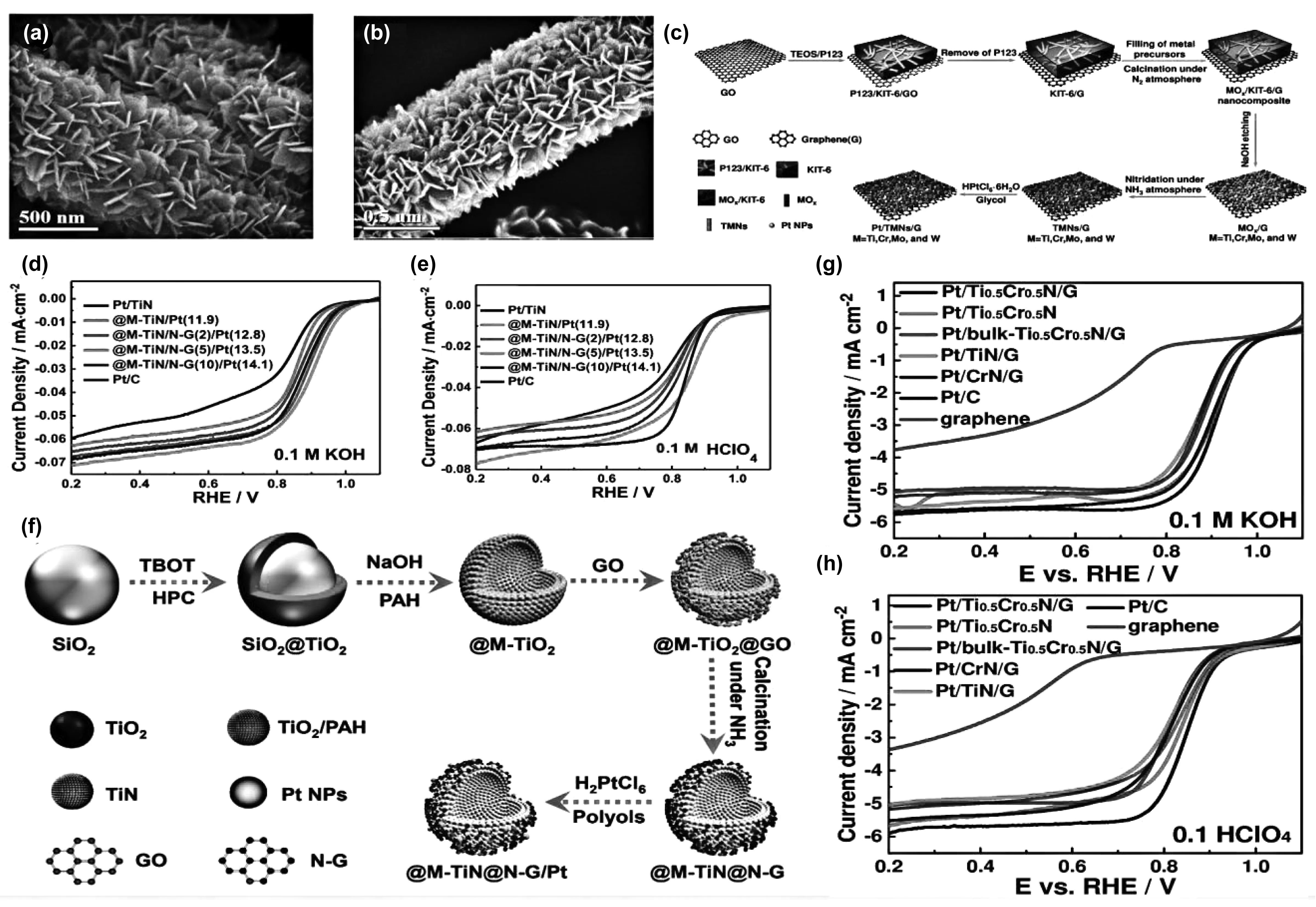
图4 (a)Ti0.9Ni0.1N NTs放大的SEM图像和(b)Pt/Ti0.9Ni0.1N NTs的SEM图像[41];(c)二维介孔Pt/TMNs/G的制备示意图,不同催化剂在(d)氧气饱和的0.1 mol/L KOH溶液和(e)0.1 mol/L HClO4溶液中的极化曲线[46];(f)中空介孔壳状@M-TiN/N-G/Pt的制备示意图,不同催化剂在(g)氧气饱和的0.1 mol/L KOH溶液和(h)0.1 mol/L HClO4溶液中的极化曲线[48]
2.2 氮化钛非贵金属催化剂
综上所述,TiN载Pt贵金属催化剂在ORR领域表现出优异的电催化性能。然而,受制于Pt储量稀少,价格昂贵,开发新型非贵金属催化剂已成为推动ORR快速发展中极具挑战性的课题。近年来,TiN凭借其优异的导电性,耐蚀性与调控活性组分电子结构的能力,表现出类似贵金属的潜在催化性能,TiN现已成为最有潜力的ORR催化剂之一。
2.2.1 氮化钛催化剂
1966年Giner等[49]证明了TiN在碱性介质中的ORR活性优于纯钛和金属锆、铪。随后Kazunari等[50]通过对比TaN、NbN、TiN等过渡金属氮化物时发现,TiN在酸性介质中表现出最佳的ORR性能。此外,Zhou等[51]通过对比微米(0.5~2 mm)和纳米级(4 nm)TiN在碱性介质中的ORR催化活性,证明纳米级TiN相较于微米级TiN有更优的催化活性。两种尺寸TiN在催化机理上存在差异,其中微米级TiN以“连续二电子”途径催化ORR,而纳米级TiN催化ORR时,两个“二电子”步骤以较小间隔进行,即O2还原为HO2后,HO2立即开始反应,并没有表现出整体可区分的步骤。此外,纳米和微米TiN都对ORR表现出电催化活性,尤其是纳米TiN,可与纳米四氧化三锰媲美。
2.2.2 过渡金属掺杂氮化钛催化剂
与贵金属Pt基催化剂相比,TiN催化剂在提升ORR性能方面仍存在一定差距。目前,基于电子效应,将具有富d电子态的过渡金属掺杂进入TiN晶格,将促进Ti d态电子密度增加,进而提高TiN的电催化性能。Liao等[52]将Ni掺杂在TiN NPs中制备了Ti0.95Ni0.05N催化剂(图5(a))。在0.1 mol/L HClO4溶液中,该催化剂的起始电势为0.85 V,极限扩散电流密度为4 mA/cm2。在耐久性测试后,其电流密度仅略微下降。这是由于掺杂的过渡金属Ni将向Ti传递电子,使Ti原子的d带空位减少,促使Ti的d电子在费米能级附近具有更高的浓度,增加了催化剂向吸附氧供给电子的能力,进而增强ORR活性。该课题组还通过溶剂热法合成了管状Ti0.8Co0.2N(图5(b-d))[53]。由于Co掺杂引起TiN的电子结构的改变,提高了TiN的固有活性。
2.2.3 氮化钛/碳复合催化剂
近年来,利用碳载体的高导电性、比表面积等优势,将TiN负载在各类碳载体上,可增强TiN的电子转移效率、传质速率以及活性位点数量,从而进一步提高ORR性能。
(1)氮化钛/碳材料
Kazunari等[54]通过耦合TiN的催化活性与碳黑(CB)的导电性成功制备了TiN/CB,并作为聚合物电解质燃料电池ORR的有效催化剂。Li等[55]以三聚氰胺作为碳源成功合成了碳包覆TiN NTs催化剂。结果表明,碳包覆TiN NTs在碱性条件中起始电位为-0.17 V,且经25 000 s测试后,电流密度仅衰减15%。Jun等[56]通过分子协同组装合成了双峰介孔TiN/C微纤维,可有效催化ORR和析氧反应。同时,Wang等[57]采用硬模板法制备了TiN中空球(HSs)。通过调节煅烧温度和碳含量,在提高催化剂电导率的同时形成更多N-C活性位点。因此TiN HSs-325在碱性介质中表现出高ORR活性与稳定性,起始电位为0.85 V,且极限扩散电流密度达4.5 mA/cm2。
将具有特殊结构及大比表面积的石墨烯材料与TiN结合,可极大提高TiN的分散程度、传质速率以及活性位点数量。如Ghorbani[58]等使用超临界苯介质合成了TiN/C/石墨烯复合材料(SIV),在0.1 mol/L NaOH溶液中SIV具有四电子催化途径,H2O2产量约为16%,减轻了催化剂表面中毒。Lee等[59]通过urea-glass路径制备了TiN,并负载在碳纳米管和石墨杂化形成的复合材料上(CNT-GR),形成TiN/CNT-GR(图5(e))。TiN/CNT-GR在酸性介质中起始电位达0.83 V。此外,Olabi等[60]通过水热法在还原氧化石墨烯(Gr)表面上制备了Co NPs与TiN的复合材料(Co-TiN/Gr)。由于热处理过程中硝酸钴前驱体分解为钴基氧化物,激发钴基氧化物和TiN间协同作用,同时GO还原过程中形成氮掺杂Gr,Co-TiN/Gr在酸性介质中的起始电位为0.925 V,且经1 000次循环伏安测试后,性能无明显衰减。
(2)氮化钛/氮掺杂碳材料
由于氮原子与碳原子电负性的差异,将氮原子掺杂进碳骨架中,将改变催化剂表面的电子构型,为氧气分子及其还原中间体的选择性吸附创造更多活性位点[61]。同时,比碳原子多一个电子的氮原子掺杂将使碳材料的费米能级更接近导电带,赋予其更强的导电性。此外,碳与氮间形成强共价键,也可增强其稳定性[62-63]。Li等[64]通过一步煅烧法成功合成了氮掺杂石墨烯(NG)载TiN(TiN/NG)催化剂。TiN/NG在碱性介质中起始电位为-0.13 V,同时在持续测试25 000 s后,其电流密度仅衰减10%且具有优异的抗甲醇性能。在TiN上沉积一层氮掺杂碳材料是提高复合材料导电性和稳定性的另一种方法。Liao等[65]通过浸渍法和后氮化法制备了三维氮掺杂碳层Ti0.95Co0.05N复合材料,在碱性条件下20% C-Ti0.95Co0.05N具有接近20% Pt/C的催化活性(图5(f))。同时,Zhang等[66]采用双氰胺作为氮源合成了氮掺杂碳材料(NC)包覆的Ti0.95Co0.05N复合材料(Ti0.95Co0.05N@NC)。Ti0.95Co0.05N@NC在碱性介质中的半波电位为0.76 V。
除上述氮掺杂碳材料外,石墨烯是碳原子以sp2杂化轨道组成的纳米薄片,将杂原子掺入石墨碳的sp2晶格中可改变电子供体的性质,为氧吸附创造活性位点,并通过过渡金属氮化物和氮掺杂氧化石墨烯(N-rGO)间的协同作用可赋予催化剂高ORR活性。例如,Liao等[67]通过将 TiCoNx载于N-rGO 上构建了新型TMN/N-rGO复合催化剂(图5(g、h))。XPS结果表明过渡金属氮化物与N-rGO结合可改变含N物种的含量和分布,且由于Co原子的引入,Ti原子从Co原子得到电子,导致费米能级附近Ti原子d带电子浓度增加,增加向吸附氧物质供给电子数量,从而促进ORR性能。因此,TiCoNx/N-rGO 在碱性介质中表现出优异的氧还原活性,具有长期稳定性和甲醇耐受性。
(3)氮化钛/金属-氮-碳材料
以Fe-N-C为典型代表的金属-氮-碳催化剂,因具有高比表面积、新颖的电子结构和性质、Fe-Nx和C-N催化活性位点等优势,在提高ORR反应动力学速率上备受关注[68]。然而,在酸性介质中,Fe活性中心将与ORR中间产物H2O2发生Fenton反应,致使碳原子表面发生氧化反应,极大削弱Fe-N-C催化剂的稳定性,限制了其进一步发展和应用[69-70]。基于TiN材料优越的化学稳定性、优良的耐腐蚀性能,有望研发具有催化活性位点充分暴露、导电性良好、电化学稳定性优异的新型TiN/Fe-N-C复合催化剂。Li等[71]采用原位自模板法制备了TiN NPs与Fe、N共掺杂碳纳米片层状复合材料(TiN/Fe-N-CNS)(图5(i))。在TiN/Fe-N-CNS中吡啶氮和石墨氮含量相对较高,可促进铁活性中心的形成;TiN可诱导形成更多Fe-Nx活性位点,TiN/Fe-N-CNS在碱性条件下半波电位达0.87 V,且经过25 000 s测试后,电流密度分别保持初始值的95.4%。
3 结 论
为缓解资源匮乏与环境污染问题,燃料电池技术逐渐得到发展。在本综述中,总结了TiN在燃料电池ORR中的研究进展。将TiN作为贵金属载体可调控Pt表面电子结构,同时在TiN中掺杂过渡金属时,掺杂过渡金属与Pt间形成Pt-M合金也可有效调控Pt的电子性质,导致Pt d带位置下降,从而改变催化剂与含氧中间物的吸附特性,提高ORR活性。此外,TiN具有优异的电导性和耐腐蚀性,本身可作为氧化还原反应的催化剂。因此制备不同结构TiN对提高ORR中传质、电子转移、活性位点暴露具有重要作用,并且TiN中的Ti原子可从掺杂的过渡金属得到电子,使Ti原子的d带空位减少,从而使Ti的d电子在费米能级附近具有更高的浓度,增加催化剂向吸附氧供给电子的能力[52]。最后,TiN与碳材料形成复合材料可提高催化剂导电性,从而使得ORR活性得到增强。尽管对TiN基催化剂的研究已取得相当大的进展,但仍存在许多不足。因此,可从以下基本方面进行进一步研究。
(1)为降低成本,当TiN作为ORR载体时,负载贵金属载量应尽可能小,故贵金属的负载方法及负载形式是需面临的挑战;(2)为建立高效TiN催化剂的调控制备方法,构建结构和性能间相互作用模型是TiN合成过程中需考虑的另一个问题;(3)过渡金属与TiN界面处金属键的形成机理和调控规律尚不明确,此外,ORR机理与动力学理论不足。因此,根据理论计算模拟,探索TiN催化氧还原的基本规律,从本质上解释催化剂活性及稳定性增强机理,对实现燃料电池商业化与大规模应用至关重要。
