鸡蛋中氟苯尼考质控样品的研制及稳定性评价
2022-06-02蔡若纯邓皇翼刘耀慧刘鹏展罗志浩刘海虹
蔡若纯,邓皇翼,刘耀慧,刘鹏展,罗志浩,刘海虹,雷 毅
(广东省食品检验所,广东 广州 510435)
氟苯尼考又称氟甲砜霉素,是新一代氯霉素类动物专用抗生素,具有抗菌谱广、毒副作用小等特点,是农业部批准使用的动物专用抗菌药,被广泛应用于动物养殖业[1-2]。GB 31650—2019《食品中兽药最大残留限量》[3]规定了不同动物种类的氟苯尼考兽药最大残留限量,其中产蛋期禁止使用氟苯尼考。国家食品药品监督管理局也对氟苯尼考做出风险提示,成人(以60 kg计算)每日从饮食中摄取 0~180 μg的氟苯尼考,正常情况下不会有风险,但长期食用氟苯尼考残留超标的鸡蛋,对人体健康会产生一定危害[4]。
目前氟苯尼考的实验室检测方法主要有气相色谱法[5-7]、高效液相色谱法[8-9]、液相色谱-质谱联用法等[10-13],检出限范围为0.1~1.0 μg/kg。由于兽药残留大部分为痕量检测,在日常检测及方法确认过程中,常采用加标回收和基体标准样品等质控手段进行质量控制[14-15],但加标回收难以反映出真正阳性样品的提取效率,而现有基体标准样品的价格昂贵、基质品种有限,未能满足实际工作需求。此外,随着食品快速检测方法的发展,因快速检测产品具有操作简便、成本低、检测周期短等特点,快速检测方法和技术逐渐广泛应用于氟苯尼考兽药残留的现场筛查[16-18]。在快速检测产品[19]和快检方法评价[20]验证过程中往往需要自制特定项目、基质和浓度的质控样品,对快速检测产品性能指标和快速检测整体过程进行质量控制。本研究从日常快速检测和实验室检测的不同需求出发,最终设置0.25、0.4 μg/kg和2.0 μg/kg三个添加量,提供一种鸡蛋中氟苯尼考质控样品研制方法,弥补有证的基体标准物质却可选项目少、浓度水平单一、采购成本高、定制周期长等问题,同时探究影响氟苯尼考质控样品稳定性的因素,自主研制均稳性良好的质控样品可推广应用于快速检测及实验室检测等不同领域。
1 材料与方法
1.1 材料与试剂
鸡蛋 市购;氟苯尼考标准物质(99.82%) 德国Dr.Ehrenstorfer公司;正己烷、丙酮(均为分析纯)广州化学试剂厂;正丙醇(分析纯) 天津市永大化学试剂有限公司 ;乙腈(色谱纯) 德国Merck公司;实验用水均为超纯水。
1.2 仪器与设备
T Q-S 超高效液相色谱-三重四极杆质谱联用仪美国Waters公司;GM200刀式研磨仪 德国Retsch公司;Scientz 50F/A真空冷冻干燥机 宁波新芝生物科技股份有限公司;EFAA-HM-01多孔涡旋振荡器 上海ANPEL科技股份有限公司;Multifuge X3R高速冷冻离心机 美国Thermo Fisher Scientific公司;RV10旋转蒸发仪 德国IKA公司;HBE-12B固相萃取装置 天津市恒奥科技发展有限公司;Milli-Q 超纯水制备仪德国Merck公司;国产标准试验筛(40 目)。
1.3 方法
1.3.1 基质的选择与准备
采用GB/T 22338—2008《动物源性食品中氯霉素类药物残留量测定》[21]对样品中氟苯尼考的含量进行检测,检测结果数值低于方法检出限,则选择作为制备质控样品的空白基质。
1.3.2 方法回收率
为确保仪器检测质控样品均匀性和稳定性结果的科学性,在开展质控样品制备之前先验证鸡蛋中氟苯尼考添加回收率[22-23]。选取不含氟苯尼考的鸡蛋为空白基质,预处理匀浆后制成鸡蛋液,根据快检产品及快检方法评价技术规范相关要求质控样品以1~2 倍氟苯尼考快检方法或产品检出限为典型含量水平,同时为更好应用于实验室氟苯尼考检测的质量控制,质控样品充分考虑满足不同检测方法的鸡蛋氟苯尼考检出限范围为0.1~1.0 μg/kg,氟苯尼考标准物质的添加量为0.25、0.4 μg/kg和2.0 μg/kg三个水平,采用GB/T 22338—2008的方法检测其含量,并计算回收率。
1.3.3 质控样品的制备
以不含氟苯尼考的鸡蛋液为空白基质,添加一定的氟苯尼考标准物质,添加量为0.25、0.4 μg/kg和2.0 μg/kg三个水平,4 000 r/min均质混匀2 min(采用20 s间歇式搅拌,搅拌6 次)制备成氟苯尼考阳性新鲜质控样品(非冻干组),将新鲜质控样品经过24 h冷冻干澡、2 次混匀(4 000 r/min均质混匀2 min)、过40 目试样筛及分装等步骤,制备成氟苯尼考阳性冻干质控样品(冻干组),具体制备流程如图1所示。

图1 鸡蛋中氟苯尼考质控样品的制备流程Fig.1 Preparation process of quality control samples for determination of florfenicol in eggs
1.3.4 质控样品中氟苯尼考的检测
准确称取一定量的新鲜阳性质控样品或冻干阳性质控样品(其中冻干样品按照1∶4比例加蒸馏水复溶,涡漩混匀恢复至蛋液状态),采用GB/T 22338—2008方法进行测定,冻干样品结果以复溶后样品质量计算,保留小数点后两位。
液相色谱条件:ACQUITY UPLC BEH C18色谱柱(180 mm×2.1 mm,3.5 μm);流动相:A为水,B为乙腈;梯度洗脱程序:0~1.0 min,90% A、10% B;1.0~3.5 min,90%~10% A、10%~90% B;3.5~4.5 min,10% A、90% B;4.5~4.6 min,10%~90% A、90%~10% B;4.6~6.0 min,90% A、10% B。流速0.35 mL/min;柱温35 ℃;进样体积1 μL。
质谱条件:电喷雾离子源;负离子模式;多反应监测模式;电喷雾电压3.5 kV;离子源温度500 ℃;碰撞气为氩气;干燥气为氮气;流量1 000 L/h。质谱参数见表1。

表1 氟苯尼考的质谱参数Table 1 Mass spectrometric parameters for determination of folrfenicol
1.3.5 质控样品的均匀性评估
依据CNAS-GL003:2018《能力验证样品均匀性和稳定性评价指南》[24]和RB/T 031—2020《能力验证计划的选择与核查及结果利用指南》[25]要求,随机称取上述冻干组(固态)和非冻干组(液态)氟苯尼考质控样品各10 份(n=10),每份样品重复测定2 次,并采用单因子方差分析法计算F值,进行均匀性评估分析。若计算得到的方差分析F<F0.05(9,10),则判定样品均匀性良好。
1.3.6 质控样品的稳定性
1.3.6.1 短期稳定性
参照CNAS-GL003:2018,每隔1 个月随机抽取6 个样品(n=6),采用独立样本t检验法,与均匀性检验数据的初始值进行比较分析,从而监测不同制备方式、贮存温度、加标量条件下样品中氟苯尼考含量变化,考察各条件对短期稳定性的影响。
将上述冻干组和非冻干组质控样品置于-18 ℃贮存,考察不同样品状态对质控样品稳定性的影响。
将冻干组质控样品分别置于25、4、-18 ℃贮存,考察不同贮存温度对冻干质控样品稳定性的影响。
将3 个添加量的冻干组质控样品置于-18 ℃贮存,考察不同加标量对冻干质控样品稳定性的影响。
1.3.6.2 长期稳定性
长期稳定性研究12 个月,每隔3 个月时间随机抽取6 个样品,平行测定2 次取平均值,采用t检验法对数据进行统计分析。
1.3.7 质控样品的定值
参照CNAS-CL04:2007《标准物质标准样品生产者能力认可准则》[26]和JJF 1343—2012《标准物质定值的通用原则及统计学原理》[27]。本研究选取冻干质控样品为例,采用6 家中国合格评定国家认可委员会认可的实验室进行联合定值的方式,给每个实验室发放3 份质控样品,每个样品测定2 次平行,采用实验室认可的国家标准检测方法分别测定氟苯尼考含量,通过吉布斯G检验和科克伦C检验判定检测结果无异常值后,最终将测定的总平均值作为质控样品的参考值。
2 结果与分析
2.1 添加回收率结果
选取经GB/T 22338—2008方法确证不含有氟苯尼考的鸡蛋作为空白基质,分别添加0.25、0.4 μg/kg和2.0 μg/kg三个水平的目标物,验证鸡蛋中氟苯尼考回收率。经仪器测定结果表明本方法添加氟苯尼考回收率在85.8%~113.7%之间(表2),符合GB/T 27417—2017《合格评定化学分析方法确认和验证指南》[28]方法回收率偏差范围相关要求,表明仪器检测方法准确、可靠。
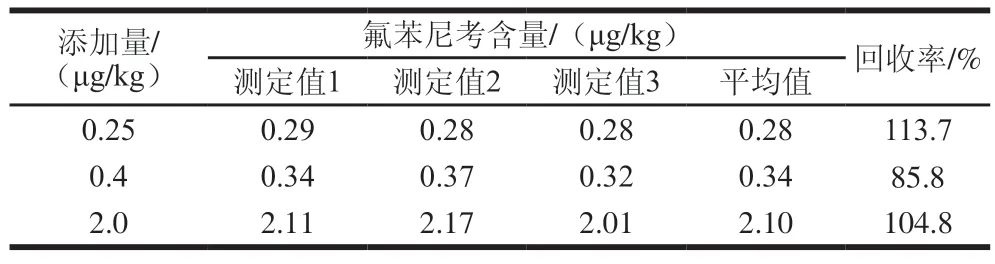
表2 鸡蛋中氟苯尼考回收率Table 2 Recoveries of florfenicol spiked in eggs
2.2 氟苯尼考质控样品的均匀性
采用GB/T 22338—2008方法分别测定非冻干组(A)和冻干组(B)质控样品3 个添加量的氟苯尼考含量,测量结果采用单因子方差统计分析法(F检验)分析处理,SPSS软件分析实验结果的F值,结果见表3和表4。
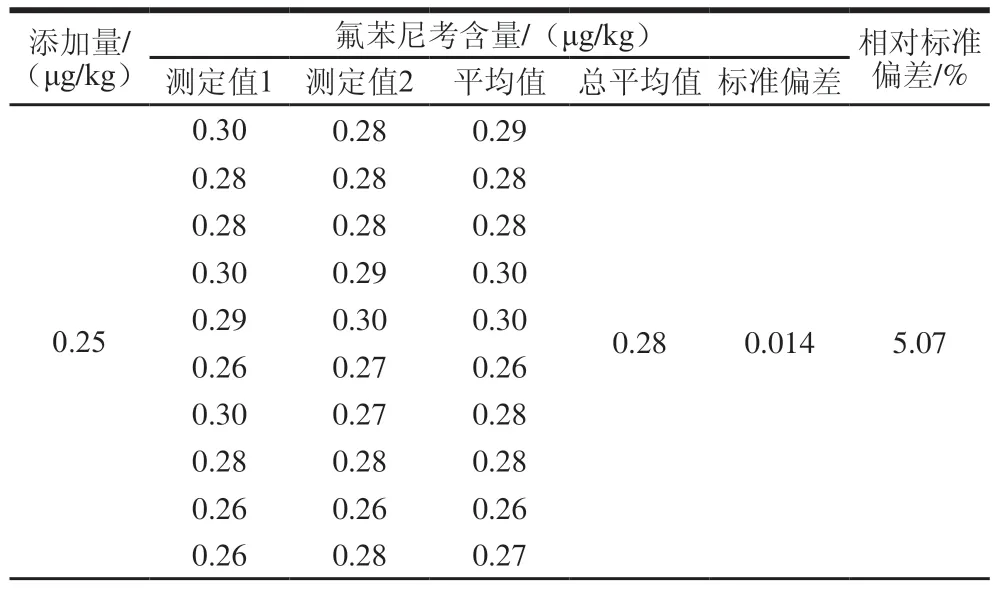
表3 非冻干组(A)质控样品均匀性检验结果Table 3 Results of homogeneity test for non-lyophilized samples (A)

续表3

表4 非冻干组(B)质控样品均匀性检验结果Table 4 Results of homogeneity test for non-lyophilize samples (B)
实验测试的组内自由度为10,组间自由度为9,经统计分析,非冻干组(A)3 个水平的F值在2.562~2.914之间,冻干组(B)3 个添加量的F值在1.970~2.804之间,均小于临界值F0.05(9,10)=3.020,P值均大于0.05,表明在显著水平α=0.05时,添加同一添加量的样品之间不存在显著性差异,添加的氟苯尼考标准物质在鸡蛋基质中均匀分散,均匀性验证方差分析结果见表5。

表5 均匀性验证方差分析结果Table 5 Results of variance analysis
2.3 氟苯尼考质控样品的稳定性
2.3.1 短期稳定性
2.3.1.1 样品状态对质控样品稳定性的影响
制备分装完成的非冻干组(液态)和冻干组(固态)质控样品分别置于-18 ℃贮存,每隔1 周检测1 次,每组测定6 个样品,检测平均值即为质控样品氟苯尼考含量,监测3 个月内2 组质控样品目标物含量变化。从图2可以看出,冻干质控样品较非冻干质控样品含量变化趋势更平缓。按CNAS-GL003:2018稳定性检验要求,将每次检测平均值与初始检测平均值进行一致性比较,计算t值,其中冻干质控样品第1个月至第3个月的t值在0.802~1.641之间,均小于t临界值(2.145)。非冻干质控样品第1个月至第3个月的t值在2.786~7.472之间,第3个月t值大于t临界值(2.145)。结果表明冻干质控样品较非冻干质控样品在-18 ℃条件贮存3 个月的短期稳定性更高。
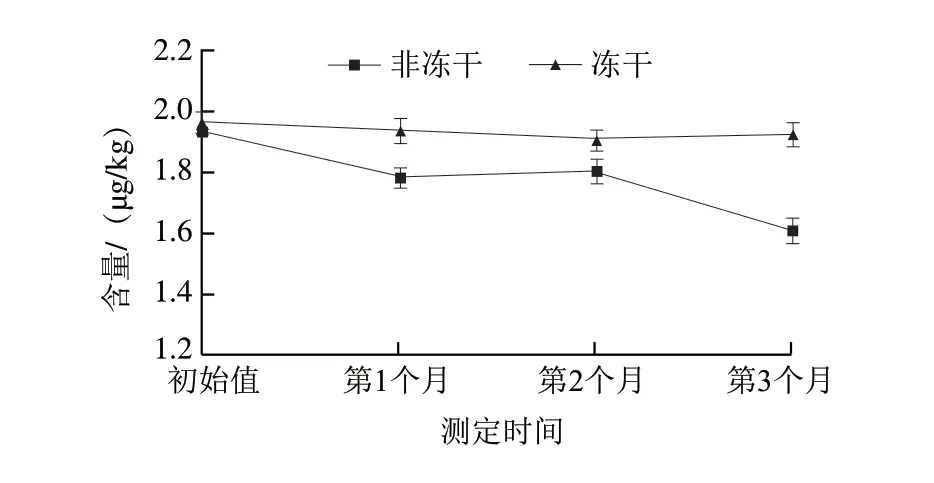
图2 样品状态对质控样品稳定性的影响Fig.2 Impact of sample state on the stability of quality control samples
冻干质控样品基本不含水分,在-18 ℃贮存条件下鸡蛋的蛋白质不易发生不可逆变性,因此其抗冻性和稳定性较强。目前已有相关研究表明鸡蛋主要成分卵白蛋白经过冷冻干燥后,结构上并未发生断裂和重组,并且化学性质均未发生明显变化,说明冷冻干燥处理不会对鸡蛋中蛋白质产生较大影响[29-30]。与冻干组相比,非冻干组样品在冷冻过程中容易产生蛋白质变性,使与蛋白质结合的氟苯尼考状态受到一定程度的影响,此外蛋白质不可逆变性产生的絮状物分层也影响了样品基质的分散性和稳定性,从而导致非冻干组质控样品稳定性降低。综上,分析原因可能是冻干组样品抗冻能力强,蛋白质不易变性使其具有更高的稳定性。
2.3.1.2 贮存温度对质控样品稳定性的影响
冻干质控样品不容易变质,可以在不同条件下贮存,日常检验工作应用也更为广泛,因此本研究以冻干质控样品为对象,探究温度条件对质控样品稳定性的影响。将制备分装完成的冻干质控样品分组放置于25、4、-18 ℃贮存,监测3 个月内不同温度贮存的质控样品目标物含量变化,由图3可以看出,-18 ℃组质控样品氟苯尼考含量变化趋于平缓,25 ℃组和4 ℃组质控样品氟苯尼考含量在第3个月有明显下降。

图3 不同贮存温度对质控样品稳定性的影响Fig.3 Impact of storage temperature on the stability of quality control samples
经t检验,冻干质控样品在-1 8 ℃条件贮存1~3 个月的t值范围在0.802~1.641之间,均小于t临界值(2.145)。在25 ℃条件下贮存1~3 个月的t值在0.458~8.501之间,第3个月t值为8.501,大于t临界值(2.145)。在4 ℃条件下贮存1~3 个月的t值在1.053~4.845之间,其中第3个月t值为4.845,大于t临界值(2.145)。上述结果表明质控样品在-18 ℃条件下贮存3 个月的短期稳定性良好,且较4 ℃和25 ℃条件贮存更为稳定。分析原因可能是受微生物繁殖的影响,由于质控样品制备过程未进行灭菌处理,样品存在有一定基数的微生物,其中鸡蛋中主要的微生物种群为沙门氏菌、大肠杆菌、李斯特菌等,其最适生长温度在20~40 ℃之间,在25 ℃(常温)条件贮存微生物生长繁殖最快,所以添加的抗生素在微生物作用下迅速降解。而贮存温度降低则会明显减缓微生物的生长繁殖,从而降低氟苯尼考的消耗和降解速率,故在-18 ℃(冷冻)条件下贮存的质控样品氟苯尼考含量变化趋势平缓。目前已有研究表明微生物对氟苯尼考等抗生素的降解起主导作用[31-32],这说明贮存温度对氟苯尼考质控样品稳定性的影响可能主要来自对微生物繁殖的影响。
2.3.1.3 加标量水平对质控样品稳定性的影响
将不同添加量的冻干质控样品置于-18 ℃贮存,监测3 个月内不同添加量的质控样品氟苯尼考含量变化,由图4可以看出不同添加量(0.25、0.4 μg/kg和2.0 μg/kg)的质控样品目标物含量变化趋势均较为平缓。经t检验,0.25 μg/kg的质控样品稳定性检验t值在0.684~1.932之间,0.4 μg/kg的t值在0.437~1.689之间,2.0 μg/kg的t值在0.802~1.641之间,均小于t临界值(2.145)。上述结果表明不同浓度质控样品在-18 ℃条件下贮存3 个月的短期稳定性良好。
2.3.2 长期稳定性
将不同含量分装好的冻干质控样品贮存于-18 ℃,放置12 个月,期间每间隔3 个月随机抽取6 份进行测定,监测该质控样品长期稳定性,所有t值均小于t临界值(2.145),结果见表6。结果表明不同添加量的质控样品在12 个月存储期间,稳定性良好。

表6 质控样品的长期稳定性测定结果Table 6 Results of long-term stability test for quality control samples
2.4 质控样品的定值
本研究按照自主研制3 个添加量的氟苯尼考质控样品,经均匀性和稳定性验证结果满足CNAS-GL003:2018相关要求,以冻干质控样品(固态)为例,选取6 家CNAS认证的实验室,采用GB/T 22338—2008标准方法检测冻干质控样品目标物含量,分别汇总各组参加合作定值数据,结果见表7。
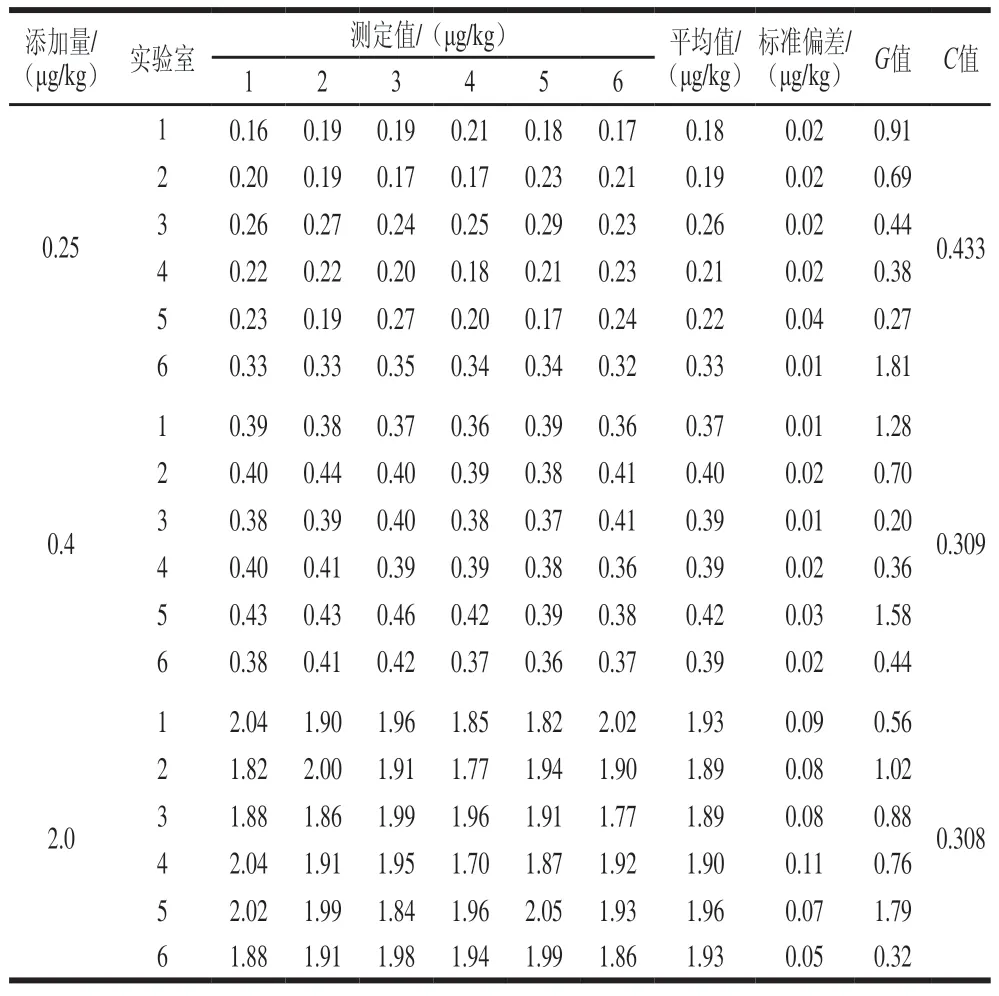
表7 质控样品的定值数据及结果Table 7 Analytical results for certification of quality control samples
通过吉布斯检验,发现所有实验数据G值均不大于G0.05临界值(查表得1.89),表明数据不存在异常值,再通过用科克伦检验确定6 个实验室对不同添加量质控样品的检测数据C值不大于C0.05(6,6)临界值(查表得0.445),表明没有随机误差太大的实验室,各实验室间的测量属于等精度测量,因此将所有实验室每个添加量质控样品的总平均值作为氟苯尼考标准样品含量定值结果:X1=0.23 μg/kg,X2=0.39 μg/kg,X3=1.92 μg/kg,3 个添加量的质控样品可应用于快速检测或实验室检测的质量控制及能力验证等领域。
3 结论
采用鸡蛋基质分别添加标准溶液的方式成功研制了3 个添加量的液态质控样品,另外将液态样品采用真空冷冻干燥的方式,制得固态冻干粉,2 种状态质控样品均匀性均较良好。通过考察3 个月短期稳定性,结果发现不同样品状态、不同贮存温度对质控样品稳定性有影响,不同的添加量则对质控样品稳定性无影响。该方法制备的冻干质控样品比非冻干质控样品稳定性更高,分析原因可能是冻干组抗冻性能更好,蛋白质不易变性使其具有更高的稳定性。为了保证质控样品稳定性,建议采用冷冻干燥方式去除水分。冻干质控样品在冷冻(-18 ℃)贮存12 个月稳定性良好,但在冷藏(4 ℃)和常温(25 ℃)贮存3 个月稳定性有所下降,可能是受微生物繁殖的影响,贮存温度降低会明显减缓微生物的生长繁殖,从而降低氟苯尼考的消耗和降解速率。本研究制备的冻干质控样品不易变质,冷冻条件下可稳定保存12 个月,可应用于实验室日常检测作为质量控制手段,并推广应用于快检产品评价、快检机构考核、快检方法研制等快检各个领域。
