锂离子电池胀气行为及改性策略的研究进展
2022-05-26傅儒生刘兆平邵光杰
石 玥,傅儒生,刘兆平,邵光杰
(1.中国科学院宁波材料技术与工程研究所动力锂电池工程实验室,浙江宁波 315201;2.燕山大学环境与化学工程学院,河北秦皇岛 066004;3.燕山大学亚稳材料制备技术与科学国家重点实验室,河北秦皇岛 066004)
锂离子二次电池具有能量密度高、输出电压高、生命周期长、充电速度快、运行温度范围广等优点,但是随着使用时间的延长,锂离子电池易产气膨胀,使电池循环稳定性急剧恶化,同时伴有较大的安全隐患。胀气行为不仅存在于液态锂离子电池,也存在于全固态电池[1]。尤其电池在化成和储存阶段产生气体是一个较为复杂的问题,它严重制约了锂离子电池的使用寿命和安全性。
近年来,电池胀气引起了很多科研人员的关注,进行了深入的机理分析和抑制方案探索。通常引起电池胀气的因素有很多,本文分析了胀气产生的原因、产气的反应机制和对电池性能的影响,并详细分析了最新的补救措施,对于锂离子电池工业生产具有很好的借鉴意义。
1 电池胀气原因分析
电池无论在常温循环、高温循环还是高温搁置过程中,均会存在不同程度的胀气现象。电池胀气主要与正负极活性材料、荷电态(SOC)、电解液的电化学稳定性(溶剂和溶质)、水含量和温度等因素有关。
1.1 正负极稳定性
在充电过程中富锂锰基正极材料中的晶格氧O2-易被氧化形成分子氧(O2),从材料表面释放出氧气,氧气会进一步氧化电解液[2]。通常,高镍层状氧化物正极材料表面残碱量(碳酸锂、碳酸氢锂和氢氧化锂)较高,残碱与电解液中的酸性成分反应产生CO2气体。同时,碳酸脂类溶剂在高镍层状正极材料充电至≥3.8 V 时,发生脱氢氧化[3]。另外,电解液中的HF可与硅负极反应,生成四氟化硅和氢气[4-5]。
1.2 电解液分解
通过气相色谱分析气体的种类发现H2、CO 和CO2是大多数电解质中产生的主要气体成分[6]。电池产气量与种类随电解液成分的变化而变化。徐等[7]研究了钛酸锂负极在不同电解液体系中产生的气体成分,提出了直链的碳酸酯溶剂分解产生H2,而环状的碳酸酯分解主要产生烃类气体和不可溶解的无机盐。吴凯[8]研究报道含有DMC 电解液的钛酸锂电池产气量最高,体积膨胀率为325%,而含有PC、EMC 和DEC 电池的产气含量依次减少。Schiele 等[9]研究了硅基负极在不同电解液中电池产气情况,其中EC 作为电解质的主要气体成分是H2和CO2,而FEC 作为电解质的主要气体成分是H2、C2H4和CO。如图1 所示,Lin 等[10]报道硅基负极材料表面的硅羟基键可以与LiPF6反应形成POF3,引起溶剂分解产生CO2气体。
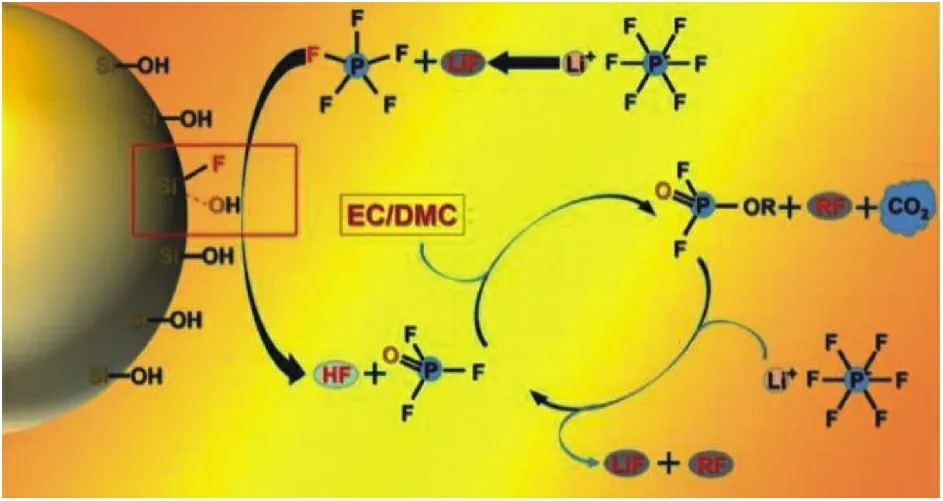
图1 硅表面羟基促进电解质分解原理图
1.3 水含量超标
电极、隔膜和电解液中水分超标是导致锂离子电池产生气体的重要原因。粘合剂丁苯橡胶SBR 和流变助剂羧甲基纤维素(CMC)是整个阳极结构中具有最大的水分吸收能力的物质[11]。H2O 的存在,会导致LiPF6水解产生HF,腐蚀电池;会导致LiCO3的分解,破坏固态电解质界面膜(SEI),而SEI 膜的再生会导致更多气体的产生,同时伴随电解液的消耗,带来严重的安全隐患。另外,过量H2O 的存在还会消耗掉锂离子,生成LiOH、Li2O 和H2,导致电池胀气,如式(1)和式(2)所示。

1.4 电池过充/过放
一般锂离子电池充电至电压高于4.2 V 称为过充,电池放电至电压低于2.5 V 称为过放。当电池过充过放时,会引起正负极活性物质结构变化及电解液的分解,产生大量气体。Kong 等[12]报道了容量为1 Ah 的18650 电池(石墨为负极),5 V过充时,具有不同正极材料的电池产生的气体成分没有变化,只是相对数量发生了变化。Yuan 等[13]对NCM333/石墨全电池的过充行为进行研究,发现当电池过充到180%SOC时,阴极与电解液界面变得高度活性并发生剧烈反应,电池内部温度升高至200 ℃以上,同时有大量气体产生。赵等[14]认为当电池持续放电,负极电势会升高,当其电势高至SEI 膜的氧化电位时就会导致SEI 膜的氧化分解,产生CO2,如式(3)所示。

1.5 温度引起的热分解
锂离子电池内部短路时大量的电流通过短路区域,在短路区域产生大量的焦耳热,热量向周围区域扩散,温度升高,继而引发电解液分解和SEI 膜分解、再生[15]。王书洋[16]研究发现电池内部短路时,Li0.5CoO2能与电解液发生剧烈反应,生成大量CO2使电池胀气。
电池过充过放滥用测试和热滥用测试排放出相似成分的气体,表明氧化还原反应似乎对电池释放气体的作用不大,而温度是关键参数[17]。Liao 等[18]研究发现电解质的热分解是锂离子电池热失控过程中释放气体的主要来源之一。实验结果显示1 mol/L LiPF6/(EC+DMC) (体积比1∶1)的电解液随着温度的升高,释放出的气体种类增多。
2 电池胀气对电化学性能的影响
电池胀气对锂离子电池的首次放电容量、内阻、循环性能、安全性能等各个方面有很大的影响[19]。目前限制锂离子电池进一步推广应用的因素主要在电池的循环性能上。Ouyang 等[20]对LiyNi1/3Co1/3Mn1/3O2+LiyMn2O4复合正极锂离子电池的过充电诱导容量衰减行为进行了研究,详细解释了过充过程对电池的影响。当SOC<120%时,过充对电池性能没有影响;在接下来的循环过程中,锂离子和阴极活性物质发生损失,容量衰减;当SOC>140%时,阴极和阳极均出现活性物质损失,电解液氧化,电池开始膨胀;最终由于内部短路,所有储存的能量瞬间释放,电池破裂。
电池的水分含量是影响电池胀气的主要因素。吸附水对电池性能的影响似乎取决于所使用的材料。Starke 等[21]没有观察到LiFeMnPO4阴极中残留水分对电池性能的任何影响。然而,在大多数文献中,已经发现使用普通材料的电池的稳定性与其水分含量之间存在相关性。Michael 等[22]报道,高水含量(1 000 ×10-6)的LiFePO4/石墨扣式电池[1 mol/L LiPF6/(EC+DEC)]在循环过程中容量衰减更快。而Li 等[23]研究了不同残留含水量下NMC532 半电池的电化学性能,如图2 所示。结果表明,残余水分降低了第一次循环的库仑效率,但对短期循环寿命的影响不显著。
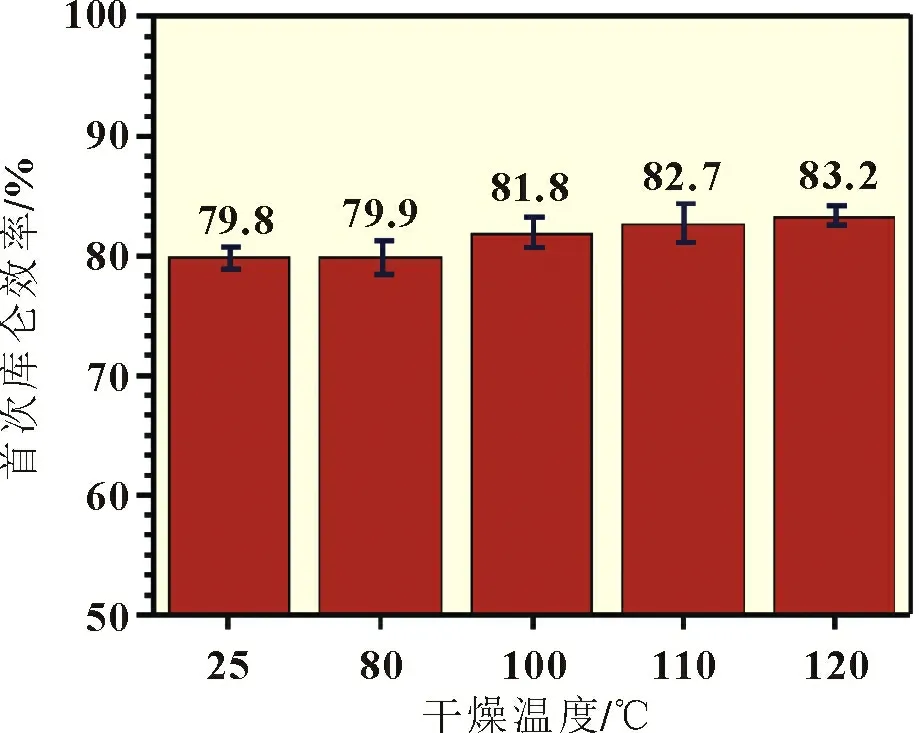
图2 不同温度下NMC532/Li首次库仑效率
Dahn 等[24]通过控制残余水分含量,对比了添加电解液添加剂前后水分对LiFePO4容量衰减的影响。研究发现,当不使用电解液添加剂时,水的存在会严重影响电池性能。当使用有效添加剂时,电池中的过量水不会显著影响循环寿命和容量。说明水分对电池的影响受电解液添加剂的影响。Wang 等[25]指出电解质中引入1-乙基-3-甲基咪唑四氟硼酸盐离子液体(EMI-BF4)作为添加剂,可以参与NCM532/石墨电池的阴极和阳极表面上稳定低阻抗SEI 膜的构建,与未添加添加剂的电池相比,添加1% EMI-BF4添加剂的电池在低温下循环150 次后,容量保持率从82.3%提高到93.8%。因此对水分-电解质-气体影响的更好理解可以在开发高性能锂离子电池、电池安全性等方面做进一步改进。
3 解决方案
为了降低胀气对电池性能的影响,近年来研究学者们进行了大量的工作,可以从材料设计、优化电解液和工艺控制等方面着手解决。
3.1 材料设计
通过使用掺杂、包覆和复合等改性手段,不仅可以达到抑制胀气的目的还可以提高倍率和循环性能。Lee 等[26]报道,使用标准固态方法将氟引入无序锂镍钛钼氧化物(Li1.2Ni0.333Ti0.333Mo0.133O2)的主体中,随着氟降低平均阴离子化合价,更多的Ni2+可以被结合,不仅增加了镍的氧化还原储库,而且防止了化合物利用过多的氧化还原而引发氧损失。Wang 等[27]研究揭示了钛酸锂(Li4Ti5O12)电极放气行为的可能机制,提出胀气行为与副反应有关,副反应由Li4Ti5O12电极的电位决定,其中电极/电解质界面的活性位点控制反应程度。在Li4Ti5O12颗粒表面包覆碳是抑制Li4Ti5O12电极上电解质还原分解的有效途径[28]。另外,氧化铝包覆钴酸锂同样可以抑制电池产气[22]。
材料也可以通过改变自身性质减少对水的吸附。颗粒材料以各种不同的尺寸、结构和比表面积存在,其水分吸脱附情况也不同。吴宁宁等[29]考察了不同比表面积、pH 值等物性参数的锰酸锂正极材料的吸水特性影响,发现低比表面和低pH 值的锰酸锂吸水性最弱。Ramakrishnan 等[30]研究表明,稀硫酸处理的富锂材料表面杂质减少,界面稳定性提高,第一次循环中无O2释放且CO2释放量显著降低,表现出良好的长期循环性能和倍率性能。
3.2 电解液改性
Guillot 等人[31]开发的新型电解液添加剂有机硅腈(OS),在NMC622/石墨软包电池中,显著抑制了CO2产气(主要来源于碳酸乙烯脂EC),减幅达94%~98%,同时在高压下(4.2~4.35 V)可降低CO 和CH4产气量,减幅达25%~39%。OS 掺入正极表面,一方面抑制高压晶格氧释放,另一方面抑制了迁移到正极的Li2CO3或碳酸亚乙酯锂氧化分解,并且溶解在电解液体相中的OS 可抑制EC 分解产生CO2。Hamidah 等[32]研究了氟邻苯二烯二马来酰亚胺(F-MI)添加剂存在时电解液分解的产物SEI 的形成。由于马来酰亚胺基添加剂具有高电负性和高吸电基团,氟的存在可以增加存储容量和可逆放电容量。含0.1%(质量分数)F-MI 基添加剂的电解液可以引发SEI膜形成,从而抑制剩余电解液的分解。Xia 等[33]研究发现,在测试到4.5 V 的高电压Li(Ni0.4Mn0.4Co0.2)O2/石墨袋型锂离子电池中,含有1 mol/L LiPF6的环丁砜(SL)∶碳酸乙酯(EMC)=3∶7的电解质混合物与碳酸乙烯酯和其他电解质添加剂的电解质混合物显示出良好的循环和存储性能,如图3 所示。1-戊烯-1,3-磺内酯(PES)、亚甲基甲二磺酸盐(MMDS)等含硫添加剂和磷酸三烯丙酯(TAP)等被证明是很好的气体还原剂。含TAP 添加剂气体明显减少,可能是因为添加剂形成厚的SEI膜,减少了电极和电解质之间的寄生电解质氧化反应,因此减少了气体释放并改善了循环和储存性能。然而,包含VC、含硫添加剂和TTSPi 这些三元添加剂的混合物在高温储存期间会产生大量气体。Xu 等[34]在NCM622/人造石墨袋型电池中,发现VC 和1,3-丙磺酸内酯(PS)体系产生了最少的气体,说明PS 的加入可以有效地抑制电解液中VC 的分解。同时六氟磷酸钾(F6KP)[35]、Li(CnF2n+1SO2)2(n为2、3 或4)[36]等电解液添加剂也都对锂离子电池胀气有显著的改善效果。目前没有一种电解液添加剂可以完全避免产气。因此,寻找合适的电解液添加剂作为气体减速器是非常关键的。
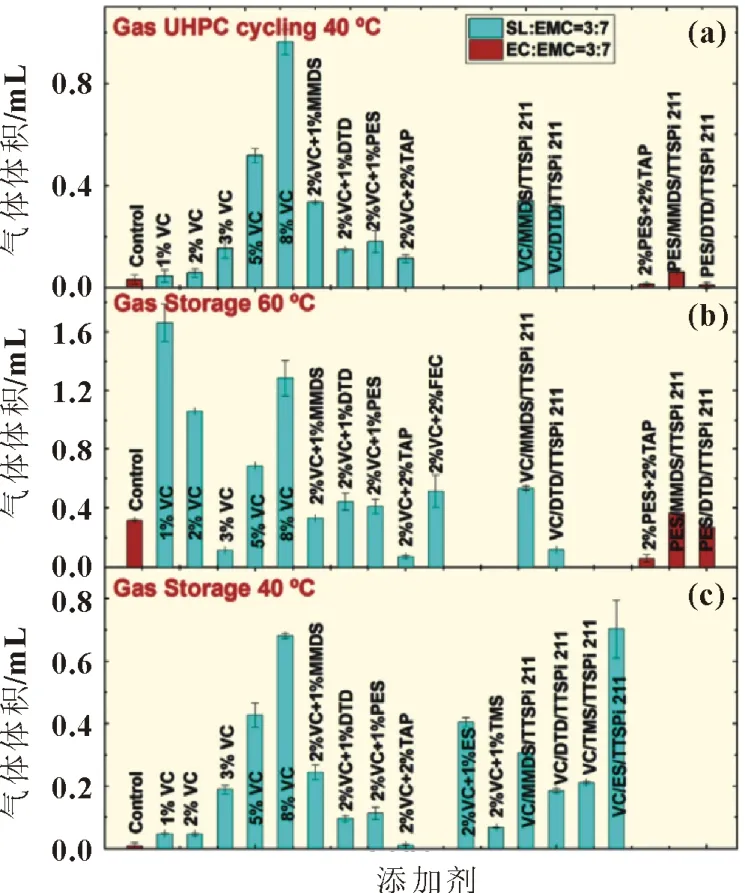
图3 Li(Ni0.4Mn0.4Co0.2)O2/石墨袋型锂离子电池在不同电解液添加剂下4.5 V 储存500 h产生的气体体积
近几年锂离子电池固态电解质研究快速发展,固态电解质包覆材料缓解电池胀气现象也随之得到了充分关注。Nie等[37]为了避免二氧化硅(SiO2)和PEO 之间的直接接触,采用Li1.4Al0.4Ti1.6(PO4)3(LATP)离子导体对SiO2表面进行包覆,减轻了SiO2与PEO 的表面催化效应(释放H2气体的根本原因),并且在4.6 V 电压下,电池依然没有气体产生。Daigle 等[38]报道使用1,8-二氮杂二环[5.4.0]十一烷-7-烯(DBU)添加剂,改变了钛酸锂与电解液的固态电解质界面膜的形成机制,获得了一层稳定的SEI 层,可最大限度地减少危险气体(如HF、C3H6和O2)的释放,并且在锂盐存在下,DBU 促进碳酸丙烯在LTO表面的原位开环聚合(ROP),在不增加电池内阻的情况下,将气体释放量减少了9.7%(体积分数)。
3.3 工艺控制
严格控制电池中各个组成部件和生产过程环境中的水含量,注液时控制干燥房内空气中水含量≤2%,电解液中水分含量≤20×10-6[39]。电池隔膜是一种多孔性的塑料薄膜,吸水性较强,可通过Al2O3包覆和静电纺丝工艺改善隔膜的吸水性[40]。
4 结论与展望
锂离子电池发展已初具规模,但电池胀气行为带来的安全隐患严重制约其发展。电池水分含量、电解液的分解和高温、过充过放等因素对电池胀气和循环性能具有深刻影响。电池中的水分含量是影响电池胀气行为的主要因素,水含量超标严重影响电池的循环性能和安全性能,但在生产过程中只能通过控制操作工艺和环境来控制电池的水分含量,并不能得到很好的控制。因此需要更清楚地了解有关界面产气的基本反应机理,包括电荷和电子转移过程、材料表面结构演变、电解质溶剂分解机理、表面化学对产气的影响等。电解液添加剂可以拓宽电池的工作温度与电压范围,使电解液在高温高压环境下保持稳定;固态电解质和电解液添加剂可以形成稳定的SEI 膜,阻隔电极材料与电解液的接触,减少它们之间的氧化反应;不同电解液添加剂之间也相互影响。寻找最佳电解液与添加剂的种类与配比,对缓解电池胀气具有深远的影响。
