川崎病致儿童急性心肌梗死1例
2022-05-21黄晓碧徐艳艳
黄晓碧 徐艳艳
作者单位: 230051 安徽合肥 安徽省儿童医院儿童心血管科
1 病例资料
患儿,男性,8岁,因“发热8天”于2021年1月31日入院。患儿入院前8天出现发热,体温最高达39.0℃,呈弛张热型,口服布洛芬后体温可降至正常,病程中有一过性皮疹,现已消退,在当地医院先后给予头孢克肟和阿莫西林克拉维酸钾口服治疗1周,仍反复发热,热型不规则,且出现球结膜充血,杨梅舌等表现,考虑“川崎病可能”,遂转入我院进一步治疗。入院查体:体温37.8℃,心率105次/分,呼吸20次/分,体质量26.5 kg,血压96/62 mmHg(1 mmHg≈0.133 kPa)。双眼球结膜充血、无渗出,口唇干裂,可见杨梅舌,双侧颈部可触及数枚肿大淋巴结,较大约2.5 cm×2.0 cm,心肺腹查体无异常,手足无硬肿。入院当天实验室检查示:白细胞计数19.39×109/L,中性粒细胞比84.8%,血红蛋白 121 g/L,血小板346×109/L,C反应蛋白99.6 mg/L,血沉 72 mm/h,清蛋白24.7 g/L,丙氨酸氨基转移酶 103.2 IU/L,尿白细胞76个/HPF;心肌酶及凝血功能未见异常。经胸超声心动图(transthoracic echocardiography ,TTE)示左冠状动脉主干(left main coronary artery,LMCA)内径3.1 mm,左前降支(left anterior descending branch ,LAD)内径3.2 mm,左回旋支(left circumflex branch, LCX)内径2.7 mm,右冠状动脉(right coronary artery,RCA)开口内径3.5 mm,近中段扩张,最宽处内径8.5 mm,各房室腔大小正常,无心包积液。结合患儿临床表现及影像学资料,入院诊断:川崎病(Kawasaki disease,KD),冠状动脉动脉瘤(coronary artery aneurysm,CAA)。入院当天给予静注人免疫球蛋白(intravenous immunoglobulin ,IVIG)2 g/(kg·d)及口服大剂量阿司匹林30 mg/(kg·d)标准治疗,患儿在IVIG治疗72 h后仍反复高热,最高体温达38.8℃,复查TTE示冠状动脉内径较前增宽,再次使用IVIG 2 g/(kg·d)并联合英夫利昔单抗5 mg/kg,甲泼尼龙2 mg/kg和低分子肝素100 μ/(kg·d) 治疗,病情稳定2周后出院,继续口服阿司匹林,美托洛尔及华法林,并监测国际标准化比值(international standardization rate,INR)于1.5~2.5。病程1个月复查心电图示窦性心律,TTE示RCA最宽处内径20 mm,可见稍高回声,考虑冠状动脉内血栓形成,调整低分子肝素用量至200 μ/(kg·d),加用氯吡格雷1 mg/(kg·d)口服。病程2个月患儿晨起出现胸痛、呕吐、大汗、面色苍白等症状,持续约30 min后症状稍缓解,再次入住我科复查TTE示LMCA内径2.8 mm,LCX内径2.4 mm,LAD内径2.8 mm,远端扩张,最宽处内径13.0 mm,RCA开口内径3.8 mm,近中段扩张,最宽处内径21 mm,可见片状高回声,冠状动脉内血栓形成,左室收缩功能减低,室壁运动减弱。见图1。心电图:窦性心律,前壁、高侧壁ST-T变化。见图2。心脏标志物检查:肌钙蛋白I(cardiac troponin I,cTnI)17.63 ng/mL(0~0.06 ng/mL),肌红蛋白 301.6 ng/mL(0~48.8 ng/mL),肌酸激酶同工酶(creatine kinase isoenzymes,CK-MB)128 U/L(0~30 U/L), N末端脑钠肽前体(N-terminal pro-brain natriuretic peptide, NT-proBNP)999.9 pg/mL(0~250 pg/mL)均升高。考虑存在急性非ST段抬高型心肌梗死,给与静脉泵入硝酸甘油0.5 μg/(kg·min)和米力农0.25 μg/(kg·min)治疗,2周后复查心电图示窦性心律,Ⅲ导联可见病理性Q波,下壁导联T波倒置,肢体导联低电压。见图3。TTE示左室收缩功能恢复正常,cTnI 0.033 ng/mL,CK-MB 11 U/L,NT-proBNP 759.2 pg/mL。并继续给与抗血小板、抗凝、β-受体阻滞剂和血管紧张素转换酶抑制剂药物口服,随访中患儿无血栓及出血事件发生。
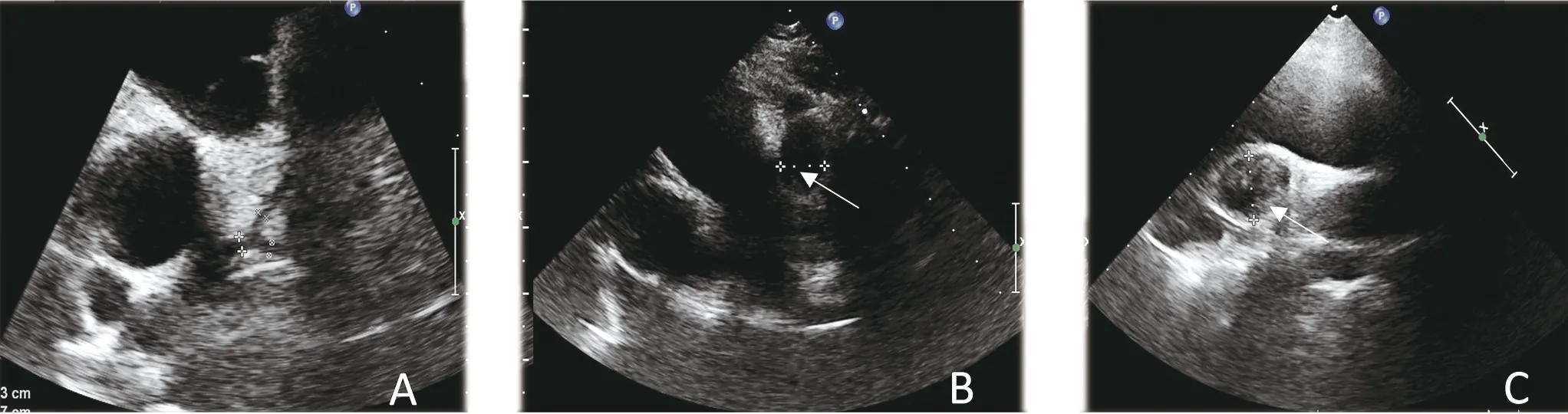
注:A为LMCA、LAD和LCX近端未见扩张,B为LAD远端明显扩张,C为RCA近中端明显扩张并可见冠状动脉内血栓形成。

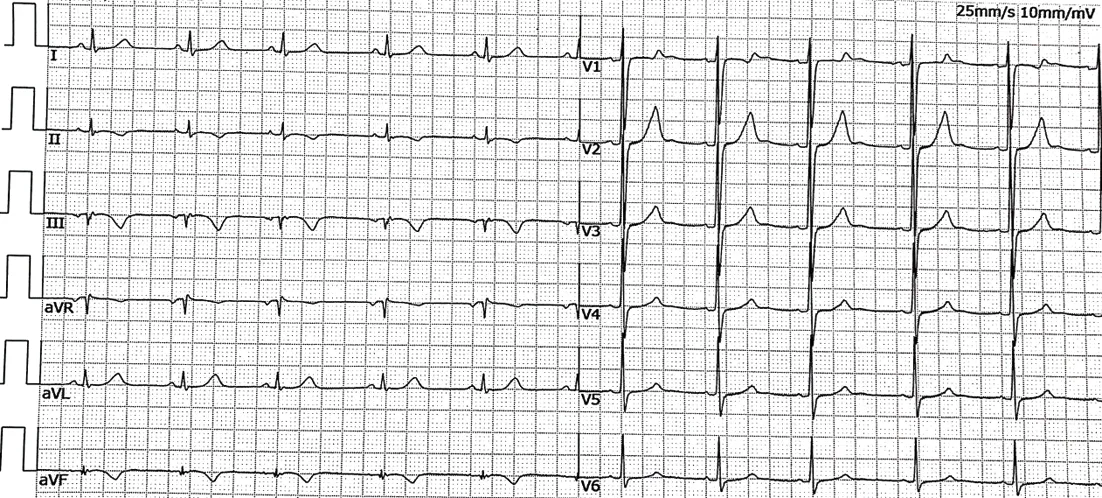
注:窦性心律,前壁、高侧壁ST-T变化。
注:窦性心律,病理性Q波(Ⅲ)、下壁导联T波倒置、肢体导联低电压。
2 讨论
KD是一种以全身血管炎为主要病理改变的疾病,多见于5岁以下儿童,未治疗的患儿中约30%可能会导致冠状动脉病变[1],冠状动脉病变的患儿可并发冠状动脉血栓或狭窄,是儿童获得性心脏病的主要病因。本例患儿病程中有发热8天、皮疹、淋巴结肿大、球结膜充血、杨梅舌临床表现,TTE可见巨大CAA,依据2017年美国心脏病学会诊断标准[2],KD、CAA诊断明确。
IVIG联合阿司匹林是KD的标准治疗方案,但约10%~15%的患儿对IVIG无反应,需要使用糖皮质激素、英夫利昔单抗等二线药物治疗[2],从而迅速控制发热和减轻冠状动脉病变。血浆NT-proBNP升高[3]、IVIG无反应[4]等是KD并发CAA的危险因素,冠状动脉血栓和狭窄的风险和CAA的大小相关[5],联合使用抗凝和抗血小板药物可以降低CAA患儿血栓事件发生。本例患儿在使用IVIG治疗前已出现CAA,且对IVIG治疗无反应,虽积极给与补救治疗,TTE监测冠状动脉仍在进一步扩张,故需早期诊断和及时治疗KD,从而减轻冠状动脉的损伤。
该患儿在病程2个月突发胸痛,心电图表现新发ST-T变化,TTE提示冠状动脉血栓形成、左室收缩功能减低,CK-MB、cTnⅠ升高,根据文献[6]诊断急性心肌梗死。儿童心肌梗死较罕见[5],且部分KD合并CAA患儿可以形成明显的侧枝循环,不会导致典型心肌缺血症状[7],故需及时完善心脏标志物、心电图、TTE等检查,早期识别急性心肌梗死。尽管积极管理此类患儿,急性心肌梗死仍不能完全避免,这些患儿随着年龄的增长风险越大[8],故后期需积极行冠状动脉旁路移植术等方法重建冠状动脉血流[9],避免再发心肌梗死甚至心脏破裂[10]。因此,对于KD合并CAA患儿存在长期的心血管并发症风险,需要长期的在专科门诊随诊,早期诊断和治疗心肌梗死,以改善预后。
