城市污泥中胡敏酸和富里酸测定方法研究
2022-05-20倪晓晓
倪晓晓,阎 亮,马 振,王 贤
(青岛市排水运营服务中心,山东 青岛 266002)
城市污水处理过程排放大量的剩余污泥,剩余污泥成分复杂,如何将其有效利用一直是影响城市发展的重要问题。腐殖质是污泥颗粒结构的重要组成部分[1],含有丰富的官能团,在污泥堆腐熟化过程中发挥着关键作用,同时也是重要的肥料成分和土壤基质[2]。腐殖质由胡敏酸(俗称腐殖酸)、富里酸和胡敏素组成;胡敏酸溶于碱、在pH<2酸液中会形成沉淀,富里酸为在酸、碱溶液中均可溶解的低分子物质,胡敏素既不溶于碱也不溶于酸[3]。其中可提取检测的成分为胡敏酸和富里酸,近几年引起较多关注。
李欢等[4]在《污水污泥中腐殖酸的提取和利用》中指出:“从污泥中提取腐殖酸,用于生产液态肥,不仅可以节约煤炭等不可再生资源,而且可以提高污泥肥料品质,扩大污泥资源化产品市场。”李会杰[5]在《腐殖酸和富里酸的提取和表征研究》中指出:“腐殖酸、富里酸结构中含有大量酚羟基、羰基等基团,因而可与氧化物、金属离子和包括有毒有害物质在内的有机物发生相互作用,从而影响这些物质的环境化学行为,包括有机物的化学降解、光解、生物吸收、迁移及挥发等方面。”由此可见,测定污泥中胡敏酸和富里酸的含量,对城市污泥的资源化利用研究,污泥絮凝性能的提高,水处理工艺的进一步改进等,具有非常重要的理论价值和现实意义。
本文研究对象为城市污泥,其中杂质极多,成分复杂,我国目前还没有关于城市污泥中胡敏酸和富里酸含量测定的标准方法。本文提供一种用于测定城市污泥中胡敏酸和富里酸含量的方法,该方法安全简单,条件温和,操作过程技术难度不高,数据可靠。
1 实验方法及原理
焦磷酸钠和氢氧化钠混合液在强碱性的介质中具有极强的络合能力,能将污泥中的难溶于水和易溶于水的结合态的腐殖质(胡敏酸和富里酸),络合成易溶于水的腐殖质钠盐。将腐殖质提取到溶液中,将其沉淀析出,用TOC法测定胡敏酸和富里酸的总碳量;将腐殖质提取液的pH调至适当酸性,使胡敏酸沉淀分离,用TOC法测定胡敏酸的碳量;两者差值为富里酸的碳量。
2 实验试剂与仪器
试剂:(1)焦磷酸钠与氢氧化钠混合提取剂:称取分析纯焦磷酸钠(Na4P2O7·10H2O)44.6 g和4 g分析纯氢氧化钠,加蒸馏水溶解后定容至1 L;(2)氢氧化钠溶液:c(NaOH)=0.05 mol/L;(3)硫酸:c(H2SO4)=0.1 mol/L;(4)硫酸:c(H2SO4)=2 mol/L。
天平:感量0.0001 g;振荡器;离心机(10000 r/min);纤维树脂滤膜(0.45 μm);电热板;水浴锅;TOC仪。
3 实验步骤与结果计算
3.1 胡敏酸含量测定
(1)称取5.00 g左右(M)污泥样品放入200 mL三角瓶中,加入100 mL(V)焦磷酸钠与氢氧化钠混合提取剂,用橡皮塞塞紧后在振荡机上振摇5 min,然后静置24 h(温度控制在20 ℃左右)。浸提液经离心机(10000 r/min)离心30 min后,过0.45 μm纤维树脂滤膜,收集滤液于三角瓶中。
(2)吸取上述滤液50 mL(v)移入烧杯中,在加热情况下,逐滴加入2 mol/L的硫酸,使溶液的pH调到3左右,此时应出现胡敏酸絮状沉淀。再将此溶液放在电热板上以80 ℃保温半小时,然后将烧杯中溶液静置24 h。
(3)将烧杯中溶液用0.45 μm纤维树脂滤膜过滤,取沉淀。用0.1 mol/L硫酸洗涤沉淀物多次,弃去滤液。将沉淀用热的0.05 mol/L氢氧化钠少量多次地洗涤,溶解到100 mL(V1)容量瓶中,用去离子水定容,摇匀待测。
(4)取待测液50 mL(v1),用2 mol/L硫酸中和到pH为7,使溶液出现混浊为止。移入已恒重为m0的蒸发皿中,置于水浴锅上蒸干。再将蒸发皿移至烘箱中(105 ℃)干燥1 h,至干燥器中室温恒重,用电子天平称其重量(m)。测定沉淀TOC百分含量(a)。
(5)污泥中胡敏酸含量的数值,以%表示:
胡敏酸含量=a(m-m0)×(V/v)×(V1/v1)/M×100%
说明:上式中字母代表意义见上述实验步骤。
3.2 富里酸含量测定
(1)称取5.00 g左右(M’)污泥样品放入200 mL三角瓶中,加入100 mL(V)焦磷酸钠与氢氧化钠混合提取剂,用橡皮塞塞紧后在振荡机上振摇5 min,然后静置24 h(温度控制在20 ℃左右)。浸提液经离心机(10000 r/min)离心30 min后,过0.45 μm纤维树脂滤膜,收集滤液于三角瓶中。
(2)吸取15 mL(v’)上述滤液逐滴加入2 mol/L的硫酸,使溶液的pH中和到7左右,使溶液出现混浊为止,可稍加热。移入已恒重为m0’的蒸发皿中,置于水浴锅上蒸干。再将蒸发皿移至烘箱中(105 ℃)干燥1 h,至干燥器中室温恒重,用电子天平称其重量(m’)。测定沉淀TOC百分含量(a)。
(3)富里酸和胡敏酸的总量=b(m’-m0’)×(V/v’)/M’×100%
说明:上式中字母代表意义见上述实验步骤。
(4)富里酸含量(%)=富里酸和胡敏酸的总量(%)-胡敏酸的含量(%)
4 结果与讨论
4.1 方法的精密度测定
选取青岛市某两座污水处理厂产生的脱水污泥,将其分别进行冷冻干燥研磨过筛后作为待测干泥样品:样品1和样品2。称取一定量的样品,按照3.1和3.2的方法分别测定胡敏酸和富里酸的含量,每个样品平行测定8次。测定结果见表1。
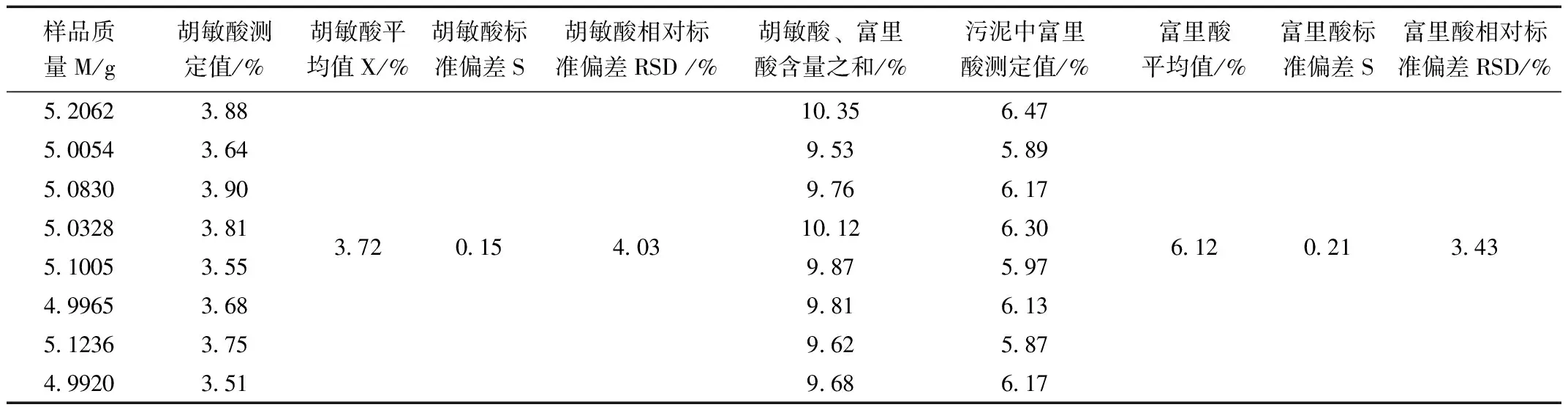
表1 样品1中胡敏酸和富里酸含量的测定结果
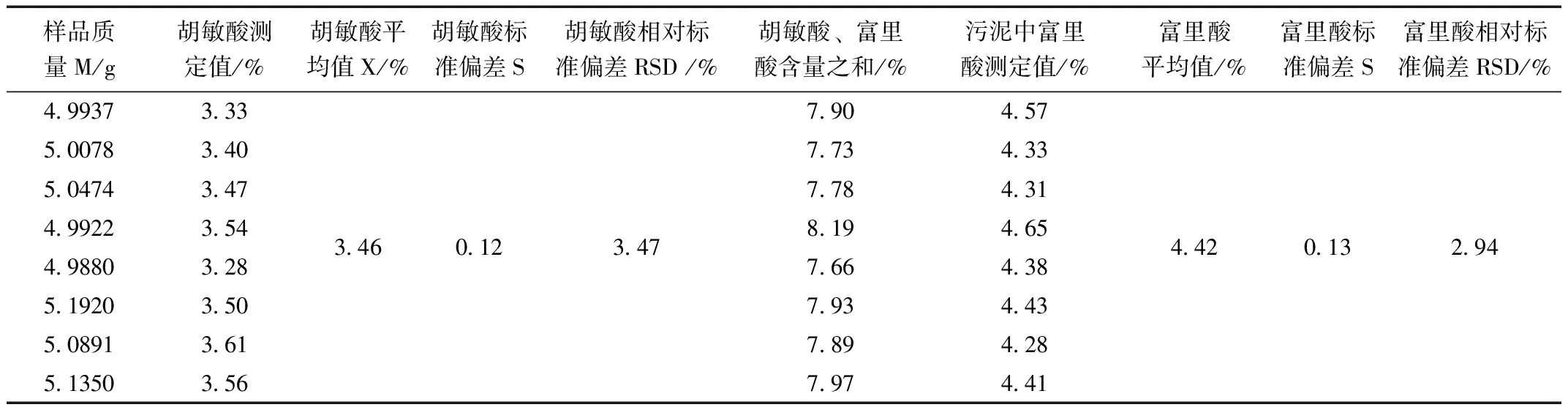
表2 样品2中胡敏酸和富里酸含量的测定结果
通过对青岛市某两座污水处理厂产生的污泥样品检测分析可知,其中样品1中胡敏酸含量平均值为3.72%,相对标准偏差(RSD)为4.03%,富里酸含量平均值为6.12%,相对标准偏差(RSD)为4.03%;样品2中胡敏酸含量平均值为3.46%,相对标准偏差(RSD)为3.47%富里酸含量平均值为4.42%,相对标准偏差(RSD)为2.94%。测定结果稳定,精密度高。
4.2 方法的实验室间比对
由两个检测机构进行实验室间比对试验,对统一样品(4.1中两个样品)进行测定,每一个样品平行测定8次。检测结果如表3、4所示。

表3 样品1实验室间比对试验测定结果

表4 样品2实验室间比对试验测定结果
两个实验室对统一样品进行测定,两个样品测定结果的实验室间相对标准偏差分别为:样品1胡敏酸4.25%、富里酸3.82%;样品2胡敏酸3.58%、富里酸3.12%。结果重现性好。
5 结 论
本方法填补了目前我国城镇污泥中胡敏酸和富里酸含量测定方法的空白,对城镇污泥的资源化处置提供理论依据,在环境保护及固体废弃物处理利用等领域具有广泛的应用前景。本方法操作安全简单,条件温和,成本低,实验过程中无任何有机试剂的添加,绿色环保,操作过程技术要求不高,结果稳定可靠,适合对污泥中胡敏酸和富里酸含量进行测定。
