利奈唑胺联合环丝氨酸胶囊治疗肺结核的疗效及对患者血清CD3+、CD4+、CD8+和肝功能的影响
2022-05-20王莎张永峰刘恒
王莎,张永峰,刘恒
西安市胸科医院神经结核科,陕西 西安 710061
肺结核又称为痨病,属于一种严重威胁公共安全卫生的慢性消耗性和传染性疾病,主要与结核分枝杆菌经空气传播途径感染有关,临床主要表现为咳嗽、咯血、低热、盗汗、消瘦、乏力等,严重降低患者生活质量[1]。目前,肺结核耐药已成为结核病防控成效的主要难题,该病的迅速传播和广泛分布已使全世界疫情变得非常严峻,给结核病防控工作带来沉重负担。据世界卫生组织(WHO)发布的2016年核病报告表明,全球目前新发耐多药结核病患者截止2015年已达48万,2013年全球耐多药患者成功治愈率仅为52%[2]。环丝氨酸(cycloserine,CS)是WHO所推荐的二线抗结核口服制剂,具有良好抗结核分枝杆菌功效和低耐药率等优势,广泛用于临床[3]。利奈唑胺属于一类新型恶哇烷酮类抗生素,对G-杆菌全面抵抗作用最强,有效阻断细菌蛋白合成的结合位点,用于结核病特别是耐药结核病的效果较佳[4]。笔者将上述两种抗结核药物联合应用于肺结核患者的标准用药方案中,探讨其疗效及对患者外周血T 淋巴细胞亚群水平(CD3+、CD4+、CD8+)和肝功能的影响,现报道如下:
1 资料与方法
1.1 一般资料 选取2016 年2 月至2019 年2 月期间在西安市胸科医院神经结核科住院治疗且符合以下纳入和排除标准的124例肺结核患者作为研究对象。由软件RandA1.0 随机产生随机数字表,以1∶1比例随机将患者分为对照组和观察组,每组62例。两组患者的基础资料比较差异均无统计学意义(P>0.05),具有可比性,见表1。本研究经医院伦理委员会批准,所有患者均签订知情同意书。
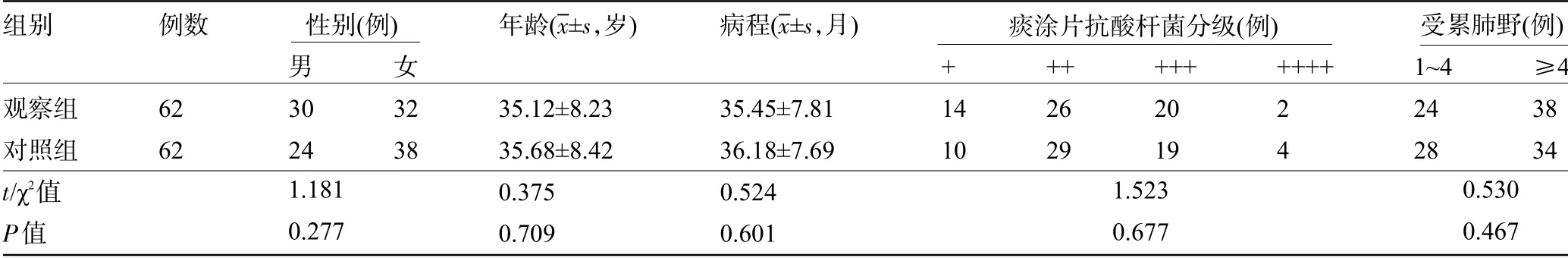
表1 两组患者的基线资料比较
1.2 纳排标准 纳入标准:(1)符合肺结核的诊断标准[5],痰结核分枝杆菌培养阳性,痰结核菌涂片(+),痰结核菌培养证实对异烟肼和利福平均耐药,胸片检查显示有肺内结核病变,有或无空洞者;(2)本研究符合《赫尔辛基基本宣言》对于人体实验伦理要求者。排除标准:(1)广泛耐药结核病者;(2)合并其他肺部疾病者;(3)近6 个月内接受免疫调节剂治疗者;(4)合并酒精性肝炎、非酒精性肝炎疾病或脂肪肝等其他肝脏疾病者;(5)伴有自身免疫性疾病者;(6)癫痫者;(7)合并血液系统疾病者;(8)伴有心、脑、肾等重要脏器功能障碍者;(9)合并恶性肿瘤者;(10)精神疾患或认知功能障碍者;(11)既往颅脑损伤史者;(12)对本研究药物存在禁忌证或过敏体质者;(13)妊娠、哺乳期者。
1.3 治疗方法 所有患者均给予常规对症治疗,内容涉及营养支持、氧疗、解痉祛痰、解痉祛痰、全程加用葡醛内酯片以保护肝脏等;均采用中国全球基金耐多药肺结核病防治项目标准用药方案6个月吡嗪酰胺(Z)+卡那霉素(Km)+左氧氟沙星(Lfx)+丙硫异烟胺(Pto)+对氨基水杨酸(PAS)/18 个月吡嗪酰胺(Z)+左氧氟沙星(Lfx)+丙硫异烟胺(Pto)+对氨基水杨酸(PAS)(6 Z Km Lfx Pto PAS/18 Z Lfx Pto PAS)进行治疗,即6 个月内注射期给予Z [艾康礼德制药(浙江)有限公司,国药准字H33022098,规格:0.25 g)0.5 g/次,3次/d,Km(上海禾丰制药有限公司,国药准字H31020546,规格:0.5 g)1 g/d 肌肉注射,Lfx(海南中和药业有限公司,国药准字H20052719,规格:0.1g)0.75 g/d,清晨口服,Pto(江苏正大天晴药业股份有限公司,国药准字H32022859,规格:0.1 g) 0.25 g/次,3 次/d,PAS (辽宁倍奇药业有限公司,国药准字H21022194,规格:4 g)4 g/次,2次/d,酸性饮料送服;之后18个月非注射期内给予Z 0.5 g/次,3 次/d,Lfx 0.75 g/d,清晨口服,Pto 0.25 g/次,3次/d,PAS 4 g/次,2次/d,酸性饮料送服。对照组基于以上治疗方法和治疗时间给予环丝氨酸(CS)(浙江海正药业股份有限公司,国药准字H20130063,规格:0.25 g)治疗,体质量<33 kg者口服CS 15 mg/(kg·d),体质量在33~50 kg 者口服500 mg/d,体质量>51 kg 者口服750 mg/d,分2~3 次/d 口服,每使用250 mg CS 需服用维生素Β650 mg(甘肃祁连山药业股份有限公司生产,国药准字H62020395),连续治疗24 个月。观察组基于以上治疗方法和治疗时间给予CS 联合利奈唑胺片治疗,CS 用药方法同对照组,同时间点给予利奈唑胺片(美国PfizerIn,注册证号:H20090516,规格:600 mg)600 mg/次口服,1 次/d,若出现严重不良反应则减量至300 mg/d,共治疗24 个月。治疗期间,两组患者每次在直接观察下(DOTS)服用药物。
1.4 观察指标 (1)痰结核菌阴转测定:记录两组患者治疗3、6、12 及24 个月后的痰结核菌转阴率。痰抗酸菌涂片和结核分枝杆菌培养:取痰标本3 份进行痰涂片抗酸染色,涂阳或性状较好痰涂片2 份,采用ΒactecMGIT960快速培养法进行结核分枝杆菌培养和分离阳性菌株,遵循中国防痨协会《结核病诊断实验室检验规程》[6]采用绝对浓度法进行药敏试验和菌种鉴定,涂片抗酸杆菌分级用“+”表示,表明痰结核分枝杆菌负荷量,“+”越多表明菌量越大。(2)症状改善时间:记录两组患者病灶吸收时间、空洞闭合时间、抗酸染色涂片阴性时间及痰培养转阴时间。(3)外周血T淋巴细胞亚群水平:选择在治疗前及治疗24个月后清晨,采集两组空腹外周血,采用三色免疫荧光多参数流式细胞术检测者外周血T淋巴细胞亚群的相对百分数(CD3+T淋巴细胞计数、CD4+T淋巴细胞计数、CD8+T 淋巴细胞计数),计算CD4+/CD8+T 淋巴细胞比值。(4)肝功能损伤评估:选择在治疗24 个月后清晨,采集两组患者的空腹静脉血,样血装置于含EDTA 二钾一次性真空抗凝管内,室温下经离心分离,取上清液冷藏备检,应用日立7180 全自动生化分析仪,采用乙肝两对乙肝两对半的定量法检测血清总蛋白(TP)和清蛋白(ALΒ)水平,并计算白蛋白/球蛋白(A/G),将肝功能合成功能和损伤程度依照A/G 值分为正常(A/G 值≥1.5)、轻度损伤(A/G 值1.0~1.5)及重度损伤(A/G 值<1.0),对比两组肝功能损伤程度。
1.5 疗效评定标准[7]显效:痰涂片以连续2 个月痰菌阴性且不再复阳,阴转病灶吸收面积≥原病灶面积1/2,空洞闭合或阻塞闭合。有效:痰涂片最后1个月末因无痰无法进行痰涂片、痰培养,此前痰涂片或培养阴性,病灶吸收面积<原病灶面积1/2,空洞缩小≥原空洞直径1/2。无效:痰涂片未转阴,病灶面积未吸收甚至扩大或出现新病变,空洞缩小或增大<原空洞直径1/2,或空洞增大>原空洞直径1/2。临床总有效率=[(显效+有效)/总病例数×100%]。
1.6 统计学方法 由Excel 表格收集所有数据,应用SPSS19.0 软件分析处理。计量资料符合正态分布、方差齐性,以均数±标准差(±s)表示,两组间比较采用独立样本t 检验,组内治疗前后采用配对t 检验;有序多分类重复测量资料采用广义估计方程评估,计数资料采用χ2检验,等级资料采用Willcoxon秩和检验法检验。以P<0.05为差异有统计学意义。
2 结果
2.1 两组患者治疗后不同时间点的痰结核菌阴转情况比较 广义估计方程分析显示:痰结核菌阴转率组别效应检验,差异均有统计学意义(Wald χ2=7.992,P<0.05),时间效应检验,差异均有统计学意义(Wald χ2=7.992,P<0.05);组间进一步比较,观察组治疗3 个月后的痰结核菌阴转率虽高于对照组,但差异无统计学意义(P>0.05),治疗6、12 及24 个月后的痰结核菌阴转率高于对照组,差异均有统计学意义(P<0.05),见表2。

表2 两组患者治疗后不同时间点的痰结核菌阴转情况比较[例(%)]
2.2 两组患者的临床疗效比较 观察组患者的临床疗效等级分布明显优于对照组,观察组患者的临床总有效率明显高于对照组,差异均有统计学意义(P<0.05),见表3。

表3 两组患者的临床疗效比较[例(%)]
2.3 两组患者的症状改善时间比较 观察组患者的病灶吸收时间、空洞闭合时间、抗酸染色涂片阴性时间及痰培养转阴时间明显于对照组,差异均有统计学意义(P<0.05),见表4。
表4 两组患者的症状改善时间比较(±s,d)
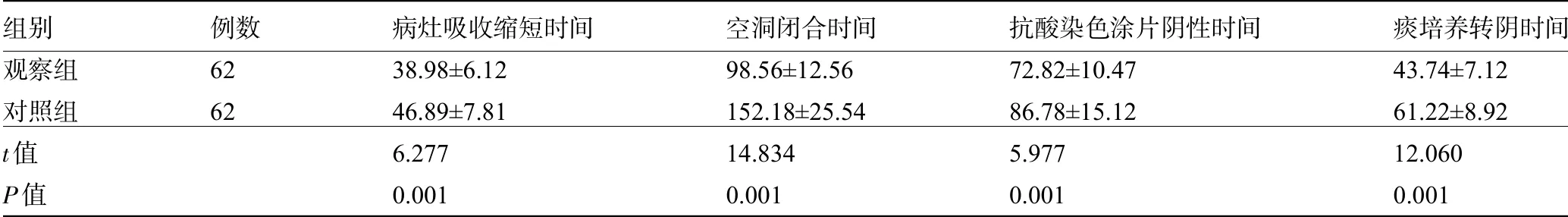
表4 两组患者的症状改善时间比较(±s,d)
组别观察组对照组t值P值例数62 62病灶吸收缩短时间38.98±6.12 46.89±7.81 6.277 0.001空洞闭合时间98.56±12.56 152.18±25.54 14.834 0.001抗酸染色涂片阴性时间72.82±10.47 86.78±15.12 5.977 0.001痰培养转阴时间43.74±7.12 61.22±8.92 12.060 0.001
2.4 两组患者治疗前后的外周血T 淋巴细胞亚群水平比较 治疗前,两组患者的外周血CD3+、CD4+、CD8+的T 淋巴细胞计数和CD4+/CD8+T 淋巴细胞比值比较差异均无统计学意义(P>0.05);治疗24 个月后,两组患者的外周血CD3+、CD4+的T 淋巴细胞计数和CD4+/CD8+T 淋巴细胞比值明显高于治疗前,且观察组明显高于对照组,CD8+T 淋巴细胞比值明显低于治疗前,且观察组明显低于对照组,差异均有统计学意义(P<0.05),见表5。
表5 两组患者治疗前后的外周血T淋巴细胞亚群水平比较(±s)

表5 两组患者治疗前后的外周血T淋巴细胞亚群水平比较(±s)
注:与本组治疗前比较,aP<0.05。
组别观察组对照组t值P值例数62 62治疗前55.98±9.12 55.25±8.99 0.449 0.654治疗后68.14±12.52a 61.23±11.41a 3.212 0.002治疗前22.56±4.12 22.10±4.21 0.615 0.540治疗后35.23±6.31a 30.12±5.89a 4.661 0.001治疗前28.31±5.31 28.29±5.29 0.021 0.983治疗后21.82±4.62a 25.13±5.03a 3.816 0.001治疗前1.02±0.21 1.06±0.23 1.011 0.314治疗后1.61±0.34a 1.32±0.27a 5.259 0.001 CD3+(%) CD4+(%) CD8+(%) CD4+/CD8+
2.5 两组患者治疗后的肝功能损伤情况比较 两组患者间的A/G 值不同等级变化比较差异无统计学意义(Z=0.182,P=0.856>0.05),见表6。

表6 两组患者治疗后的肝功能损伤情况比较[例(%)]
3 讨论
近年来,我国肺结核发病率和病死率居高不下,其发病人数在全世界甲、乙类传染病的位居前列,仅次于印度[8]。目前,随着抗结核药物的相继问世,我国实施结核病防治规划取得较佳结果,但结核病的高耐药性仍是我国结核病防治工作的重点、难点。结核分枝杆菌耐药性能决定抗结核治疗的成败,其耐药原因多与医嘱用药依从性不良、临床医师不规范及不合理使用抗结核药物有关。因此,针对肺结核耐药现状,制定合理、有效的抗结核治疗方案在临床中显得十分必要。
CS 的首次发现在1952 年,并应用于临床抗结核中。随着吡嗪酰胺、利福平等一线强效抗结核药物的上市,CS 逐渐淡出抗结核病治疗领域,但由于异烟肼和利福平等一线抗结核药物因高耐药性问题,目前已无法满足临床治疗需求,而中国已近20年未使用CS,对耐药结核杆菌有一定敏感度,且因其低耐药性和与其他抗结核药物无交叉耐药性等优势,其在临床中逐渐广泛应用[9]。CS药理机制是通过竞争性地阻断细胞浆中D-丙氨酸合成酶和L-丙氨酸消旋酶的结合位点,影响结核杆菌细胞壁肽聚糖的合成,进而破坏结核分枝杆菌细胞壁完整性,并削弱其耐酸能力,从而起到一定杀菌和抑菌作用[9-10]。CS 尤其针对链霉素、异烟肼,对氨基水杨酸钠等耐药结核菌的抗菌活性更佳。利奈唑胺在2016年首次被WHO的耐药结核病指南提出列为二线核心药物。利奈唑胺属于一种抑制细菌蛋白质合成制剂,对抵抗耐药革兰阳性菌感染有着显著优势,其作用机制是通过作用于细菌50S 核糖体亚单位23S RNA的不同部位结合,以阻断mRNA与核糖体的链接,进而影响细菌70S起始复合物的形成,从而达到抑制细菌蛋白质的合成、促进细菌凋亡的功效[4,10]。国内多项病例报道证实,利奈唑胺在耐药结核分枝杆菌上表现出较佳的抑菌活性,疗效良好[11]。本文现将利奈唑胺联合环丝氨酸胶囊应用于我院31 例肺结核患者的标准用药方案(6 Z Km Lfx Pto PAS/18 Z Lfx Pto PAS)中(观察组)发现,治疗6、12 及24 个月后,观察组的痰结核菌阴转率可达64.52%、77.42%及90.32%,明显高于我院采用单纯环丝氨酸胶囊治疗的患者(对照组)的38.71%、48.39%及58.06%,且观察组的临床总有效率可达93.55%,高于对照组的83.87%;进一步观察两组症状改善时间发现,观察组的病灶吸收时间、空洞闭合时间、抗酸染色涂片阴性时间及痰培养转阴时间明显缩短,且均短于对照组,提示利奈唑胺联合环丝氨酸胶囊应用肺结核患者的标准用药方案中疗效显著,可提高患者痰结核菌阴转率,促进其病情恢复,与梁建琴等[12]和韩莉[13]结果相似。
其次,研究发现,细胞免疫功能影响肺结核患者的病情进展和疾病归转,其中CD3+、CD4+T 淋巴细胞可反映辅助性T细胞活性,而CD8+T淋巴细胞属于抑制性T 淋巴细胞表面标志物,CD3+、CD4+T 淋巴细胞计数和CD4+/CD8+T 淋巴细胞比值降低,CD8+T 淋巴细胞升高,可提示着机体细胞免疫功能下降[14]。本研究中,观察组治疗24个月后的CD3+、CD4+的T淋巴细胞计数和CD4+/CD8+T 淋巴细胞比值明显提高,CD8+T淋巴细胞比值明显降低(P<0.05),改善效果均优于对照组,提示上述利奈唑胺联合环丝氨酸胶囊能纠正肺结核患者的T淋巴细胞亚群水平紊乱,调节其机体免疫功能,有助于患者疾病康复。考虑其原因可能为CS和利奈唑胺产生协同效应,提高抗结核药物有效率;同时,两者药物对免疫应答中的多个反应环节产生调节作用,从而改善机体免疫功能。
最后,有学者发现,抗结核药物会经过静脉、消化道等途径,极易增加肝脏功能损伤风险,其药物性肝损害的发生率可达3%~10%,对患者药物治疗耐受性和依从性造成一定影响,从而不利于防治结核整体疗效提升,肝损害严重者甚至可能引发死亡[15]。本文对比两组肝脏损伤情况发现,观察组治疗24 个月后的A/G 值不同等级变化情况较对照组并无显著性差异,说明利奈唑胺并未额外增加肝脏功能损伤风险,提示该药联合环丝氨酸胶囊应用于肺结核患者的标准抗结核用药方案中安全性良好。
综上所述,利奈唑胺联合环丝氨酸胶囊能明显拮抗结核分枝杆菌,提高肺结核患者的痰培养转阴率和临床疗效,加快患者病灶吸收、空洞闭合、抗酸染色涂片转阴及痰培养转阴时间,在不额外增加肝功能损伤的情况下,提高患者机体免疫功能,有助于患者疾病康复,临床应用价值确切,可积极用于抗结核病治疗。
