582例高危妊娠产前羊水染色体微阵列检测的临床应用分析
2022-05-16张胜利齐波杨庆慧陶华娟
张胜利 齐波 杨庆慧 陶华娟*
(1. 潍坊市妇幼保健院, 山东 潍坊 261011; 2. 浙江博圣生物技术股份有限公司, 浙江杭州 310007)
染色体是支配人类正常生长发育的遗传物质,若发生变异则会导致人类机体功能异常,且不易治愈,对患儿及家庭带来沉重的负担,因此,通过产前诊断排查胎儿的健康状况是最有效的防治策略。胎儿染色体异常的诊断方法包括核型分析、染色体微阵列分析(chromosomal microarray analysis,CMA)和荧光原位杂交(fluorescent in situ hybridization,FISH)等,其中核型分析是染色体疾病诊断的金标准,但传统的核型分析无法检出<10 Mb的染色体结构异常[1]。伴随着人类基因组计划的完成及近年来分子遗传学方向的迅速发展, CMA在临床上的应用得到快速的发展,已被推荐为儿童不明原因的发育迟缓及产前超声异常的胎儿遗传学检测的首选诊断方法[2-4],可用于检测人类染色体微重复或微缺失引起的各种疾病,填补染色体核型分析不能检测微缺失和微重复的不足[5]。临床上应用比较广泛的CMA技术平台包括单核苷酸多态性微阵列(single nucleotide polymorphism array,SNP array)和微阵列比较基因组杂交(array-based comparative genomic hybridization,aCGH)[6],相较于传统的核型分析方法,它具有自动化程度高、准确快速、灵敏度高及信息量大等优势[7]。产前诊断中常见的临床指征都适用于CMA检测,如B超异常、血清学筛查高风险、无创产前检测(non-invasive prenatal testing,NIPT)高风险、不良孕产史、高龄、夫妻一方染色体异常等,因此,对产前诊断临床指征的准确把握可能是困惑临床一线医生的主要原因。本研究通过探讨CMA在高危妊娠人群中临床应用的可行性,指导临床医生准确把握产前诊断的临床指征,并充分做好遗传咨询,达到优生优育的目的。
1 材料与方法
1.1 研究对象 选取2018~2020年在潍坊市妇幼保健院行介入性产前诊断的孕妇582例,所有孕妇各项辅助检查无明显禁忌证,且均签署产前诊断知情同意书。
1.2 方法
1.2.1 核型分析 在超声引导下行羊膜腔穿刺术抽取20 ml羊水,1500 rpm离心10 min,收集羊水细胞行常规培养,G显带,参考2016年人类细胞遗传学国际命名体系(International System for Human Cytogenomic Nomenclature,ISCN)进行核型分析及计数。
1.2.2 CMA 在超声引导下行羊膜腔穿刺术抽取10 ml羊水,使用基因组DNA提取试剂盒(北京天根生化科技)提取gDNA,经过SNP array 750K芯片(Affymetrix,美国)检测,结合Chromosome Analysis Suite (ChAS) 3.2分析软件和国际常用的公共数据库(DECIPHER、OMIM、ClinGen、PubMed、DGV)进行检索和判读。
1.3 CMA检测结果的判读及报告发放 在50kb/25marker缺失,100kb/25marker重复的分辨率水平对样本进行分析,报告致病变异、可能致病变异和临床意义未明变异(variants of uncertain significance,VOUS);不报告全基因组中已知属于正常多态的拷贝数变化;提示3 Mb以上的杂合性缺失片段;对于判读为VOUS的拷贝数变异(copy number variation,CNV)片段,建议结合父母验证结果明确CNV来源,若CNV遗传自亲代,判读为偏良性的VOUS片段,若为新发变异则需进一步的遗传咨询。
1.4 数据统计 采用EXCEL表格录入数据,统计学处理582例高危妊娠产前羊水样本的CMA检测结果,使用计数和频率描述统计结果。
2 结果
2.1 CMA检测结果的异常类型分析 582例高危妊娠产前羊水中,CMA共检出86例致病性和可能致病性变异,共占14.78%;其中常染色体数目异常病例39例,占比45.35%,常染色体杂合性缺失病例6例,占比6.98%,性染色体数目异常病例11例,占比12.79%,致病性CNV病例30例,占比34.88%。在致病性CNV病例中,小片段异常(<10 Mb)病例19例,占比22.09%,占总样本数量的3.26%(表1)。
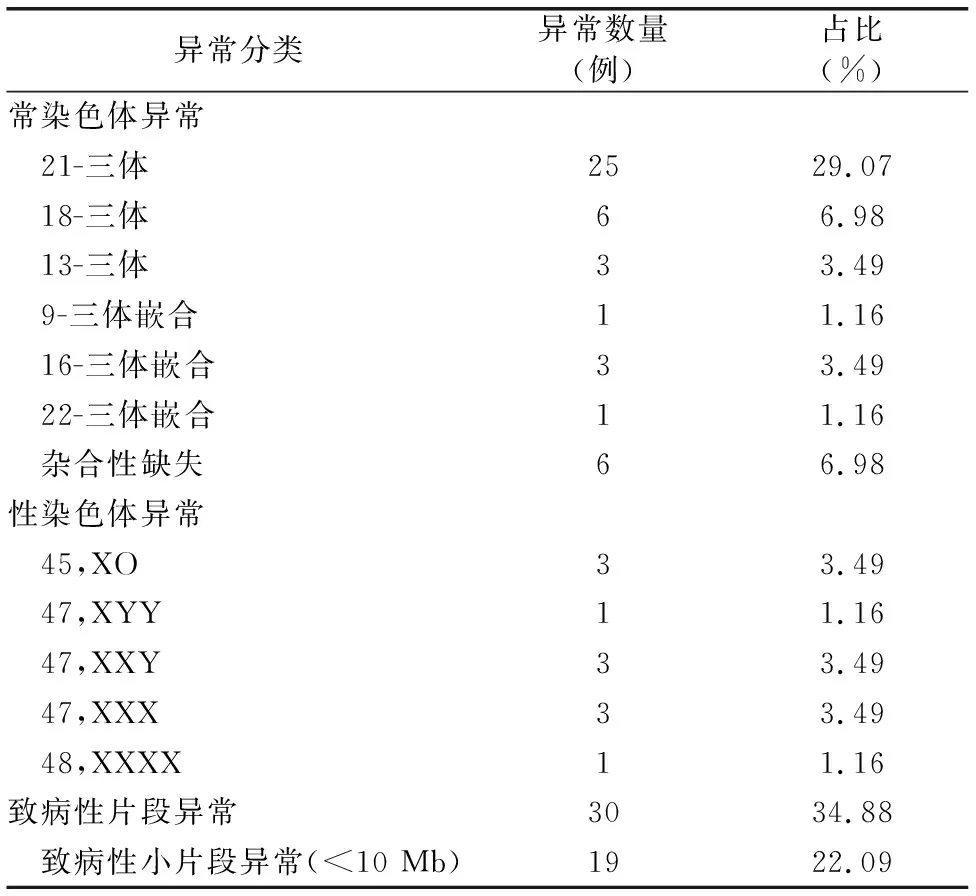
表1 CMA检测结果的异常类型分析(n=86)
2.2 CMA与传统核型分析检出异常类型的对比分析 除去6例杂合性缺失病例,CMA检出的80例异常病例中,常染色体数目异常病例39例,与核型分析检出一致;性染色体数目异常检出病例11例,相较于核型分析多检出2例低比例嵌合病例,可能与培养后的细胞优势生长有关;致病性片段异常CMA检出30例,核型分析检出11例,CMA较核型分析多检出19例致病性小片段异常(表2)。

表2 80例染色体异常病例的对比分析
2.3 不同羊水穿刺指征的CMA检出率分析 高危妊娠孕妇的临床指征可分为B超异常、血清学筛查高风险、NIPT高风险、不良孕产史、夫妻一方染色体异常、高龄和其他(包括孕期服药、试管婴儿和孕妇要求等)共7个部分。在不区分多种临床指征共存的情况下,统计分析发现高龄和NIPT高风险为CMA诊断率最高的临床指征,共占52.63%;CMA诊断率较低的产前诊断指征包括夫妻一方染色体异常、不良孕产史和其他类型(表3)。

表3 不同羊水穿刺指征的CMA检出率分析
2.4 CMA与NIPT的对照研究分析 NIPT检出的173例异常病例中,CMA共确诊40例,占比23.12%;统计分析发现性染色体数目异常的符合度最高,假阳性率最低,另外,非目标区域的常染色体数目异常假阳性率最高(表4)。
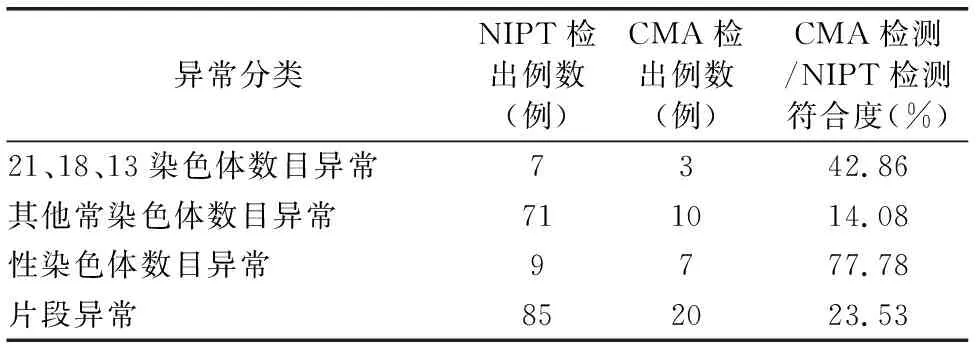
表4 CMA与NIPT的对照研究分析
2.5 不同B超异常病例的CMA检出率分析 582例产前羊水中,B超异常病例共有300例,其中CMA确诊病例45例(含1例杂合性缺失病例)。按照B超系统分类统计分析发现,多系统异常病例(包含2个及2个以上的B超异常指征)43例,CMA检出异常病例9例,占比20.93%;单系统B超异常病例257例,CMA检出异常病例35例,占比13.62%。在不区分B超多系统异常和单统异常的情况下进行常见B超异常指征分类,统计分析发现胸腹部异常(40%)、生长受限(37.5%)、肠管异常(27.27%)、脉络丛囊肿(22.22%)和胎儿颈部透明带(NT)异常(21.28%)的CMA检出率较高,肾脏异常没有异常病例检出(表5)。

表5 不同B超异常病例的CMA检出率分析(例,n=300)
2.6 高危妊娠孕妇的临床结局分析 随访480例病例中,45例随访失败(无致病性病例,致病性病例随访率100%)。在随访病例中,正常活产胎儿CMA检出非整倍体异常病例4例(均为性染色体异常病例),检出临床意义未明CNV(VOUS)异常病例33例,CMA检测正常病例268例,无致病性CNV病例检出;引产胎儿CMA检测非整倍体38例,检出VOUS异常病例5例,CMA检测正常病例31例,检出致病性CNV病例26例;出生异常胎儿CMA检出非整倍体1例(性染色体异常病例),检出VOUS异常病例4例,CMA检测正常病例20例,检出致病性CNV病例1例(表6)。

表6 435例随访病例的妊娠结局分析[例(%)]
3 讨论
孕期检测发现的血清学筛查高风险、NIPT高风险及B超异常等病例,通过羊水穿刺术,结合产前诊断技术实现对染色体数目及结构异常的准确分辨是非常有临床价值的;同时,在确定染色体异常来源的情况下,明确的诊断结果可以更好地评估再发风险,指导下一胎生育。本研究的结果显示,CMA可检出的染色体异常类型包括非整倍体异常、杂合性缺失异常和染色体微缺失/微重复异常等。另外,CMA相较于传统的核型分析,可多检出19例病例,将产前诊断率提升3.26%。与本研究相似,已有很多相关的报道也提到了CMA在产前诊断领域的临床应用,肯定了CMA在产前诊断领域的应用价值[8,9]。
高危妊娠孕妇的CMA诊断率较高的临床指征为高龄和NIPT高风险,分别为29.51%和23.12%,其中部分高龄孕妇合并其他异常,这可能是导致高龄孕妇诊断率较高的原因之一;此外,已有大量研究报道表明高龄是主要的产前诊断指征之一[10,11]。NIPT检测采用新一代高通量测序技术,结合生物信息分析,用于评估胎儿患染色体疾病的风险[12],准确度较高,是产前筛查与产前诊断的有效补充。本研究显示,性染色体异常的病例确诊率较高,甚至已经超过了NIPT目标疾病(21、18、13染色体数目异常)的诊断率,同时也有研究肯定了NIPT对于性染色体非整倍体的检测效能[13]。本研究还发现NIPT检出的85例胎儿染色体片段异常中,经过CMA验证有20例确诊为致病性片段。Pei等[14]的研究显示NIPT检测染色体片段异常的阳性预测值(positive predictive value,PPV)为14.89%,提示NIPT可作为胎儿染色体片段异常的筛查方法,CMA是确诊胎儿染色体异常片段的最佳方法,NIPT与CMA的联合应用将会进一步提升染色体异常的检测效率,进一步奠定其在产前诊断中的应用价值。
本研究中B超异常是主要的产前诊断临床指征,通过CMA实现对B超异常病例的及时诊断是非常有临床意义的。通过对B超异常病例的分类分析发现,多系统异常病例的阳性率明显高于单系统异常病例的阳性率,提示遗传咨询中需更加关注B超多系统异常病例,合理开展相关的检查。此外,相较于传统的核型分析,针对B超异常病例,CMA可多检出2.67%的异常胎儿,大大提高异常胎儿的检出率。随着CMA在产前诊断中的深入应用,中外权威机构先后出台了相应指南规范,推荐CMA为产前B超异常胎儿遗传学检测的首选方法[4,15]。然而,目前国内相关的临床数据仍需要更多的积累,来进一步证实CMA在产前诊断中的应用价值。
虽然CMA可以检出更多的染色体异常,但是CMA的高分辨率也会检出较多的临床意义未明CNV,又称VOUS,给孕妇造成巨大的精神压力,可能会导致不必要的引产。因此,应严格界定产前诊断的临床指征,且在进行产前诊断前充分做好遗传咨询[16]。本研究中约有9.11%为临床意义未明CNV病例,高于国外研究VOUS占比不超过5.00%的报道[17]。对本研究VOUS占比高于国外的一些报道进行分析,我们发现,需要通过及时结合新指南调整VOUS片段的报告标准,减少不必要的VOUS片段报告;进一步完善父母验证的临床路径,排除家族良性的可能;另外,需要多中心合作,积累中国人群的检测数据,完善基于中国人群的本地化数据库,提高国内产前诊断基因芯片诊断的质量。
本研究435例随访病例中,正常活产的胎儿VOUS病例占10.82%(33/305),提示CMA检出VOUS病例有些是没有致病意义的,因此,检测后的遗传咨询为至关重要的环节,需谨慎对待,本研究为产前遗传咨询指导优生优育提供了重要的数据支撑。出生异常胎儿CMA检测正常的病例占76.92%(20/26),一是考虑CMA不能检测点突变和平衡性结构重排等异常,二是考虑遗传因素为胎儿缺陷的主要原因,不能排除环境污染、病毒感染、滥用药物、生活习惯等其他因素导致的胎儿缺陷。提示产前遗传咨询需结合孕妇的生活工作环境等因素综合评估胎儿的生长情况,切实做好出生缺陷防控工作。
4 结论与展望
染色体异常是导致胎儿畸形的重要原因之一,针对染色体异常检测发展出了不同的检测方法,如核型分析可检出大片段染色体异常和平衡性结构重排,CMA可检出小片段的染色体变异,全外显子组测序(whole exome sequencing,WES)可检出基因点突变,这些技术的联合应用基本可以检出常见的遗传性变异,而CMA在其中扮演着非常重要的角色。同时也说明每项技术都有其局限性,正如NIPT检测准确性较高,但仍属于筛查,不能替代羊膜腔穿刺术[18],同样也不能取代血清学筛查。因此,实现多技术的联合应用,可为孕妇提供更全面客观的临床信息,有助于临床医生做出更准确的判断,提出更合理的建议,进而为降低出生缺陷贡献力量,同样这也为临床实验室提出了更高的要求,想必也是大势所趋。
本研究由于样本量有限,部分结果可能与现有报道存在一定的差异,为进一步提高数据的可信度,未来需要统计更多的临床病例或者开展多中心合作。
