布鲁氏菌病微量补体结合试验的方法改进和应用
2022-05-16蒋卉冯宇秦玉明朱良全范学政丁家波
蒋卉,冯宇,秦玉明,朱良全,范学政,丁家波*
布鲁氏菌病微量补体结合试验的方法改进和应用
蒋卉1,冯宇2,秦玉明2,朱良全2,范学政1,丁家波1*
1中国农业科学院北京畜牧兽医研究所,北京 100193;2中国兽医药品监察所,国家/OIE布鲁氏菌病参考实验室,北京 100081
【目的】补体结合试验是布鲁氏菌病(简称“布病”)血清学确诊方法。现行国家标准《动物布鲁氏菌病诊断技术》(GB/T 18646-2018)中收录的补体结合试验分为常量法补体结合试验(CFT)和微量法补体结合试验(mCFT),但两者之间的相关技术参数和结果判定标准均存在差异,导致常量法CFT和mCFT检测结果不一致。笔者通过对mCFT参数的改进优化,使现行标准中mCFT的检测结果等效于常量法CFT,实现布病CFT的高通量准确诊断,对现有布病检测方法进行了补充。【方法】参照布病常量法CFT反应条件和诊断标准,对现行国标中mCFT的反应时间、稀释液、效价测定方法、结果判定等相关参数进行改进优化。改进后的mCFT方法与原mCFT方法相比,效价测定中受检血清的稀释度由1﹕2—1﹕64稀释改为1﹕10稀释,稀释方法与常量法CFT相同,确保微量法的检测临界值与常量法一致;采用酶标仪读取OD600值判定溶血强度,降低了试验人员肉眼判定的误差,提升了结果判定的效率和准确性;反应时间由37℃水浴30 min缩短为20 min,提高了检测效率又不影响检测结果;稀释液由巴比妥缓冲液改为生理盐水,与常量法使用相同稀释液并可获得理想结果。用改进的mCFT与国标的mCFT、常量法CFT分别对来自内蒙古、山东、北京、江苏等地区的409份临床牛、羊血清样品(牛血清163份、羊血清246份)进行检测,分析比较其符合率。【结果】采用改进的mCFT与常量法CFT对409份临床样品进行比对检测,改进的mCFT方法检出53份阳性、11份可疑、345份阴性;常量法CFT检出53份阳性、9份可疑、347份阴性。比较两者检测结果,只有2份牛血清样品用改进的mCFT方法检测为可疑,而常量法CFT检测为阴性,其余407份样品检测结果均一致。其中牛血清样品的符合率98.77%,羊血清样品的符合率100%,总符合率99.51%。而国标mCFT方法因阳性判定标准低于常量法CFT,且不设可疑区间,结果检出97份阳性、312份阴性。与常量法CFT结果相比较,牛血清样品的符合率88.34%,羊血清样品的符合率89.84%,总符合率为89.24%,远低于本研究改进的mCFT方法与常量法CFT 99.51%的符合率。【结论】通过对mCFT方法各参数的优化,建立了一种与常量法CFT判定标准一致,且检测结果高度符合的mCFT方法。
布鲁氏菌病;微量法补体结合试验;方法改进;应用
0 引言
【研究意义】布鲁氏菌病(Brucellosis,简称布病)是由布鲁氏菌引起的一种世界性重要人畜共患病,也是最易被忽视的重要传染病之一[1-4]。家畜感染布病后主要表现为流产、早产、不孕、瘦弱、关节肿大和产奶量减少等。人感染布鲁氏菌可表现出多种热型,同时具有多汗、乏力、头痛与骨关节肌肉疼痛等症状,若不及时治疗,往往难以治愈。因而,布病严重危害全球牛羊养殖业和人类健康[5-6]。该病属于《中华人民共和国传染病防治法》规定的乙类传染病;《一、二、三类动物疫病病种名录》(中华人民共和国农业部公告第1125号)规定的二类动物传染病。上世纪90年代,通过疫苗免疫等防控措施,我国曾有效控制了畜间和人间布病疫情的发生。然而进入21世纪之后,随着我国畜牧养殖业的快速发展和家畜频繁跨区域流动,畜间和人间布病疫情出现明显反弹,并逐年递增。当前,布病防控形势依然十分严峻,根据国家卫健委网站发布公告统计,2020年我国人间布病新增病例为47 245人,比2019年上升了7.29%。人患布病主要是因接触患病动物或饮用被布鲁氏菌污染的生乳品而感染[7-9],准确诊断是有效防控动物布病的前提[10]。【前人研究进展】我国《动物布鲁氏菌病诊断技术》(GB/T 18646-2018)国家标准(以下简称“布病国标”)中布病血清学诊断方法主要有虎红平板凝集试验(RBT)、全乳环状反应(MRT)、试管凝集试验(SAT)、补体结合试验(CFT)、iELISA、cELISA[11],其中CFT是国标和世界动物卫生组织(OIE)推荐的布病血清学确诊方法[12-14]。CFT与SAT相比,具有更高的特异性;虽比ELISA操作复杂,但该方法是布病阳性血清定值的标准方法。CFT包括常量法和微量法,微量法补体结合试验(mCFT)是在常量法CFT基础上改进而来,与经典的常量法CFT相比,试剂用量小,操作简便,能满足高通量检测需求。【本研究切入点】我国现行布病国标中已纳入CFT的常量法和微量法,但是两种方法对于同一份血清样本的判定标准却不一致,常量法阳性判定标准的临界值是微量法的2.5倍,这种因标准差异导致的检测结果差异常常给检验人员造成困扰。另外,通过肉眼观察mCFT溶血抑制程度进行结果判定不仅带有一定的主观性,而且效率较低。【拟解决的关键问题】本研究通过统一mCFT与常量法CFT的判定标准,实现了检测结果的高度符合;同时通过读取OD600nm值代替肉眼对溶血程度的判定,提高结果读取效率和结果判断的准确性。并进一步采用常量法CFT、国标mCFT和本方法对内蒙古、山东、北京、江苏地区的牛、羊血清样品进行检测,比较其符合率,确认改进mCFT方法的可靠性。
1 材料与方法
1.1 试验时间和地点
本试验于2020年12月至2021年1月在北京中国兽医药品监察所国家/OIE布鲁氏菌病参考实验室进行。
1.2 主要试验材料、仪器与样品
抗原、冻干补体由中国兽医药品监察所生产供应,批号分别为202001、201904。溶血素购自索莱宝生物科技有限公司,批号20180810。生理盐水和阿氏液由国家/OIE布鲁氏菌病参考实验室参照《兽用生物制品规程》(2000 版)制备[15]。红细胞采自公绵羊,按1﹕1(体积比)保存于阿氏液中,存放于4℃。布病阳性血清标准品购买自英国The National Institute for Biological Standards and Control (NIBSC),经CFT标定为1000 IU,批号2BADS。日立离心机,型号:HITACHI CF16RN;涡旋器,型号:Kylin-Bell VORTEX-5;全波长酶标仪,型号:Molecular Devices MAX 190,由中国兽医药品监察所提供。临床样品来源于2019—2020年分别从内蒙古、山东、北京、江苏4个不同的省份的采集的牛、羊血清409份。
1.3 2.5%红细胞悬液的制备
取在阿氏液中保存了7 d的绵羊红细胞(Sheep red blood cell,SRBC),以5—10倍体积的生理盐水离心沉淀并洗涤3次,最后一次以2 000 r/min离心10 min,弃去上清,取沉淀红细胞,用生理盐水配制成2.5%红细胞悬液。
1.4 标准比色孔的配制
取500 μL 2.5%红细胞悬液离心后去上清,加入2 mL蒸馏水,用力振摇,使红细胞完全溶解,再加入500 μL 4.5% NaCl溶液,制成100%溶血液。再取500 μL 2.5% 红细胞悬液,加入2 mL生理盐水,混匀后制成100%不溶血液。取96孔U型底微孔板,按表1制成标准比色孔,使用酶标仪读取并记录11个标准溶血孔的OD600nm值。
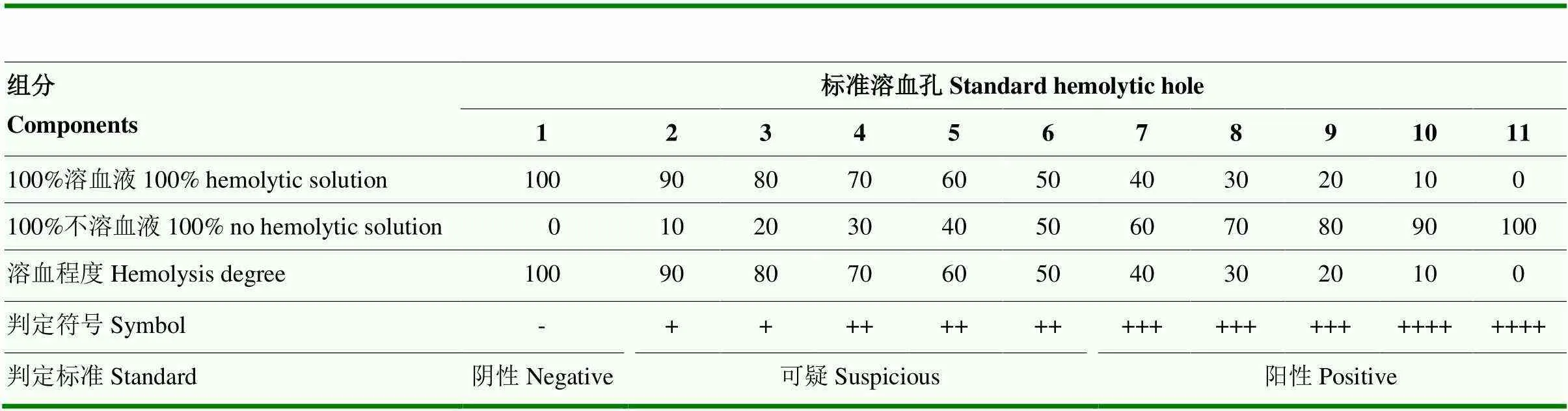
表1 标准比色孔的配制
1.5 溶血素、补体和抗原效价的测定
1.5.1 溶血素效价的测定 取0.1 mL溶血素加生理盐水4.9 mL,制成1﹕100稀释液(因商品化溶血素均含有等量甘油作防腐剂,因此0.1 mL中实际只含有0.05mL标定效价的溶血素)。再取1﹕100稀释液1 mL加生理盐水4 mL,制成1﹕500基础稀释液。取1﹕500基础稀释液按下表2制成不同稀释度溶血素。取1瓶冻干补体,用生理盐水配制1﹕10稀释液。取96孔U型底微孔板,按表3依次加入不同稀释度溶血素、2.5%红细胞、1﹕10稀释补体、生理盐水,使总量为125 μL。振荡混匀后置37℃水浴作用20 min,取出后立即用酶标仪读取并记录各孔的OD600nm值,并参照标准溶血孔的OD600nm值判定结果。
1.5.2 补体效价的测定 以生理盐水配制1﹕10补体基础稀释液(如补体活力高可配制1﹕20基础稀释液)和一个工作量的抗原稀释液。取96孔U型底微孔板,按表4依次加入补体稀释液、抗原、生理盐水于A行各孔,B行不加抗原用生理盐水补充,其余成分与A行相同。振荡混匀后置37℃水浴作用20 min。取出后每孔加入2.5%红细胞和2个单位溶血素各25 μL,振荡混匀后再置37℃水浴作用20 min,取出后立即用酶标仪读取并记录各孔的OD600nm值,并参照标准溶血孔的OD600nm值判定结果。

表2 溶血素的稀释
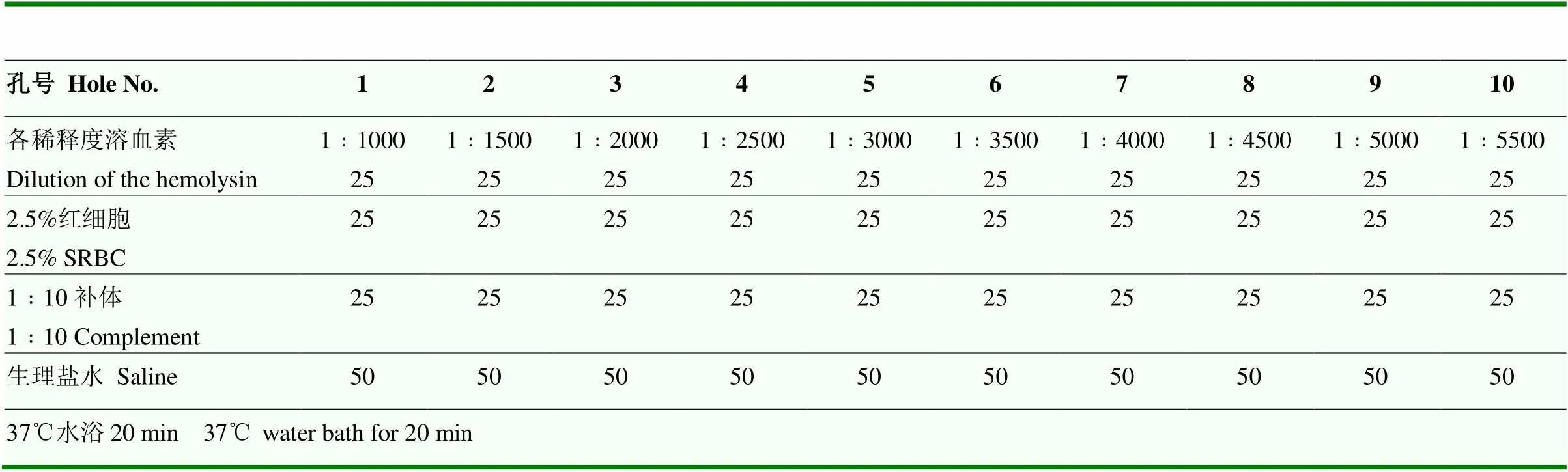
表3 溶血素效价的测定

表4 补体效价的测定
1.5.3 抗原效价的测定 商品化抗原可按说明书稀释到工作量使用。如要测定效价,可用生理盐水将抗原原液制成1﹕10、1﹕50、1﹕75、1﹕100、1﹕150、1﹕200、1﹕250、1﹕300、1﹕400和1﹕500稀释液。用生理盐水将布病阳性血清标准品制成1﹕120、1﹕160、1﹕200、1﹕240、1﹕280稀释液,将布病阴性血清制成1﹕10稀释液。稀释后的阴、阳性血清56℃水浴灭能30 min。取96孔U型底微孔板,按表5依次加入稀释抗原、稀释血清、工作补体、生理盐水,振荡混匀后置37℃水浴作用20 min。取出后每孔加入2.5%红细胞和2个单位溶血素各25 μL,振荡混匀后再置37℃水浴作用20 min,取出后立即用酶标仪读取并记录各孔的OD600nm值,并参照标准溶血孔的OD600nm值判定结果。
1.6 临床样品的检测
1.6.1 改进的mCFT检测 通过上述溶血素、补体、抗原最佳浓度的测定后,将临床血清409份(其中牛血清163份、羊血清246份)、阳性对照血清和阴性对照血清在96孔深孔稀释板中用生理盐水作1﹕10倍稀释,放入水浴锅中灭能,牛血清样品用56℃灭能30 min,羊血清样品用58℃灭能30 min。然后取96孔U型底微孔板按表6进行临床样品的检测,用酶标仪读取并记录各孔的OD600nm值并判定结果。阳性血清加抗原对照孔和溶血素对照孔,须完全抑制溶血;阳性血清不加抗原对照孔和其他对照孔完全溶血,试验成立。被检临床血清不加抗原对照孔应完全溶血,表明反应结果符合要求,可判定被检临床血清加抗原检测孔结果,对照表1标准比色孔OD600nm值判定结果。100%溶血判定为阴性;50%—90%溶血判为可疑;0%—40%溶血判为阳性。
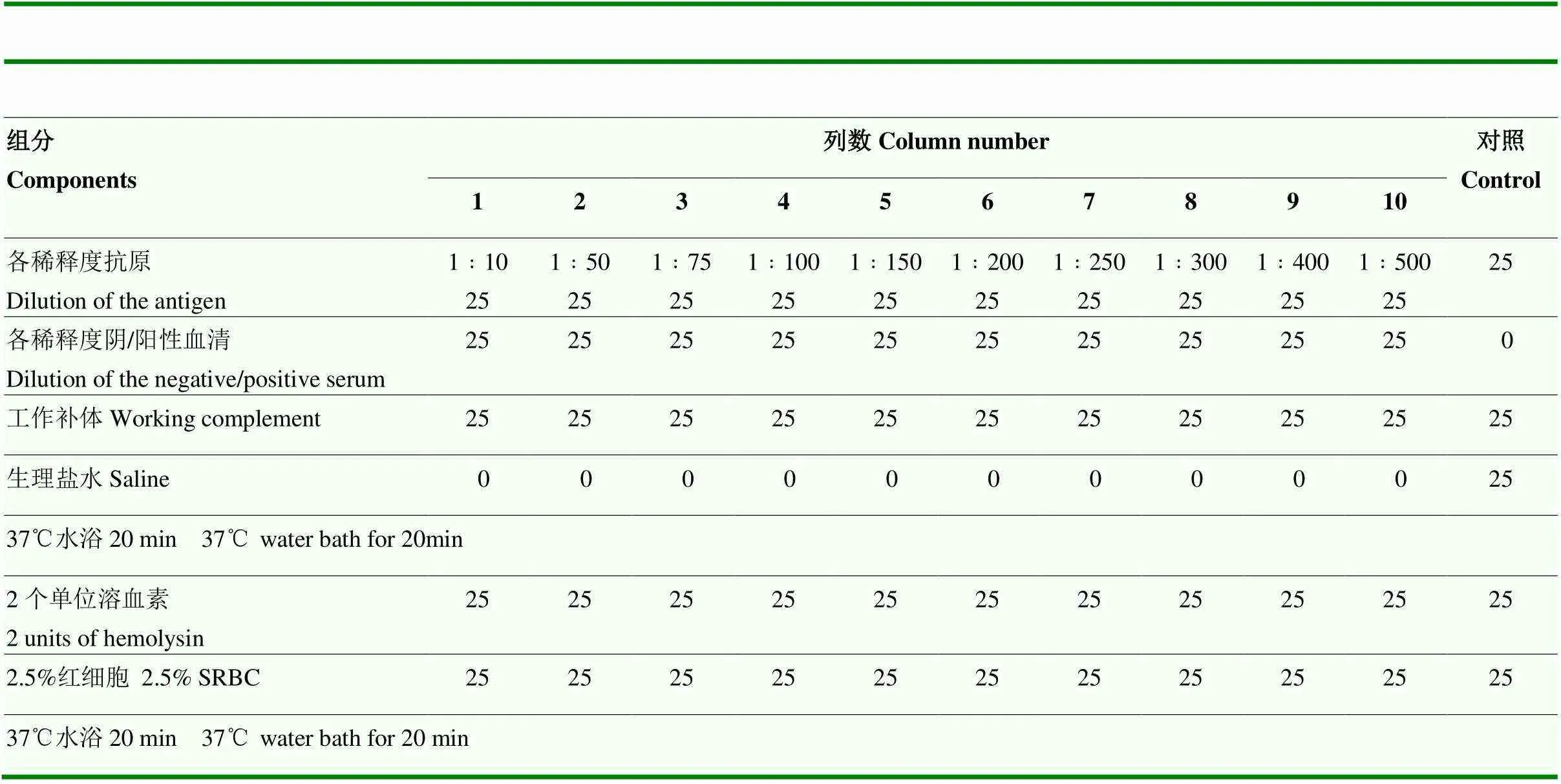
表5 抗原效价的测定
1.6.2 国标mCFT和常量法CFT检测 按照国家标准《动物布鲁氏菌病诊断技术》(GB/T 18646-2018)[9]对409份临床血清样品分别进行mCFT和常量法CFT检测,将1.6.1中改进mCFT、1.6.2中国标mCFT的检测结果分别与常量法CFT进行符合率比较。
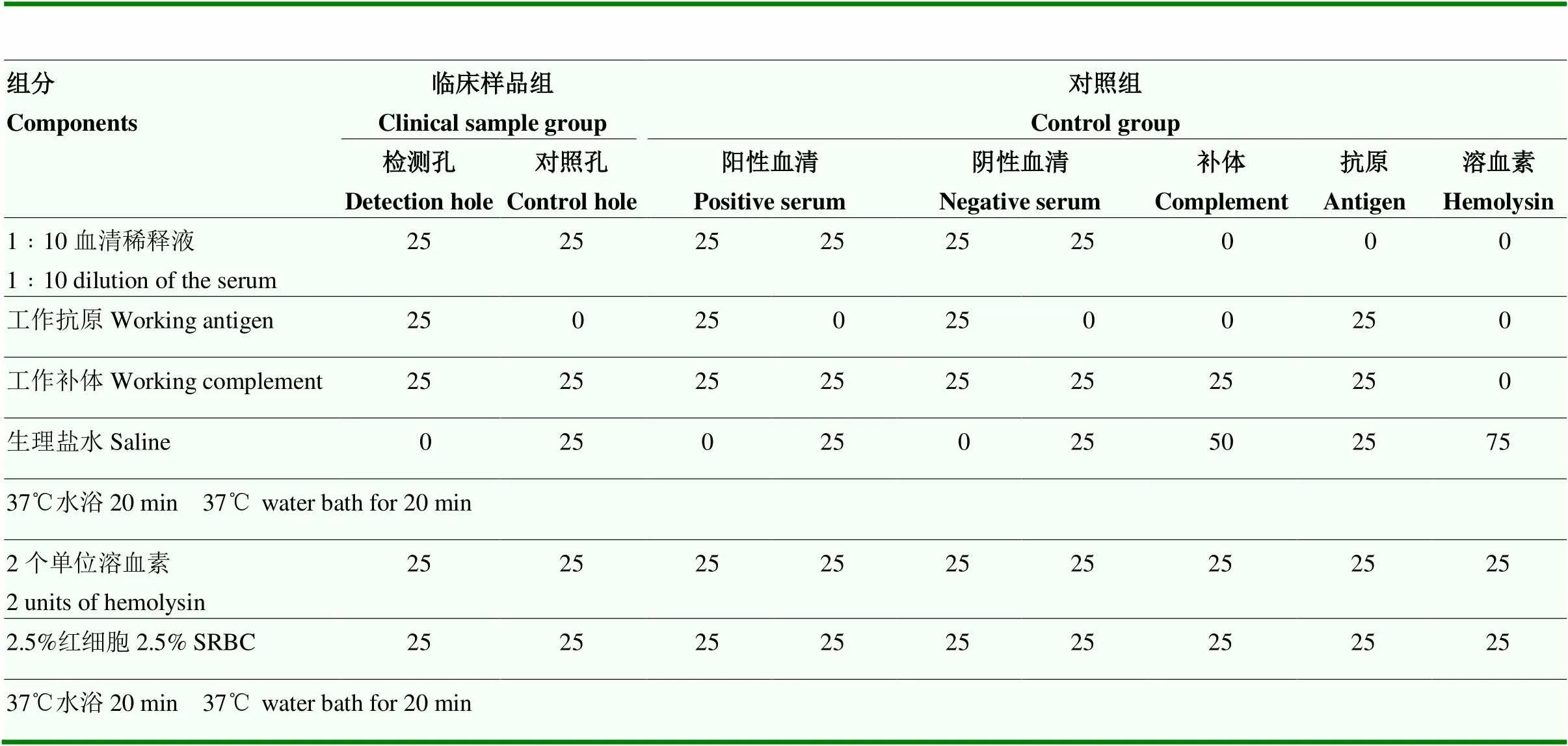
表6 临床样品的检测
2 结果
2.1 溶血素效价测定
在过量补体的存在下,能使25 μL的2.5%红细胞完全溶血的溶血素最高稀释度,即为溶血素效价。本试验测得溶血素效价为1﹕3 000,进行正式试验时,溶血素的使用浓度比其效价大一倍(即2个单位),为1﹕1 500。
2.2 补体效价测定
在2个单位溶血素的存在下,能使25 μL的2.5%红细胞完全溶血的补体最小使用量,即为补体效价。按公式计算,原补体稀释倍数=补体稀释倍数/稀释后补体加入量×正式试验时每管需要加入的工作补体量。本试验测得第5孔为能使25 μL的2.5%红细胞完全溶血的补体最小使用量,对照表4即使用的补体稀释倍数为10,稀释后补体加入量为11,正式试验时每管需要加入的工作补体量为25,因此原补体稀释倍数为10/11×25≈22.7,补体应作1﹕22.7倍使用。考虑到补体的不稳定性,正式试验时工作补体浓度应比补体效价大10%,即本试验工作补体浓度为1﹕20。
2.3 抗原效价的测定
对布病阳性血清标准品各稀释度均发生最强抑制溶血的抗原最高稀释度,即为抗原的效价。本试验测得抗原在1﹕150倍稀释时与布病阳性血清标准品各稀释度均能发生最强抑制溶血反应,因此抗原效价为1﹕150。实际使用时应比测得的效价提高25%的浓度使用,即本试验工作抗原浓度为1﹕112.5。
2.4 临床样品的检测
在2.1、2.2和2.3结果的基础上,按照表6的操作方法对来自北京(牛血清94份)、山东(牛血清69份)、内蒙古(羊血清140份)和江苏(羊血清106份)的409份临床血清样品进行检测。结果阳性血清加抗原对照孔和溶血素对照孔须完全抑制溶血,阳性血清不加抗原对照孔和其他对照孔完全溶血,试验成立。被检临床血清不加抗原对照孔完全溶血,表明反应结果符合要求。根据判定标准,读取被检临床血清加抗原检测孔的OD600nm值,对照表1标准比色孔OD600nm值判定结果。409份临床牛、羊血清中53份阳性、11份可疑、345份阴性。另外按照国家标准《动物布鲁氏菌病诊断技术》(GB/T 18646-2018)[9]对上述409份样品进行国标mCFT和常量法CFT平行检测。结果常量法CFT检出53份阳性、9份可疑、347份阴性,与本研究改进的mCFT检测结果相比较,只有2份牛血清样品用改进的mCFT方法检测为可疑,而常量法CFT检测为阴性,其余407份样品检测结果均一致。牛血清样品的符合率98.77%,羊血清样品的符合率100%,总符合率99.51%。而国标mCFT方法因阳性判定标准低于常量法CFT,且不设可疑区间,结果检出97份阳性、312份阴性,与常量法CFT相比较,牛血清样品的符合率88.34%,羊血清样品的符合率89.84%,总符合率为89.24%。具体结果见表7。

表7 临床样品布鲁氏菌病补体结合试验检测结果
3 讨论
3.1 现行国标中CFT常量法与微量法的结果制定存在差异
补体结合试验是一种经典的抗原、抗体检测方法,可用于诊断各种传染病,是免疫学上一个应用较广泛的重要试验[16-17]。在布病的血清学诊断方法中,相较于其他方法,CFT具有更高的特异性[18-20],是国际公认的确诊方法之一[21-23],但是该方法操作复杂,实验体系包括溶血素、红细胞、补体、血清、抗原、生理盐水等多种成分[24-25],除生理盐水以外,其余5种成分相互间存在着严格的量值关系[26]。因此该试验对操作人员的要求较高,且用时长,未能在基层实验室得到广泛应用[27-28]。尽管如此,CFT方法作为布病阳性血清定值的标准方法[13, 29],是用于国际间布病实验室能力比对的重要方法之一,在布病血清学诊断中具有不可替代性。
我国布病诊断国标中CFT包括常量法和微量法两种。常量法试剂使用量较大,摆放和标记试管费时费力,不适合大量样本的检测。微量法相对于常量法更容易操作,适用于大量样本的检测。目前布病诊断国标中采用的微量法与常量法对阴阳性结果的判定标准存在较大差异,比如在常量法中,对布病阳性的判定值≥50 IU·mL-1;而在微量法中,布病阳性的判定值为≥20 IU·mL-1。因此,当某一份血清其布病抗体效价介于20—50 IU·mL-1时,微量法检测为阳性,而常量法则判为阴性或可疑。因此,统一微量法与常量法的判定标准十分必要。另外,由于微量法在判定溶血抑制程度时是通过肉眼比较各反应孔与溶血标准比色孔之间的接近程度进行的,主观性强,而且费时费力,误差较大。
3.2 改进后的微量法CFT与常量法判定标准一致
针对布病诊断国标中mCFT存在的突出问题,本研究参照常量法CFT的反应条件和判定标准,从反应时间、稀释液、效价测定方法、结果判定等各方面对国标mCFT进行了改进,改进后的方法既提升了mCFT的检测效率,又能达到了常量法的准确性。为了克服检验人员对96孔U型底微孔板溶血程度判定的误差,本研究采用了酶标仪读取溶血强度;反应时间由37℃水浴30 min缩减为20 min,与常量法CFT反应时间一致,既提高的检测效率又不影响检测结果;稀释液由巴比妥缓冲液改为生理盐水,主要是巴比妥类试剂为中枢神经系统的镇静剂,可用于镇静与麻醉,难以购买获得,而与常量法CFT一样使用生理盐水作为稀释液亦可获得满意的结果;效价测定中受检血清的稀释度由1﹕2—1﹕64稀释改为1﹕10稀释,稀释方法与常量法CFT一致,确保了微量法与常量法判定标准一致。在此基础上,我们用改进的mCFT方法与常量法同时对409份临床牛、羊血清样品进行检测,结果符合率99.51%,高于国标中mCFT与常量法89.24%的符合率。
需要注意的是补体结合试验各成分之间量的关系起始于红细胞,以红细胞作为基础尺度,才能规定溶血素和补体的用量[30]。有了补体的用量,衡量受检血清的阴、阳性才有了标准。如果红细胞的用量改变了,则规定出来的补体用量和阴、阳性标准也就改变了。因此每次试验操作中红细胞的浓度和用量必须准确,新配制的红细胞悬液应重新配置标准溶血孔并读取OD600nm值,重新滴定溶血素和补体的效价,才能使每次试验得到相同的结果,确保试验结果的准确性和可重复性。
4 结论
通过对微量法补体结合试验(mCFT)各参数的优化,建立了一种与常量法补体结合试验(CFT)判定标准一致,且检测结果高度符合的mCFT方法,特别是通过酶标仪读数代替肉眼观察,保证了检测结果的准确性,同时缩短了检测时间。与常量法CFT相比较,操作步骤相对简单,适用于实验室大量样本的检测,更易在基层实验室推广应用。在国家/OIE布病参考实验室大量临床样本的检测中,该方法与布病间接ELISA方法的联合使用,提高了检测结果的准确性,是对现有布病诊断方法的完善与补充。
[1] DEAN A S, CRUMP L, GRETER H, SCHELLING E, ZINSSTAG J.Global burden of human brucellosis: a systematic review of disease frequency.PLoS Neglected Tropical Diseases, 2012, 6(10): e1865.doi:10.1371/journal.pntd.0001865.
[2] MCDERMOTT J, GRACE D, ZINSSTAG J.Economics of brucellosis impact and control in low-income countries.Revue Scientifique et Technique (International Office of Epizootics), 2013, 32(1): 249-261.doi:10.20506/rst.32.1.2197.
[3] SELEEM M N, BOYLE S M, SRIRANGANATHAN N.Brucellosis: a re-emerging zoonosis.Veterinary Microbiology, 2010, 140(3/4): 392-398.doi:10.1016/j.vetmic.2009.06.021.
[4] TADESSE G.Brucellosis seropositivity in animals and humans in Ethiopia: a meta-analysis.PLoS Neglected Tropical Diseases, 2016, 10(10): e0005006.doi:10.1371/journal.pntd.0005006.
[5] HARRISON E R, POSADA R.Brucellosis.Pediatrics in Review, 2018, 39(4): 222-224.doi:10.1542/pir.2017-0126.
[6] ZHANG N, HUANG D S, WU W, LIU J, LIANG F, ZHOU B S, GUAN P.Animal brucellosis control or eradication programs worldwide: a systematic review of experiences and lessons learned.Preventive Veterinary Medicine, 2018, 160: 105-115.doi:10.1016/ j.prevetmed.2018.10.002.
[7] MORENO E.Retrospective and prospective perspectives on zoonotic brucellosis.Frontiers in Microbiology, 2014, 5: 213.doi:10.3389/ fmicb.2014.00213.
[8] TSCHOPP R, BEKELE S, MOTI T, YOUNG D, ASEFFA A.Brucellosis and bovine tuberculosis prevalence in livestock from pastoralist communities adjacent to Awash National Park, Ethiopia.Preventive Veterinary Medicine, 2015, 120(2): 187-194.doi:10.1016/ j.prevetmed.2015.03.004.
[9] NJERU J, WARETH G, MELZER F, HENNING K, PLETZ M W, HELLER R, NEUBAUER H.Systematic review of brucellosis in Kenya: disease frequency in humans and animals and risk factors for human infection.BMC Public Health, 2016, 16(1): 853.doi:10.1186/ s12889-016-3532-9.
[10] 丁家波, 董浩.动物布鲁氏菌病.北京: 中国农业出版社, 2020.
DING J B, DONG H.Animal Brucellosis.Beijing: Chinese Agriculture Press, 2020.(in Chinese)
[11] GB/T 18646-2018.动物布鲁氏菌病诊断技术.2018.
GB/T 18646-2018.Diagnostic technology for animal brucellosis.2018.(in Chinese)
[12] 朱良全, 王芳, 蒋卉, 冯宇, 张金亚, 张阁, 张振, 皮向成, 王楠, 毛开荣, 丁家波.动物布鲁菌病补体结合试验诊断方法比较研究.中国兽医学报, 2016, 36(2): 357-361, 368.doi:10.16303/j.cnki.1005- 4545.2016.02.33.
ZHU L Q, WANG F, JIANG H, FENG Y, ZHANG J Y, ZHANG G, ZHANG Z, PI X C, WANG N, MAO K R, DING J B.A comparative study on the complement fixation test for diagnosis of animal brucellosis.Chinese Journal of Veterinary Science, 2016, 36(2): 357-361, 368.doi:10.16303/j.cnki.1005-4545.2016.02.33.(in Chinese)
[13] Officeinter national des epizooties.OIE Terrestrial Manual.World Organization for Animal Health, 2018.
[14] 王芳, 冯宇, 张阁, 蒋卉, 朱良全, 丁家波.牛布鲁氏菌间接ELISA抗体检测方法的建立.中国农业科学, 2016, 49(9): 1818- 1825.doi:10.3864/j.issn.0578-1752.2016.09.018.
WANG F, FENG Y, ZHANG G, JIANG H, ZHU L Q, DING J B.Development of indirect ELISA for antibody of.Scientia Agricultura Sinica, 2016, 49(9): 1818-1825.doi:10.3864/j.issn.0578-1752.2016.09.018.(in Chinese)
[15] 农业部兽用生物制品规程委员会.中华人民共和国兽用生物制品规程.化学工业出版社,2000.
Veterinary Biological Products Regulation Committee of the Ministry of Agriculture.Rules of veterinary biological products of the people's Republic of China.Chemistry Industry Press, 2000.(in Chinese)
[16] 孙向彬, 贺亚玲, 袁俐, 王仙.控制好补体活性的理化因素提高“补体结合试验”效果.农垦医学, 2014, 36(3): 283-284.doi:10.3969/ j.issn.1008-1127.2014.03.033.
SUN X B, HE Y L, YUAN L, WANG X.Controlling the physical and chemical factors of complement activity to improve the effect of complement fixation test.Journal of Nongken Medicine, 2014, 36(3): 283-284.doi:10.3969/j.issn.1008-1127.2014.03.033.(in Chinese)
[17] NEUBAUER H, SPRAGUE L D, ZACHARIA R, TOMASO H, AL DAHOUK S, WERNERY R, WERNERY U, SCHOLZ H C.Serodiagnosis ofinfections in horses: state-of- the-art and perspectives.Journal of Veterinary Medicine Series B, 2005, 52(5): 201-205.doi:10.1111/j.1439-0450.2005.00855.x.
[18] STEMSHORN B W, FORBES L B, EAGLESOME M D, NIELSEN K H, ROBERTSON F J, SAMAGH B S.A comparison of standard serological tests for the diagnosis of bovine brucellosis in Canada.Canadian Journal of Comparative Medicine, 1985, 49(4): 391-394.
[19] MATOPE G, MUMA J B, TOFT N, GORI E, LUND A, NIELSEN K, SKJERVE E.Evaluation of sensitivity and specificity of RBT, c-ELISA and fluorescence polarisation assay for diagnosis of brucellosis in cattle using latent class analysis.Veterinary Immunology and Immunopathology, 2011, 141(1/2): 58-63.doi:10.1016/j.vetimm.2011.02.005.
[20] PFUKENYI D M, MELETIS E, MODISE B, NDENGU M, KADZVITI F W, DIPUO K, MOESI K, KOSTOULAS P, MATOPE G.Evaluation of the sensitivity and specificity of the lateral flow assay, Rose Bengal test and the complement fixation test for the diagnosis of brucellosis in cattle using Bayesian latent class analysis.Preventive Veterinary Medicine, 2020, 181: 105075.doi:10.1016/j.prevetmed.2020.105075.
[21] NIELSEN K.Diagnosis of brucellosis by serology.Veterinary Microbiology, 2002, 90(1/2/3/4): 447-459.doi:10.1016/S0378-1135 (02)00229-8.
[22] LAKEW A, HIKO A, ABRAHA A, HAILU S M.Sero-prevalence and community awareness on the risks associated with Livestock and Human brucellosis in selected districts of Fafan Zone of Ethiopian- Somali National Regional State.Veterinary and Animal Science, 2019, 7: 100047.doi:10.1016/j.vas.2019.100047.
[23] SYLLA S, SIDIMÉ Y, SUN Y X, DOUMBOUYA S, CONG Y L.Seroprevalence investigation of bovine brucellosis in macenta and yomou, Guinea.Tropical Animal Health and Production, 2014, 46(7): 1185-1191.doi:10.1007/s11250-014-0625-2.
[24] KHAN I, WIELER L H, MELZER F, GWIDA M, DE A SANTANA V L, DE SOUZA M M A, SAQIB M, ELSCHNER M C, NEUBAUER H.Comparative evaluation of three commercially available complement fixation test antigens for the diagnosis of glanders.Veterinary Record, 2011, 169(19): 495.doi:10.1136/vr.d5410.
[25] KHAN I, WIELER L H, SAQIB M, MELZER F, SANTANA V L D A, NEUBAUER H, ELSCHNER M C.Effect of incubation temperature on the diagnostic sensitivity of the glanders complement fixation test.Revue Scientifique et Technique (International Office of Epizootics), 2014, 33(3): 869-875.doi:10.20506/rst.33.3.2324.
[26] 赵凤菊, 李井春, 于学武.动物布鲁菌病补体结合试验的影响因素及应注意的问题.畜牧与饲料科学, 2010, 31(9): 144-145.doi:10.16003/j.cnki.issn1672-5190.2010.09.026.
ZHAO F J, LI J C, YU X W.Influencing factors and notable problems of complement fixation test for brucellosis of animals.Animal Husbandry and Feed Science, 2010, 31(9): 144-145.doi:10.16003/ j.cnki.issn1672-5190.2010.09.026.(in Chinese)
[27] ELSCHNER M, LAROUCAU K, SINGHA H, TRIPATHI B N, SAQIB M, GARDNER I, SAINI S, KUMAR S, EL-ADAWY H, MELZER F, KHAN I, MALIK P, SAUTER-LOUIS C, NEUBAUER H.Evaluation of the comparative accuracy of the complement fixation test, Western blot and five enzyme-linked immunosorbent assays for serodiagnosis of glanders.PLoS One, 2019, 14(4):e0214963.
[28] 沈红霞, 倪柏锋, 王彬, 虞一聪, 周炜, 周芷锦, 穆琳, 桂平雄, 赵灵燕.动物布鲁氏菌病抗体补体结合试验与cELISA检测结果比较.浙江畜牧兽医, 2021, 46(1): 1-4.
SHEN H X, NI B F, WANG B, YU Y C, ZHOU W, ZHOU Z J, MU L, GUI P X, ZHAO L Y.The comparison of the results of complement fixation test and cELISA for animal brucellosis antibody.Zhejiang Journal Animal Science and Veterinary Medicine, 2021, 46(1): 1-4.(in Chinese)
[29] CORRENTE M, DESARIO C, PARISI A, GRANDOLFO E, SCALTRITO D, VESCO G, COLAO V, BUONAVOGLIA D.Serological diagnosis of bovine brucellosis using B.melitensis strain B115.Journal of Microbiological Methods, 2015, 119: 106-109.doi:10.1016/j.mimet.2015.10.012.
[30] 蒋卉, 彭小薇, 张阁, 冯宇, 张振, 孙翠丽, 朱良全, 丁家波.绵羊红细胞敏感性对补体结合试验的最佳反应时间.微生物学通报, 2016, 43(9): 2102-2104.doi:10.13344/j.microbiol.china.151039.
JIANG H, PENG X W, ZHANG G, FENG Y, ZHANG Z, SUN C L, ZHU L Q, DING J B.The optimum reaction time of sheep red blood cell sensitivity on complement fixation test.Microbiology China, 2016, 43(9): 2102-2104.doi:10.13344/j.microbiol.china.151039.(in Chinese)
Method Improvement and Its Application of Micro Complement Fixation Test for Brucellosis
JIANG Hui1, FENG Yu2, QIN YuMing2, ZHU LiangQuan2, Fan XueZheng1, DING JiaBo1*
1Institute of Animal Sciences of Chinese Academy of Agricultural Sciences, Beijing 100193;2National/OIE Reference Laboratory for Brucellosis, China Institute of Veterinary Drug Control, Beijing 100081
【Objective】 The complement fixation test is used as a confirmatory test for the serodiagnosis of brucellosis.The complement fixation tests are divided into constant complement fixation test (CFT) and micro complement fixation test (mCFT) in diagnostic techniques for animal brucellosis (GB/T 18646-2018).However, there are differences in the related technical parameters and judgment of the result between them, which lead to the inconsistency of CFT and mCFT results.In this study, By the improvement and optimization of the parameters of mCFT, this study made the detection results ofmCFT equivalent to classicalCFT, and achieved the high-throughput and accurate diagnosis of CFT for brucellosis.【Method】 According to classical CFT reaction conditions and diagnostic criteria, the reaction time, diluent, titer determination, result judgment and other related parameters for the current national standard of mCFT were optimized and improved.Compared with the original method, the dilution of the tested serum was changed from 1:2-1:64 to 1:10.The dilution method was the same as classical CFTso that the detection critical value was consistent with the constant method.The OD600value was read by the microplate reader to determine the hemolysis intensity, which reduced the error caused by visual judgmentandimproved the efficiency and accuracy of result judgment.The reaction time was shortened from 30 min to 20 min in water bath at 37℃, which improved the detection efficiency without affecting the results.The diluent was changed from barbital buffer to normal saline, which used the same diluent of classical CFT andachievedsatisfactory results.The 409 clinical bovine and sheep serum samples (163 bovine serum samples and 246 sheep serum samples) from Inner Mongolia, Shandong, Beijing and Jiangsu were detected by improved mCFT, the national standard mCFT,and classical CFT, respectively.The coincidence rate was analyzed and compared.【Result】By detecting the 409 clinical samples, the result showed that 53 samples were positive, 11 sampleswere suspicious and 345 were negative by improved mCFT.The 53 positivesamples, 9 suspicioussamples and 347 negative samples were detected by classical CFT.Compared with the results of the two methods, only two bovine serum samples were suspicious by the improved mCFT, which were negative by classical CFT.The results of the other 407 samples were consistent.The coincidence rate of bovine serum samples was 98.77%, which of sheep serum samples was 100%, and the total coincidence rate was 99.51% between improved mCFT and classical CFT.However, the positive criteria of national standard mCFT were lower than that of classical CFT, and no suspicious interval was set.The results showed that 97 samples were positive and 312 samples were negative.Compared with the results of classical CFT, the coincidence rate of bovine serum samples was 88.34%, which of sheep serum samples was 89.84%; the total coincidence rate was 89.24%, which was far lower than 99.51% of improved mCFT and classical CFT.【Conclusion】 By optimizing the parameters of mCFT, the mCFT method was established, which was highly consistent with the criterion and the results of the classical CFT.
brucellosis; micro complement fixation test; method improvement; application
2021-04-12;
2021-05-31
国家重点研发计划(2016YFD0500902)
蒋卉,E-mail:15011216921@163.com。通信作者丁家波,Tel:010-61255327;E-mail:dingjiabo@126.com
(责任编辑 林鉴非)
