ICU中新发急性肾损伤首次连续肾脏替代治疗患者死亡的危险因素分析及风险预测模型构建
2022-05-16蒋怡佳席修明贾会苗李文雄
蒋怡佳, 席修明, 郑 爔, 贾会苗, 郑 悦, 李文雄
急性肾损伤(acute kidney injury, AKI)是指多种诱发因素导致的急性肾功能下降,以肌酐升高和(或)少尿为临床特点的常见综合征[1]。重症医学科(intensive care unit, ICU)患者AKI的发病率可高达57.3%[2]。对于合并难治性并发症的严重AKI患者,连续肾脏替代治疗(continuous renal replacement therapy, CRRT)是重要的治疗手段[3-4]。国外研究[5-7]显示,因AKI接受CRRT患者的住院病死率为38.6%~62.4%,目前国内尚无针对ICU患者的多中心研究数据。本研究将基于一项前瞻性多中心临床研究的数据库,回顾性分析ICU中因新发AKI接受CRRT治疗患者的临床特征和危险因素,并构建患者首次CRRT后28 d死亡的危险预测模型和列线图,以便于临床医生能早期判断患者预后并实施恰当的干预,从而有可能降低其病死率。
1 资料与方法
1.1研究对象 本研究数据来源于一项由全国17个ICU参与、关于脓毒症流行病学的观察性研究(CCCST研究)。CCCST研究前瞻性收集了2014年1月至2015年8月期间4910例ICU患者的临床资料。CCCST研究通过了各个参研中心的伦理委员会审核,总伦理审批号为2013FXHEC-KY2018,注册号为ChiCTR-ECH-13003934。本研究对象为转入ICU后的前7 d内出现新发AKI而接受CRRT治疗的患者。
1.1.1 纳入标准 ①年龄≥18岁;②ICU住院时间≥48 h;③在ICU前7 d内出现新发AKI且接受CRRT的患者。
1.1.2 排除标准 ①既往患有慢性肾功能不全者;②接受肾脏切除或肾脏移植手术者;③入住ICU前已经存在AKI者;④因非肾脏原因接受CRRT治疗者;⑤临床数据收集不全者。
1.2研究内容
1.2.1 数据采集 收集CCCST研究数据库中新发AKI并接受CRRT治疗患者的人口学资料、慢性合并症情况、疾病严重程度、临床及实验室数据和ICU治疗情况。人口学资料包括年龄、性别和慢性合并症情况。疾病严重程度包括急性生理学评分(APS)和启动CRRT时序贯器官衰竭评分(SOFA)。考虑到临床常用的急性生理与慢性健康状况评分Ⅱ(APACHEⅡ)包含年龄评分,而本研究统计时又纳入年龄变量,为避免统计偏移,应用APS评分来反映患者生理紊乱的严重程度。临床和实验室数据包括每日血肌酐和每小时尿量、启动CRRT时生命体征、是否应用机械通气及血管活性药物(去甲肾上腺素、肾上腺素、多巴胺)、是否合并脓毒症、AKI分级、CRRT开始日期及启动原因、首次CRRT治疗模式及抗凝方式、CRRT结束日期、ICU住院时间及总住院时间。本研究以患者首次CRRT后28 d是否存活为观察终点,并据此将患者分为存活组和死亡组。
1.2.2 定义和诊断标准 AKI诊断和分级标准依据2012年改善全球肾脏病预后(KDIGO)制定的指南[8],即符合以下任一项者可诊断为AKI:①血肌酐在48 h内升高绝对值≥0.3 mg/dL(26.5 μmol/L);②血肌酐较基线值升高≥1.5倍,已知或推测在之前的7 d内发生;③尿量<0.5 mL/(kg·h)超过6 h。血肌酐的基线值定义为纳入研究之前6个月至6 d内的5次血肌酐平均值,如果不能获得纳入前的血肌酐值,则应用改良饮食修正公式(MDRD)推算其血肌酐基线值[9]。AKI的分级标准见表1,如果患者同时满足血肌酐标准和尿量标准,取其中AKI分级最高者。新发AKI定义为患者入ICU后发生的AKI[10],转入ICU时已经存在AKI者不纳入本研究。脓毒症的诊断标准依据脓毒症和脓毒性休克国际会议共识确定的Sepsis 3.0定义[11]。
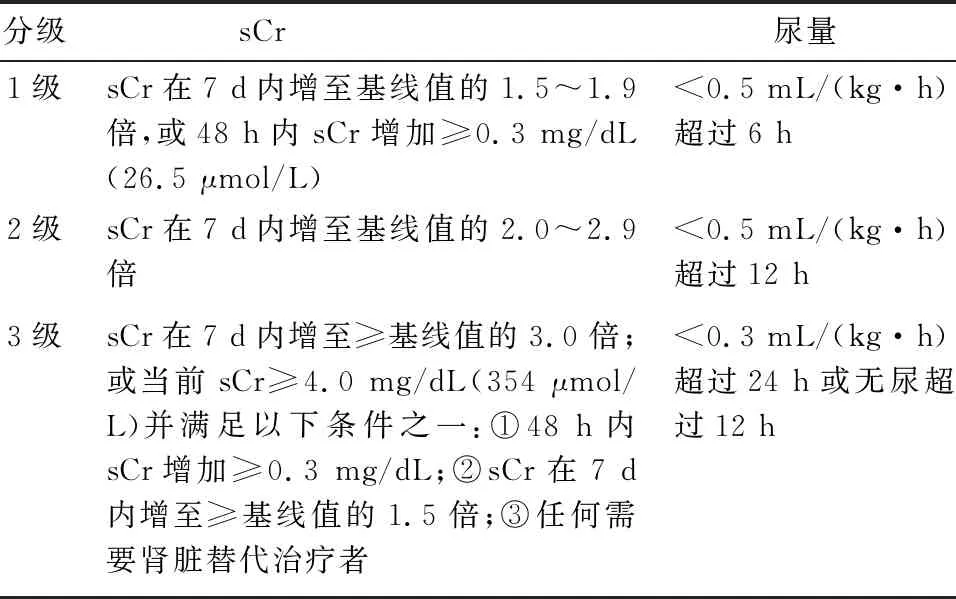
表1 AKI的分级标准
1.3统计学处理 采用SPSS 24.0软件进行统计学分析。计量资料以中位数(四分位间距)[M(P25~P75)]表示,组间比较采用非参数秩和检验;计数资料以频数(百分率)表示,组间比较采用χ2检验。将单因素分析具有统计学差异的变量和与临床密切相关的指标纳入多因素Logistic回归,采用逐步回归法(选入变量标准为P<0.1),筛选出CRRT患者28 d死亡的独立危险因素。将影响28 d死亡的危险因素引入R 3.6.1软件,应用rms程序包构建列线图(nomogram)预测模型,完成Logistic回归分析的可视化。通过Bootstrap重抽样法进行模型的内部验证并绘制校准曲线。绘制受试者工作特征(ROC)曲线评价列线图的预后预测能力。P<0.05为差异有统计学意义。
2 结果
2.1ICU中新发AKI合并CRRT患者的临床特征 筛查CCCST研究中4910例ICU患者的数据,1174例患者在入ICU后的前7 d内出现新发AKI。223例接受CRRT的新发AKI患者最终被纳入本研究,其中男性142例(63.7%),中位数年龄(四分位间距)67(48~78)岁;入ICU的前三位原因为脓毒症(53.4%)、术后监护(14.3%)及呼吸系统疾病(5.4%)。患者入ICU当天的中位数APS评分及启动CRRT时SOFA评分分别为20(13~25)分和10(7~13)分。首次开始CRRT治疗时,141例(63.2%)患者接受了机械通气,100例(44.8%)患者接受了血管活性药物治疗。首次启动CRRT时的AKI分级为2级(49.3%)和3级(50.7%)。其中152例(68.2%)患者满足AKI的血肌酐诊断标准,179例(80.3%)患者满足AKI的尿量诊断标准,108例(48.4%)患者同时满足血肌酐和尿量诊断标准。在开始CRRT治疗后的28 d,117例患者死亡,106例患者存活,病死率为52.5%。见表2。

表2 223例ICU中首次CRRT的新发AKI患者的临床特征
2.2CRRT相关数据 启动CRRT治疗的主要原因为少尿/无尿(82.5%)、严重酸中毒(43.0%)、顽固性高钾血症(31.8%)、容量过负荷(8.5%)、全身炎症反应综合征(SIRS)合并多器官功能障碍综合征(MODS)6.7%。CRRT的首次治疗模式主要为连续静脉-静脉血液滤过(CVVH,80.3%),主要抗凝方式为枸橼酸局部抗凝(62.7%)。存活组和死亡组患者CRRT启动原因、首次治疗模式和穿刺置管部位比较差异均无统计学意义。CRRT持续时间为6(2~12)d,其中存活组和死亡组患者的持续时间分别为9(4~15)d和4(2~11)d。见表3。

表3 223例ICU中新发AKI患者 CRRT相关数据
2.3首次CRRT后28 d死亡的危险因素分析 单因素分析结果显示,存活组和死亡组年龄、是否合并糖尿病、APS和SOFA评分、心率、平均动脉压、是否行机械通气、是否需要升压药及是否诊断为脓毒症比较差异有统计学意义。将单因素分析中P<0.1的变量纳入多因素回归分析。由于APS和SOFA评分存在线性相关(r2=0.49,P<0.001),且APS评分与患者预后相关性更好,因此仅将APS评分作为变量纳入到预测模型。多因素分析结果显示,年龄、APS评分和合并脓毒症是ICU中新发AKI患者首次CRRT后28 d死亡的独立危险因素。见表4。

表4 ICU中新发AKI患者首次CRRT后28 d死亡的危险因素分析
2.4构建首次CRRT后28 d死亡的预测模型和列线图
根据多因素回归分析结果,28 d死亡的预测概率1/(1+e-z),Z=0.031×年龄+0.072×APS+0.964×脓毒症-3.779。取具有最大约登指数的预测概率值为临界点,临界点概率值为0.602,当患者的预测概率高于0.602时28 d死亡的风险较高。
应用R软件建立预测AKI患者CRRT后28 d死亡的列线图。根据列线图上每个变量在不同取值下对应的单项得分,将每个单项得分相加计算出总分,从而获得相应的死亡风险(见图1)。通过Bootstrap重抽样法绘制校准曲线(见图2),校准曲线显示斜率为接近于1的直线,表明该列线图可以较准确预测28 d的死亡风险。通过绘制ROC曲线,对列线图预测模型的预测能力进行评价。结果显示,列线图预测模型的ROC曲线下面积(AUROC)为0.786(95%CI0.725~0.846,P<0.001)。见图3。

图1 ICU中新发AKI患者首次CRRT后28 d死亡风险的Nomogram模型构建

图2 ICU中新发AKI患者首次CRRT后28 d死亡风险预测模型的校准曲线
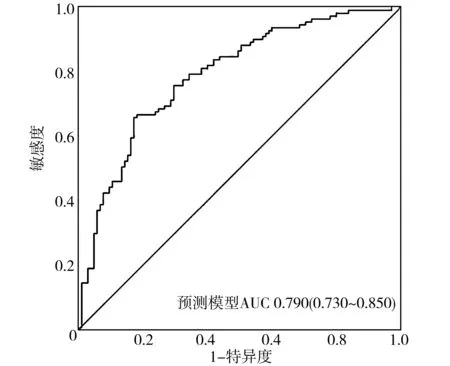
图3 ICU中新发AKI患者首次CRRT后28 d死亡风险预测模型的ROC曲线
3 讨论
本研究基于一项前瞻性多中心研究的数据库资料,分析了ICU中新发AKI行CRRT患者首次CRRT后28 d死亡相关的危险因素,并通过多因素回归分析构建了预测模型。由于入ICU时已经存在AKI或因AKI接受CRRT治疗患者的部分临床资料难以收集,因此,本研究选择的研究对象为ICU中因新发AKI接受CRRT治疗的患者,其28 d病死率高达52.5%,与国外报道基本一致[5-7]。
本研究结果显示,首次CRRT启动原因主要为少尿/无尿、严重酸中毒、顽固性高钾血症和容量过负荷,与BESTKidney研究结果基本相似[12]。然而,BESTKidney研究中超过一半患者因为高血肌酐/尿素氮而启动CRRT,而本研究中这部分患者不足5.4%。这体现了国内医生对血肌酐/尿素氮的耐受程度较高。另外,部分(6.7%)患者因SIRS合并MODS而启动CRRT,这一比例明显高于先前的研究[13]。这可能是因为一些患者同时存在多种启动原因,而SIRS合并MODS是原因之一,亦提示仍有不少临床医生认为CRRT是治疗全身严重炎症反应的可选择方案之一。但近期的研究显示,CRRT清除炎症因子的能力有限,在无肾脏适应证的情况下进行CRRT并不能改善脓毒症患者的生存率[14]。本研究结果显示,大部分(62.7%)患者的抗凝方式为枸橼酸局部抗凝,仅12.3%患者采用了肝素全身抗凝。这体现了临床医生对指南中首选枸橼酸抗凝这一意见的接受和执行程度较高。另外,建立CRRT血管通路的首次置管位置按照频率高低依次为股静脉(70.0%)、颈内静脉(24.2%)和锁骨下静脉(5.8%),这和KDIGO指南中关于血管通路穿刺部位的推荐(依次为右侧颈内静脉、股静脉和左侧颈内静脉)有所差异[8]。
本研究结果显示,年龄和APS评分是与患者28 d死亡相关的独立危险因素,与既往研究结果相似[5-6,15]。ICU中接受CRRT治疗的高龄患者死亡风险显著高于50岁以下患者,且年龄超过80岁是住院死亡的独立危险因素(OR=2.59,95%CI1.66~4.03)[16]。另外,本研究结果发现,在合并脓毒症的患者中,28 d死亡的风险是无脓毒症患者的 2.675倍(OR=2.675,95%CI1.336~5.353)。脓毒症是诱发AKI的最常见原因之一[10]。多个研究显示,脓毒症及脓毒性休克引起的低血压[6,16]、血管活性药物依赖及器官功能障碍引起的SOFA评分增高[5-6]均为患者住院死亡的危险因素。因此,积极处理脓毒症对提高患者生存率具有极为重要的意义。
本研究在逻辑回归分析的基础上构建了预测患者首次CRRT后28 d病死率的列线图,通过可视化的预测模型,有助于直观了解单变量对病死率的影响权重,并可以获得基于个体水平的具体死亡风险数值,协助医生筛选出死亡高危患者,以便对其实施更为精细化的评估和治疗。该模型预测患者首次CRRT后28 d病死率的AUROC接近于0.8,显示出较好的预测价值[17],同时,模型的校准曲线与标准曲线贴合良好,表明该模型具有良好的区分度和校准度。
本研究存在一些局限性。首先,本研究除外了既往存在慢性肾功能不全病史的患者,由于合并慢性肾功能不全患者启动CRRT的原因及预后的评估往往不同于新发AKI[18],故本研究排除了这部分患者;其次,由于缺乏患者长期预后的数据,本研究仅探索了ICU中新发AKI接受CRRT治疗患者的短期预后及其死亡相关危险因素。另外,本研究没有记录CRRT时的治疗剂量,这可能会影响研究结果。但近年来的研究显示[19],CRRT治疗剂量对AKI患者病死率无显著影响。
综上所述,ICU中新发AKI患者首次CRRT启动原因主要为少尿/无尿、严重酸中毒、顽固性高钾血症和容量过负荷;年龄、APS评分及合并脓毒症是患者28 d死亡的独立危险因素;构建列线图预测模型有助于评估患者预后。
