莪术油注射液抗新型冠状病毒作用的体内外研究
2022-05-12周园园戴志娟张淑君李岳春戴元荣吴海林冯梦晴李校堃黄晓晖朱光辉
周园园,戴志娟,张淑君,李岳春,戴元荣,王 贺,吴海林,冯梦晴,李校堃,黄晓晖,朱光辉
新型冠状病毒疾病2019(coronavirus disease 2019, COVID-19),由严重急性呼吸综合征冠状病毒2(severe acute respiratory syndrome coronavirus 2, SARS-CoV-2)引起,已成为全球突发公共卫生事件[1]。患者以发热为主要表现。严重者发展为急性呼吸窘迫综合征、脓毒症休克等。确诊患者死亡率达4.3 %[2]。目前尚无特效药物,国家卫健委先后发布了多版诊疗方案,推荐使用安宫牛黄丸和醒脑静注射液,其组方中均含莪术[3]。莪术根茎提取的莪术油为莪术油注射液的主要成分,具有抗肿瘤、抗炎、抗病原体等多种药理作用。研究显示SARS-CoV-2与SARS中的酶具有高水平的序列相似性[4],SARS患者进行中西医结合治疗(憋喘期,联用莪术油注射液),临床症状严重程度显著改善,重症患者病死率低[5-7]。故推测莪术油注射液对SARS-CoV-2也可能有效。现对莪术油注射液体内外抗新型冠状病毒作用进行研究,评价该药治疗COVID-19的有效性和安全性,以期为COVID-19治疗提供更多的证据。
1 材料与方法
1.1 材料
1.1.1药物与细胞株 莪术油(浙江天瑞药业有限公司,批号:5190527,浓度:1 000 μg /ml);莪术油注射液(浙江天瑞药业有限公司,莪术油含量10 ml ∶0.1 g,国药准字H20064312)。人肾上皮细胞株293 T(由中科院合肥物质科学研究院健康所惠赠)。
1.1.2试剂与仪器 转染试剂Lipofiter 3.0[汉恒生物科技(上海)有限公司,货号:HB-LF3-1000];Opti-MEM(1X)(赛默飞世尔科技(中国)有限公司,货号:31985-070);Renilla-Glo荧光素酶检测系统(普洛麦格生物技术有限公司,货号:E2720);pHB、pAX 2、SARS-CoV-2 S、ACE 2-pcDNA 3.1由合肥中科普瑞昇生物医药科技有限公司构建。细胞计数仪(上海睿钰生物科技有限公司,型号:IC1000),酶标仪(珀金埃尔默股份有限公司,型号:EnVision)。
1.2 莪术油体外抗新冠类病毒作用实验采用Renilla-Glo荧光素酶检测系统检测莪术油抗SARS-CoV-2类病毒活性作用。
1.2.1细胞培养 从液氮中取出冻存的293T细胞,37 ℃融化复苏细胞,在超净工作台内,将细胞悬液转移到含有2 ml培养基的无菌离心管中,800 r/min离心5 min,弃去上清液,加入适量DMEM完全培养基重悬细胞后转移至培养皿中,置于恒温培养箱(培养条件为37 ℃、5 %CO2、相对湿度75%)中培养两代,待测试。
1.2.2类病毒及293T-ACE2细胞准备 提前20~24 h将293 T细胞接种至6孔板中,当细胞汇合度达到60%~70%时,分别使用转染试剂Lipofiter 3.0将3 μg质粒[pHB:pAX 2:SARS-CoV-2 S(2 ∶2 ∶1)]和3 ug质粒(ACE2-pcDNA 3.1)进行包装转染,将6孔板在37 ℃、5%CO2培养,转染48 h后收取病毒上清溶液,病毒立即使用或-80 ℃冻存保管。
1.2.3细胞消化 瞬时转染48 h后,用胰酶将293T-ACE2消化,用完全培养基重悬细胞后,利用细胞计数仪进行计数后,接种至96孔板,每孔体积为50 μl(25 000个细胞/孔),在37 ℃、5 %CO2培养12 h,待细胞贴壁。
1.2.4溶液制备 取莪术油50 μl,加入50 μl DMEM,先横向梯度设置2×稀释,再纵向稀释10倍,取10 μl加96孔板,重复3次。
1.2.5铺板读数 取出培养箱中贴壁12 h的96孔白色细胞培养板,取10 μl制备好的样品溶液加入上述含有50 μl细胞的96孔培养板中,每个浓度梯度3个复孔,将培养板置于37 ℃、5 %CO2培养箱中孵育1 h后,每孔加入40 μl制备完成的类病毒溶液,并加入终浓度6 μg/ml的增强剂,再将培养板置于37 ℃、5 %CO2培养箱中孵育24 h后更换100 μl新鲜的DMEM完全培养基继续培养24 h后检测。将Renilla-Glo荧光素酶检测系统检测试剂融化并放置至室温,取出细胞培养板放置10 min使其平衡至室温,在每孔中加入100 μl的检测试剂,将培养板在轨道摇床上振摇2 min以诱导细胞裂解,培养板在室温放置5 min以稳定发光信号,在酶标仪读板器上检测发光信号。酶标仪检测得出对应的每孔荧光值(relative light unit,RLU)。计算不同浓度化合物对应的相对荧光值RLU比率(%)采用下列公式:相对荧光值RLU比率(%)=RLUDRUG/RLUDMSO×100%。
1.3 莪术油注射液体内抗新型冠状病毒作用研究采用随机、开放、平行对照临床试验设计。该项临床研究申办方为合肥市未来药物开发有限公司,并已获得温州医科大学附属第二医院医学伦理委员会批准(伦理批准编号:LCKY2020-11)。
1.3.1研究对象 选取2020年2月至3月在温州医科大学附属第二医院瓯江口院区住院且同意(签署知情同意书)参加本试验的新冠肺炎患者,随机分配至试验组或对照组,两组等比例分配。
1.3.2纳入和排除标准 纳入标准:① 年龄≥ 18周岁,性别不限;② 咽拭子标本实时荧光RT-PCR检测新型冠状病毒核酸阳性,或咽拭子阴性伴肺部影像学未完全吸收;③ 临床分型为普通型或重型;④ 已签署知情同意书。
排除标准:① 已知或怀疑对莪术油注射液组成成分过敏,或过敏体质。② 轻型与危重型患者。③ 合并严重的肝脏疾病(如Child-Pugh评分≥C级,总胆红素(total bilirubin,TBIL)≥2倍正常值上限,谷丙转氨酶(alanine aminotransferase ,ALT)/ 谷草转氨酶(aspartate aminotransferase,AST)≥5倍正常值上限)。④ 合并有重度肾功能不全[估算的肾小球滤过率(estimated glomerular filtration rate,eGFR)≤30 ml/(min·1.73 m2)]或正在接受连续性肾脏替代治疗、血液透析、腹膜透析。⑤ 妊娠期、哺乳期妇女或在试验期间及结束6个月内有生育计划。⑥ 入组前3个月内参加过其他临床试验。⑦ 根据研究者的判断,具有不适合参加本试验的其他情况者。
1.3.3治疗方法 所有受试者统一按照《新型冠状病毒肺炎诊疗方案(试行第六版)》[3]给予常规治疗: 选用α-干扰素(每次500万U或相当剂量,加入灭菌注射用水2 ml,每日2次雾化吸入)和利巴韦林(500 mg/次,每日2至3次静脉输注,疗程不超过10 d),同时给予有效氧疗措施;试验组将在常规治疗基础上给予莪术油注射液20 ml于250 ml 0.9%氯化钠注射液稀释后缓慢滴注,每日1次,连续用药7 d,不满7 d出院则用至出院时(停药后观察期不满14 d提前出院者需在满14 d后回院访视)。
1.3.4观察指标 主要疗效指标:① 咽拭子标本实时荧光RT-PCR检测新型冠状病毒核酸转阴率(用药结束后)和转阴时间;② 临床改善的时间(time to clinical improvement, TTCI);③ 通过胸部CT检查病变区域的大小变化情况;④ 退热时间。
次要疗效指标:① 临床恢复时间(time to clinical recovery,TTCR)定义:从开始治疗到发热、呼吸频率、血氧饱和度转为正常和咳嗽症状消失,持续至少48 h。正常的评估标准:发热:腋温≤ 37 ℃;呼吸频率:≤24次/min(室内空气下,如果患者吸氧,需注明氧疗方式及浓度);血氧饱和度:>93%(室内空气下,如果患者吸氧,需注明氧疗方式及浓度)。② 病情进展的病例比例参照《新型冠状病毒肺炎诊疗方案(试行第六版)》,病情分型由普通型转为重型/危重型以及重型进展为危重型的病例比例。③ 咳嗽消失率和消失时间:入组时存在咳嗽的受试者咳嗽症状消失的时间和病例比例。④ 全因死亡率。
安全性指标:收集与监测发生的不良反应,静脉滴注过快可有胸闷、面部潮红、呼吸困难等症状。
1.4 统计学处理莪术油体外抗新型冠状病毒作用实验运用GraphPad 7.0 Prism软件进行ANOVA单因素方差分析。P<0.05表示差异有统计学意义。莪术油注射液体内抗新型冠状病毒作用研究采用描述性统计。
2 结果
2.1 莪术油体外抗新型冠状病毒作用实验结果分析用酶标仪检测0.39、0.78、1.56、3.13、6.25、12.50、25.00、50.00、100.00 μg/ml 莪术油处理后的SARS-CoV-2类病毒细胞株(图1),结果显示,随着莪术油浓度增加,相对荧光值逐渐减弱,与0 μg/ml莪术油组比较,差异有统计学意义 (P<0.05),IC50值为0.26 μg/ml(图2)。
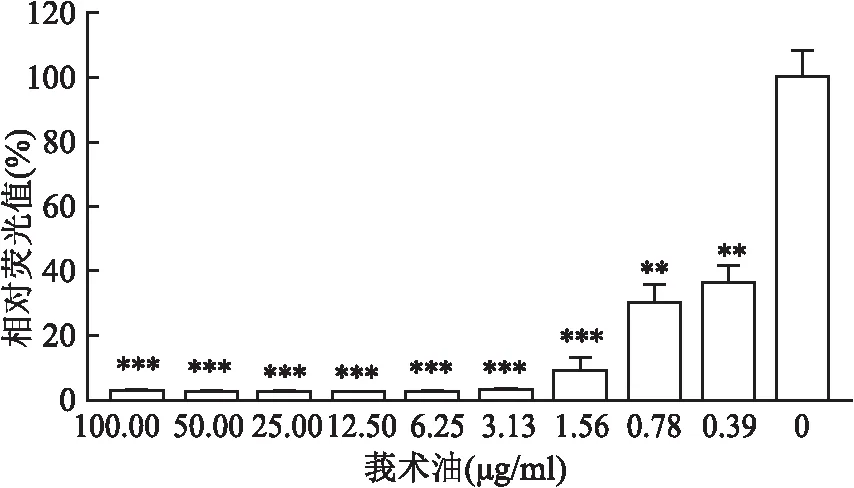
图1 不同浓度莪术油诱导SARS-CoV-2类病毒细胞后的活性与0 μg/ml莪术油组比较:*P<0.05,**P<0.01,***P<0.001
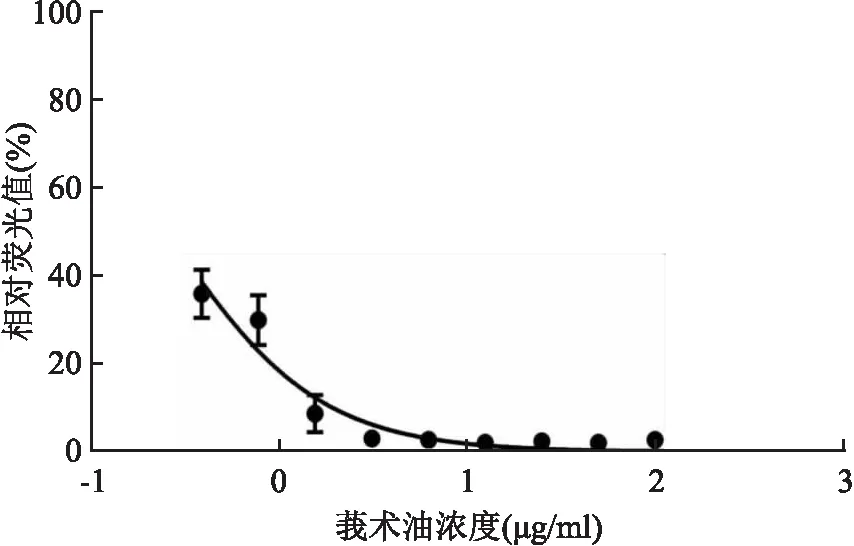
图2 莪术油对SARS-CoV-2类病毒的浓度抑制曲线
2.2 莪术油注射液体内抗新型冠状病毒作用研究结果分析
2.2.1患者入组及用药情况 试验拟招募患者60例,因浙江省温州市新冠疫情得到有效控制,研究实际入组COVID-19普通型患者4例,试验组和对照组各2例,两组均为男性,入组时肝肾功能、生命体征均正常,其中试验组年龄大于对照组,试验组病例2表现为频繁咳嗽,且无相关既往病史。根据患者诊疗进程,试验组病例1、2分别使用莪术油注射液4天和7天。
2.2.2疗效指标 研究纳入的所有患者体温、呼吸均正常,试验组病例1粪便新型冠状病毒核酸用药后3 d转阴,试验组病例2咳嗽症状明显缓解,无1例发展为重症。对照组咽拭子转阴时间分别为5、7 d。所有患者肺部影像学均有不同程度吸收,以试验组病例2吸收较明显(图3),3月1日左右下肺出现阴影,呈磨玻璃密度影,病灶里的肺间质有些增厚,3月2日患者开始接受莪术油注射液治疗,3月8日复查,肺泡内渗出液逐渐被吸收,阴影减小。出院后2、4周随访所有患者新型冠状病毒核酸呈阴性,血常规、肝肾功能无异常,试验组病例2肺部影像学阴影逐渐消失,且肺间质增厚改善。
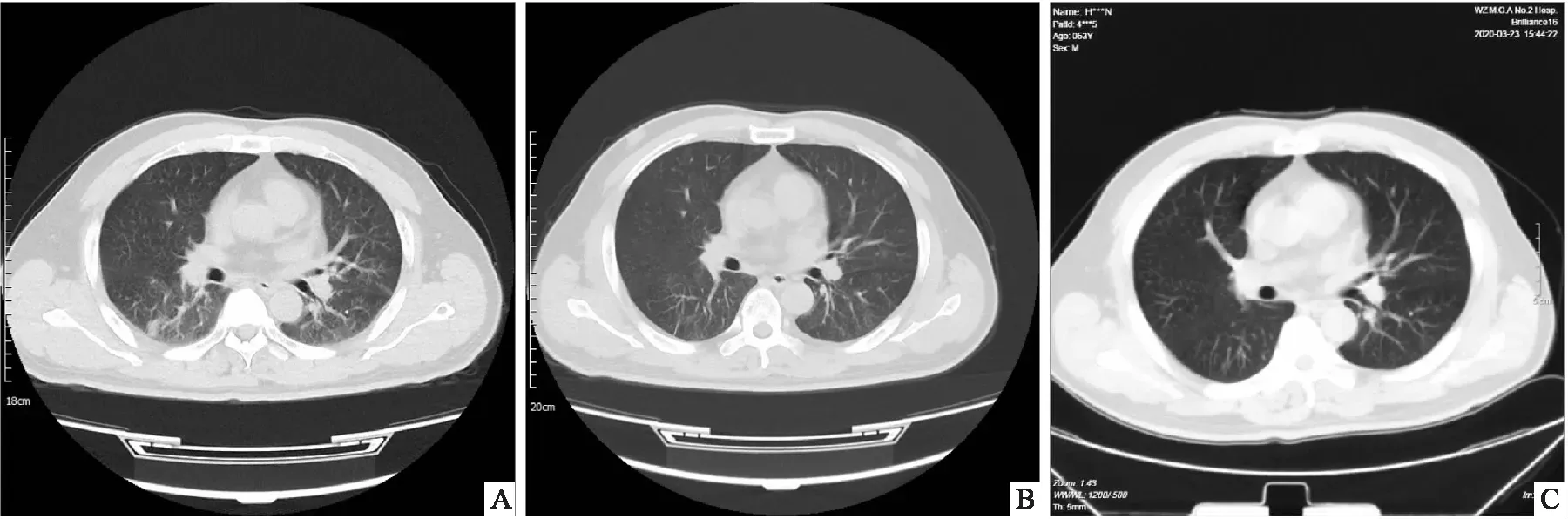
图3 试验组病例2肺部影像学(CT)变化A:3月1日;B:3月8日;C:3月24日
2.2.3安全性分析 在应用莪术油注射液联合常规治疗过程中,血常规、肝肾功能等实验室检查均未出现加重情况。与治疗前比较,所有患者除原有的呼吸道症状之外,均未出现新的不适症状或加重体征情况。
3 讨论
莪术油注射液具有显著抗病毒功效(如流感病毒、呼吸道合胞病毒等)[8-10],《浙江省抗新冠肺炎临床诊疗用药推荐目录》推荐其为抗新冠肺炎药物。秦宇雯 等[6]总结中药莪术抗病毒的作用机制研究,发现其可能通过抑制病毒 NP 蛋白,调控 PI 3 K/Akt/mTOR 信号通路,直接灭活病毒,抑制相关炎症因子,抗肺纤维化等途径实现抗 COVID-19。推测莪术可降低新冠肺炎患者炎症水平,改善患者咳嗽、发热、肺部啰音等体征,同时在抑制病毒复制和感染,提升机体免疫力和改善患者肺功能损伤程度等方面发挥作用,且无激素类药物的不良反应[6-7,11-13]。
本研究从细胞水平和临床研究两方面探讨了莪术油注射液抗新型冠状病毒作用。通过体外制备SARS-CoV-2类病毒细胞株,用9组不同浓度莪术油进行处理,观察和记录细胞数及相对荧光值,计算IC50值为0.26 μg/ml(黄芪醇提取物的体外抗柯萨奇病毒效果与利巴韦林接近,其IC50值为(6.4±0.5)μg/ml,表明莪术油对SARS-CoV-2类病毒活性有较强抑制作用,且具有浓度依赖性。莪术油注射液治疗COVID-19的随机开放平行对照研究显示,试验组在常规治疗基础上联用莪术油注射液,患者核酸转阴时间缩短,可能改善SARS-CoV-2感染引起的咳嗽等症状,促进SARS-CoV-2转阴及肺部病灶吸收,降低肺损伤,并且相对安全。
综上所述,体内外研究显示,莪术油注射液具有较强的抗新型冠状病毒活性作用,对于COVID-19患者的救治可能具有重要的临床价值。需要指出的是,由于项目启动时间晚,研究立项审批通过时国内疫情已得到很好控制,实际可入组患者少,造成整体研究样本量偏少。另外,因本研究纳入患者所在病房为隔离病房,管控严格,入组患者详细治疗数据无法进行充分记录,致使部分原始研究数据缺失。且入组时样本病程已较长,故结果存在不确定性,确切的临床疗效尚需大样本、前瞻性临床研究进行评价,如追踪病毒的复阳率、肺部影像学转归等。但基于现有莪术油的体内外及药理学研究,后期可扩大莪术油注射液治疗COVID-19临床研究范围,为莪术油等相关产品的开发应用和COVID-19的治疗提供有力的科学依据。
