镍卟啉加氢反应和扩散行为
2022-05-11陈振涛杨浩轩于佳欢刘雅欣赵芳钰徐春明
陈振涛, 蒋 涛, 杨浩轩, 于佳欢, 赵 洋, 刘雅欣, 赵芳钰, 徐春明
(中国石油大学(北京) 化学工程学院 重质油国家重点实验室,北京 102249)
随着原油重劣质化趋势逐渐加剧和油品质量标准的日趋严格,劣质重油的高效轻质化和清洁化生产已成为当前关注的热点。渣油是原油经蒸馏的残余物,通常占原油总量的40%以上。从组成上来看,渣油是由各种类型的较大分子组成的复杂混合物,含有大量的硫、氮、氧和金属等杂原子化合物。镍、钒化合物是重质油加工中危害最大的2种金属化合物,它们在加氢处理和催化裂化过程中逐渐沉积在催化剂的表面,大幅度降低催化剂的活性、选择性和使用寿命,从而造成了炼油厂运行成本的攀升以及经济效益的降低。因此,金属镍、钒的脱除是改善重质油加工性能的最有效方法。
渣油加氢脱金属是应用最广且最为有效的脱除镍、钒的方法。大量研究表明,镍、钒化合物在催化剂孔道中的加氢脱金属反应受到较为严重的扩散阻力。不同结构和尺寸的金属有机物,其在催化剂中的扩散和反应行为将会表现各异。正是由于金属镍、钒化合物结构的复杂性,致使渣油加氢脱金属(HDM)反应机理及其在催化剂孔道中扩散行为的研究极为困难。早期研究表明,卟啉分子是渣油中金属化合物的重要组成部分。近期的先进仪器分析结果进一步显示,“非卟啉”组分中仍含有一定的卟啉结构金属化合物[1]。基于此,学者多以初卟啉(ETIO)、四苯基卟啉(TPP)和八乙基卟啉(OEP)为镍、钒特征模型化合物进行加氢脱金属反应机理和动力学行为的探索。在相关研究中,Wei课题组的科研人员[2-6]在镍钒卟啉加氢产物中结合紫外可见光谱分离鉴定出中间产物二氢卟吩,并提出其加氢反应分为卟啉的可逆加氢/脱氢和不可逆氢解的分步动力学模型;此外发现,相同结构卟啉化合物的反应网络相同,而与催化剂无关。Long等[7]发现初卟啉钒化物加氢产物存在四氢卟啉,由此得出反应需要经过连续两步可逆加氢生成四氢卟啉,然后发生氢解从而脱除金属。García-López等[8]发现Ni-TPP的加氢同样遵循连续两步加氢的反应历程。
基于中间产物很难分析鉴定,Janssens等[9]利用分子模拟通过分析中间产物的生成热和稳定构型提出了金属四苯基卟啉的加氢反应机理,认为TPP类型金属卟啉经过连续加氢生成六氢卟啉,然后在连接2个吡咯环的甲基桥处加氢后发生氢解反应。徐海[10]对镍、钒OEP和TPP的加氢反应进行了较为系统的研究,并得出与Wei课题组相近的反应机理。但是,徐海应用紫外光谱结合飞行时间质谱检测出产物中存在少量的金属四氢卟啉,而Wei课题组在ETIO型卟啉的加氢反应中只鉴定出二氢卟啉。
在进行上述加氢反应之前,金属镍、钒化合物首先需要扩散到达催化剂活性位。催化剂孔道金属沉积的大量研究结果显示,渣油的加氢脱金属反应存在极为严重的扩散限制[11-12]。一方面,这将降低渣油分子在催化剂活性位的可接近性,导致反应速率和渣油转化率大幅下降;另一方面,扩散受阻的金属镍、钒将在催化剂孔口处不断沉积,最终导致催化剂失活,从而造成生产成本大幅提高。
Ware等[6]建立了包含扩散系数的镍、钒卟啉HDM反应动力学模型,但是研究者是通过人为调整扩散系数从而获得动力学数据。结果显示,当镍卟啉加氢反应中间产物的扩散系数调整为反应物的2倍时,模型计算出的产物含量和金属在催化剂中沉积量与实验结果相一致。Smith等[13]对镍、钒卟啉的加氢反应动力学研究则表明,镍卟啉的HDM处于反应控制区域,而钒卟啉在相同催化剂孔道中的扩散系数降低一个数量级以上,其HDM反应受到严重的扩散限制。催化剂的复杂结构是金属卟啉加氢过程扩散行为研究未能深入的原因之一。
基于上述分析可见,渣油组成复杂且卟啉分子是其重要的金属有机物结构。学者们应用镍、钒卟啉为模型化合物对其反应机理及其在催化剂中的扩散和反应行为展开研究。但由于分析手段所限,反应中间产物的鉴定大多依靠紫外可见光谱,样品的溶液环境对定量结果的影响制约准确动力学参数的获取[14],且扩散结果存在矛盾之处。此外,催化剂的孔径是影响催化转化过程反应物分子扩散性能的关键因素之一。工业加氢催化剂普遍采用γ-Al2O3作为载体,催化剂较宽的孔径分布决定了难以获得较为准确的扩散结果。基于此,笔者合成出孔径较为均一的介孔NiMo/Zr-SBA-15催化剂,并结合工业NiMo/γ-Al2O3催化剂获得对镍卟啉加氢反应和扩散行为的深入认识。
1 实验部分
1.1 原料和试剂
八乙基镍卟啉(Ni-OEP),美国Frontier Scientific公司产品;四苯基镍卟啉(Ni-TPP),美国Strem Chemicals公司产品;(EO)20(PO)70(EO)20,美国Sigma-Aldrich公司产品;四氢萘、乙腈、ZrOCl2·8H2O,阿拉丁(上海)试剂有限公司产品;环己烷,天津市致远化学试剂有限公司产品;甲醇,北京化工厂产品;正硅酸乙酯,国药集团化学试剂有限公司产品;甲苯,天津市津东天正精细化工试剂厂产品;氟化铵,天津市光复科技发展有限公司产品;甲酸、氨水,北京化学试剂公司产品;以上试剂均为分析纯。NiMo/γ-Al2O3催化剂,中国石化大连石化研究院提供。
1.2 镍卟啉模型化合物及其反应溶液的制备
选取八乙基镍卟啉和四苯基镍卟啉作为加氢脱金属反应研究的模型化合物,其中Ni-OEP与石油初卟啉的结构相近,Ni-TPP用于模拟渣油中芳香性较高的金属化合物。Ni-OEP和Ni-TPP的相对分子质量分别为591.45和671.44。笔者所在课题组所研究相平衡结果显示,四氢萘在340 ℃和6 MPa条件下主要呈现液相,且其在大量H2存在下的供氢作用基本可以忽略[15]。由此,在加氢实验中,将Ni-OEP和Ni-TPP溶于四氢萘分别配制成质量分数为82.2和93.7 μg/g的溶液,且配制过程经过溶剂脱气和N2保护。
1.3 加氢处理催化剂的制备和表征
NiMo/Zr-SBA-15催化剂载体的合成采用水热法,以ZrOCl2·8H2O为锆源进行原位锆改性,合成具有2种不同孔径大小的Zr-SBA-15载体,然后担载金属得到催化剂,具体合成方法参考课题组前期研究[16]。其中,应用(EO)20(PO)70(EO)20、正硅酸乙酯和ZrOCl2·8H2O,通过调节适宜晶化条件合成出平均孔径较小的载体Zr-SBA-15-A,在此基础上通过引入扩孔剂NH4F得到平均孔径较大的载体Zr-SBA-15-B。然后采用等体积分步浸渍法,将活性金属Ni、Mo分别担载在Zr-SBA-15-A和Zr-SBA-15-B上制得NiMo/Zr-SBA-15-A和NiMo/Zr-SBA-15-B催化剂。其中,Mo以MoO3计,质量分数为12%,Ni以NiO计,质量分数为3%。由于工业加氢催化剂与实验室合成的NiMo/Zr-SBA-15催化剂密度相差较大,笔者以催化剂质量为基础进行反应动力学数据的求取和对比分析。
采用德国Bruker公司生产的D8 Advance型X射线小角散射仪对载体Zr-SBA-15-A和Zr-SBA-15-B进行分析,利用美国麦克公司生产的Micromeritics ASAP 2010吸附分析仪对合成的2种NiMo/Zr-SBA催化剂和1种工业NiMo/γ-Al2O3催化剂进行孔结构分析,应用美国伯乐太平洋公司生产的Digilab FT-IR吡啶红外光谱仪对上述3种催化剂进行酸性质分析。
1.4 加氢实验
采用固定床加氢微型反应装置进行镍卟啉Ni-OEP和Ni-TPP的加氢实验,如图1所示。其主要由进料系统、反应系统及分离系统3部分组成。其中,反应管内径为0.9 cm、长度为70 cm,采用三段控温电加热炉维持反应器中部催化剂床层区域温度恒定。
加氢催化剂装填后先经过气密性检查,并经过预硫化和稳定后用于镍卟啉Ni-OEP和Ni-TPP的加氢实验。其中,预硫化过程压力6 MPa,液时空速4 h-1,氢/油体积比200,室温升至230 ℃保持12 h,然后升温至320 ℃保持12 h。预硫化后,在上述其他条件不变的情况下,使反应溶液在300 ℃下反应24 h进行第一段活性稳定,并降温至240 ℃继续反应44 h达到活性稳定区。经稳定后的催化剂用于Ni-OEP和Ni-TPP的加氢反应历程和动力学研究。
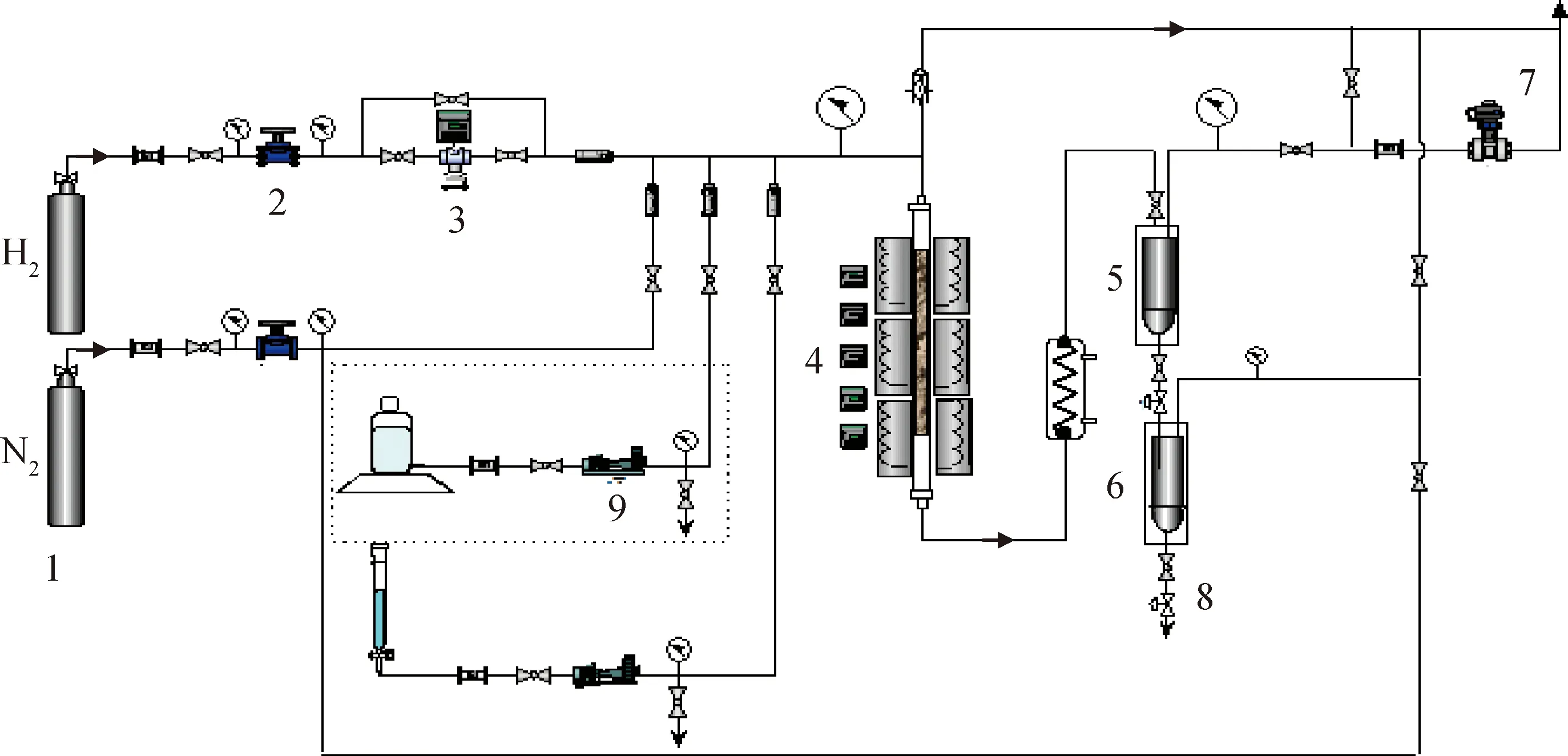
1—Cylinder; 2—Valve; 3—Flow controller; 4—Reactor; 5—High-pressure separator;6—Low-pressure separator; 7—Back pressure valve; 8—Sampling; 9—Feedstock pump图1 固定床高压加氢微型反应装置示意图Fig.1 Schematic diagram of high pressure fixed-bed hydrogenation micro reaction system
Ni-OEP和Ni-TPP的加氢脱镍转化率(XHNNi,%)根据式(1)进行计算。
(1)
式中:w0和wf分别为镍卟啉Ni-OEP和Ni-TPP中及其加氢反应产物中的镍质量分数,μg/g。
本课题组采用制备的NiMo/Zr-SBA-15-A和NiMo/Zr-SBA-15-B以及工业NiMo/γ-Al2O3催化剂对Ni-OEP和Ni-TPP加氢过程中的扩散和反应行为进行了详细研究。由于催化剂NiMo/Zr-SBA-15与NiMo/γ-Al2O3密度相差较大,加氢实验催化剂的装填量略有差异。其中,催化剂NiMo/Zr-SBA-15装填0.7 g,而NiMo/γ-Al2O3催化剂装填1.0 g,后续动力学参数则采用以催化剂质量为基础的形式进行求取。
1.5 镍卟啉及其加氢产物表征
1.5.1 UV-Vis表征
采用美国安捷伦公司生产的Cary-60紫外可见分光光度计(UV-Vis)测定镍卟啉Ni-OEP和Ni-TPP及其加氢产物的含量,并用于其反应动力学参数求取。其中,镍卟啉Ni-TPP和Ni-OEP的检测波长分别为528和519 nm。加氢实验中,每个条件下均取2~3个平行样品进行UV-Vis定量分析。
1.5.2 Orbitrap质谱表征
采用美国赛默飞公司生产的四极杆-静电场轨道阱-线性离子阱三合一组合式质谱仪Thermo Scientific Orbitrap Fusion进行卟啉Ni-OEP和Ni-TPP及其加氢产物的定性分析,其超高场Orbitrap质量分析器具有高分辨、高灵敏度和多级质谱能力。将加氢反应后样品使用等体积混合的甲苯、甲醇溶液稀释1×104倍后,取1.5 mL稀释后样品,向其中加入10 μL甲酸和20 μL氨水作为促电离剂强化电离效果[17],利用Orbitrap Fusion在+ESI电离模式下对加氢反应后样品进行质谱分析。质谱表征采用全谱模式,相对分子质量范围为 200~800,碰撞池累积时间为0.2 s,飞行时间为1.3 ms,电离电压为3500/3000 V,雾化气流速为2.0 L/min。
1.6 加氢反应动力学参数求取
采用的固定床微型反应装置内径和催化剂床层高度远大于催化剂颗粒尺寸,且实验采用较高的反应物料空速进行,因此加氢反应过程中的传热传质效应可忽略。对于镍卟啉的加氢脱金属反应,其反应速率可用式(2)表示。
(2)
式(2)中:k为反应速率常数,单位随反应级数而变;CP为镍卟啉浓度,mol/m3;CH2为H2浓度,mol/m3;α和β分别为镍卟啉和H2对应的反应级数。由于本研究中采用的镍卟啉反应物料浓度较低,且反应的压力和氢/油比均较大,可认为H2对加氢脱金属的影响可忽略。对于一级反应,基于固定床反应器的平推流假设,反应速率常数可由式(3)计算得到。
(3)
式(3)中:k为加氢脱镍反应速率常数,m3/(g·h);F为反应物进料流率,m3/h;m为催化剂质量,g;X为镍卟啉加氢脱金属转化率。
前已述及,Ni-OEP和Ni-TPP在加氢过程中将受到明显的内扩散阻力影响。基于本课题组前期的动力学实验[15],发现在粒径60~80目催化剂中模型化合物和馏分油的加氢反应基本可以消除内扩散的影响。因此,采用粒径80~100目和20~40目催化剂分别获得Ni-TPP的本征和表观反应动力学常数。由此,加氢脱镍反应内扩散有效因子(η)通过式(4)计算得到。
(4)
式(4)中:ka为反应在粒径20~24目催化剂中的表观反应速率常数,m3/(g·h);kin为反应在粒径80~100目催化剂中的本征反应速率常数,m3/(g·h)。
对于球形催化剂,η与Thiele模数(φ)的关系如式(5)和式(6)所示。
(5)
(6)
式(5)和式(6)中:R为催化剂颗粒半径,m;ρb为催化剂堆密度,g/m3;De为反应物分子通过催化剂孔道内的有效扩散系数,m2/s。
2 结果与讨论
2.1 催化剂NiMo/Zr-SBA-15的性质
图2为2种Zr-SBA-15载体的小角XRD谱图。由图2可见,2种载体均呈现出SBA-15材料典型的(100)、(110)和(200)晶面特征衍射峰,说明所合成的载体均具有高度规整的二维六方型拓扑结构。
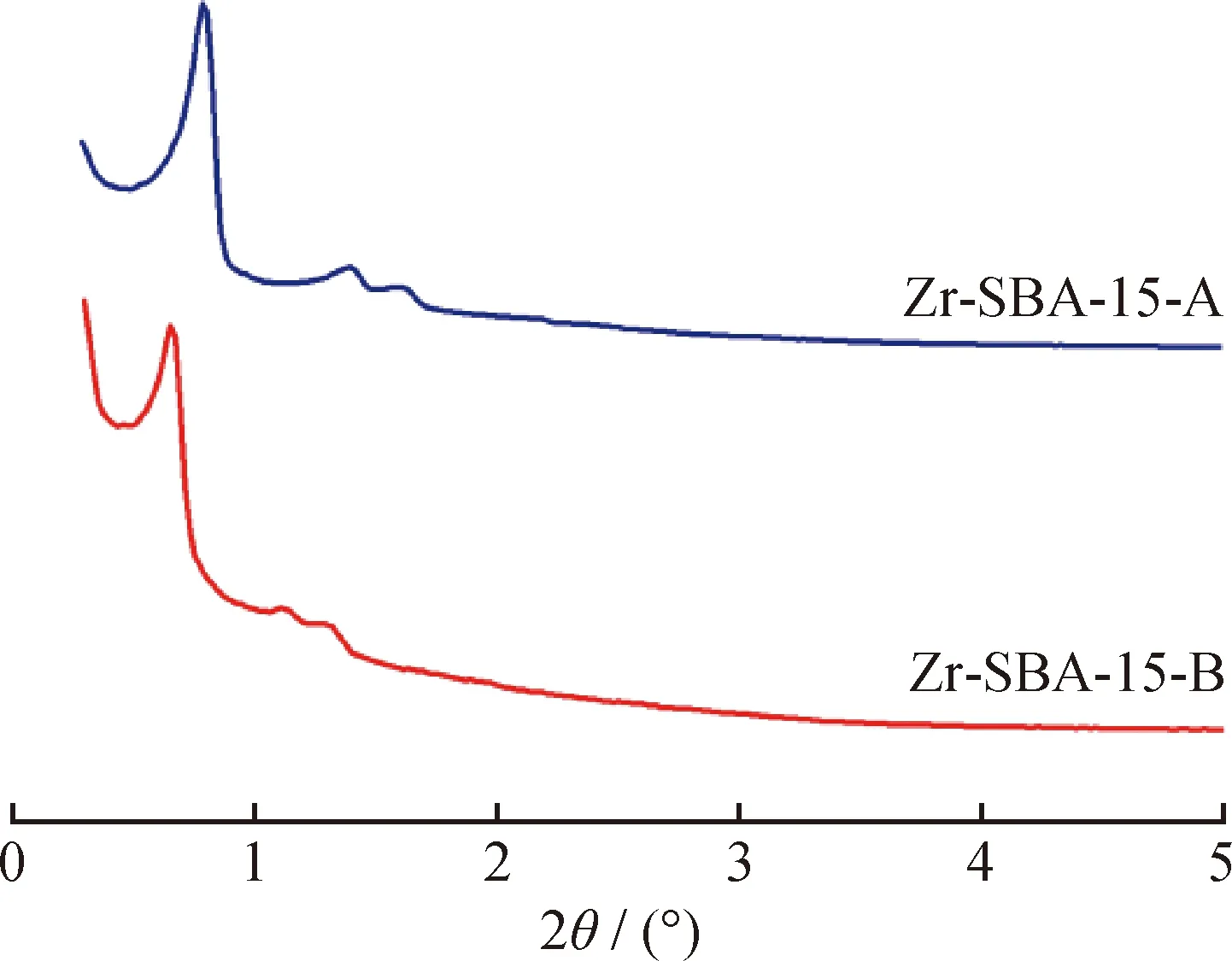
图2 2种Zr-SBA-15载体的小角XRD谱图Fig.2 Small-angle XRD patterns of two kindsof Zr-SBA-15 carriers
2种载体材料的衍射峰位置略有差异,表明不同的添加组分和合成条件导致材料的晶胞参数(a0)不完全相同。
2种NiMo/Zr-SBA-15催化剂以及工业NiMo/γ-Al2O3催化剂的N2吸附-脱附等温曲线和孔径分布如图3所示。由图3(a)可见,催化剂NiMo/Zr-SBA-15-A和NiMo/Zr-SBA-15-B呈现出Ⅳ型吸附脱附曲线,属于H1类迟滞环,表明2种催化剂均具有有序的圆柱形介孔结构,其为镍卟啉的受阻扩散研究提供了较规整的多孔材料。相对于NiMo/Zr-SBA-15-A而言,NiMo/Zr-SBA-15-B催化剂在更大的p/p0处展现出毛细凝聚现象,表明后者具有更大的介孔尺寸[18]。NiMo/γ-Al2O3催化剂呈现出Ⅳ型吸/脱附曲线和H4类迟滞环。由图3(b)可进一步验证2种NiMo/Zr-SBA-15催化剂孔径大小的推断,并且显示这2种催化剂孔分布较集中。这是由SBA-15材料具有二维均一且有序的介孔结构决定的。相比之下,NiMo/γ-Al2O3催化剂的孔径分布较为分散,且向中大孔处偏移。
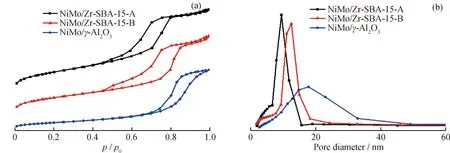
图3 3种催化剂的N2吸附-脱附曲线及孔径分布Fig.3 N2 adsorption-desorption curves and pore size distribution of three catalysts(a) N2 adsorption-desorption isotherms; (b) Pore diameter distributions
基于N2吸附-脱附等温曲线,应用BJH方法计算得出催化剂的性质参数,如表1所示。由表1可以看出,催化剂NiMo/Zr-SBA-15-A和NiMo/Zr-SBA-15-B的孔径存在明显差异,但其比表面积和孔体积数据较为相近,从而为金属卟啉的扩散研究提供了较好的催化材料。对比发现,工业NiMo/γ-Al2O3催化剂具有更大的孔径,其比表面积和孔体积均远小于2种NiMo/Zr-SBA-15催化剂,此工业催化剂中γ-Al2O3载体形成的无规则堆积孔结构是造成上述结果的主要原因。

表1 3种催化剂的结构性质Table 1 Structural properties of three catalysts
表2为NiMo/Zr-SBA-15-A、NiMo/Zr-SBA-15-B和NiMo/γ-Al2O33种催化剂的酸性质结果。由表2可知,2种NiMo/Zr-SBA-15催化剂均具有相对较多的弱L酸(即表2中473 K下的L酸)。这是由于当Zr原子进入硅基骨架后,会使催化剂表面SiO —H键的键能发生变化,更容易失去H质子,从而促进L酸位的形成。同时,由于Zr主要以7和8配位为主,而Si主要是4配位,此配位差异会促进少量B酸位的形成。由此表明,合成的锆改性SBA-15基催化剂具有一定的加氢反应活性。但相对于工业NiMo/γ-Al2O3催化剂而言,NiMo/Zr-SBA-15催化剂的强B酸和L酸酸量明显偏低。这可能是后者的催化加氢活性低于前者的主要原因之一。
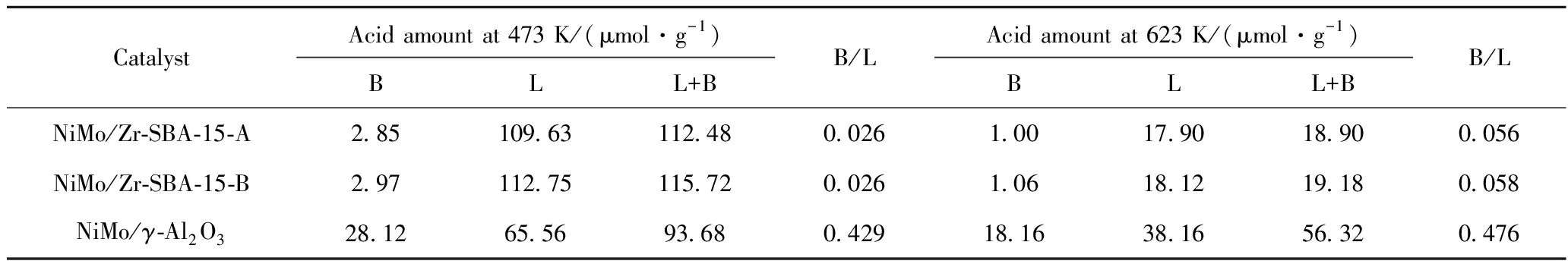
表2 吡啶红外分析测得的3种催化剂的酸量Table 2 Acid amounts of three catalysts determined by pyridine-FTIR
2.2 卟啉Ni-OEP和Ni-TPP的加氢反应历程
本研究采用固定床高压加氢微型反应装置对镍卟啉Ni-OEP和Ni-TPP进行临氢热反应和催化加氢实验,表3为部分条件下反应产物的脱镍转化率结果。由表3对比发现,在无催化剂加入的反应样品中,存在少量镍卟啉转化为其他化合物,表明在240 ℃条件下,2种镍卟啉均发生轻微的热反应。对比可见,尽管2种镍卟啉在催化剂NiMo/γ-Al2O3中进料流率为NiMo/Zr-SBA-15-B中的2倍以上,两者的加氢脱镍转化效果较接近。由此初步显示,合成的NiMo/Zr-SBA-15-B催化剂的加氢活性低于工业NiMo/γ-Al2O3催化剂。

表3 镍卟啉Ni-OEP和Ni-TPP临氢热反应条件和加氢脱镍反应的转化结果Table 3 Thermal reaction conditions for nickel-porphyrins Ni-OEP and Ni-TPP under hydrogen atmosphereand conversion results of hydrogenation de-nickel reaction
为了获得对2种镍卟啉的加氢反应历程的深入认识,本研究利用Thermo Orbitrap Fusion对Ni-TPP及其加氢产物样品(见表3中样品A、C、E)进行质谱分析。经甲酸铵促电离效果验证实验后,确定向1.5 mL的甲苯-甲醇稀释样品中加入10 μL甲酸和20 μL氨水的优化方案。Ni-TPP及其在催化剂NiMo/γ-Al2O3和NiMo/Zr-SBA-15-B中加氢产物样品的质谱及局部质量放大的质谱图如图4所示。其中,左下角为质荷比m/z为668~678的质谱结果,右侧小图均为m/z间隔范围0.07的局部质量放大图。
从图4可以看到,Ni-TPP在加氢反应前后的质谱图中峰型和分布变化不大,但分别对m/z为673、674和675局部质量范围进行放大后,可清晰地看到Ni-TPP加氢前后样品质谱的差异。在m/z为673局部放大图可以明显看出,经NiMo/γ-Al2O3和NiMo/Zr-SBA-15-B 2种催化剂加氢反应后样品中均出现了新的质谱峰,识谱后确认其为Ni-TPP在反应过程中加2个氢的产物二氢镍卟吩(Ni-TPPH2)电离峰。在m/z为674和675局部质量范围可见Ni-TPPH2同位素峰的存在。由此可以证明,在表3相应的反应条件下,卟啉Ni-TPP加氢脱金属反应过程中会生成二氢镍卟吩。由图4(c)可见,样品E存在Ni-TPPH4质子化离子峰,但其峰强度极低,且其他质量点处未发现同位素峰的存在。由此推测,较多氢取代的中间产物极不稳定,易于快速发生氢解从而脱除金属镍,由此通过取样后分析的离线手段很难及时捕捉其存在信息。
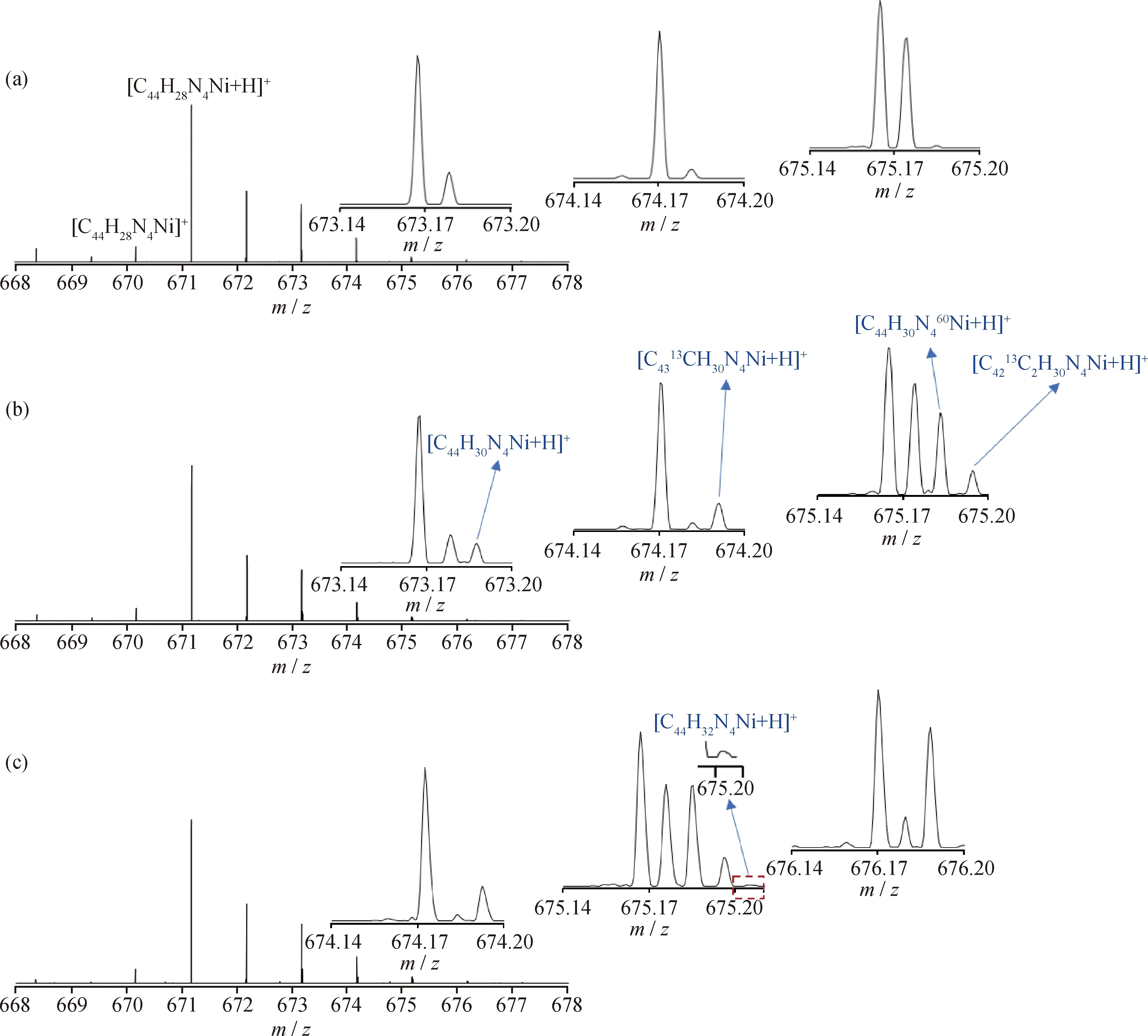
图4 Ni-TPP及其加氢后样品的Orbitrap质谱图Fig.4 Orbitrap mass spectra of Ni-TPP and its hydrogenated samples(a) Sample A; (b) Sample C; (c) Sample E
图5为Ni-OEP及其在催化剂NiMo/γ-Al2O3和NiMo/Zr-SBA-15-B中加氢产物样品(见表3中样品B、D、F)的质谱及局部质量放大质谱图。由图5可以看出,在m/z为592局部质量放大图中可见二氢中间产物Ni-OEPH2的分子离子峰。在m/z为593、594和595局部质量点处存在Ni-OEP的同位素峰、Ni-OEP的质子化离子峰、Ni-OEPH2的同位素峰、Ni-OEPH2的质子化离子峰以及Ni-OEPH2的质子化离子的同位素峰,说明在Ni-OEP的加氢脱金属反应过程中会生成中间产物Ni-OEPH2。Bonné等[19]通过质谱中m/z为594和596处存在谱峰,认为Ni-OEP的加氢过程生成四氢和八氢产物。但其低分辨率的质谱表征无法识别局部质量点的多种离子及其同位素峰。对比图5的结果发现,样品F在m/z为594和596局部质量点处存在较为明显的Ni-OEPH4的分子离子峰及其同位素峰,由此获得了Ni-OEP在加氢过程中存在四氢中间产物的直接质谱证据。对比谱峰的相对丰度可见,四氢中间产物含量较低,同样表明Ni-OEP卟啉分子的二氢以上中间产物不稳定,易于发生氢解从而脱除金属镍。
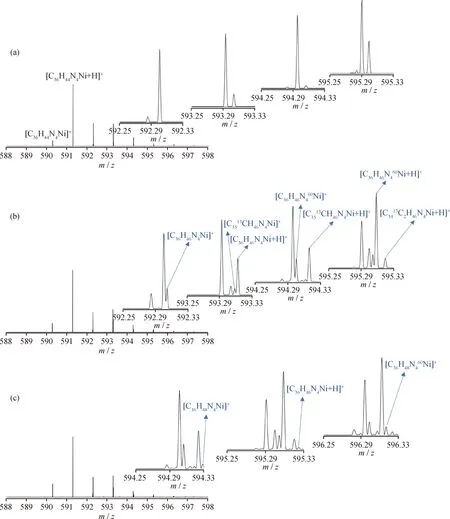
图5 Ni-OEP及其加氢后样品的Orbitrap质谱图Fig.5 Orbitrap mass spectra of Ni-OEP and its hydrogenated samples(a) Sample B; (b) Sample D; (c) Sample F
基于上述分析可见,镍卟啉Ni-OEP和Ni-TPP的加氢样品中发现二氢和四氢产物。早期研究者应用紫外-可见光谱[20]对加氢反应前后产物进行表征,从而推测出Ni-TPP连续加氢的反应历程。本研究应用Orbitrap MS不仅给出2种镍卟啉加氢中间产物的直接质谱证据,而且由相对丰度可获得中间产物含量很低的新认识。由此表明,Ni-OEP和Ni-TPP生成的加氢中间产物极不稳定,易于在反应中快速氢解从而沉积于催化剂表面。因此,应用镍卟啉Ni-OEP和Ni-TPP的消失速率反映其加氢脱金属反应动力学行为切实可行。另一方面,镍卟啉在2种类型催化剂加氢过程中的加氢是控制步骤,加氢中间产物一旦生成,就会通过氢解快速脱除金属。因此,需要催化剂提高加氢活性以改进其本征反应性能。
2.3 Ni-OEP和Ni-TPP加氢过程的反应规律
2.3.1 Ni-TPP的加氢反应规律
重油中金属卟啉化合物在加氢过程中将受到明显的扩散阻力。尽管早期对镍钒金属卟啉的加氢反应动力学开展了相关研究,但其中的扩散行为及其对加氢反应的影响鲜有报道。本课题组采用小型固定床微型反应装置对镍卟啉进行加氢实验,操作条件为:反应温度240 ℃,反应压力6 MPa,氢/油体积比200,液时空速20~100 h-1。Ni-TPP的加氢脱镍转化率随着液相进料流率与催化剂装填质量之比(F/m)的变化规律如图6所示。
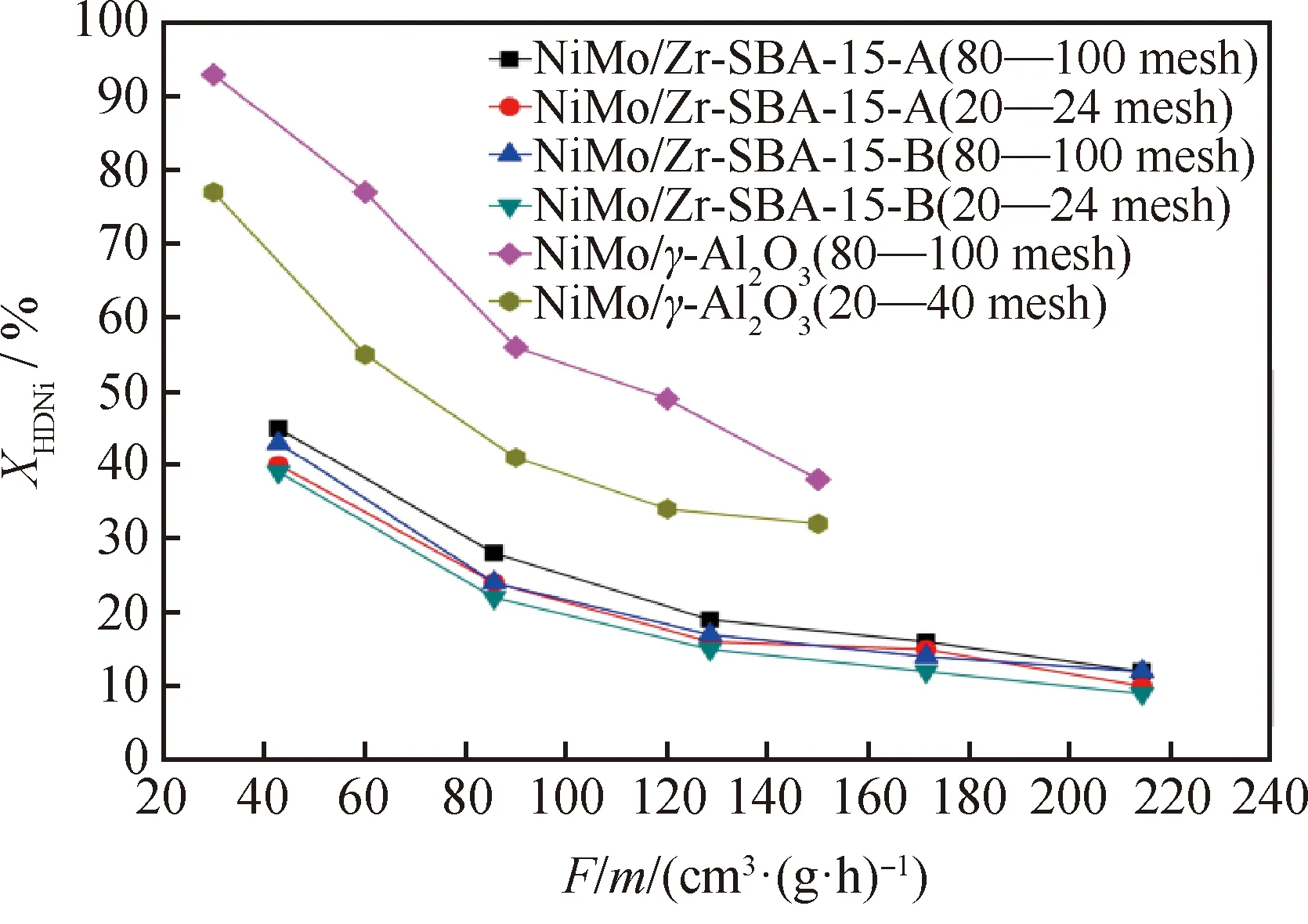
F—Feed flow rate; m—Catalyst mass图6 Ni-TPP加氢脱镍转化率(XHDNi)随F/m变化规律Fig.6 Change law of conversion rates (XHDNi) forhydrogenation de-nickel reaction ofNi-TPP over different F/mT=240 ℃; p=6 MPa; V(H2)/V(Oil)=200;LHSV=20-100 h-1
由图6可见,随着液相进料流率的不断增大,Ni-TPP的加氢脱镍转化率逐渐降低。Ni-TPP在NiMo/Zr-SBA-15-A和NiMo/Zr-SBA-15-B催化剂上不仅加氢脱镍转化率的变化趋势相同,且相同条件下的加氢脱镍转化率相近。对比较小粒径80~100目催化剂的结果发现,Ni-TPP在NiMo/Zr-SBA-15-A和NiMo/Zr-SBA-15-B催化剂中的加氢脱镍转化率相近,表明合成的这2种NiMo/Zr-SBA-15催化剂的加氢脱镍反应活性相差不大;对比NiMo/Zr-SBA-15催化剂的结果发现,催化剂粒径的改变对Ni-TPP的加氢脱镍转化率影响相差不大,表明内扩散对HDNi反应的影响不明显。相同催化剂粒径条件下,工业NiMo/γ-Al2O3催化剂加氢脱镍转化率明显高于2种NiMo/Zr-SBA-15催化剂,展现出较高的加氢活性。此外,对比催化剂2种粒径的结果可见,Ni-TPP在粒径80~100目的NiMo/γ-Al2O3中的加氢脱镍反应活性明显高于粒径20~40目下该催化剂的结果,表明反应物在其孔道中的扩散阻力对HDNi反应存在较为明显的影响。
为了深入对比Ni-TPP化合物在加氢过程中的扩散和反应性能,将图6加氢脱镍数据按照一级反应动力学进行拟合,得到图7。由图7可以看出,Ni-TPP加氢反应的-ln(1-X)与m/F呈现较好的线性关系。这表明在本研究中考察的240 ℃和6.0 MPa的条件下,NiMo/Zr-SBA-15和NiMo/γ-Al2O3催化剂中Ni-TPP的加氢脱镍遵循拟一级反应动力学规律。由此,可由图7中拟合直线的斜率得到该加氢脱镍的反应速率常数,结果列于表4。由图7的结果可初步看出,Ni-TPP在NiMo/γ-Al2O3催化剂中的加氢活性明显高于Zr-SBA-15催化剂,且NiMo/γ-Al2O3催化剂的本征和表观加氢脱镍活性差异较大。
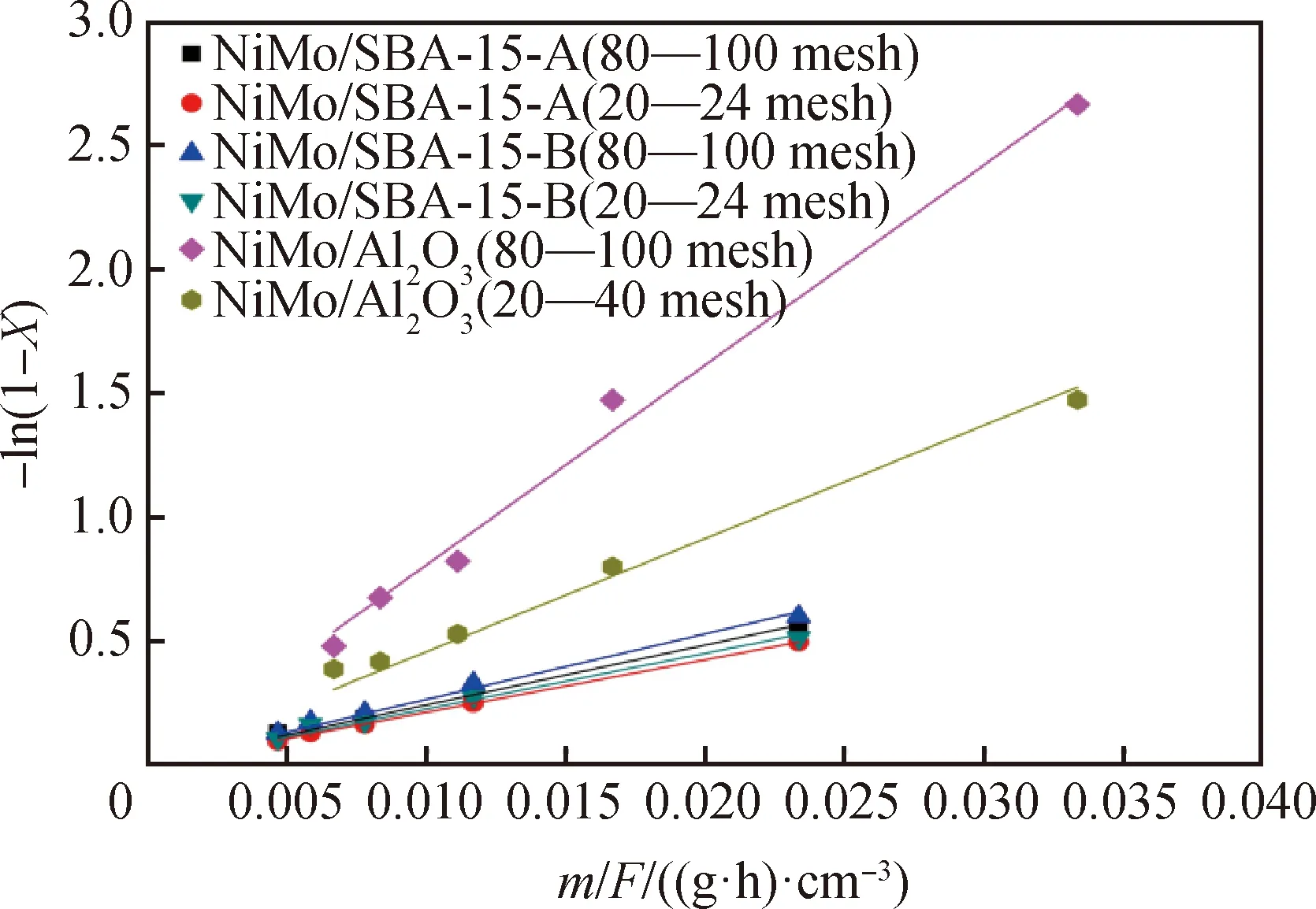
图7 Ni-TPP加氢脱镍反应动力学数据拟合Fig.7 Kinetic data fitting for hydrogenationde-nickel reaction of Ni-TPP
2.3.2 镍卟啉Ni-OEP的加氢反应规律
本研究以镍卟啉Ni-OEP为反应物,在反应温度240 ℃、反应压力6 MPa、氢/油体积比200、液时空速20~100 h-1的条件下进行加氢实验,镍卟啉Ni-OEP加氢脱镍转化率随着F/m的变化规律如图8所示。
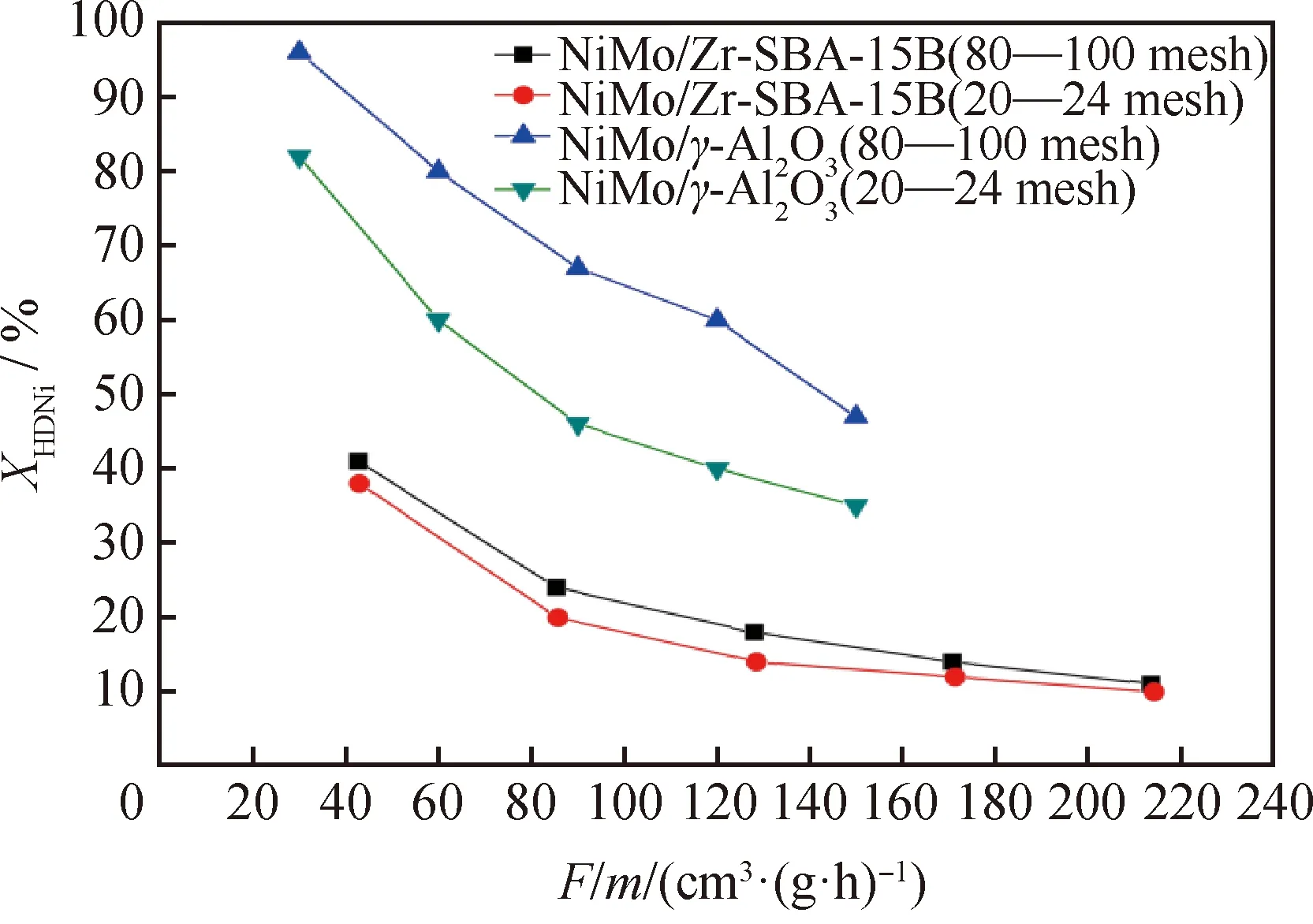
F—Feed flow rate; m—Catalyst mass图8 Ni-OEP加氢脱镍转化率(XHDNi)随F/m变化规律Fig.8 Change law of conversion rats (XHDNi) forhydrogenation de-nickel reaction ofNi-OEP over different F/mT=240 ℃; p=6 MPa; V(H2)/V(Oil)=200;LHSV=20-100 h-1
由图8可以看出,Ni-OEP的加氢反应规律与Ni-TPP的结果(见图7)相近。随着液相进料流率的不断增大,Ni-OEP的加氢脱镍转化率逐渐降低。对比发现,Ni-OEP在NiMo/γ-Al2O3催化剂的加氢脱镍转化率明显高于2种NiMo/Zr-SBA-15催化剂。此外,对比NiMo/γ-Al2O3催化剂2种粒径的结果可见,Ni-OEP在粒径80~100目中的加氢脱镍转化率明显高于粒径20~40目中的结果,同样显示出较为明显的内扩散影响。但是,镍卟啉Ni-OEP在2种粒径NiMo/Zr-SBA-15B催化剂的加氢脱镍转化率相差不大,初步表明内扩散对其加氢反应的影响不明显。
将图8中加氢脱镍数据按照一级反应动力学进行拟合得到图9。由图9可以看出,在反应温度240 ℃和反应压力6.0 MPa的条件下,Ni-OEP在NiMo/Zr-SBA-15和NiMo/γ-Al2O32种催化剂上的加氢脱镍同样遵循拟一级反应动力学规律。由此,可由图9中拟合直线的斜率得到该加氢脱镍的反应速率常数,结果列于表4。由图9中4条直线的斜率大小可以初步得出,Ni-OEP在NiMo/γ-Al2O3催化剂上的加氢脱镍活性明显高于其在NiMo/Zr-SBA-15催化剂上的结果,且Ni-OEP在NiMo/γ-Al2O3催化剂中的本征和表观加氢脱镍活性差异较大。
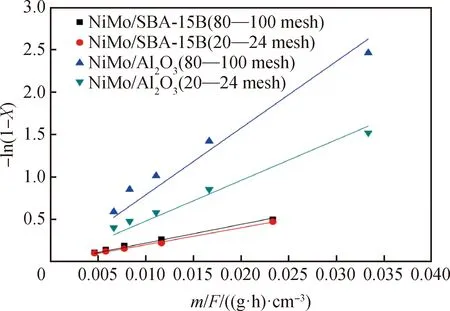
图9 Ni-OEP加氢脱镍反应动力学数据拟合Fig.9 Kinetic data fitting for hydrogenationde-nickel reaction of Ni-OEP
2.4 镍卟啉Ni-OEP和Ni-TPP加氢反应动力学
将Thiele关系和非均相催化反应动力学数据相结合可以得出内扩散系数和有效因子等参数,从而利于剖析内扩散对非均相反应的影响。本课题组利用上述方法对镍卟啉Ni-OEP和Ni-TPP在加氢反应动力学参数进行求取,结果如表4所示。
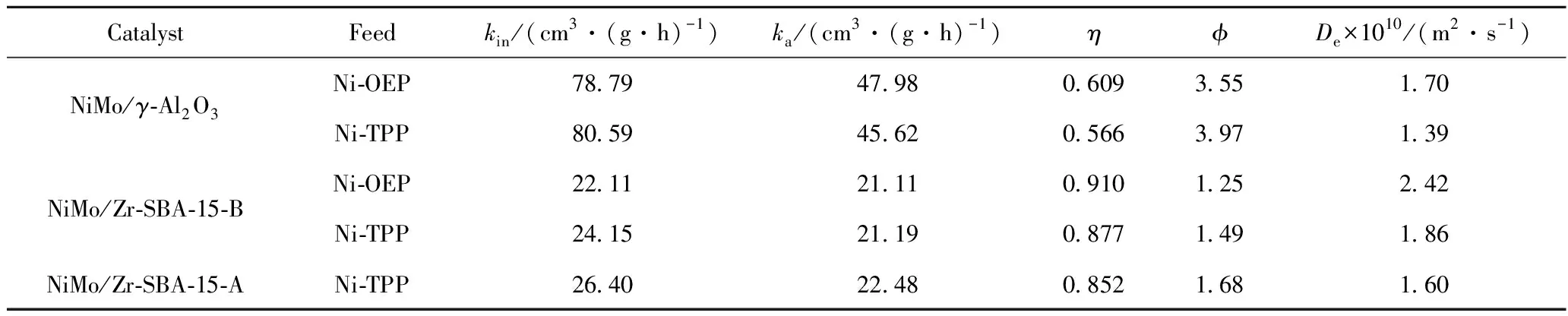
表4 镍卟啉加氢脱金属反应动力学参数Table 4 Kinetic parameters of nickel-porphyrin hydrogenation demetallization reaction
由表4可知,Ni-OEP和Ni-TPP在2种NiMo/Zr-SBA-15催化剂上的加氢脱金属反应速率远小于NiMo/γ-Al2O3催化剂。这主要是由于NiMo/γ-Al2O3基催化剂的酸量明显高于锆改性硅基催化剂,导致后者对卟啉类化合物的加氢开环反应活性明显降低。正是由于NiMo/γ-Al2O3催化剂的较高加氢反应活性,导致Ni-OEP和Ni-TPP在催化剂孔道中的内扩散对反应产生较为显著的影响,表观反应速率常数相对于本征结果降低约40%。对比发现,尽管Ni-TPP相对于Ni-OEP在NiMo/γ-Al2O3催化剂上具有较高的本征反应活性,但后者在NiMo/γ-Al2O3催化剂上的表观反应活性高于前者。这主要是由于Ni-OEP和Ni-TPP均具有相同的4个吡咯环构筑的共轭结构,两者的加氢活性较为接近。但Ni-TPP分子具有4个苯基取代基,而Ni-OEP具有8个乙基取代基,前者具有相对较大的分子尺寸,从而导致其在催化剂孔道中的扩散阻力较大,扩散对反应造成的抑制作用更为明显。
进一步对比发现,Ni-OEP和Ni-TPP在NiMo/Zr-SBA-15催化剂上的本征反应速率常数较接近;尽管表观反应速率常数相对于本征反应而言有所降低,但降低幅度并不明显。由于NiMo/Zr-SBA-15催化剂具有较为均一的圆柱形介孔孔道,其为非均相催化反应中的扩散行为考察提供了较理想的多孔材料。对比发现,催化剂NiMo/Zr-SBA-15-B 上Ni-OEP的HDNi有效因子明显大于Ni-TPP。由于相对于Ni-TPP而言,Ni-OEP具有相对较小的分子尺寸,从而使得内扩散对Ni-OEP加氢脱镍反应的影响小于Ni-TPP。这与Ni-OEP在NiMo/Zr-SBA-15-B上有效扩散系数明显高于Ni-TPP的结果(见表4)相一致。对于同种反应物分子,由于催化剂NiMo/Zr-SBA-15-B的平均孔径大于催化剂NiMo/Zr-SBA-15-A,因此2种镍卟啉在催化剂NiMo/Zr-SBA-15-B中的有效扩散系数明显大于催化剂NiMo/Zr-SBA-15-A的结果,内扩散对HDNi反应的影响有所缓解。
工业NiMo/γ-Al2O3催化剂展现出较高的HDNi活性,这是造成内扩散抑制此加氢反应的一个重要原因。由表1可知,NiMo/γ-Al2O3催化剂的平均孔径为17.8 nm,明显高于本研究中合成的2种NiMo/Zr-SBA-15催化剂。由于NiMo/γ-Al2O3催化剂是由无定形结构的基质材料堆积形成的无规则孔道,孔径的无序收缩和弯曲造成反应物分子在其中的扩散受阻较为严重。这也表明此种催化材料的平均孔径无法准确反映出反应物分子在其孔道中运动的受阻情况。尽管2种NiMo/Zr-SBA-15催化剂的平均孔径较小,但其孔道尺寸均一且结构规整,导致反应物分子运动较为顺畅,扩散受阻程度明显低于NiMo/γ-Al2O3催化剂。
基于上述分析可见,在NiMo/Zr-SBA-15催化剂上,镍卟啉Ni-OEP和Ni-TPP的加氢反应主要受本征活性的制约,内扩散对其HDNi反应影响较小。而对于NiMo/γ-Al2O3催化剂而言,其对Ni-OEP和Ni-TPP的本征加氢反应活性较高,但无规则的孔道结构使得其在孔道中内扩散对加氢反应的影响显著。因此,可以适当增大催化剂孔径或提高催化剂孔道间的贯通性,从而通过强化反应物分子的扩散传质实现这种较大尺寸有机金属化合物的高效加氢转化。
3 结 论
采用合成的2种NiMo/Zr-SBA-15介孔催化剂和工业NiMo/γ-Al2O3催化剂对Ni-OEP和Ni-TPP进行加氢实验,通过Orbitrap质谱分析获得对镍卟啉HDNi反应路径的新认识,并剖析出其加氢过程中的扩散和反应行为,得出结论如下:
(1)Ni-OEP和Ni-TPP加氢样品的Orbitrap质谱图中发现了增加2个氢和4个氢原子产物存在的直接证据,其中Ni-TPP中加4个氢原子产物的谱峰相对强度较低,且其他质量点处未发现同位素峰的存在,意味着加2个氢原子以上中间产物不稳定,易于发生氢解脱金属。
(2)Ni-OEP和Ni-TPP的加氢反应均遵循拟一级动力学,且其在工业NiMo/γ-Al2O3催化剂上的加氢活性明显高于NiMo/Zr-SBA-15催化剂;尽管NiMo/γ-Al2O3催化剂具有较大的平均孔径,但无规则的孔道结构造成镍卟啉较低的扩散性能,导致扩散对HDNi反应的影响显著。
