经典名方枳实薤白桂枝汤物质基准的量值传递研究
2022-05-06徐瑞杰宫静雯赵晓莉许金国严国俊陆兔林毛春芹
徐瑞杰,薛 蓉,梅 茜,宫静雯,张 倩,娄 悦,赵晓莉,许金国,严国俊,陆兔林,毛春芹
经典名方枳实薤白桂枝汤物质基准的量值传递研究
徐瑞杰,薛 蓉,梅 茜,宫静雯,张 倩,娄 悦,赵晓莉,许金国,严国俊,陆兔林*,毛春芹*
南京中医药大学药学院,江苏 南京 210023
建立经典名方枳实薤白桂枝汤(Zhishi Xiebai Guizhi Decoction,ZXGD)基准样品的HPLC特征图谱并对其进行多成分含量测定,研究ZXGD物质基准量值传递规律,为复方制剂研究奠定基础。制备20批ZXGD基准样品,建立其特征图谱,明确其特征峰并对其进行特征峰的归属;对ZXGD基准样品进行多成分含量测定,分析主要成分从饮片-物质基准的传递规律。20批ZXGD基准样品的特征图谱相似度均大于0.93,共匹配得到11个特征峰,分别来自于方中枳实(峰1、3~5、9)、厚朴(峰2、10、11)、桂枝(峰6~8);各指标性成分的含量范围及饮片-基准样品的平均转移率分别为辛弗林0.46%~0.85%和103.80%,橙皮苷0.58%~1.07%和42.36%,肉桂酸0.025%~0.047%和105.53%,桂皮醛0.09%~0.17%和5.40%,厚朴酚与和厚朴酚0.005 6%~0.010 3%和0.23%。采用HPLC特征图谱和多成分含量测定对ZXGD物质基准的量值传递规律进行研究,该方法科学合理,且明确了饮片-物质基准的传递规律,实现了对经典名方ZXGD开发研究的全过程质量控制。
经典名方;枳实薤白桂枝汤;基准样品;物质基准;特征图谱;量值传递;枳实;厚朴;桂枝;辛弗林;橙皮苷;肉桂酸;桂皮醛;厚朴酚;和厚朴酚
枳实薤白桂枝汤(Zhishi Xiebai Guizhi Decotion,ZXGD)来源于东汉张仲景的《金匮要略》[1],全方共由枳实、薤白、桂枝、瓜蒌、厚朴5味药组成,主要治疗胸痹等疾病。现代临床上主要应用于心脑血管系统、消化系统以及呼吸系统等方面疾病,其对冠心病、心绞痛、高脂血症、功能性消化不良、肺栓塞等都有一定的治疗作用[2-7]。近年来,国家大力支持古代经典名方中药复方制剂的开发,对于经典名方的申报可免临床研究资料,虽然与其他复方制剂的开发过程相比减少了临床研究,但对其质量控制方面却有着严格的要求。而特征图谱和多成分含量测定是对经典名方质量控制研究的2个重要手段,特征图谱结合多成分含量测定可较为全面地对经典名方物质基准的量值传递过程进行分析,从而对经典名方的质量控制提供参考价值[8-10]。
目前,针对ZXGD的报道主要集中于其药理作用和临床相关应用,对于其质量控制研究较少[11-14],通过建立ZXGD特征图谱且结合多成分含量测定的研究还未见报道。为了进一步推进经典名方ZXGD中药复方制剂的研究应用,根据国家药品监督管理局发布的《古代经典名方中药复方制剂物质基准的申报资料要求》[15],开展有关ZXGD的特征图谱、多成分含量测定及物质基准的量值传递研究[16-18]。通过对国家发布的古代经典名方关键信息的考证[19],并结合具体情况研制ZXGD基准样品,通过特征图谱及指标成分的含量测定对ZXGD饮片-基准样品研究全过程进行质量控制。为下一步进行ZXGD中药复方制剂的研究奠定基础,也为古代经典名方的开发与利用提供参考。
1 仪器与材料
1.1 仪器
岛津LC-20AD型高效液相色谱仪,日本Shimadzu公司,包括LC-20AD溶剂输送泵,SIL-20A自动进样器,CTO-20AC柱温箱,SPD-M20A紫外-可见检测器,CBM-20A色谱数据工作站;FA1104N型电子分析天平,上海菁海仪器有限公司;MS-105DU型电子分析天平,瑞士梅特勒-托利多公司;KQ-500B型超声波清洗器,昆山市超声仪器有限公司;AE-1106A型多功能红外炉,中山市爱米生活电器有限公司;FD-1A-50型冷冻干燥机,上海利闻科学仪器有限公司。
1.2 材料
枳实、厚朴、薤白、桂枝、瓜蒌5味药材购于雷允上药业有限公司,均来源于道地产区或主产区,经南京中医药大学药学院陈建伟教授鉴定,5味药材的基原分别为芸香科柑橘属植物酸橙L.的干燥幼果、木兰科木兰属植物厚朴Rehd.et Wils.的干燥干皮、百合科葱属植物小根蒜Bge.的干燥鳞茎、樟科樟属植物肉桂Presl的干燥嫩枝、葫芦科栝楼属植物栝楼Maxim.的干燥成熟果实。每味药材共采购5批,参照《中国药典》2020年版进行炮制,每批药材炮制得3批饮片,因此得枳实、厚朴、薤白、桂枝、瓜蒌各15批饮片。
对照品辛弗林(批号110727-201809,质量分数99.5%)、和厚朴酚(批号110730-201614,质量分数99.3%)、厚朴酚(批号110729-201714,质量分数100.0%)、桂皮醛(批号110710-201821,质量分数99.6%)、橙皮苷(批号110721-201818,质量分数96.2%)、肉桂酸(批号110786-201604,质量分数98.8%),均购自中国食品药品检定研究院。
甲醇,分析纯,山东禹王实业有限公司化工分公司;甲醇,色谱纯,江苏汉邦科技有限公司;娃哈哈纯净水,杭州娃哈哈集团有限公司;乙腈,色谱纯,德国Merck公司;磷酸,色谱纯,上海阿拉丁生化科技股份有限公司。
2 方法与结果
2.1 20批ZXGD基准样品的制备
根据对《金匮要略》中记载的ZXGD的处方原文和国家发布的关键信息进行考证,并通过对浸泡时间、加盖与否、滤过方式等因素进行考察,最终确定ZXGD基准样品的制备工艺。
取枳实9 g、厚朴12 g,置陶瓷锅中,加水1000 mL,浸泡60 min,以武火煮沸后,转文火继续煎煮至400 mL,2层纱布趁热滤过。取薤白24 g、桂枝3 g、瓜蒌15 g,置于上述滤液中,浸泡60 min,武火沸腾后,转文火继续煎煮至100 mL,2层纱布滤过,滤液放冷至室温。取滤液至−80 ℃冰箱预冻12 h后,放入冷冻干燥机,于−54 ℃、0.74 Pa真空度冷冻干燥为冻干粉,即得。
同法制备单味饮片及缺单味药阴性样品。
将枳实、厚朴、薤白、桂枝、瓜蒌各15批次饮片随机组合形成20批次基准样品,编号为ZXGD1~ZXGD20,具体批次组合信息见表1。
2.2 ZXGD基准样品特征图谱的建立
2.2.1 色谱条件 Kromasil C18色谱柱(250 mm× 4.6 mm,5 μm),流动相为乙腈-0.05%磷酸水溶液,梯度洗脱:0~7 min,1%乙腈;7~8 min,1%~5%乙腈;8~12 min,5%~15%乙腈;12~30 min,15%~20%乙腈;30~40 min,20%乙腈;40~50 min,20%~25%乙腈;50~51 min,25%~26%乙腈;51~65 min,26%~27%乙腈;65~68 min,27%~30%乙腈;68~70 min,30%~45%乙腈;70~75 min,45%乙腈;75~79 min,45%~65%乙腈;79~96 min,65%~95%乙腈;体积流量为1 mL/min;柱温30 ℃;检测波长为290 nm;进样量10 μL。
表1 20批ZXGD基准样品随机组合信息
Table 1 Information table of random combination of 20 batches of ZXGD reference samples
编号枳实厚朴薤白桂枝瓜蒌 ZXGD1ZS-M1811004-3HP180612-2XB180321-3GZ-181014-2GL181016-3 ZXGD2ZS-M1811004-1HP180609-2XB180322-3GZ-181012-3GL181015-3 ZXGD3ZS-M1811004-1HP180610-1XB180322-3GZ-181014-3GL181016-3 ZXGD4ZS-M1811004-3HP180611-1XB180322-3GZ-181011-1GL181019-1 ZXGD5ZS-M1811002-3HP180612-3XB180323-2GZ-181015-1GL181018-2 ZXGD6ZS-M1811005-2HP180609-2XB180324-1GZ-181013-3GL181015-1 ZXGD7ZS-M1811001-3HP180609-2XB180323-2GZ-181011-2GL181018-1 ZXGD8ZS-M1811003-2HP180611-3XB180320-2GZ-181011-3GL181019-3 ZXGD9ZS-M1811005-1HP180610-1XB180323-3GZ-181014-1GL181016-1 ZXGD10ZS-M1811004-1HP180612-2XB180320-2GZ-181015-1GL181018-3 ZXGD11ZS-M1811001-3HP180612-3XB180320-3GZ-181013-1GL181016-2 ZXGD12ZS-M1811003-2HP180608-1XB180323-3GZ-181014-2GL181019-1 ZXGD13ZS-M1811004-3HP180610-1XB180322-2GZ-181013-3GL181017-3 ZXGD14ZS-M1811002-3HP180608-2XB180321-2GZ-181015-1GL181019-3 ZXGD15ZS-M1811002-2HP180608-3XB180321-1GZ-181013-2GL181019-3 ZXGD16ZS-M1811004-3HP180608-3XB180322-2GZ-181015-3GL181015-3 ZXGD17ZS-M1811004-3HP180608-3XB180322-2GZ-181015-3GL181015-3 ZXGD18ZS-M1811004-3HP180608-3XB180322-2GZ-181015-3GL181015-3 ZXGD19ZS-M1811004-3HP180608-3XB180322-2GZ-181015-3GL181015-3 ZXGD20ZS-M1811004-3HP180608-3XB180322-2GZ-181015-3GL181015-3
2.2.2 供试品溶液的制备 取10 mL煎煮液对应的冻干粉,置50 mL量瓶中,加甲醇40 mL,加蒸馏水至刻度,称定质量,超声处理(功率500 W、频率40 kHz)20 min,放冷,再称定质量,用80%甲醇补足减失的质量,摇匀,滤过,取续滤液,即得供试品溶液。
2.2.3 精密度试验 取编号为ZXGD1的基准样品1份,按照“2.2.2”项下方法制备供试品溶液,按照“2.2.1”项下色谱条件连续进样6次,记录色谱图。以橙皮苷为参照峰,计算各特征峰相对保留时间和相对峰面积,结果各特征峰的相对保留时间RSD均小于0.28%,相对峰面积RSD均小于4.88%,表明仪器精密度良好。
2.2.4 稳定性试验 取编号为ZXGD1的基准样品一份,按照“2.2.2”项下方法制备供试品溶液,按照“2.2.1”项下色谱条件分别在0、2、4、8、12、24 h进样,记录色谱图。以橙皮苷为参照峰,计算各特征峰相对保留时间和相对峰面积,结果各特征峰的相对保留时间RSD均小于0.31%,相对峰面积RSD均小于3.56%,表明供试品溶液在24 h内稳定性良好。
2.2.5 重复性试验 取编号为ZXGD1的基准样品一份,按照“2.2.2”项下方法平行制备6份供试品溶液,按照“2.2.1”项下色谱条件进样,记录色谱图。以橙皮苷为参照峰,计算各特征峰相对保留时间和相对峰面积,结果各特征峰的相对保留时间RSD均小于0.29%,相对峰面积RSD均小于3.62%,表明该方法重复性良好。
2.2.6 特征峰的指认 按照“2.2.2”项下方法制备20批供试品溶液,按照“2.2.1”项下色谱条件进样,记录20批色谱图。将20批ZXGD基准样品特征图谱以AIA格式导入《中药色谱指纹图谱相似度评价系统(2012版)》,以S1为参照图谱,采用平均数法,时间窗设为0.5,并计算相似度。20批ZXGD(ZXGD1~ZXGD20)基准样品特征图谱的相似度分别为0.961、0.959、0.960、0.966、0.941、0.969、0.955、0.972、0.936、0.942、0.957、0.955、0.950、0.959、0.976、0.935、0.941、0.962、0.961、0.968,特征图谱相似度均大于0.93,表明ZXGD的质量稳定均一,各批次间物质群较为稳定,特征图谱叠加图见图1。
ZXGD基准样品特征图谱共标定了11个特征峰,通过与对照品色谱峰进行比对,指认到6个特征峰,其中1号峰为辛弗林、4号峰为橙皮苷、6号峰为肉桂酸、7号峰为桂皮醛、10号峰为和厚朴酚、11号峰为厚朴酚,混合对照品及ZXGD基准样品特征图谱见图2。ZXGD基准样品特征图谱中有11个特征峰,其中6个峰(峰1、4、6、7、10、11)分别与相应的参照物保留时间相同,以橙皮苷参照物峰相应的峰为S峰,计算其余特征峰的相对保留时间,其相对保留时间应在规定值的±5%之内。规定值为0.52(峰2)、0.91(峰3)、1.51(峰5)、1.94(峰8)、2.08(峰9)。
2.2.7 饮片-基准样品特征峰的传递 对ZXGD基准样品中特征峰从饮片到基准样品的传递规律进行分析。枳实、厚朴、桂枝单味饮片及缺单味饮片阴性样品的特征图谱分别见图3。对ZXGD基准样品中特征峰进行归属,其中1(辛弗林)、3、4(橙皮苷)、5、9号峰归属于枳实;2、10(和厚朴酚)、11(厚朴酚)号峰归属于厚朴;6(肉桂酸)、7(桂皮醛)、8号峰归属于桂枝。大部分色谱峰具有良好的传递性,且归属关系清晰,饮片中的物质群能够较为稳定的向基准样品中传递。
2.3 ZXGD基准样品多成分含量测定
2.3.1 色谱条件 Kromasil C18色谱柱(250 mm×4.6 mm,5 μm),以乙腈-0.05%磷酸水溶液为流动相,梯度洗脱:0~7 min,1%乙腈;7~8 min,1%~5%乙腈;8~12 min,5%~15%乙腈;12~30 min,15%~20%乙腈;30~40 min,20%乙腈;40~50 min,20%~25%乙腈;50~51 min,25%~26%乙腈;51~65 min,26%~27%乙腈;65~68 min,27%~30%乙腈;68~70 min,30%~45%乙腈;70~75 min,45%乙腈;75~79 min,45%~65%乙腈;79~96 min,65%~95%乙腈;体积流量为1 mL/min;柱温30 ℃;检测波长为214 nm(辛弗林)、290 nm,进样量10 μL。
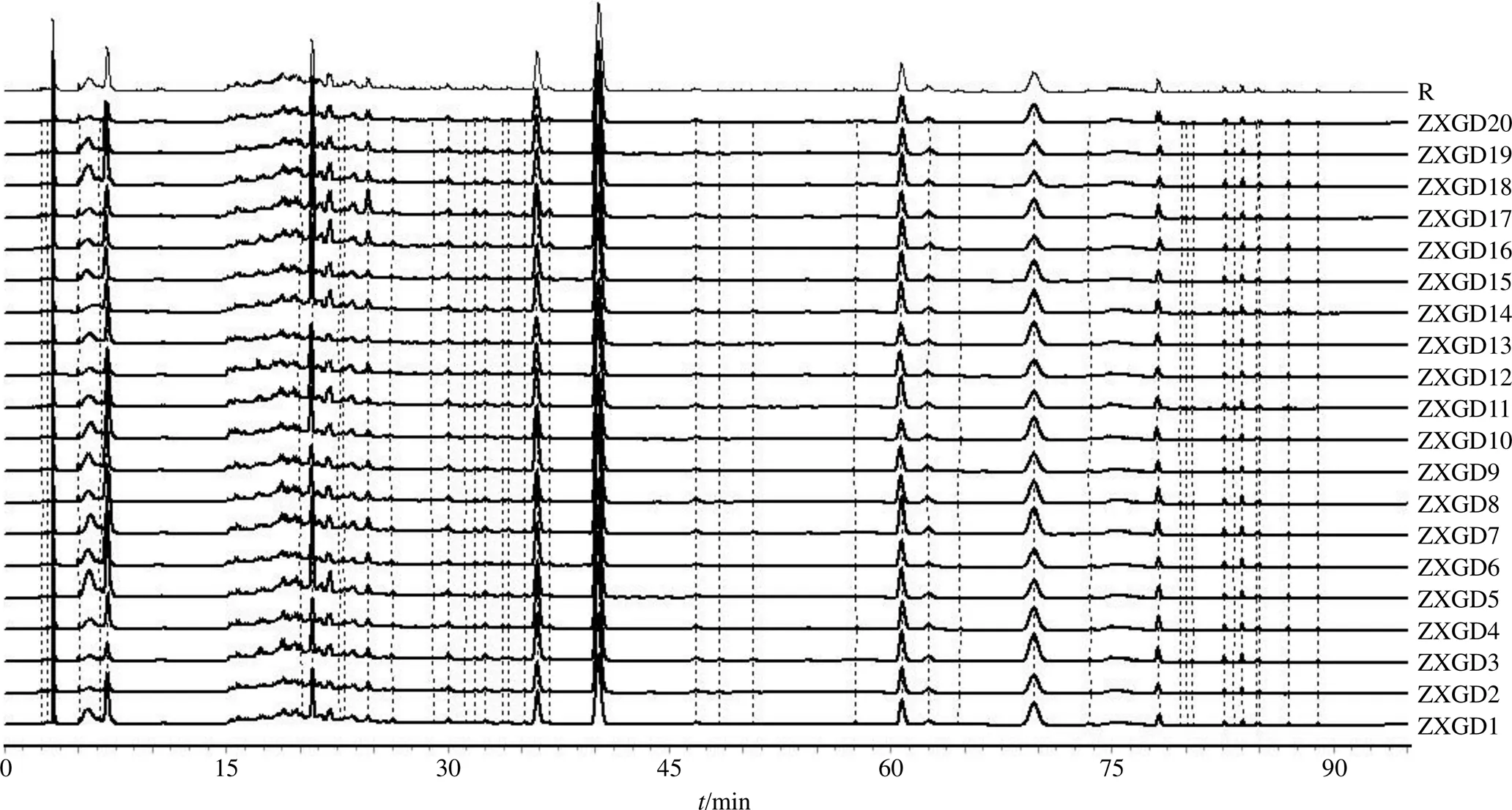
图1 20批ZXGD基准样品HPLC特征图谱叠加图

1-辛弗林 4-橙皮苷 6-肉桂酸 7-桂皮醛 10-和厚朴酚 11-厚朴酚

图3 ZXGD特征峰传递图谱
2.3.2 供试品溶液的制备 与“2.2.2”项下供试品溶液的制备方法一致。
2.3.3 对照品溶液的制备 取辛弗林、橙皮苷、肉桂酸、桂皮醛、和厚朴酚、厚朴酚对照品适量,精密称定,加甲醇制成质量浓度为600.96、506.00、10.10、24.78、2.14、4.00 μg/mL的混合对照品溶液。
2.3.4 线性关系考察 精密量取“2.3.3”项下混合对照品溶液,按照2、4、6、8、16的倍数进行倍比稀释,以甲醇为溶剂制成系列混合对照品溶液。按照“2.3.1”项下色谱条件进样,记录各指标成分峰面积,以进样质量浓度为横坐标(),峰面积为纵坐标(),进行线性回归分析。得到回归方程及线性范围分别为辛弗林=2 493.47-46 034.63,=0.999 7,线性范围37.56~600.96 μg/mL;橙皮苷=15 493.88-42 649.10,=0.999 8,线性范围31.63~506.00 μg/mL;肉桂酸=66 637.13- 10 059.70,=0.999 8,线性范围0.63~10.10 μg/mL;桂皮醛=105 449.40+49 387.90,=0.999 1,线性范围1.55~24.78 μg/mL;和厚朴酚=17 489.30-154.06,=0.999 8,线性范围0.13~2.14 μg/mL;厚朴酚=14 415.17-366.31,=0.999 9,线性范围0.25~4.00 μg/mL;结果表明,6种指标成分在各自线性范围内线性关系较好。
2.3.5 精密度试验 取编号为ZXGD1的基准样品一份,按照“2.2.2”项下方法制备供试品溶液,按照“2.3.1”项下色谱条件连续进样6次,记录各成分峰面积。计算辛弗林、橙皮苷、肉桂酸、桂皮醛、和厚朴酚、厚朴酚含量的RSD值,分别为0.41%、0.54%、1.23%、0.26%、1.95%、3.72%,表明仪器精密度良好。
2.3.6 稳定性试验 取编号为ZXGD1的基准样品一份,按照“2.2.2”项下方法制备供试品溶液,按照“2.3.1”项下色谱条件分别在0、2、4、8、12、24 h进样,记录各成分峰面积。计算辛弗林、橙皮苷、肉桂酸、桂皮醛、和厚朴酚、厚朴酚含量的RSD值,分别为0.58%、1.19%、2.48%、0.60%、1.60%、2.94%,表明供试品溶液24 h稳定性良好。
2.3.7 重复性试验 取编号为ZXGD1的基准样品一份,按照“2.2.2”项下方法平行制备6份供试品溶液,按照“2.3.1”项下色谱条件进样,记录各成分峰面积。计算辛弗林、橙皮苷、肉桂酸、桂皮醛、和厚朴酚、厚朴酚含量的RSD值,分别为2.35%、1.80%、1.74%、2.86%、3.57%、3.00%,表明方法重复性良好。
2.3.8 准确度试验 取5 mL已知含量的ZXGD基准样品对应的冻干粉,共取6份,分别加入与其各成分含量相等的对照品(辛弗林对照品3.08 mg、橙皮苷对照品3.8 mg、肉桂酸对照品0.05 mg、桂皮醛对照品0.25 mg、和厚朴酚对照品0.017 mg、厚朴酚对照品0.085 mg),按照“2.2.2”项下方法制备成供试品溶液,按照“2.3.1”项下色谱条件进样,记录各指标成分峰面积,并计算加样回收率。辛弗林、橙皮苷、肉桂酸、桂皮醛、和厚朴酚、厚朴酚含量的RSD值分别为1.60%、0.39%、1.22%、1.68%、1.34%、2.52%,各成分的平均加样回收率分别为102.60%、101.70%、103.29%、98.63%、100.53%、101.46%,表明方法准确度良好。
2.3.9 多成分含量测定 按照“2.2.2”项下方法制备20批ZXGD供试品溶液,并按照“2.3.1”项下色谱条件进样,对20批ZXGD基准样品进行含量测定,混合对照品和基准样品的色谱图见图4,多成分含量测定结果见表2。20批ZXGD基准样品中各成分质量分数为辛弗林0.35%~0.87%;橙皮苷0.62%~1.00%;肉桂酸0.029%~0.043%;桂皮醛0.10%~0.17%;厚朴酚与和厚朴酚0.003 3%~0.016 1%。根据《古代经典名方中药复方制剂及其物质基准的申报资料要求》中含量测定的波动范围一般不超过均值的70%~130%,因此,暂定ZXGD基准样品中各成分的含量范围为辛弗林0.46%~0.85%,橙皮苷0.58%~1.07%,肉桂酸0.025%~0.047%,桂皮醛0.09%~0.17%,厚朴酚与和厚朴酚0.005 6%~0.010 3%。

1-辛弗林 2-橙皮苷 3-肉桂酸 4-桂皮醛 5-和厚朴酚 6-厚朴酚
2.4 量值传递关系研究
20批ZXGD基准样品和对应饮片中指标成分含量测定结果及转移率见表3。20批ZXGD基准样品中辛弗林质量分数为0.46%~0.85%,平均转移率为103.80%;橙皮苷质量分数为0.58%~1.07%,平均转移率为42.36%;肉桂酸质量分数为0.025%~0.047%,平均转移率为105.53%;桂皮醛质量分数为0.09%~0.17%,平均转移率为5.40%;厚朴酚与和厚朴酚质量分数总量为0.005 6%~0.010 3%,平均转移率为0.23%。
根据相关规定,不同批次基准样品的转移率也应在其均值的70%~130%,在本研究中辛弗林、橙皮苷、肉桂酸和桂皮醛4个成分的转移率基本都在其均值的70%~130%,说明前期枳实和桂枝的饮片及基准样品的制备工艺相对稳定可行。但是部分批次中厚朴酚与和厚朴酚的转移率超出了其均值的70%~130%,考虑到由于厚朴酚与和厚朴酚为木脂素类成分,难溶于水,而ZXGD基准样品的制备工艺是加水煎煮,因此在基准样品中该类成分含量较小,取其均值的70%~130%,存在的误差相对较大,且厚朴各批次间含量差异也较大[20]。因此,在制备ZXGD基准样品时,要严格把控所用原料饮片的质量,确定饮片中各成分的标准范围,保证饮片质量的均一和稳定。
表2 20批ZXGD基准样品含量测定
Table 2 Content determination of 20 batches of ZXGD reference samples
编号质量分数/%编号质量分数/% 辛弗林橙皮苷肉桂酸桂皮醛厚朴酚与和厚朴酚总量辛弗林橙皮苷肉桂酸桂皮醛厚朴酚与和厚朴酚总量 ZXGD10.800.650.0300.140.005 2ZXGD130.610.620.0340.150.005 0 ZXGD20.580.760.0330.130.004 2ZXGD140.860.890.0390.140.010 4 ZXGD30.680.920.0370.170.003 8ZXGD150.700.820.0290.130.010 4 ZXGD40.730.880.0350.140.011 2ZXGD160.710.850.0390.100.013 0 ZXGD50.680.930.0380.130.012 8ZXGD170.530.840.0420.120.007 8 ZXGD60.530.820.0300.120.005 4ZXGD180.590.990.0340.100.016 1 ZXGD70.691.000.0430.160.005 1ZXGD190.550.780.0400.100.009 8 ZXGD80.690.850.0400.140.003 3ZXGD200.650.770.0360.120.009 0 ZXGD90.540.820.0360.120.006 2均值0.650.820.0360.130.008 0 ZXGD100.350.660.0330.140.004 7均值70%~0.46~0.58~0.025~0.09~0.005 6~ ZXGD110.870.870.0380.120.008 5130%0.851.070.0470.170.010 3 ZXGD120.700.770.0390.120.007 2
表3 ZXGD基准样品指标成分含量测定及转移率
Table 3 Content and transfer rate of indicator components in ZXGD
编号辛弗林/%橙皮苷/%肉桂酸/%桂皮醛/%厚朴酚与和厚朴酚/% 饮片基准样品转移率饮片基准样品转移率饮片基准样品转移率饮片基准样品转移率饮片基准样品转移率 ZXGD10.700.80114.292.010.6532.340.0310.03096.772.430.145.764.070.005 20.13 ZXGD20.720.5880.561.940.7639.180.0280.033117.862.380.135.463.080.004 20.14 ZXGD30.720.6894.441.940.9247.420.0290.037127.592.210.177.692.080.003 80.18 ZXGD40.700.73104.292.010.8843.780.0310.035112.902.430.145.763.170.011 20.35 ZXGD50.540.68125.931.860.9350.000.0420.03890.482.610.134.984.010.012 80.32 ZXGD60.550.5396.361.730.8247.400.0290.030103.452.410.124.983.080.005 40.18 ZXGD70.620.69111.291.981.0050.510.0300.043143.332.510.166.373.080.005 10.17 ZXGD80.540.69127.782.050.8541.460.0380.040105.262.300.146.093.130.003 30.11 ZXGD90.550.5498.181.770.8246.330.0390.03692.312.470.124.862.080.006 20.30 ZXGD100.720.3548.611.940.6634.020.0420.03378.572.610.145.364.070.004 70.12 ZXGD110.620.87140.321.980.8743.940.0330.038115.152.260.125.314.010.008 50.21 ZXGD120.540.70129.632.050.7737.560.0310.039125.812.430.124.943.010.007 20.24 ZXGD130.700.6187.142.010.6230.850.0290.034117.242.410.156.222.080.005 00.24 ZXGD140.540.86159.261.860.8947.850.0420.03992.862.610.145.365.600.010 40.19 ZXGD150.560.70125.001.860.8244.090.0480.02960.422.330.135.583.740.010 40.28 ZXGD160.700.71101.432.010.8542.290.0360.039108.332.320.104.313.740.013 00.35 ZXGD170.700.5375.712.010.8441.790.0360.042116.672.320.125.173.740.007 80.21 ZXGD180.700.5984.292.010.9949.250.0360.03494.442.320.104.313.740.016 10.43 ZXGD190.700.5578.572.010.7838.810.0360.040111.112.320.104.313.740.009 80.26 ZXGD200.700.6592.862.010.7738.310.0360.036100.002.320.125.173.740.009 00.24 平均值0.640.65103.801.950.8242.360.0350.036105.532.400.135.403.450.008 00.23
3 讨论
ZXGD由枳实、厚朴、薤白、桂枝、瓜蒌5味药组成,主要用于治疗胸痹等症。为促进ZXGD中药复方制剂的开发利用,本实验从ZXGD基准样品特征图谱及多成分含量测定2个方面的关键质量属性,全面分析了ZXGD物质基准的量值传递规律。
本研究在对特征图谱及多成分含量测定方法建立过程中,分别考察了甲醇-水、乙腈-水、乙腈-磷酸水溶液等不同体系、不同比例的流动相系统,结果表明乙腈-0.05%磷酸水溶液为流动相,基线平稳、色谱峰分离良好;分别考察不同波长,全波长扫描结果表明在290 nm时各成分色谱行为良好,在214 nm时辛弗林色谱峰响应较好,杂质干扰小;分别考察不同柱温,结果表明,30 ℃时辛弗林、肉桂酸色谱峰分离较好。因此,明确流动相为乙腈-0.05%磷酸水溶液,特征图谱波长为290 nm,含量测定波长为290 nm(橙皮苷、肉桂酸、桂皮醛、厚朴酚与和厚朴酚)、214 nm(辛弗林),柱温为30 ℃。
特征图谱及多成分含量测定色谱峰均来自于枳实、厚朴、桂枝3味药,薤白和瓜蒌的药味信息未能很好的体现,可能是由于在本研究中的实验条件下,薤白和瓜蒌的成分含量较低达不到定量限或洗脱程序不适合等因素导致。因此目前对薤白和瓜蒌2味药的定量分析还存在困难,后期将采用适宜的方法如LC-MS、GC-MS等对该2味药进一步分析,以较多地体现药味信息[21-22],对ZXGD进行全方位的质量控制研究。
在对20批ZXGD基准样品的含量测定和转移率分析时,发现辛弗林、橙皮苷、肉桂酸和桂皮醛基本都在其均值的70%~130%,但是厚朴酚与和厚朴酚的含量却出现了离散数据。在对厚朴饮片进行研究时发现,同一批厚朴药材含量有高有低,因此,炮制出的同一批饮片含量也存在差异,而在制备ZXGD基准样品时,每一批基准样品仅投料厚朴饮片12 g,投料量较小,也有可能会导致厚朴饮片取样不均,从而使得厚朴酚与和厚朴酚的含量出现离散数据。其次,厚朴酚与和厚朴酚为木脂素类成分,难溶于水,在基准样品中含量较低,计算其均值的70%~130%就会出现相对更大的误差[23],因此是否可考虑对含量高低不同的成分进行具体分析,而不是都把范围限定在其均值的70%~130%,以减少误差。在后期实验中可进一步严格把控厚朴饮片质量,并增加基准样品批次的制备,从而降低离散数据的影响。
对于ZXGD基准样品的研究是其中药复方制剂研究中的关键,同时也是经典名方中药复方制剂“遵古”的体现,而物质基准是包含了基准样品中饮片质量、制备工艺稳定性等信息的标准[24]。本研究通过对ZXGD物质基准的量值传递规律进行分析,明晰了饮片-物质基准的传递规律,能更好地指导原料饮片的质量控制,为确保ZXGD基准样品的质量稳定提供有效手段,同时也为后续ZXGD复方制剂的研究,实现全过程的质量控制奠定有力基础。
利益冲突 所有作者均声明不存在利益冲突
[1] 东汉·张仲景.金匮要略 [M].何任, 何若苹整理.北京: 人民卫生出版社, 2005: 31-32.
[2] 李楠楠, 石月萍.加减枳实薤白桂枝汤通过AC/cAMP通路对缺血再灌注大鼠心肌组织水通道蛋白表达的影响 [J].中国动脉硬化杂志, 2018, 26(3): 237-244.
[3] 姜晓旭.枳实薤白桂枝汤对ET-1诱发家兔冠脉痉挛干预及机制研究 [D].哈尔滨: 黑龙江中医药大学, 2017.
[4] 马旬旬.黄连枳实薤白桂枝汤对痰阻心脉证冠心病心绞痛患者Hey、SOD、hs-CRP的影响[D].南京: 南京中医药大学, 2018.
[5] 刘宇, 邵金博, 郭立中.枳实薤白桂枝汤治疗冠心病合并高脂血症的疗效及对内皮功能和脂代谢的影响 [J].中药材, 2018, 41(2): 476-478.
[6] Tang Y, Cai H R, Zhan Z Y,.Herbal medicine (Zhishi Xiebai Guizhi Decoction) for unstable angina: Protocol for a systematic review and meta-analysis [J]., 2018, 97(52): e13965.
[7] 张长喜.枳实薤白桂枝汤治疗功能性消化不良50例 [J].中国中医药现代远程教育, 2015, 13(20): 45-46.
[8] 杨艳玲, 刘彩凤, 黄嘉怡, 等.经典名方桃红四物汤的物质基准量值传递分析 [J].中国中药杂志, 2021, 46(4): 801-809.
[9] 彭梅梅, 郭爽, 陈琪, 等.基于特征图谱和网络药理学的经典名方黄连汤质量标志物(Q-Marker)预测分析 [J].中草药, 2021, 52(18): 5514-5523.
[10] 齐琪, 赵(王月)瑛, 张晴, 等.经典名方小承气汤的物质基准量值传递研究 [J].中草药, 2021, 52(10): 2927-2937.
[11] 袁海建, 李卫, 祝一飞, 等.枳实薤白桂枝汤HPLC指纹图谱及10种指标成分含量测定研究 [J].中草药, 2020, 51(9): 2448-2459.
[12] 闫红, 余洪, 潘小丹, 等.枳实薤白桂枝汤合理中汤加减辅助治疗稳定型心绞痛及对炎症因子和血管内皮功能的影响 [J].中国实验方剂学杂志, 2020, 26(17): 83-88.
[13] 李楠楠, 石月萍.加减枳实薤白桂枝汤通过AC/cAMP通路对缺血再灌注大鼠心肌组织水通道蛋白表达的影响 [J].中国动脉硬化杂志, 2018, 26(3): 237-244.
[14] 何学春.四妙勇安汤合枳实薤白桂枝汤治疗冠心病临床疗效分析 [J].亚太传统医药, 2014, 10(14): 108-109.
[15] 国家药品监督管理局.公开征求古代经典名方中药复方制剂及其物质基准申报资料要求意见[EB/OL].[2019-03-27].https://www.nmpa.gov.cn/xxgk/zhqyj/ zhqyjyp/20190327150 101694.html.
[16] 刘冬涵, 薛宇涛, 罗菊元, 等.经典名方苓桂术甘汤的物质基准量值传递分析 [J].中国中药杂志, 2019, 44(24): 5421-5428.
[17] 成颜芬, 杜克群, 吴亿晗, 等.基于化学特征与核心功效分析经典名方桃红四物汤复方合煎与单煎差异研究 [J].中草药, 2021, 52(19): 5879-5890.
[18] Sang Q N, Jia Q Q, Zhang H Y,.Chemical profiling and quality evaluation of Zhishi-Xiebai-Guizhi Decoction by UPLC-Q-TOF-MS and UPLC fingerprint [J]., 2021, 194: 113771.
[19] 国家中医药管理局.关于发布《古代经典名方目录(第一批)》的通知[EB/OL].[2018-04-16].http://kjs.satcm.gov.cn/zhengcewenjian/2018-04-16/7107.html.
[20] 荆文光, 张权, 杜杰, 等.不同产地厚朴药材中3种木脂素类成分含量测定及聚类分析 [J].世界科学技术—中医药现代化, 2018, 20(10): 1822-1827.
[21] 王宇卿, 黄涵.UPLC-Q-TOF/MS法分析瓜蒌薤白半夏汤中主要化学成分 [J].中国医院药学杂志, 2018, 38(19): 2017-2021.
[22] 李欣, 唐力英, 许静, 等.基于UPLC-LTQ-Orbitrap高分辨质谱的中药瓜蒌化学成分分析 [J].中国实验方剂学杂志, 2019, 25(1): 201-210.
[23] 范琪.厚朴抗氧化活性成分的提取分离及其抗氧化活性测试研究 [D].重庆: 重庆大学, 2014.
[24] 国家药品监督管理局.关于发布《中药配方颗粒质量控制与标准制定技术要求》的通告(2021年第16号)[EB/OL].[2021-01-26].https:www.nmpa.gov.cn/xxgk/ ggtg/qtggtg/20 210210145453181.html.
Research on quantitative transmitting of classical prescription Zhishi Xiebai Guizhi Decoction substance benchmarks
XU Rui-jie, XUE Rong, MEI Xi,GONG Jing-wen, ZHANG Qian, LOU Yue, ZHAO Xiao-li, XU Jin-guo, YAN Guo-jun, LU Tu-lin, MAO Chun-qin
School of Pharmacy, Nanjing University of Chinese Medicine, Nanjing 210023, China
To establish the HPLC characteristic map of the reference samples of the classical prescription Zhishi Xiebai Guizhi Decoction (ZXGD, 枳实薤白桂枝汤) and to determine the content of its multi-components, to study the transfer rule of the substance benchmark value of ZXGD, for the follow-up study of Chinese medicine compound preparations lay the foundation.Twenty batches of ZXGD reference samples were prepared, and their characteristic map was established, its characteristic peaks was clarified and assigned to the characteristic peaks; Multi-component content determination on the reference samples of ZXGD was carried out, and the transfer law of main components were analyzed from the decoction pieces to the substance benchmark.The similarities of the characteristic maps of the 20 batches of ZXGD reference samples were all greater than 0.93, and a total of 11 characteristic peaks were matched, which were from Zhishi (, peaks 1, 3—5, 9), Houpo (, peaks 2, 10, 11), Guizhi (, peaks 6—8); The content range of each index component and the average transfer rate of decoction pieces-reference samples were 0.46%—0.85% and 103.80% for synephrine, respectively, hesperidin 0.58%—1.07% and 42.36%, cinnamic acid 0.025%—0.047% and 105.53%, cinnamaldehyde 0.09%—0.17% and 5.40%, magnolol and honokiol 0.005 6%—0.010 3% and 0.23%.The HPLC characteristic map and multi-component content determination are used to study the quantity value transfer law of ZXGD.The whole process quality control of the development and research of classical prescription ZXGD.
classic prescriptions; Zhishi Xiebai Guizhi Decoction; reference samples; substance benchmark; characteristic chromatogram; quantitative transmitting;;;; synephrine; hesperidin;cinnamon acid;cinnamaldehyde; magnolol; honokiol
R283.6
A
0253 - 2670(2022)09 - 2650 - 09
10.7501/j.issn.0253-2670.2022.09.007
2021-11-22
2018国家重点研发计划项目(2018YFC1707000)
徐瑞杰,硕士研究生,主要从事中药炮制及中药饮片质量标准研究。E-mail: xuruijier@126.com
通信作者:毛春芹,正高级实验师,主要从事新药研发及中药质量研究。E-mail:300555@njucm.edu.cn
陆兔林,教授,博士生导师,主要从事中药炮制及中药饮片质量标准研究。E-mail: ltl2021@njucm.edu.cn
[责任编辑 郑礼胜]
