基于2019-nCoV 3CL Mpro筛选祛肺毒一号方的活性成分及其治疗COVID-19的分子机制*
2022-04-28孙洁蒋士卿
孙洁,蒋士卿
1.焦作市妇幼保健院,河南 焦作 454000; 2.河南中医药大学,河南 郑州 450046
新型冠状病毒肺炎(corona virus disease 2019,COVID-19),简称“新冠肺炎”,是由一种新型冠状病毒导致的严重传染性疾病,目前正在全球范围内暴发。从临床情况来看,该疾病具有传播速度快、传染性强、无特定易感人群等特点,且无特效药物可用。在临床治疗过程中,西医主要以对症支持治疗为主,针对高热、咳嗽、肺部CT异常、氧饱和率低、甚至呼吸困难等症状,做出维持水、电解质与酸碱平衡,氧疗与呼吸支持,抗病毒,抗细菌的治疗等。中医认为新冠肺炎是疫毒闭肺证,病因主要是感受疫疠之气和正气亏虚两方面,表现为高热、或身热不退或往来寒热,咳嗽痰少、或有黄痰,烦躁,胸憋闷,气促,舌质红或紫暗,舌苔黄燥,脉滑数。中医药在治疗COVID-19时具有一定优势,尤其是在救治危重型患者方面,大大提高了患者的好转率、治愈率,改善了重型、危重型患者预后较差的状况。祛肺毒一号方(生晒参30 g,荆芥15 g,金银花 15 g,玄参15 g,连翘30 g,皂角刺 10 g,杏仁 10 g,露蜂房10 g,甘草6 g)具有补气养阴、清热解毒、止咳祛痰平喘的功效,在定点医院收治的重型/危重型新冠肺炎患者中取得了良好的临床治疗效果[1],但由于该方的活性物质基础和作用机制尚未明确,使其在抗新冠病毒使用和推广等方面都受到了一定的限制。
分子对接技术利用计算机模拟药物分子与蛋白质相互作用的结合过程,预测药物分子和靶点的结合方式和亲和力,可用于药物的分子机制研究[2]。新冠肺炎病毒是一种正链病毒,RNA直接附着于宿主细胞核糖体上,翻译出大分子蛋白,并迅速被蛋白水解酶降解[3]。2019-nCoV 冠状病毒3CL水解酶(2019-nCoV 3CL Mpro)常被认为是理想的抗SARS-CoV药物筛选靶标[4]。因此,本研究以 2019-nCoV 3CL Mpro作为抗新冠肺炎病毒的靶蛋白进行祛肺毒一号方成分的筛选,并利用网络药理学从分子水平探究了祛肺毒一号方治疗新冠肺炎的物质基础和作用机制,旨在为中医药治疗新冠肺炎的研究和祛病毒一号方的临床应用提供理论依据。
1 资料与方法
1.1 小分子数据库的建立祛肺毒一号方由生晒参、荆芥、金银花、玄参、连翘、皂角刺、杏仁、露蜂房、甘草9味中药组成。采用中药系统药理学数据库与分析平台(traditional chinese medicine systems pharmacology database and analysis platform,TCMSP)检索祛肺毒一号方组方中药的化学成分。露蜂房的化学成分未在TCMSP数据库中检索到,故通过查阅文献[5-7]进行搜集。以类药性(drug likeness,DL)≥0.18及口服生物利用度(oral bioavailability,OB)≥30%为标准进行筛选,将所得的化学成分建立小分子数据库。
1.2 分子对接及验证采用Chem 3D软件构建小分子数据库中化学成分的三维分子结构,并利用MM2分子力学方法优化。从结构生物信息学研究合作实验室蛋白质数据库(research collaboratory for structural bioinformatics protein data bank,RCSB PDB,http://www.rcsb.org)中下载2019-nCoV 3CL Mpro的三维结构,利用Autodocktools 1.5.6工具删除晶体中的结晶水,并为蛋白添加氢原子和gasteiger电荷。采用AutoDock 4.2程序进行分子对接[8],评价祛肺毒一号方中的化学成分与2019-nCoV 3CL Mpro的结合活性。对接的活性位点参数如下:盒子坐标为(-9.732,11.403,68.639),盒子三维的格点数为(40,55,40),采用拉马克遗传算法,其他参数采用默认设置。为了验证autodock程序对本研究体系对接的可靠性,将靶蛋白复合物6LU7的原有配体抽离,再重新对接到靶蛋白的活性口袋,并计算对接后配体的构象与原始晶体结构中配体构象的均方根偏差值(root-mean-square deviation,RMSD)。一般认为当RMSD值≤2.0Å时,该对接方法可以较好地重现配体受体原来的结合模式,表明对接参数设置合理[9]。
1.3 “活性成分-疾病”交集靶点筛选以 -9 kcal·mol-1为筛选标准对对接的化合物进行筛选,并将筛选出的化合物导入SwissTargetPrediction(http://www.swisstargetprediction.ch/)数据库[10]预测化合物的作用靶点。以“novel coronavirus”为关键词,在人类基因数据库(the human gene database,GeneCards,https://www.genecards.org/)[11]、美国国立生物技术信息中心(national center for biotechnology information,NCBI,https://www.ncbi.nlm.nih.gov/)数据库[12]以及CTD(http://ctdbase.org/)数据库[13]进行疾病相关靶点检索。其中CTD的数据以“inference score”进行中位值筛选以获得相关性更强的靶点。将筛选出的药物靶点与疾病靶点输入韦恩图制作软件venny 2.1,交集靶点即为药物作用于疾病的靶点。
1.4 蛋白质-蛋白质相互作用(protein - protein interaction,PPI)网络构建蛋白质-蛋白质相互作用是认识生命活动基本规律、探索疾病发生发展和防治的重要途径。将活性成分作用于疾病的靶点导入STRING 11.0(https://string-db.org/)数据库[14],将生物种类设定为“Homo sapiens”,设置可信度>0.9,最终获得蛋白质相互作用网络图。采用拓扑分析和聚类分析筛选得到关键靶点及核心基因。
1.5 富集分析将药物作用于疾病的靶点基因导入DAVID(https://david.ncifcrf.gov/)数据库,进行基因本体(gene ontology,GO)功能富集分析和京都基因与基因组百科全书(kyoto encyclopedia of genes and genomes,KEGG)信号通路富集分析,将富集结果导入Omi share Tools(http://www.omicshare.com/tools/index.php/)绘制对应的柱形图及高级气泡图。
1.6 “中药活性成分—疾病—通路—靶点”网络构建将祛肺毒一号方治疗COVID-19的靶点与活性成分进行映射关联,得到“活性成分-靶点”关联表,与PPI网络共同导入Cytoscape3.7.2软件,构建“中药活性成分-疾病-通路-靶点”网络。
2 结果
2.1 祛肺毒一号方化学成分的筛选通过检索 TCMSP 数据库与文献查找筛选出祛肺毒一号方的化学成分,其中人参22个、荆芥11个、金银花23个、玄参9个、连翘23 个、皂角刺11个、杏仁19个、露蜂房53个、甘草92个,删除重复及未报道结构的成分,最终得到220个化合物。
2.2 分子对接方法可靠性验证靶蛋白(PDB ID:6LU7)是2019-nCoV 3CL Mpro和化合物N3的复合物[15],两者的结合能ΔGbinding=-9.40 kcal·mol-1。将靶蛋白原始晶体结构中配体构象与对接后配体的构象叠合可以明显看出,对接后的配体构象与原始晶体结构中的配体构象基本重合,且N3对接前后的RMSD值均为0.82Å,表明本对接方法及对接参数设置合理,可信度高。见图1。
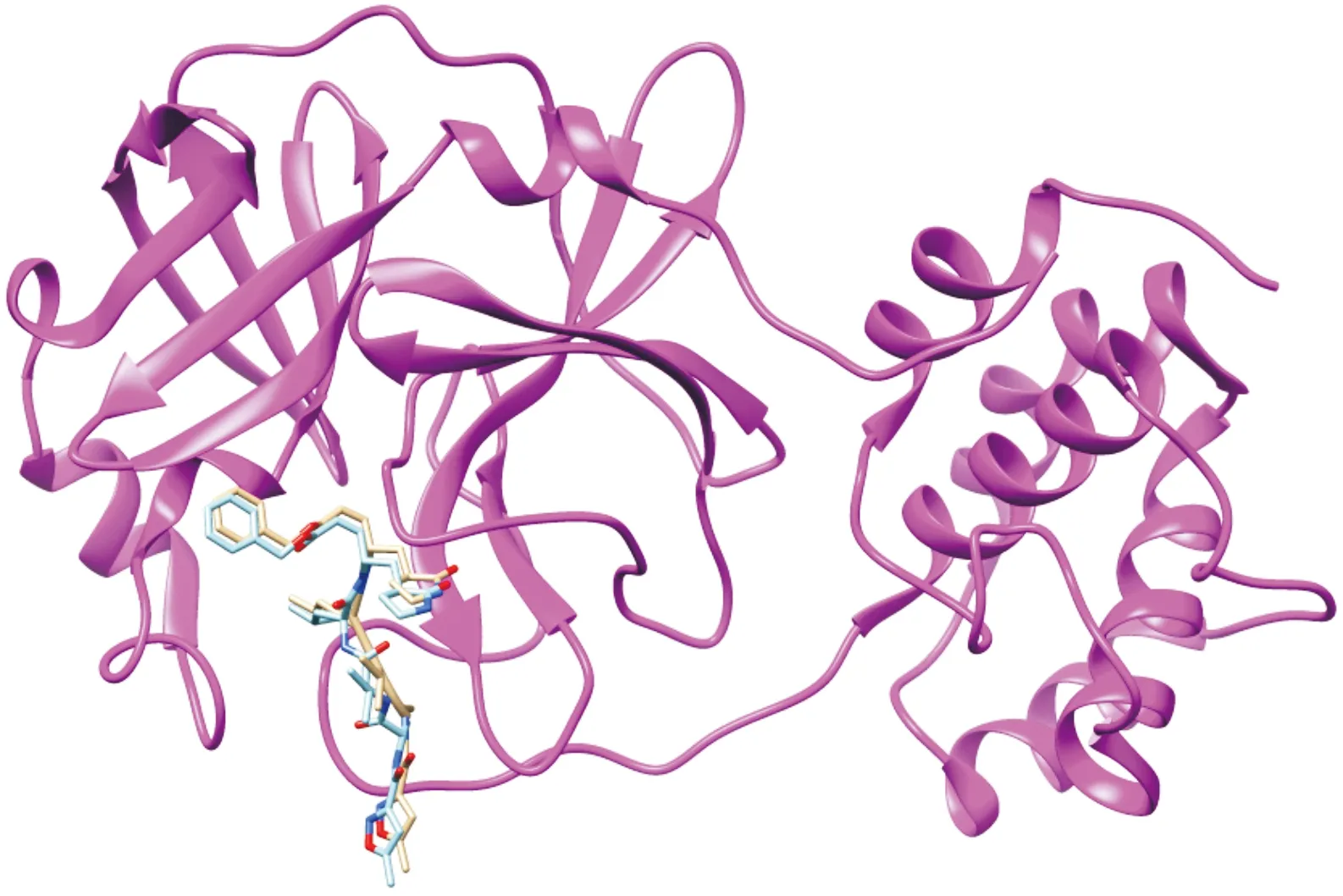
注:图中玫红色为靶点蛋白(飘带模型);金色为原始配体;蓝色为对接后的配体
2.3 祛肺毒一号方活性成分筛选当ΔGbinding<0时,表明配体分子与受体分子可以自发结合,ΔGbinding越低,则配体和受体的结合越稳定。按照ΔGbinding≤-6 kcal·mol-1、-7 kcal·mol-1、-8 kcal·mol-1、-9 kcal·mol-1的标准分析对接结果发现,祛肺毒一号方的220种化学成分的占比分别为84.6%、73.35%、48.8%、15.1%,其中人参、连翘及露蜂房中具有较低结合能的化学成分占比较高。以ΔGbinding≤-9 kcal·mol-1为标准筛选得到33个活性成分,且与2019-nCoV 3CL Mpro结合能较低的前5位成分分别是化合物109:(2S)-2-[4-hydroxy-3-(3-methylbut-2-enyl)phenyl]-8,8-dimethyl-2,3-dihydropyrano[2,3-f]chromen-4-one;化合物78:xambioona;化合物26:菠菜甾醇;化合物141:3,22-dihydroxy-11-oxo-delta(12)-oleanene-27-alpha-methoxycarbonyl-29-oic acid;化合物110:euchrenone。这些化合物与靶蛋白的关键氨基酸残基不但能够形成氢键,还能形成疏水等作用,占据靶蛋白的活性位点,使靶蛋白2019-nCoV 3CL Mpro失活。见表1,图2。

表1 祛肺毒一号方中筛选出的33个活性成分

注:表示疏水相互作用;----表示氢键作用;A:化合物109;B:化合物26;C:化合物141;D:化合物178;E:化合物110
2.4 多配体—单靶点对接中药成分复杂,在治疗疾病的过程中,往往可以通过多途径、多靶点协同发挥作用[16]。中药多成分多靶点协同作用网络中存在多成分单靶点叠加作用,可实现中药的科学配伍,提高疗效[17]。为了验证祛肺毒一号方中是否存在多成分同时作用,选择结合能最低的3个化合物依次对接到靶蛋白2019-nCoV 3CL Mpro的活性口袋,结果发现3个化合物不仅可以与靶蛋白直接建立相互作用,且3个化合物之间存在π-σ和π-π相互作用,使3个化合物形成稳定的体系,共同作用于靶蛋白,即化合物109先进入靶蛋白的活性口袋,与氨基酸His41、Cys145、His163、His172、Met165、Leu167、Met165、Pro168形成相互作用,之后化合物178进入活性口袋内部,不仅与氨基酸残基Ser46之间形成了氢键,且与化合物109之间形成了π-π等相互作用;化合物26进入活性口袋后,基本占据了活性口袋出口。3个化合物协同作用,靶蛋白活性口袋的关键氨基酸位点被完全占据,有效抑制了靶蛋白的活性。见图3,表2。

注:(a)3个活性成分与靶蛋白2019-nCoV 3CL Mpro的结合图;(b)、(c)、(d)分别为化合物109、178、26与靶蛋白2019-nCoV 3CL Mpro的相互作用模式图

表2 3个活性成分与靶蛋白2019-nCoV 3CL Mpro结合的ΔGbinding结果
2.5 祛肺毒一号方治疗COVID-19的作用靶点将祛肺毒一号方的33个活性成分导入SwissTargetPrediction数据库,筛选得到活性成分的作用靶点728个。采用GeneCards、NCBI、CTD三个数据库检索并搜集COVID-19疾病相关靶点分别791个、136个、3 593个,合并删重后得到COVID-19疾病相关靶点 4 165 个。将33个祛肺毒一号方活性成分的728个靶点与4 165个COVID-19疾病相关靶点进行映射,最终得到祛肺毒一号方治疗COVID-19的有效靶点347个。见图4。

图4 祛肺毒一号方活性成分靶点与COVID-19疾病靶点韦恩图
2.6 蛋白质相互作用网络将祛肺毒一号方治疗COVID-19的347个靶点导入STRING数据库,得到PPI网络,该网络中有347个节点,1 780条边,平均度值为10.3。导入Cystoscape 3.7.2软件绘制PPI网络图,图中节点颜色和大小根据度值调整,面积越大,颜色越深,则度值越大,线条从粗到细表示边介数从大到小。采用NetworkAnalyzer工具进行拓扑分析,以度值(degree)、中介中心性(betweenness centrality)、平均最短路径长度(average shortest path length)和紧密中心性(closeness centrality)4个参数为参考标准,通过degree排序,选取分值大于平均分的基因作为关键靶点,总共筛选出114个关键靶点,使用R 3.6.3软件绘制出前20个靶点。通过MCODE模块[18]进行基因簇的分析及核心靶点的筛选,共得到12个基因簇和11个核心基因,核心基因为CCR1、HCRTR2、MAPK3、BCL2L1、IKBKB、CYP1A2、CDK5、CCNA1、PPARG、PLAU、FLT1。见图5、图6,表3。
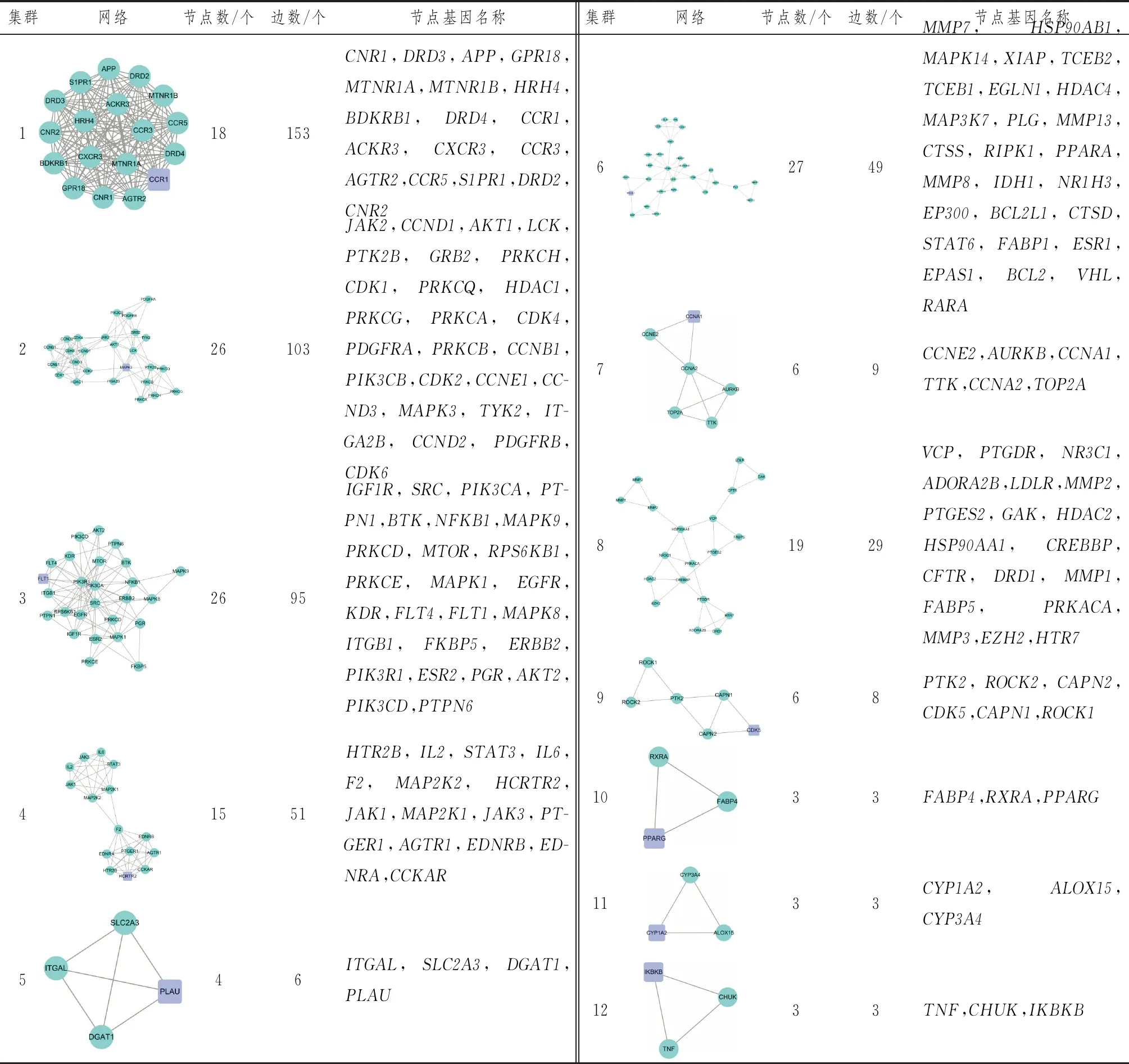
表3 12个基因簇的详细信息表

图5 PPI网络图

注:横坐标为靶点的degree值;纵坐标为靶点
2.7 GO富集分析与KEGG通路富集分析将347个祛肺毒一号方治疗COVID-19的有效靶点导入DAVID数据库进行GO生物功能富集分析和KEGG通路富集分析,以P≤0.05为标准进行筛选,共富集到GO生物功能3 210条,KEGG信号通路179条。3 210条GO生物功能包括2 871条生物过程(biological process,BP)、230条分子功能(molecular function,MF)及109条细胞组分 (cell component,CC),分子功能主要涉及丝氨酸蛋白酶激酶活性、 酪氨酸激酶活性、 磷酸酶活性 、磷酸酶结合核受体等受体的活性;生物过程主要涉及氧化应激反应、细胞对药物的反应、肽基丝氨酸修饰等;细胞组分主要涉及膜筏、膜微畴、膜区等。选取179条信号通路中排名前20的通路进行分析发现,靶点显著富集于磷酯酰肌醇3-激酶(phosphatidylinositol 3-kinase,PI3K)-蛋白激酶B(protein kinase B,Akt)信号通路、人巨细胞病毒感染、乙型肝炎、 缺氧诱导因子-1(hypoxia inducible factor-1,HIF-1)信号通路、糖尿病并发症中的糖基化终末产物(advanced glycation end products,AGE)-AGE受体(receptor for AGE,RAGE)信号通路、T细胞受体信号通路、爱泼斯坦-巴尔病毒感染等通路。见图7、图8。

图7 关键靶点的GO富集分析

图8 关键靶点的 KEGG通路富集
2.8 “中药活性成分-疾病-通路-靶点”网络构建采用Cytoscape3.7.2软件进行通路网络图的绘制,以便更直观地展示中药活性成分在治疗COVID-19过程中多成分、多靶点的作用特点。见图9。

注:蓝色为活性成分;黄色为活性成分作用于疾病的靶点;绿色为最显著的前20条通路;红色为疾病,即COVID-19
3 讨论
新冠肺炎属于中医疫毒闭肺证,是正虚邪实的表现。从中医角度分析,祛肺毒一号方以大补元气的人参与玄参共同作用达到补气养阴的功效,以金银花、连翘、荆芥、皂角刺协同使用使清热解毒能力尤佳,杏仁止咳祛痰平喘,露蜂房攻毒杀虫、祛风,甘草调和诸药。现代药理研究表明,人参中的活性物质具有提高免疫、抗病毒的作用,同时对呼吸道病毒有抑制作用[19];金银花具有抗病毒,治疗感染及各种炎症的药理作用[20-21];连翘具有清除内毒素、抗炎、增强免疫等药理作用[22];荆芥具有抗病毒、解热镇痛、抗炎的功效[23];皂角刺可治疗浸润型肺炎,还具有抗病毒、调节免疫力的作用[24-26];杏仁具有抗肺纤维化、抗高氧诱导肺损伤、免疫调节、抗肿瘤、抗炎的功效[27];露蜂房有抗炎、抗菌抗病毒及防治肺纤维化和解热镇痛的作用[28];甘草具有抗炎及免疫抑制作用,同时具有解毒、抗病毒、镇咳祛痰、抑菌、抑制气道平滑肌细胞增生的作用[29]。
通过分子对接筛选结果表明,在祛肺毒一号方中有220种活性成分符合OB≥30%且DL≥0.18的筛选标准,其中ΔGbinding≤-6 kcal·mol-1的活性成分达到总成分的84.6%;ΔGbinding≤-7 kcal·mol-1的活性成分达到总成分的73.35%;ΔGbinding≤-8 kcal·mol-1的活性成分达到总成分的48.8%;ΔGbinding≤-9 kcal·mol-1的活性成分达到总成分的15.1%,共33个。通过网络药理学分析发现PIK3R1、Akt、丝裂原活化蛋白激酶1(mitogen-activated protein kinase 1,MAPK1)、MAPK3可能是核心靶点。网络拓扑分析显示,祛肺毒一号方治疗 COVID-19的过程中涉及多种生物过程、细胞组分和分子功能,且核心靶点显著富集于PI3K-Akt信号通路、人巨细胞病毒感染、乙型肝炎、HIF-1信号通路、糖尿病并发症中的AGE-RAGE信号通路、T细胞受体信号通路、爱泼斯坦-巴尔病毒感染通路等多个通路。PI3K是肺细胞重要的调节酶之一,影响肺组织的生理和病理变化[30]。研究发现,PI3K不仅可以影响细胞内的酪氨酸激酶、丝/苏氨酸激酶的活性从而调控细胞的生物过程,而且在造成急性肺损伤的过程中起着不可忽视的作用[31],进而导致COVID-19引起急性肺损伤时炎症因子的浸润。MAPK在炎症反应中发挥重要作用,MAPK1、MAPK3两种激酶激活可调节细胞的生长、分化、应激、炎症反应等病理效应[32],从而加剧炎症反应。冠状病毒的入侵激活了人巨细胞病毒感染通路,影响磷酸酶活性和磷酸酶结合核受体活性,进入T细胞受体信号通路,逃脱PD-1/ PD-L1检查点的检查,加速了全身免疫系统的损伤。因此推测新冠病毒可能是通过入侵人体,刺激免疫反应,启动 PI3K-Akt信号通路途径,促进MAPK1、MAPK3等激酶的表达,导致肺部炎性反应,引起急性肺损伤;而祛肺毒一号方可能通过调节 PI3K-Akt等信号通路起到治疗 COVID-19的效果。
通过单配体-单靶点的对接,发现祛肺毒一号方中化合物109、178、26、141、110对2019-nCoV 3CL Mpro有较强的疏水相互作用,可占据蛋白的活性位点,抑制蛋白发挥作用,是祛肺毒一号方发挥疗效的关键成分。通过多配体-单靶点的对接发现,化合物109、178、26与2019-nCoV 3CL Mpro都有很强的结合力,导致2019-nCoV 3CL Mpro失活,提示这3种成分可直接有效的发挥抗病毒作用,且3种成分可在2019- nCoV 3CL Mpro的活性位点协同作用,共同抑制水解酶的活性,发挥抑制病毒的作用。
本研究首先采用分子对接方法筛选出祛肺毒一号方对2019-nCoV 3CL Mpro有明显抑制作用的活性成分,之后利用网络药理学方法进一步研究了祛肺毒一号方治疗COVID-19的作用机制。该研究的预测结果与相关文献[19-32]结果一致,说明本研究方法可靠,结果可信,为后续研究提供了一定的参考。
