内皮抑素、凝血酶敏感蛋白-1表达与慢性荨麻疹患者并发血管性水肿相关性及临床意义
2022-04-26周美联
周美联,卢 彬
慢性荨麻疹指风团每天发作或间歇发作>6周,病因复杂,以皮肤、黏膜小血管扩张及渗透性增加等为主要病理表现,可并发血管性水肿,增加呼吸困难、窒息等发生概率,因此早期评估患者并发血管性水肿的风险意义重大[1]。内皮抑素(ES)为内源性血管生成抑制剂,对微血管内皮细胞迁移具有特异性抑制作用,并能抑制皮肤、黏膜血管扩张与毛细血管渗透性增加[2]。凝血酶敏感蛋白-1(TSP-1)能诱导血管内皮细胞凋亡,被视为血管生成抑制因子,可降低血管通透性[3]。因此推测ES、TSP-1与慢性荨麻疹患者并发血管性水肿有关,但现阶段关于这方面的研究较少。本研究探讨ES、TSP-1表达与慢性荨麻疹患者并发血管性水肿相关性及临床意义,以期为临床早期评估血管性水肿、病情严重程度等提供参考。现报告如下。
1 资料与方法
1.1一般资料 选取2020年8月—2021年8月我院收治的慢性荨麻疹118例。纳入标准:符合慢性荨麻疹诊断标准[1];入组前2周无相关治疗史;自愿加入。排除标准:湿疹、特应性皮炎者;伴有严重内科系统疾病者;感染、昆虫叮咬等其他原因引起的血管性水肿者;癌症患者;合并急性疾病,生命体征不平稳者;遗传性血管性水肿者。并发血管性水肿诊断标准[1]:慢性荨麻疹患者;突然发作、真皮深层与皮下组织水肿;常累及黏膜组织。根据是否并发血管性水肿分为发生组54例和未发生组64例。2组年龄、性别、合并疾病等一般资料比较差异无统计学意义(P>0.05),具有可比性。本研究获医院伦理委员会审核通过,患者及家属充分知情,自愿签署知情同意书。
1.2方法
1.2.1ES、TSP-1检测:入院时采集患者肘静脉血5 ml,12 000×g离心10 min,分离血清,采用酶联免疫吸附试验检测ES、TSP-1水平,分别设标准孔、空白孔、待测样品孔,加入待测样品或标准品后,每孔中加入100 μl生物素化抗体工作液和酶结合物工作液,并加90 μl显色剂,加50 μl终止液,即刻用酶标仪测量各孔450 nm光密度。
1.2.2活动度评估:采用7日荨麻疹活动度评分(UAS7)[4]评估慢性荨麻疹的活动度,包括风团数目、瘙痒程度,每日分值范围0~6分,7 d连续最高分为42分,分值越高,病情越严重;采用血管性水肿活动度评分(AAS)[5]评估血管性水肿情况,包括身体不适、对外观影响、持续时间、对日常活动影响、总体严重程度,每个因素评分0~3分,每日分值范围0~15分,每周最高分为105分,分值越高,血管性水肿越严重。
1.3观察指标 比较2组ES、TSP-1、UAS7评分、AAS评分。分析ES、TSP-1间及与UAS7评分、AAS评分关系。分析并发血管性水肿的相关影响因素。分析ES、TSP-1及联合预测并发血管性水肿的价值。

2 结果
2.1ES、TSP-1及UAS7、AAS评分 发生组ES、TSP-1水平低于未发生组,UAS7、AAS评分高于未发生组(P<0.01)。见表1。
表1 2组慢性荨麻疹ES、TSP-1及UAS7、AAS评分比较
2.2ES、TSP-1间关系 Pearson相关分析显示,ES与TSP-1呈正相关(r=0.560,P<0.001)。
2.3ES、TSP-1与UAS7评分、AAS评分关系 Pearson相关分析显示,ES与UAS7评分、AAS评分呈负相关(r=-0.643、-0.560,P<0.001),TSP-1与UAS7评分、AAS评分呈负相关(r=-0.577、-0.500,P<0.001)。
2.4慢性荨麻疹发生血管性水肿的多因素Logistic回归分析 由于ES、TSP-1与UAS7评分、AAS评分具有相关性,且多重共线性分析发现,方差膨胀因子=6,存在多重共线性问题,故手动移除UAS7评分、AAS评分;以是否并发血管性水肿为因变量,赋值:否=0,是=1,应用多因素Logistic回归分析显示,ES、TSP-1均与血管性水肿的发生显著相关(P<0.01)。见表2。
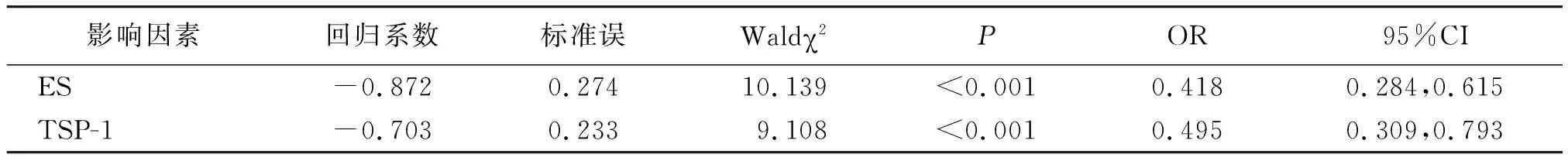
表2 影响慢性荨麻疹发生血管性水肿的多因素Logistic回归分析
2.5ES、TSP-1预测慢性荨麻疹并发血管性水肿的ROC曲线 以发生组各指标作为阳性样本数据,以未发生组各指标作为阴性样本数据,绘制ROC曲线显示,ES联合TSP-1预测并发血管性水肿的AUC大于单一ES、TSP-1检测(P<0.01),见表3。

表3 ES、TSP-1对慢性荨麻疹并发血管性水肿的预测效能
3 讨论
血管性水肿作为慢性荨麻疹一种并发症,发生率高达50%,不仅会加重病情,增加临床治疗难度,且当伴有喉头水肿时,可导致胸闷、呼吸困难,甚至窒息,因此研究血管性水肿发生的相关机制,早期预测其发生风险是必要的[6]。
研究发现,慢性荨麻疹患者血清中血管内皮生长因子浓度升高,并通过作用于血管内皮细胞迁移、增殖、促血管生成等作用,引起皮肤血管通透性增加,导致风团与血管水肿[7]。ES作为血管活性介质,可直接作用于血管内皮细胞,诱导其凋亡,并能抑制细胞外基质降解,减少血管内皮生长因子合成分泌[8-9]。本研究结果显示,与未并发血管性水肿患者比较,并发血管性水肿患者ES水平明显降低,是血管性水肿发生的相关独立影响因素,提示ES可作为预测慢性荨麻疹患者并发血管性水肿的标志物。张学玲等[10]报道,治疗后病情明显改善者外周血ES高于无明显改善者,佐证了ES在慢性荨麻疹病情进展中所起的作用。分析其原因,高水平ES能有效抑制血管内皮生长因子的血管活性作用及其介导的血管通透性增加、血管扩张、皮肤黏膜水肿等,所以可评估血管性水肿的发生与患者病情。本研究结果显示,ES与UAS7评分、AAS评分呈负相关,即ES越低,慢性荨麻疹与血管性水肿活动度越高,故推测采用相关药物靶向ES,增加其表达,可能成为防治慢性荨麻疹及血管性水肿的一个新靶点。
TSP-1除抑制血管新生和细胞基质降解外,还能破坏血管内皮细胞间的连接,阻碍其介导的风团与血管扩张效应[11-12]。孙田等[13]报道,慢性荨麻疹患者治疗后TSP-1高于治疗前,并与风团、瘙痒症状体征的缓解有关,提示TSP-1在慢性荨麻疹病情进展中起到重要作用。本研究结果显示,发生组TSP-1低于未发生组,与血管性水肿的发生显著相关,其原因与TSP-1对血管内皮间连接、血管内皮生长因子的抑制作用有关。TSP-1与UAS7评分、AAS评分呈负相关,可反映慢性荨麻疹患者病情与血管性水肿的活动度。同时本研究还发现,ES与TSP-1呈正相关,表明ES、TSP-1能相互影响,共同参与慢性荨麻疹的发病与病情进展,但遗憾的是,关于二者相互影响的详细机制尚不明确,仍需后续报道的论证。
ROC曲线分析显示,ES预测并发血管性水肿的AUC为0.783,TSP-1预测并发血管性水肿的AUC为0.762,单独应用时,因AUC均小于0.8,预测价值有限,而ES联合TSP-1预测并发血管性水肿的AUC为0.856,较单独ES、TSP-1明显升高,因此建议临床联合检测ES、TSP-1对患者并发血管性水肿的风险进行预测,其预测敏感度达90.74%,特异度为68.75%,呈现出较高的应用价值,能为临床干预提供参考依据。
综上,ES、TSP-1表达与慢性荨麻疹患者并发血管性水肿有关,并与患者病情活动度有关,联合检测可作为预测并发血管性水肿的有效方案。
