荧光光谱法探究几种金属离子与牛血清白蛋白的相互作用
2022-04-25彭婷婷
彭婷婷
(白城师范学院 化学学院,吉林 白城137000)
0 引言
金属离子在生命进程中起着重要的作用,它可以参与基因表达和酶催化反应,亦可参与人体的生长发育、新陈代谢等重要的生理活动.其在生命体内维持一定的浓度,对生理活动起着不可或缺的作用.血清蛋白是血浆里最丰富的蛋白质,担负着携带、运输各种小分子物质的功能[1].牛血清白蛋白(BSA)与人血清白蛋白具有高度的同源性,且BSA 价格较低,常用作为研究模型[2].本文在模拟人体生理环境下,利用荧光光谱法初步明确了Ni2+,Mg2+,Ca2+和Cu2+与牛血清白蛋白的相互作用机制,能为评价这四种金属离子在生物体内的吸收、代谢提供一定的参考.
1 实验部分
1.1 仪器与试剂
LS-55 型荧光光谱仪(购自美国珀金埃尔默公司);BSA(购自北京鼎国昌盛生物技术公司)用三次蒸馏水溶解配制成5.68×10-5mol·L-1的储备液,于冰箱中4 ℃保存备用;pH=7.40 的Tris 缓冲溶液;其他试剂均为分析纯,实验使用二次蒸馏水.
1.2 实验方法
在pH 为7.40的Tris缓冲溶液中加入固定量5.68×10-5mol·L-1的BSA 溶液,改变金属离子的浓度.金属离子-BSA 体系荧光光谱在λem=350 nm,λex=279 nm 处,激发狭缝宽度为10 nm 和发射狭缝宽度为5 nm,波长范围为300~400 nm时,体系在21 ℃和37 ℃下测定荧光发射光谱.
2 结果与讨论
BSA的荧光主要来自色氨酸残基和酪氨酸残基,当其附近微环境发生变化,BSA的内源荧光强度会发生变化.
2.1 BSA与金属离子作用的荧光光谱
BSA 与不同物质的量浓度的Ni2+,Mg2+,Ca2+和Cu2+溶液在温度为294 K 时的荧光光谱如图1所示.由图1 可知,随着溶液中各金属离子浓度的增大,BSA 位于350 nm 附近的荧光峰强度有规律地减弱,金属离子在300~400 nm 范围内不发射荧光,表明金属离子能够猝灭BSA 的内源性荧光.随着Ni2+,Cu2+浓度增加,色氨酸残基和酪氨酸残基的最大发射波长略有红移,说明这两种残基所处的微环境极性增加,疏水性降低[3].
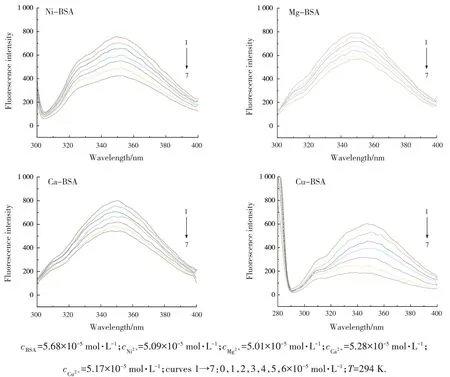
图1 BSA与金属离子作用的荧光光谱
2.2 金属离子对BSA内源荧光的猝灭类型
荧光猝灭可分为动态猝灭和静态猝灭[4],BSA 荧光猝灭可用斯特恩-沃尔默(Stern-Volmer)方程[5]进行描述,即:

其中:F0和F分别为未加入和加入金属离子时BSA 的荧光强度;[D]为金属离子的浓度;由实验数据计算出不同金属离子对BSA 的荧光猝灭的动态猝灭常数KSV,如表1 所示.根据Stern-Volmer 方程作图,如图2所示,高温斜率大于低温斜率为动态猝灭;反之,则为静态猝灭[6-7].由图2和表1可知,F0/F与[D]间存在着良好线性关系;Ni2+,Mg2+离子存在时,KSV(294 K)>KSV(310 K),可知Ni2+,Mg2+离子对BSA的荧光猝灭类型为静态猝灭;Ca2+,Cu2+离子存在时,KSV(310 K)>KSV(294 K),可知Ca2+,Cu2+离子对BSA的荧光猝灭类型为动态猝灭.

表1 BSA与金属离子作用的猝灭常数、结合常数及结合位点数
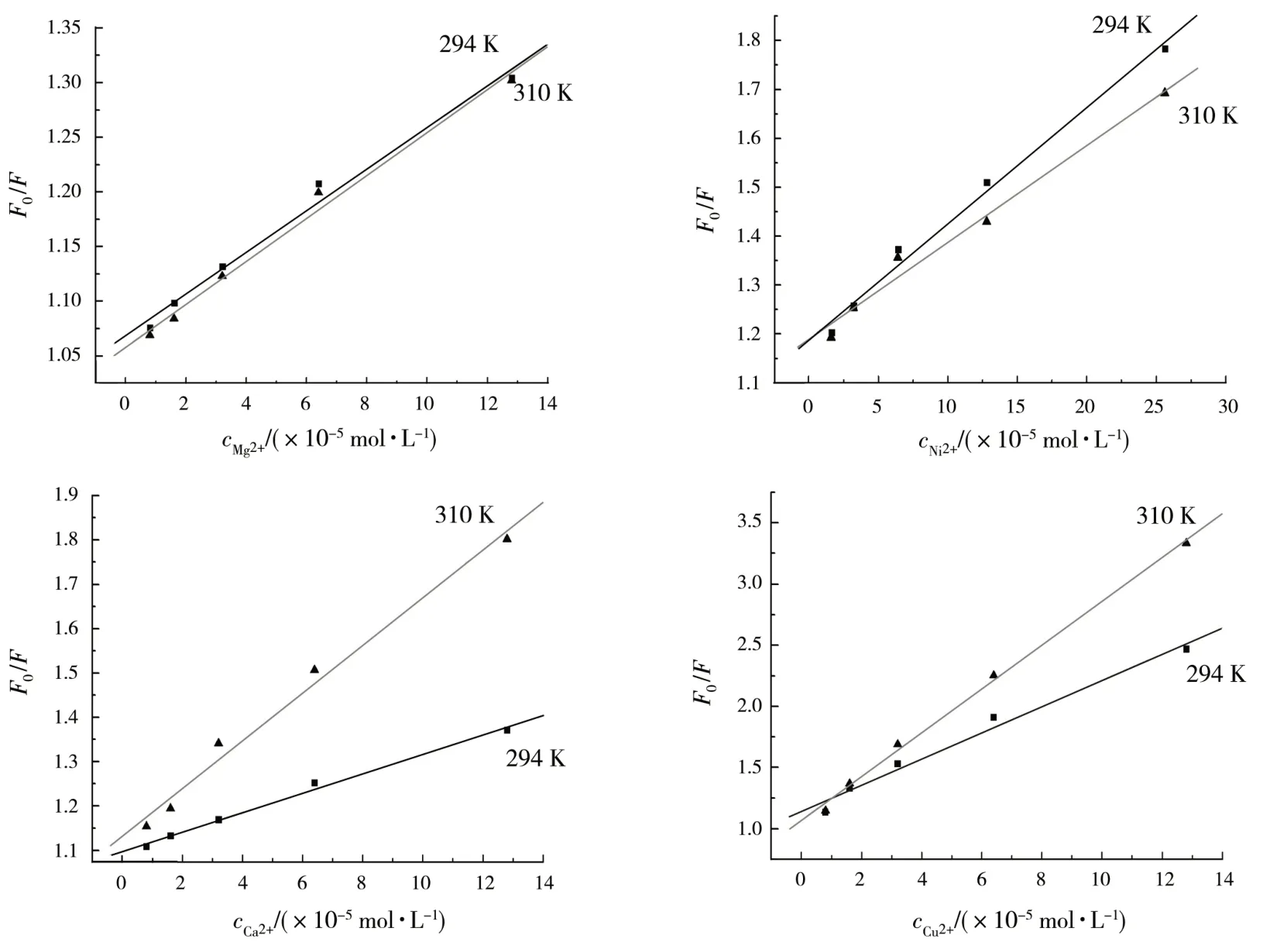
图2 BSA与金属离子相互作用的Stern-Volmer曲线
2.3 BSA与金属离子作用的猝灭常数、结合常数及结合位点数
金属离子与牛血清白蛋白之间的结合常数和结合位点数可由方程(2)进行计算:
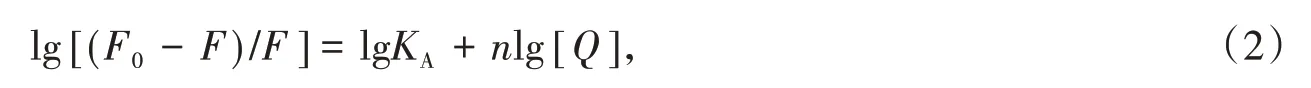
其中:[Q]为金属离子的浓度;KA为结合常数;n为结合位点数.由表1 可知,294 K 时四种金属离子与BSA 结合作用强度大小为KA(Cu2+)>KA(Ca2+)>KA(Mg2+)>KA(Ni2+).Cu2+结合常数最大,表明其与BSA形成配合物最稳定.310 K 时四种金属离子与BSA 结合常数均增大,说明温度升高,四种金属离子与BSA 作用均增强.四种金属离子与BSA 的结合位点数均小于1,说明四种金属离子与BSA 只有一个结合位点.
2.4 BSA与金属离子作用的热力学参数及作用力类型
小分子与蛋白质结合的作用力类型通过热力学参数可以确定,公式为

其中:KA1,KA2分别为T1,T2温度下的结合常数.当ΔH<0或ΔH≈0,ΔS>0时,主要的作用力是静电结合;当ΔH<0,ΔS<0时,主要作用力是范德华力或者氢键;当ΔH>0,ΔS>0时,主要作用力是疏水键[8].
根据公式(3)~(5)计算得出的热力学参数如表2所示.由表2可知,Ni2+与BSA 间的作用力主要是范德华力或者氢键;Mg2+,Ca2+,Cu2+与BSA间的作用力主要是疏水键.
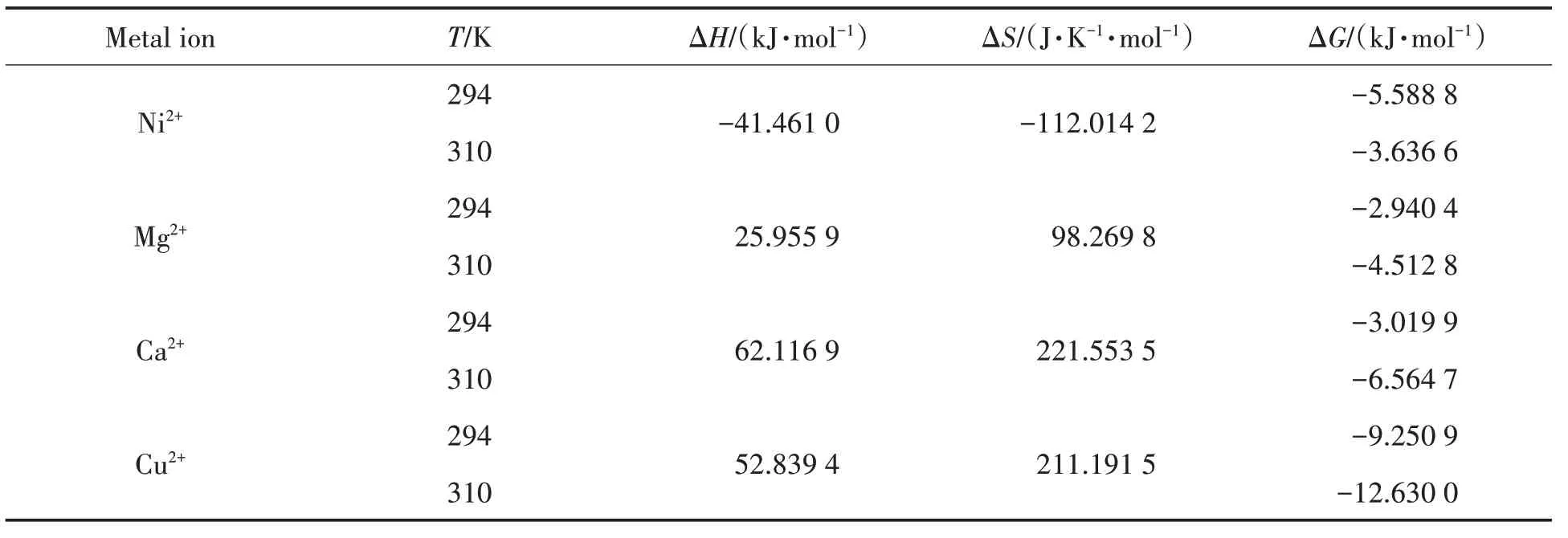
表2 BSA与金属离子作用的热力学参数
3 结论
Ni2+,Mg2+,Ca2+和Cu2+都可以与BSA 发生作用,使得BSA 的内源荧光强度降低.实验结果可得出BSA与金属离子相互作用的强弱顺序为KA(Cu2+)>KA(Ca2+)>KA(Mg2+)>KA(Ni2+).
