新型含氟基质在基质辅助激光解析电离飞行时间质谱法测定全氟磺酸中的应用
2022-04-24张雨奇于靖俞艳文王康吴婷杜一平
张雨奇,于靖,俞艳文,王康,吴婷*,杜一平
(1.华东理工大学分析测试中心,上海 200237;2.上海海关工业品与原材料检测技术中心,上海 200135)
全氟化合物(PFCs)是化合物分子中与碳原子连接的氢原子完全被氟原子所取代的一类有机化合物。C-F 键具有极高极性和键能(约110 kJ·mol-1),使PFCs在水解、代谢、光解和其他形式的降解中具有热力学稳定性和高度耐受性。相关研究表明,在长期的环境迁移转化过程中,PFCs最终降解产物以全氟辛烷磺酸(PFOS)和全氟辛酸(PFOA)为主,PFOS和PFOA 由于自身的广泛应用,成为PFCs在环境介质中检出频率最高的两种物质[1]。很明显,PFCs已经成为新出现的环境污染物,而且在职业暴露人群的流行病学调查结果中显示,血液中高浓度水平的PFOA 可以造成胆固醇和尿酸含量升高,但是并没有确凿证据表明它们会引发后续的心脑血管疾病[2]。高浓度水平的PFOA还可以提高人血液中肝酶的浓度水平[3]。此外,对美国普通成年人的健康调查显示,与健康人群相比,患有甲状腺疾病的人群体内存在更高浓度水平的PFOS和PFOA[4]。作为PFOS的替代品,全氟丁烷磺酸(PFBS)的使用逐渐增加,导致其在环境中已普遍存在。文献[5]报道PFBS可以有效破坏甲状腺内分泌腺,从而导致视觉功能受损。因此,它们的监测对于促进环境管理和人类身体健康至关重要。
基质辅助激光解析电离飞行时间质谱(MALDI-TOF MS)具有样品制备简单、分析快速、灵敏度高、耐盐性强等优点。自从20 世纪80 年代以来,MALDI一直被广泛应用于大分子物质的检测,比如蛋白质[6]、多糖[7]、脱氧核糖核酸(DNA)/核糖核酸(RNA)[8]、聚合物[9],甚至是细菌[10]。尽 管MALDI-TOF MS的高通量性使其成为分析这些物质的强有力工具,但其在小分子领域的应用受到了相当大的限制,因为常用的有机基质会产生大量的与基质相关的干扰离子[11],从而使相对分子质量低的分析物的检测变得模糊不清,如检测酸类化合物的常用基质9-氨基吖啶(9-AA)用于检测PFCs时,背景干扰严重。近些年来,许多无机材料如石墨烯[12-13]、金属氧化物纳米材料[14]以及多孔硅材料[15]已经被开发出来作为替代基质。金属共价有机骨架可以用作吸附剂和基质,以实现对PFCs的快速分析[16]。这些材料虽然可以实现基质离子的低碎片化,但是合成复杂、价格昂贵。因此,需要持续开发新的无干扰基质,以用于MALDI-TOF MS分析小分子。
本工作开发了一种新型含氟基质,提出了全氟磺酸的MALDI-TOF MS定性和定量分析方法,并用于包装材料中PFOS和PFBS的定量分析,可为该类物质的定性定量分析提供新的解决方案。
1 试验部分
1.1 仪器与试剂
AB Sciex 4800 plus MALDI TOF/TOF 型基质辅助激光解析电离飞行时间质谱仪;Vortex-Genie 2 型涡旋振荡仪;AB135-S/FACT 型电子分析天平;B2510E 型超声波清洗机;Mill-Q 型超纯水仪。
PFOA 标准储备溶液:10 g·L-1,称取适量的PFOA 标准品溶于甲醇中,配制成质量浓度为10 g·L-1的PFOA 标准储备溶液。同理,制得相同质量浓度的PFOS标准储备溶液和全氟丁烷磺酸钾标准储备溶液。
内标溶液:300 mg·L-1,称取适量的内标二十一烷酸溶于乙醇中,配制成质量浓度为300 mg·L-1的内标溶液。
十五烷酸、十七烷酸、十九烷酸、二十一烷酸混合标准溶液:0.5 g·L-1,称取适量的十五烷酸、十七烷酸、十九烷酸、二十一烷酸溶于体积比1∶1的异丙醇-乙腈混合液中,配制成质量浓度为0.5 g·L-1的混合标准溶液,待用。
9-AA 的纯度不小于99.5%;3,3′-二氟二苯甲酮的纯度为 99%;甲基三苯基溴化膦(Ph3PCH3Br)、PFOA、PFBS、PFOS标准品的纯度均不小于98%;全氟丁烷磺酸钾标准品、1,6-二苯基-1,3,5-己三烯(DPH)的纯度为98%;质量分数为1%的三氟乙酸(TFA)溶液;α-氰基-4-羟基肉桂酸(CHCA)为色谱纯;乙腈、四氢呋喃(THF)为分析纯;试验用水为超纯水。
1.2 试验方法
1.2.1 新型基质1,1-二(3-氟苯基)乙烯的合成
根据文献[17],在无水条件下,在圆底烧瓶中加入Ph3PCH3Br(11.5 g,32 mmol)、叔丁醇钾(t-Bu OK,6.3 g,56 mmol)和THF(40 mL),反应混合物在氮气氛围中室温搅拌20 min,将双(3-氟苯基)甲酮(3.4 g,15.7 mmol)溶于THF(20 mL)中,并缓慢加入反应混合物中。室温搅拌过夜后,用饱和氯化铵溶液进行淬灭。分离有机层,用乙酸乙酯萃取水层。有机层用饱和氯化钠溶液洗涤,再用无水硫酸钠干燥,过滤。滤液减压浓缩,用硅胶柱层析法纯化,得到1,1-二(3-氟苯基)乙烯(EDF)。合成路线图见图1。纯化后的产物用核磁共振氢谱(1H NMR)和配有电子轰击离子源的质谱(EI-MS)进行表征。
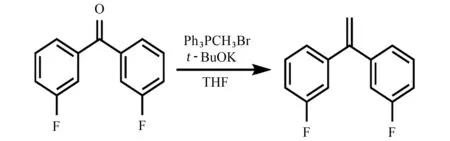
图1 EDF的合成路线Fig.1 Synthetic route of EDF
1.2.2 样品中全氟磺酸的提取
将食品级包装材料汉堡包装纸剪成0.5 cm×0.5 cm 的碎片,称取100.00 mg置于10 mL带盖玻璃瓶中,加入甲醇5 mL,并设置了空白甲醇对照组。将玻璃瓶放置在超声波清洗仪中,于室温超声2 h。超声结束后,过0.22μm 滤膜,将滤液收集至5 mL玻璃瓶中,待用。
1.2.3 MALDI-TOF MS分析
称取适量EDF 溶于二氯甲烷中,涡旋振荡5 min,配制成1 g·L-1的EDF基质溶液。采用逐层点样的方法,移取0.6μL 的EDF 基质溶液快速点在不锈钢靶板圆点处,自然干燥后,再移取0.8μL待测样品溶液点在不锈钢靶板的相同位置,待其自然挥干后进行MALDI-TOF MS分析。
2 结果与讨论
2.1 基质EDF的表征
试验对制备的新型基质EDF进行1H NMR 和EI-MS表征。图2(a)为基质EDF 的1H NMR图,1H NMR(400 MHz,CDCl3)δ:7.31(dd,J=14.9,7.6 Hz,2H),7.10(d,J=7.8 Hz,4H),6.98~7.06(m,2 H),5.51(s,2 H),与EDF 的理论氢谱相符。在图2(b)EI-MS谱图中可看到分子离子峰质荷比(m/z)216.074 9,与理论 计算C14H10F2的[M-e]+m/z216.074 5的相对误差仅1.8×10-6,同时多个碎片离子峰也进一步证实了EDF 的合成。

图2 EDF的1 H NMR 谱图和EI-MS谱图Fig.2 1 H NMR spectrum and EI-MS spectrum of EDF
2.2 基质性能考察
将EDF基质应用于全氟磺酸的MALDI-TOF MS检测中,可获得背景干净的质谱图。图3(a)为在1 g·L-1EDF基质条件下,0.5 g·L-1全氟丁烷磺酸钾(其在检测体系中即为PFBS,以下均称为PFBS)、0.5 g·L-1PFOS以及5 g·L-1PFOA 的混合标准溶液的MALDI-TOF MS谱图,图中可看出该基质能极大地改善常规有机基质在低相对分子质量端的背景干扰。相对于离子化效果更好的PFOS,PFOA 也同样在EDF 这种基质中被检测到,而且无背景干扰峰。基于对全氟磺酸的优良检测性能,试验还将该基质应用于其他酸性化合物的MALDI-TOF MS检测中。图3(b)为在1 g·L-1EDF基质条件下,0.5 g·L-1的十五烷酸、十七烷酸、十九烷酸、二十一烷酸混合标准溶液的MALDITOF MS谱图,可以看到在EDF 基质下这些脂肪酸均能获得信噪比良好的MALDI-TOF MS谱图,且同样无基质和背景干扰峰。由此可见,EDF 基质不仅可以实现各种酸性小分子的MALDI-TOF MS检测,同时可以显著改善低相对分子质量端的背景干扰。
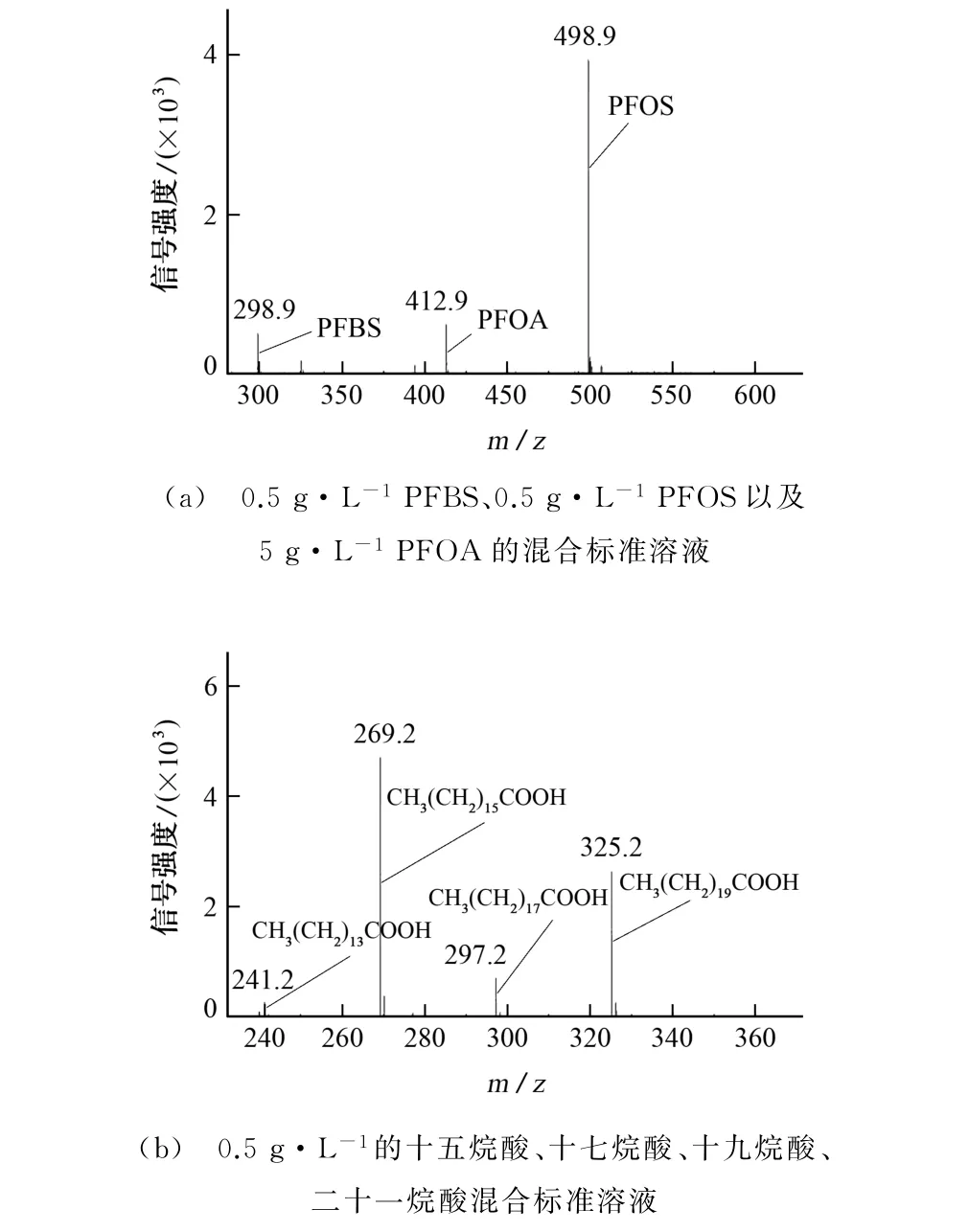
图3 典型的MALDI-TOF MS谱图Fig.3 Typical MALDI-TOF MS spectra
在后续试验研究及定量方法建立中,均以PFOS和PFBS为研究对象进行探讨。
试验将3种常见的用于小分子酸性物质检测的有机基质(CHCA、9-AA 和DPH[18])和开发的EDF基质应用在全氟磺酸PFOS 和PFBS 的MALDITOF MS检测中,并进行了结果对比。
称取适量CHCA 溶于含0.1%(质量分数)TFA 的体积比1∶1的乙腈-水混合液中,称取适量DPH 溶于THF 中,称取适量9-AA 溶于体积比2∶3的异丙醇-乙腈混合液中,称取适量EDF 溶于二氯甲烷中;涡旋振荡5 min,均配制成10 g·L-1的基质溶液。采用逐层点样的方法,移取0.6μL上述基质溶液快速点在不锈钢靶板圆点处,以二氯甲烷为溶剂的EDF基质溶液迅速挥干,因其沸点低以及移取的量少,正好覆盖圆点的范围。其他基质在室温下自然干燥后,再移取0.8μL待测样品溶液点在不锈钢靶板的相同位置,待其自然挥干后,进行MALDI-TOF MS分析。
结果显示,在4种基质中,含量较高的全氟磺酸可以获得类似的检测结果,但在含量较低的全氟磺酸的检测中EDF 显示出其独特的背景消除效应。图4为10μg·L-1的PFOS和PFBS混合标准溶液在4种基质条件下的MALDI-TOF MS谱图,除了EDF能获得信噪比可观的干净的MALDI-TOF MS谱图外,其他3种基质(CHCA、9-AA、DPH)检测的质谱图中均有严重的背景干扰峰,会给后续的分析带来困难。
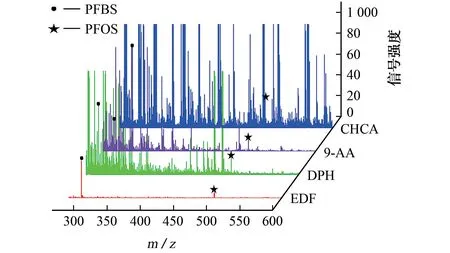
图4 10μg·L-1的PFOS和PFBS混合标准溶液在4种基质下的MALDI-TOF MS谱图Fig.4 MALDI-TOF MS spectra of 10μg·L-1 PFOS and PFBS mixed standard solution under four matrices
进一步采用密度泛函理论计算4种不同基质和PFOS之间的相互作用力,结果发现,EDF与PFOS的共结晶在激光作用下解离出全氟辛烷磺酸阴离子时所需的能量最低,其相互作用示意图及所需的能量见图5。考虑到后续实际样品的分析中所含全氟磺酸的含量极低,EDF可以作为后续分析全氟磺酸的理想基质。
图5 4种基质与PFOS之间相互作用力的理论计算Fig.5 Theoretical calculation of the interaction force between four matrices and PFOS
2.3 基质使用条件的优化
由于每种基质均有其合适的使用条件,如点样方式、基质质量浓度等,因此找到合适的基质使用条件对于分析全氟磺酸也是至关重要的。
2.3.1 点样方式
对于传统有机基质来说,点样方式分为逐层点样和混合点样两种。逐层点样是先铺分析样品,待其自然挥干之后再点基质于MALDI靶板上,或是先铺上基质,待其干燥后再铺上分析样品于MALDI靶板上。而混合点样则是先将基质与待测的分析样品均匀混合之后再一起点在MALDI靶板上进行分析。如图6所示,逐层点样相较于混合点样信号强度有明显提升。因此,为了保证更好的试验结果,试验选择逐层点样的方式。

图6 点样方式对PFOS和PFBS信号强度的影响Fig.6 Effect of spotting method on the signal intensity of PFOS and PFBS
2.3.2 基质质量浓度
传统基质的质量浓度一般配制为10 g·L-1,略高于样品质量浓度,这样足以保证样品中分析物的离子化程度,对于一种新的基质,其质量浓度对于分析物信号的影响也是需要考察的。如图7所示,EDF基质在分析全氟磺酸时信号强度最好的质量浓度为1 g·L-1,相较于常规的10 g·L-1,信号强度提升了3 倍以上。这可能跟基质本身的性状有关,EDF在常温下为液体,而非固体状态,当使用较高质量浓度的EDF 时,基质干燥不是很彻底,影响了离子传输效率,而质量浓度降低后,基质和样品能较快地干燥并形成共结晶,有助于样品中分析物的离子化。因此,试验选取的EDF 基质质量浓度为1 g·L-1。
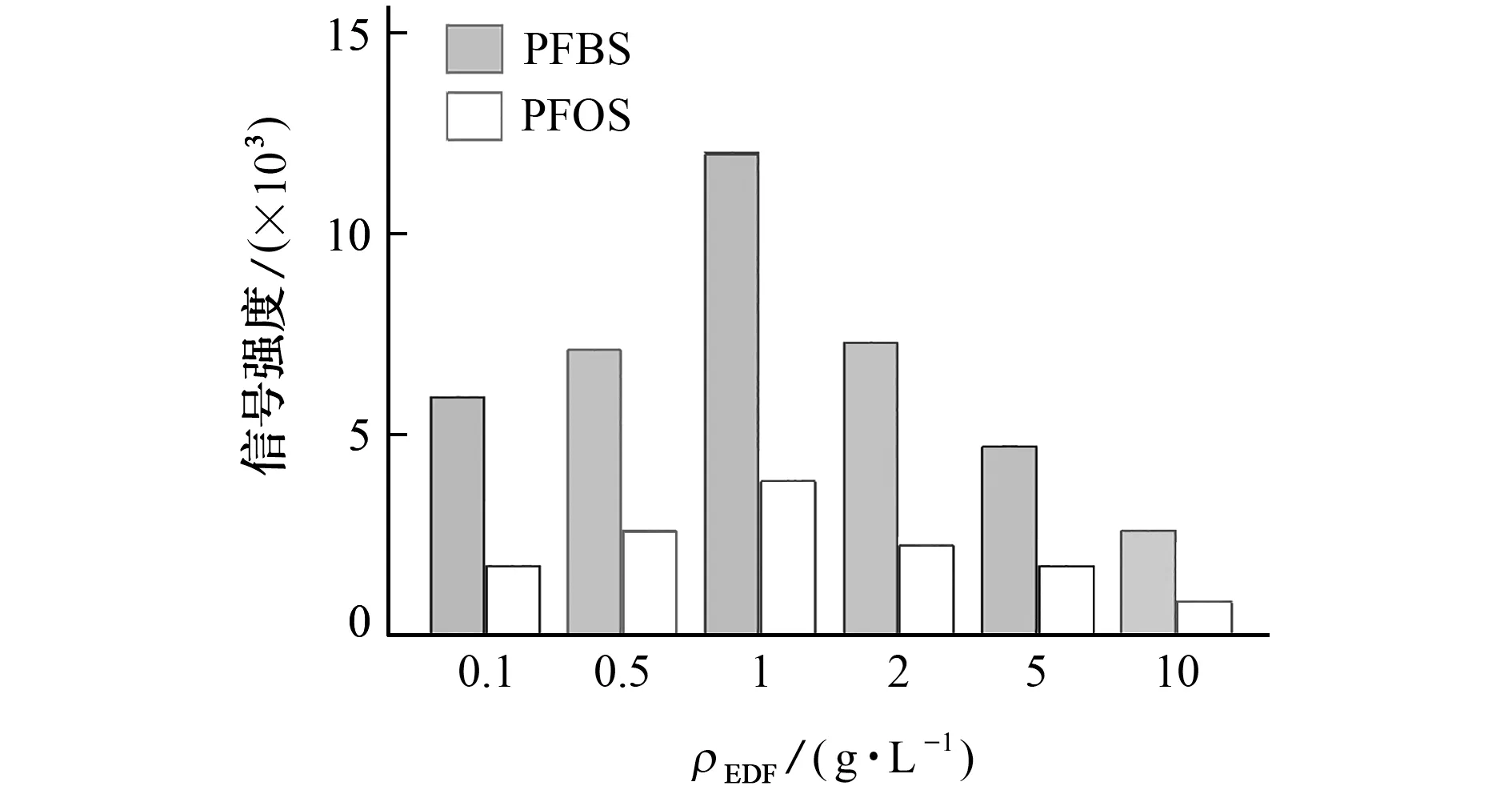
图7 EDF基质质量浓度对PFOS和PFBS信号强度的影响Fig.7 Effect of mass concentration of EDF matirx on the signal intensity of PFOS and PFBS
2.4 标准曲线和检出限
配制含有PFOS和PFBS(质量浓度分别为20,50,100,200,250 μg·L-1)和内标二十一烷酸(300 mg·L-1)的混合标准溶液系列,按仪器工作条件测定。以全氟磺酸的质量浓度为横坐标,全氟磺酸与内标的信号强度比值为纵坐标,绘制标准曲线。在最佳的试验条件下(EDF 基质质量浓度1 g·L-1,逐层点样)进行MALDI-TOF MS检测,内标法定量。结果表明,PFOS 和PFBS 标准曲线的线性范围均为20~250μg·L-1,线性回归方程和相关系数见表1。

表1 线性参数Tab.1 Linearity parameters
在最佳的试验条件下(EDF 基质质量浓度1 g·L-1,逐层点样)对PFOS和PFBS的检出限进行考察,如图8所示。按照3倍信噪比(S/N)对应的质量浓度作为检出限(3S/N),10倍信噪比对应的质量浓度作为测定下限(10S/N),得到PFOS和PFBS的检出限均为1μg·L-1,测定下限均为5μg·L-1。
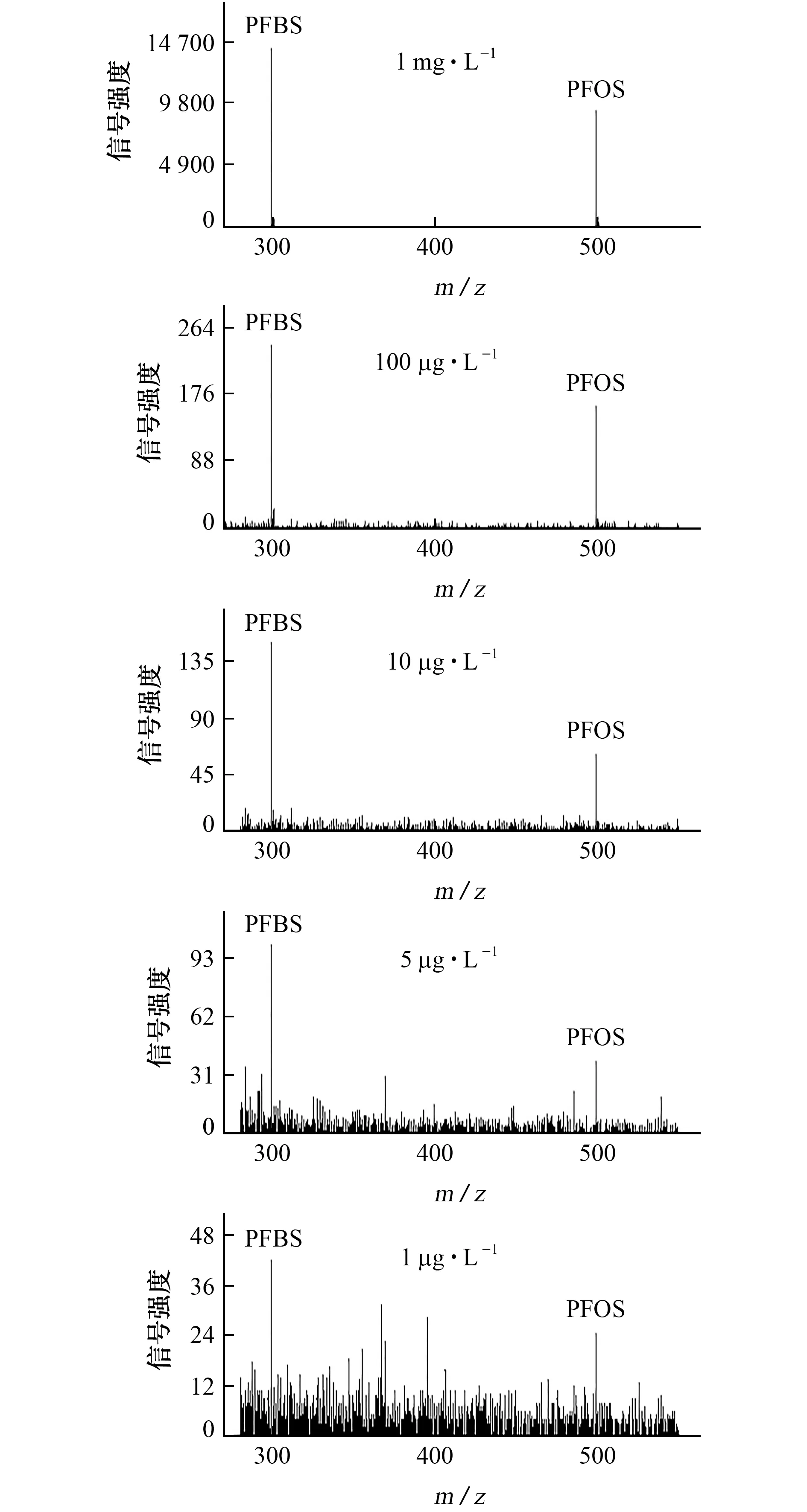
图8 PFOS和PFBS的检出限Fig.8 Detection limits of PFOS and PFBS
2.5 包装纸中全氟磺酸的测定
根据欧盟于2006年发布的《关于限制全氟辛烷磺酸的销售和使用》(2006122EC)法令规定,不得销售和投放含有以PFOS为构成物质或要素的、质量分数不小于0.005%的物质;不得销售含有PFOS质量分数超过0.1%的成品、半成品及零部件,按照1.2节的方法提取,通过换算得出,所提取出来的检测样品溶液中PFOS的质量浓度不得超过1 mg·L-1。将该新型基质EDF 应用于实际包装纸中全氟磺酸的定性定量分析中,发现在所购包装纸中未检出PFOS和PFBS,即其质量浓度低于该方法的测定下限(5 μg·L-1),说明该包装纸符合2006122EC的法令。为了进一步验证该方法的准确度,对样品中PFOS和PFBS进行3个不同浓度水平的加标回收试验,计算回收率和测定值的相对标准偏差(RSD,n=7),所得测定值的RSD 在30%以内,回收率结果如表2所示。
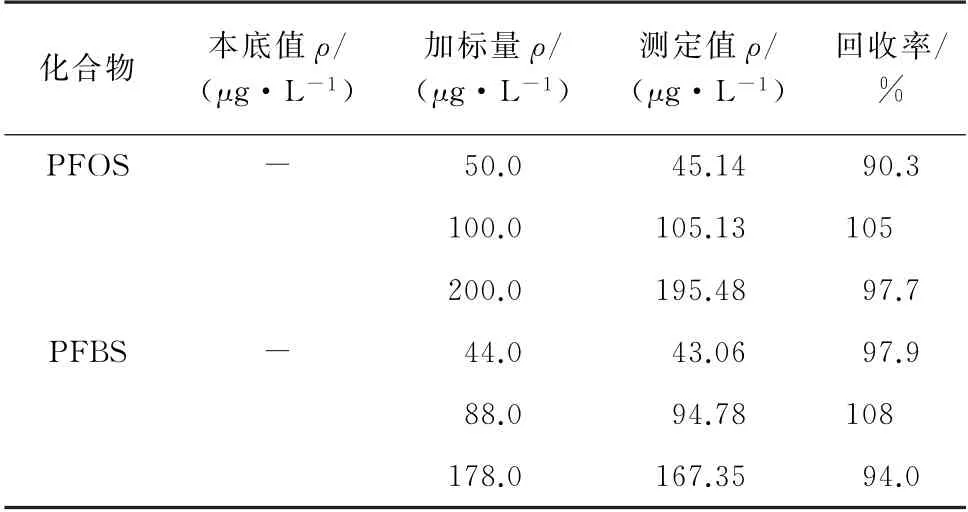
表2 回收试验结果Tab.2 Results of test for recovery
结果表明,PFOS 和PFBS 的加标回收率为90.3%~108%。
本工作合成了一种可用于酸性化合物检测的新型基质EDF,尤其是对PFOS和PFBS有着良好的检测效果,背景干净,无基质干扰峰,可达到1μg·L-1的检出限。进一步建立了PFOS和PFBS的标准曲线,在20~250μg·L-1内相关系数可达0.997 2和0.989 5。对于实际样品的分析,得到的加标回收率在90.3%~108%内,证明了该方法的可靠性。
