果胶和可溶性大豆多糖在酸性乳饮料中的应用
2022-04-11薛玉清李文强胡佳麒阮叶萍欧凯李言郡冯玉红
薛玉清,李文强,胡佳麒,阮叶萍,欧凯,李言郡,冯玉红
(杭州娃哈哈集团有限公司,浙江省食品生物工程重点实验室,杭州 310018)
0 引言
酸性乳饮料由于清爽的口感、丰富的营养和独特的风味备受广大消费者喜爱。但酸性乳饮料pH值低于酪蛋白等电点,使酪蛋白胶束间静电排斥作用减弱导致体系失稳。为保护酪蛋白防其聚集沉淀提高酸性乳饮料的稳定性,通常要添加稳定剂[1]。酸性体系常用稳定剂有果胶(Pectin)、羧甲基纤维素钠(CMC)、黄原胶、琼脂、可溶性大豆多糖(SSPS)等,CMC、黄原胶和琼脂会增加产品黏度,严重影响口感;果胶耐热性能有限,单独使用有较大风险,且用量高时成本口感均无法接受;而大豆多糖恰好具备黏度低、热稳定性好等特点[2-3],所以果胶复配大豆多糖在此类饮料中较为适用。
本文通过优化调配型酸乳饮料的加工工艺,明确果胶和SSPS在酸性乳饮料中的最佳应用条件,从而提高酸乳饮料的整体稳定性[4]。
1 材料与方法
1.1 仪器与试剂
pH计、分析天平,瑞士Mettler-Toledo公司;均质机,德国APV公司;离心机,德国Eppendorf公司;Mastersizer 2000粒度分析仪,瑞士万通公司;Turbiscan稳定性分析仪,法国Formulaction公司;LumiSizer-651稳定性分析仪,罗姆常州仪器有限公司;黏度仪LVDV-3T/8738511,美国博勒飞公司。
脱脂奶粉,新西兰恒天然公司;可溶性大豆多糖,日本不二富吉有限公司;白砂糖,北京糖业有限公司;柠檬酸、柠檬酸钠(分析纯),上海国药集团;果胶(食品级),市售。
1.2 方法
1.2.1 调酸型乳饮料的工艺流程
脱脂粉3%+果胶0.4%+大豆多糖0.3%+白砂糖6%+柠檬酸钠0.3%+超纯水→原料混合→冷却至调酸温度→调酸→定容→均质→杀菌→灌装
操作要点:(1)配料:将脱脂粉溶于55℃超纯水中,并水合30 min;将果胶和白砂糖溶于65℃超纯水中,冷却待用;将大豆多糖溶解于80℃超纯水中,冷却后与其他原料混合;(2)调酸:将料液温度冷却至20℃,用30%柠檬酸溶液调整pH值至3.8;(3)均质:均质压力为25 MPa;(4)杀菌:杀菌温度为95℃,时间为10 min,热灌。成品蛋白含量不低于0.8%
1.2.2 复配比例、pH值对乳饮料稳定性的影响
调整料液中果胶与大豆多糖浓度和复配比例,用不同用量柠檬酸和柠檬酸钠调整最终产品pH值,对产品进行Lumisizer稳定性扫描、离心沉淀率和粒度分布测定。
1.2.3 配料顺序和均质工艺对稳定性的影响
先添加果胶,剪切5 min后加入SSPS,20℃调酸均质;先添加SSPS,剪切5 min后加入果胶,20℃调酸均质;先添加SSPS,20℃进行调酸均质后,再添加果胶;果胶和SSPS混合添加后20℃再进行调酸再均质,均质压力为25 MPa。测定产品的离心沉淀率、平均粒度分布并进行稳定性扫描。
1.2.4 离心沉淀率测定
取40 mL离心管,称取管重为W1,称取一定量样品W2,放入离心机在3 000 r/min,20℃条件下离心15 min,去除上层液体,倒置15 min后称其质量为W3。离心沉淀率=(W3-W1)/W2×100%。离心3次取平均值[5]。
1.2.5 平均粒度大小测定
取样品用Mastersizer 2000粒度分析仪测定样品中粒子大小分布情况,样品用去离子水按1∶1 000(质量比)稀释后,根据文献设定相关操作参数,温度为25℃;泵速为2 200 r/min;颗粒折射率为1.52;颗粒吸收率为0.1;分散剂为水;分散剂折射率为2.33[6]。
1.2.6 Lumisizer稳定性扫描
用Lumisizer稳定分析仪进行稳定性分析,仪器参数设置:温度为(25±0.5)℃,转速为4 000 r/min;连续性扫描程序:每5 s扫描1次,连续扫描500条谱线。
1.2.7 稳定性扫描
用Turbiscan Lab稳定分析仪进行稳定性分析,仪器参数设置:温度为(25±0.5)℃;连续性扫描程序:每1 h扫描1次,连续扫描24 h[7]。
2 结果与分析
2.1 复配比例、pH值对稳定性的影响
在果胶复配大豆多糖的基础上,同时考察终产品pH值和柠檬酸钠添加量对稳定性的影响,设计四因素三水平L9(34)正交实验[8],分别以离心沉淀率和lumisizer不稳定性系数为指标进行分析,因素如水平如表1所示。

表1 正交实验因素水平 g/L
以最终产品离心沉淀率为指标,正交实验结果如表2所示。由表2结果可知,影响离心沉淀率的主次关系为:柠檬酸钠>pH值>果胶>SSPS,最优组合为A1B1C1(C3)D3,即果胶质量浓度1.5 g/L,SSPS质量浓度3 g/L,pH值为4.0或4.2,柠檬酸钠质量浓度3.8 g/L。
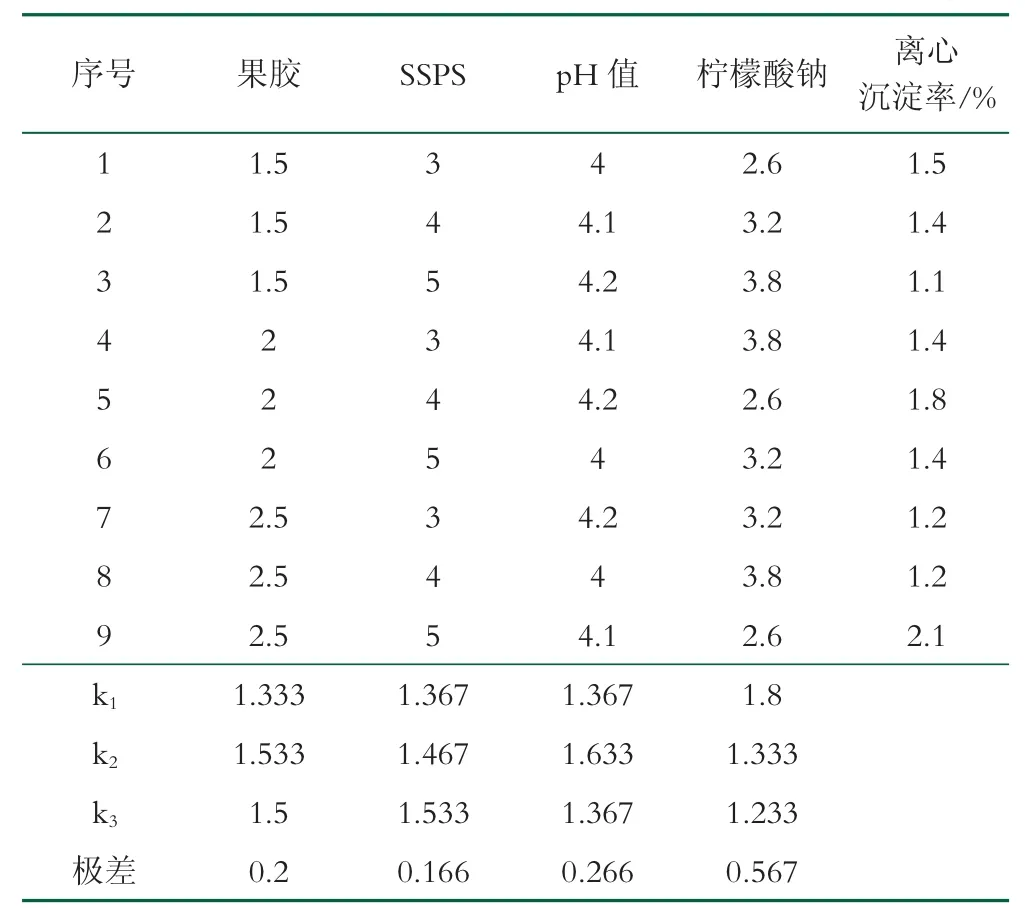
表2 正交实验设计方案和结果 g/L
正交实验方差分析如表3所示,方差分析结果表明,柠檬酸钠添加量对离心沉淀率影响显著,其他因子不显著。
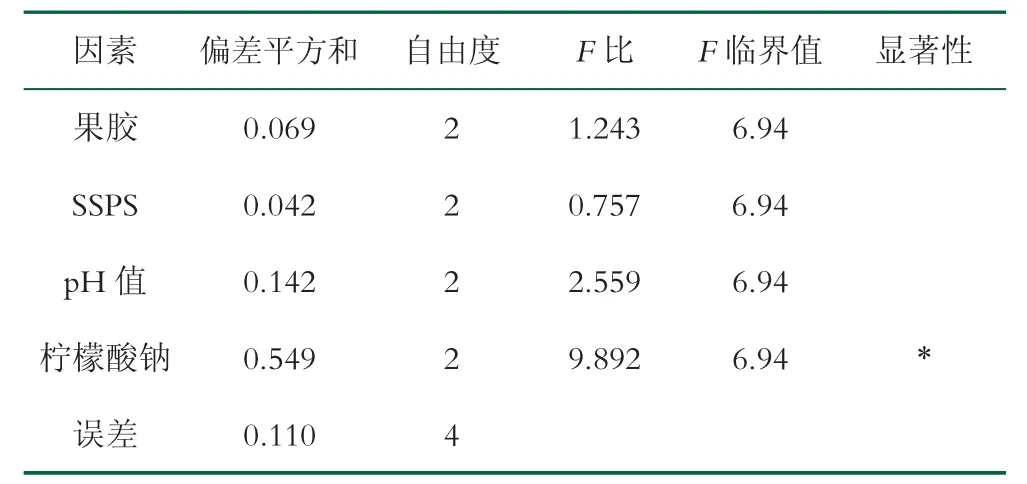
表3 正交实验方差分析
以Lumisizer稳定性分析仪不稳定性系数为指标,实验结果如表4所示。
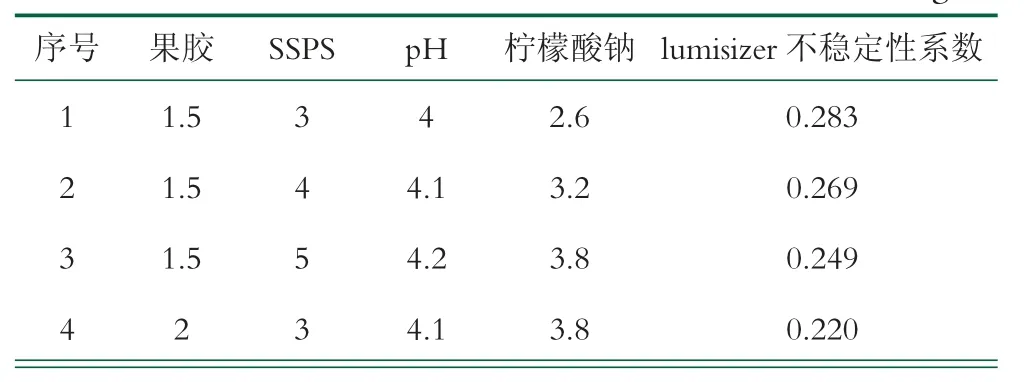
表4 正交实验设计方案和结果 g/L
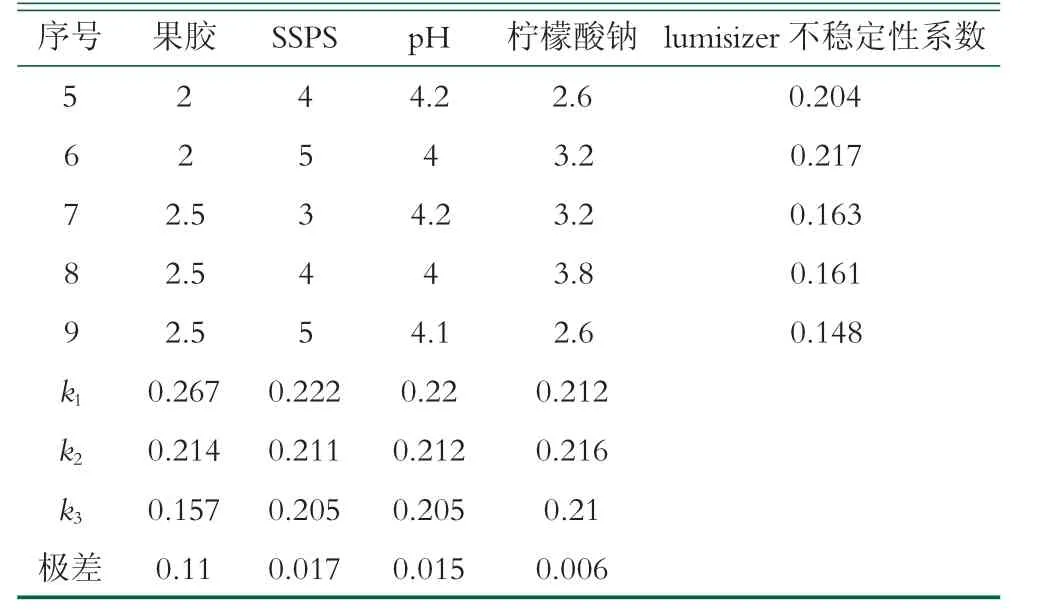
(续表4)
由表4可以看出,影响不稳定性系数的主次关系为:果胶>SSPS>pH值>柠檬酸钠,最优组合为A3B3C3D3,即果胶2.5 g/L,SSPS 5 g/L,pH值为4.2,柠檬酸钠3.8g/L。该结果与离心沉淀率差异较大,分析认为,Lumisizer不稳定性系数反映的是整个体系的透光率变化,影响透光率的因素不仅有作为分散相的蛋白质,也有少量的脂肪、胶体本身的浊度等等,这些成分在离心力作用下均会发生一定的迁移导致透光率变化,但未必会引起肉眼可见的沉淀,因此,两个指标出现不一致的情况。
2.2 配料顺序和均质工艺对稳定性影响
由图1可以看出,先添加果胶剪切后加入SSPS再调酸均质、先添加SSPS剪切后加入果胶再调酸均质与SSPS和果胶混合后剪切调酸均质的产品沉淀率、粒径差异不大,离心沉淀率均在0.266%左右。由粒径分布图2可知,先加SSPS调酸均质后再加果胶,终产品粒径和离心沉淀率大幅度降低,产品稳定性有很大提高。由于SSPS有较多支链,再加之电荷不高,因此SSPS和酪蛋白的作用力非常有限。该研究通过改善工艺,让其先和酪蛋白作用,同时通过均质使SSPS的分子结构伸展开,从而充分提高SSPS和酪蛋白的作用力,提高产品稳定性。

图1 均质工艺对酸性乳饮料沉淀率的影响
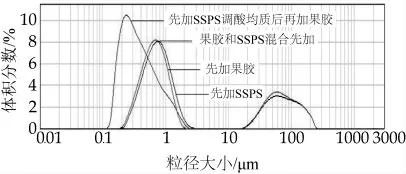
图2 均质工艺对酸性乳饮料粒径分布的影响
Turbiscan是基于多重光散射技术的稳定性分析仪,它的工作原理主要是根据反射物理模型和透射物理模型,背散射光的变化率可以反映体系的均一程度、颗粒大小和浓度,据此判断体系的稳定性[9]。同一样品不同曲线之间光强值变化越大表示体系越不稳定[10]。利用Turbiscan图谱,左边代表样品底部,右边代表样品顶部,左边曲线向上移动则说明背散射光增强样品有沉淀,向下移动则代表水析;右边顶部曲线向上则代表脂肪上浮;向下移动则代表水析;曲线中间波动较大则说明体系有聚团现象[11]。由Turbiscan图谱可知,仅先加SSPS调酸均质后再加果胶的样品整体稳定性最好,先果胶、小SSPS、果胶和SSPS混合后再调酸均质工艺的样品均底部出现沉淀与水析,上浮层下方有较大范围澄清,且图谱情况高度一致。
3 结论
由实验可知,果胶和大豆多糖在酸性乳饮料体系中的稳定性作用,取决于果胶和大豆多糖浓度、比例、产品终点pH值、配料顺序和均质工艺等因素的影响,其中,配料顺序和均质工艺影响效果最为明显,其他影响不稳定性系数的主次关系为:果胶>SSPS>pH>柠檬酸钠。蛋白质含量为0.8%的调酸型乳饮料体系中,各影响因素的最优组合为果胶2.5,SSPS 5 g/L,pH 4.2,柠檬酸钠3.8 g/L,且要使用SSPS先跟还原奶调酸后均质,再跟果胶混合的工艺,才能保证产品有较好的稳定性。另外,Lumisizer稳定性分析仪、Turbiscan稳定分析仪的结果与离心沉淀、粒径分布相同,均是一种快速准确判定产品体系稳定性的手段。
