响应面法优化酢浆草中α-葡萄糖苷酶抑制成分的提取工艺
2022-03-25郑锦丽郭少波
朱 斌,郑锦丽,梁 犇,史 娟,郭少波
(陕西省催化基础与应用重点实验室,陕西理工大学化学与环境科学学院,陕西 汉中 723001)
糖尿病是一种临床常见病,2017年的调查显示,中国Ⅱ型糖尿病人约有1.14亿,预测到2035年,该病例数将增加到约5.92亿人次,糖尿病的发病人群逐渐呈现年轻化趋势[1-2]。目前临床针对Ⅱ型糖尿病的治疗方案仍以药物治疗为主,包括胰岛素及类似物、磺酰脲类促泌剂、二甲双胍类、α-葡萄糖苷酶抑制剂等。其中,α-葡萄糖苷酶抑制剂通过抑制小肠黏膜刷状缘的α-葡萄糖苷酶,延缓碳水化合物的吸收,从而降低餐后高血糖。目前市场上销售的用于治疗糖尿病的药物阿卡波糖、伏格列波糖、米格列醇等均为α-葡萄糖昔酶抑制剂。中医药治疗糖尿病较为经典的名方如肾气丸、六味地黄丸、消渴方、白虎加人参汤等方药沿用至今,近年来对单体如黄连素、民族药如苗药糖宁通络等的研究,受到国际关注[3]。
酢浆草是酢浆草属的一种阔叶草本植物,别称大酸叶草,在我国长江流域及西南分布广泛。现代植物化学和药理学研究发现,酢浆草中含有黄酮类、酚酸类、生物碱类、挥发油等多种化学成分,其药理活性研究主要集中在抑菌、抗肿瘤、抗焦虑、抗癫痫、抗氧化、抗炎镇痛、肝肾保护、促进骨形成等方面[4-5]。Rodriguez等人[6]报道,酢浆草具有一定的降糖作用。本实验以酢浆草提取物对α-葡萄糖苷酶的抑制率为指标,在优化提取溶剂的基础上,通过单因素实验及响应面法,对酢浆草α-葡萄糖苷酶抑制成分的提取工艺进行优化,以期为酢浆草提取物未来应用于临床糖尿病治疗提供一定的参考。
1 材料和方法
1.1 材料与试剂
酢浆草,α-葡萄糖苷酶,4-硝基苯-α-D-吡喃葡萄糖苷(p-NPG)。磷酸氢二钾、磷酸二氢钾、石油醚、乙酸乙酯、无水乙醇、正丁醇、二甲基亚砜(DMSO)(均为分析纯)。自制超纯水。
1.2 主要仪器
KQ2200DE型数控超声波清洗器,DLSB-5/30低温冷却液循环泵,SHB-Ⅲ循环水式多用真空泵,RE-2000A旋转蒸发器,DF-1集热式磁力搅拌器,Cary 5000紫外可见分光光度计。
1.3 实验方法
1.3.1 实验原理
参考文献 [7]的方法,测试酢浆草提取物对α-葡萄糖酶水解p-NPG为4-硝基苯酚的抑制活性,判断酢浆草对α-葡萄糖苷酶的抑制活力,计算方法如式(1)所示:

其中,X=A对照组-A空白组;Y=A实验对照组-A实验组。
1.3.2 原料预处理
酢浆草干燥、粉碎→石油醚脱脂→滤渣烘干待用。
1.3.3 提取溶剂的选择
称取4份(2.0g)经预处理的酢浆草粉末,按液料比20∶1(mL∶g)分别加入超纯水、正丁醇、乙酸乙酯和乙醇,于70℃下提取120 min。提取液按1.3.1的方法进行测试,并计算其对α-葡萄糖苷酶的抑制率,以确定最佳提取溶剂。
1.3.4 单因素实验
以抑制率为指标,考察超声预处理时间、提取时间、提取温度及液料比等因素在不同水平值下,所得的酢浆草提取物对α-葡萄糖苷酶抑制效果的影响。每组进行3次重复实验,取平均值。
1.3.5 响应面法实验因素水平设计
在单因素实验结果的基础上,选取提取时间(A)、超声预处理时间(B)、液料比(C)、提取温度(D)这4个因素作为自变量[8],编码水平为-1、0、1,各实验因素编码和水平设计见表1。

表1 响应面设计的因素及水平
1.4 酢浆草α-葡萄糖苷酶抑制成分的纯化
将所得的酢浆草α-葡萄糖苷酶抑制成分提取浸膏分为3份,加入相同体积的水之后超声,分别用石油醚、乙酸乙酯和正丁醇萃取。将有机相减压旋蒸后,用少量中性氧化铝粉末拌匀,烘干,进行硅胶柱层析[9]。所得洗脱液浓缩后分别进行抑制率测定,以确定最优纯化方式。
1.5 酢浆草α-葡萄糖苷酶抑制剂的最佳浓度
将纯化后旋干所得的浸膏加DMSO溶解后,配成1、2、4、6、8、10 mg·mL-1的抑制剂,按1.3.1的方法进行测试,并计算其对α-葡萄糖苷酶的抑制率,以确定最佳抑制浓度。
1.6 数据处理
以上实验均进行3次重复。由Design-Expert 8.0.6软件设计实验并分析,利用Origin软件进行数据处理和作图。
2 结果与分析
2.1 不同提取溶剂降糖效果的比较
分别以石油醚、水、正丁醇、乙酸乙酯、乙醇为溶剂,得到相同提取条件下,不同溶剂提取的酢浆草α-葡萄糖苷酶抑制成分的降糖效果,结果见图1。由图1可知,乙酸乙酯作为提取溶剂时可得到最优的抑制率,故选择乙酸乙酯作为提取溶剂。

图1 不同的提取溶剂对α-葡萄糖苷酶的抑制效果
2.2 单因素实验结果与分析
2.2.1 提取时间对抑制率的影响
5份酢浆草粉末按照30∶1( mL∶g)的液料比加入溶剂中超声预处理10 min后,在70℃下分别提取60、90、120、150、180 min,实验结果如图2所示。提取时间在60~120min内,抑制率逐渐上升;120min时抑制率开始下降,160 min时出现陡降。原因是溶剂进入酢浆草植物细胞,以及细胞内的有效成分传递到溶剂,均需要消耗一定的时间,这有助于α-葡萄糖苷酶抑制成分溶出,使降糖效果提高。但长时间、较高温度的提取,会导致活性物质发生变性、分解,导致抑制率降低[10],因此最合适的提取时间为120 min。

图2 提取时间对抑制率的影响
2.2.2 超声预处理时间对抑制率的影响
提取温度70℃,提取时间120min,液料比30∶1(mL∶g),研究超声预处理时间的改变对酢浆草提取物抑制α-葡萄糖苷酶活性的影响,结果见图3。由图3可知,超声预处理时间为10 min时,抑制率达到最大值,继续增加预处理时间,抑制率略有降低。超声预处理加速了植物细胞壁的破裂,有助于酢浆草有效成分的溶出。导致抑制率下降的可能原因,是过长的超声时间导致某些热不稳定组分遭到破坏[8],因此选择最优超声时间为10min。

图3 超声预处理时间对抑制率的影响
2.2.3 液料比对抑制率的影响
在酢浆草粉末中加入提取溶剂,固定超声预处理时间10min,提取温度70℃,提取时间120min,改变液料比,测试提取物对α-葡萄糖苷酶的抑制率,结果见图4。结果表明,液料比为30∶1 (mL∶g)时有最大的抑制率84.4%。提高液料比可确保药材和提取溶剂有充分的接触面积,从而使有效成分能溶解完全。因此确定最佳液料比为30∶1 (mL∶g)。

图4 液料比对抑制率的影响
2.2.4 温度对抑制率的影响
如图5所示,提取温度在40~70℃时,抑制率呈上升趋势,70℃时抑制率达到最高值80.07%,继续提高温度,抑制率迅速下降。故选择70℃作为最佳提取温度。

图5 温度对抑制率的影响
2.3 响应面法优化分析
将单因素实验结果用Design-Expert 8.0.6软件进行处理,可获得4因素3水平中心组合的29个实验方案,所得的抑制率实验结果如表2所示。

表2 响应面实验设计与结果
2.3.1 方程回归分析和方差分析
用Design-Expert 8.0.6软件对表2的抑制率数据进行数学模型方差分析,分析结果列于表3。以酢浆草α-葡萄糖苷酶抑制成分的抑制率R为因变量,提取时间(A)、超声时间(B)、液料比(C)、提取温度(D)为自变量的二阶多项式回归方程为:

二阶多项式回归方程中的线性项、二次项和相互作用项,体现自变量对响应值的影响[10],其数值反映各因素对响应值的影响程度,数值越大,则影响越大。回归方程系数为正值则表示各变量对响应的协同效应,为负值则表示反向关系[11]。P值可用于确定模型和系数是否具有统计学意义。由表3的分析结果可知,所选用模型的P<0.0001且失拟项不显著(P=0.3349>0.05),表明模型的可靠性相对较高,也说明回归方程的拟合精度较高。模型的确定系数R2=0.9141,模型的调整确定系数R2Adj=0.8283,说明该模型的实验数据具有较好的拟合度,所以用该模型来描述抑制率与提取条件间的关系较适合,可用于初步分析和预测酢浆草的高效提取工艺参数。由此可知,方程的1次项A、B对响应值的影响极显著,C、D对响应值的影响显著。平方项A2、B2、D2对响应值的影响极为显著,C2对响应值的影响显著。交互项AB极为明显,BD对响应值的作用是显著。各个因素的F值都能够直观反映各个因素受影响的程度和大小,F值越高,其对响应值的影响越大[12]。对各单个因素进行数据分析后发现,FA=12.63,FB=15.36,FC=7.10,FD=5.11。各单因素对酢浆草抗糖抑制率影响的大小顺序为:超声预处理时间>提取时间>液料比>提取温度。
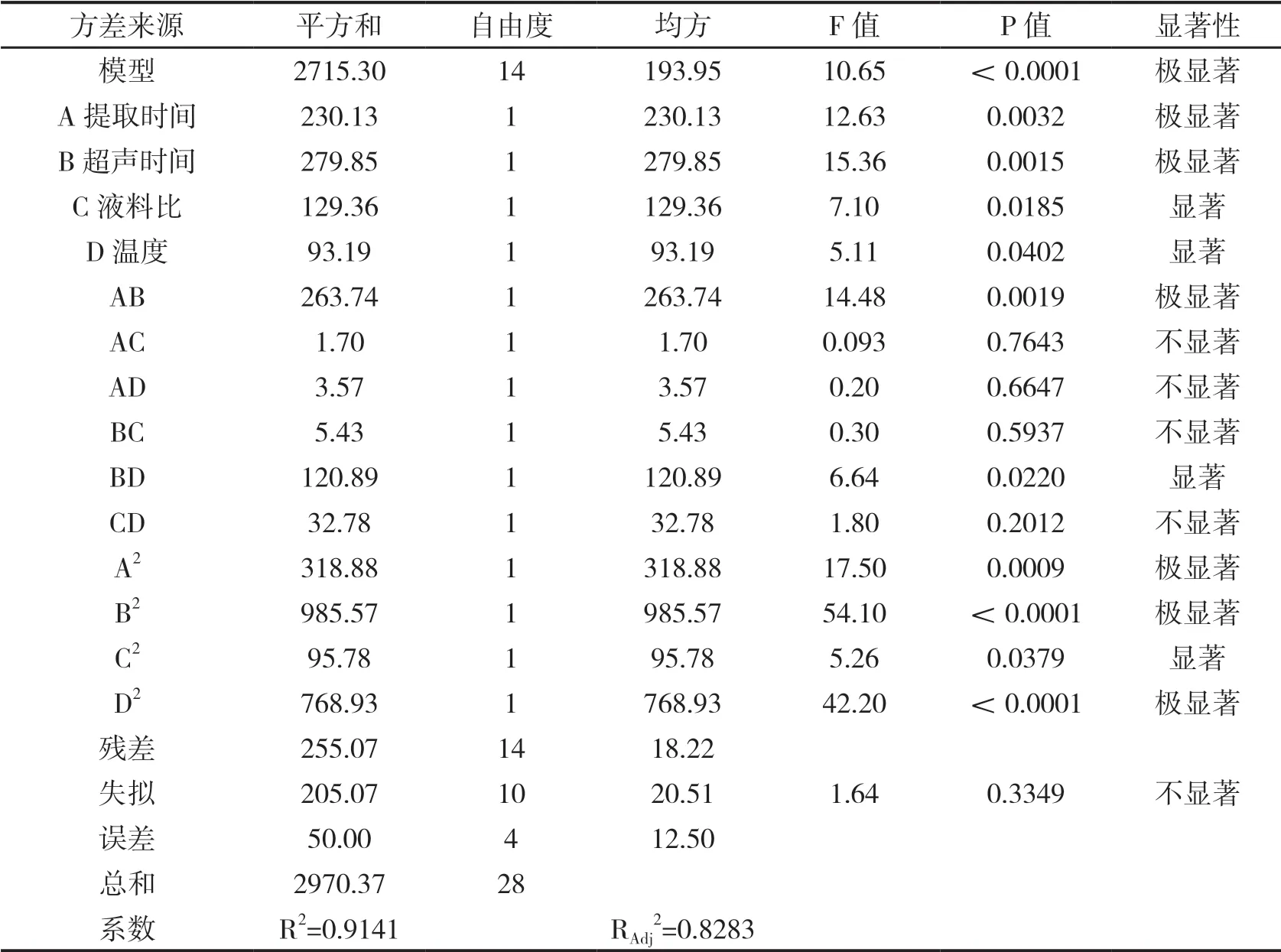
表3 回归模型方差分析
2.3.2 因素交互作用分析
为进一步分析提取时间、超声波时间、液料比、温度对抑制率的影响,固定其中2个变量,得到另外2个因素相互作用的响应面图和等高线图见图6和图7。对比表3可知,提取时间与超声预处理时间、超声预处理时间与温度这2组交互项对响应值的影响显著,其他因素的交互作用对响应值的影响不显著。

图6 超声预处理和提取时间的响应面和等高线

图7 超声预处理和温度的响应面和等高线
2.3.3 最佳工艺条件的确定和验证实验
由Design-Expert 8.0.6程序,模拟得出最佳提取工艺条件为:提取时间135.6 min、超声预处理时间12.12 min、液料比31.93∶1 ( mL∶g)、温度71.61℃,此时抑制率为85.01%。为验证响应面的可信度,结合实际情况,得到酢浆草最佳的提取条件是:液料比30∶1(mL∶g)、超声时间10 min、提取时间120 min、温度70.0 ℃,此时抑制率为84.4%,与推测相符,说明本文采用的优化方案是合理的。
2.4 最佳纯化溶剂的确定
由1.4纯化所得的3种酢浆草α-葡萄糖苷酶抑制成分的降糖抑制率如图8所示,可知正丁醇萃取后的纯化物效果较好。后续实验确定采用正丁醇二次萃取物过柱纯化后的产品。

图 8 不同萃取剂得到的纯化物的抑制率
2.5 最佳测试浓度的确定
从图9可知,酢浆草α-葡萄糖苷酶抑制成分浓度增加所导致的抑制率结果,可分为急速增长区和平缓区。在1~6 mg·mL-1范围内,抑制率从65.9%急速增长至84.6%;在6~10mg·mL-1范围内,抑制率基本维持在82%~83%。从节约成本和确保抑制效果两方面考虑,选择6mg·mL-1为后续实验的抑制剂浓度。

图9 最佳抑制浓度的确定
3 结论
本文以酢浆草为原料,考察了超声预处理时间、提取时间、液料比、提取温度等因素对酢浆草α-葡萄糖苷酶抑制成分降糖效果的影响,采用响应面法优化了酢浆草有效成分的提取工艺。结果表明,影响酢浆草降糖有效成分提取的因素顺序为:超声预处理时间>提取时间>液料比>温度。最佳提取工艺条件为:超声时间10 min、提取时间120 min、液料比30∶1(mL∶g)、提取温度70℃,在此条件下,酢浆草有效成分对α-葡萄糖苷酶的抑制率为84.4%。
