氧缺陷在CeO2催化苯甲醇和苯胺氧化偶联反应中的作用
2022-03-18瞿永泉
邹 勇,张 赛,瞿永泉
(西北工业大学 化学与化工学院,工业和信息化部特种功能与 智能高分子材料重点实验室,陕西 西安710114)
稀土氧化物是催化多种有机化学反应的重要催化剂[1-7]。二氧化铈(CeO2)作为一类应用广泛的稀土氧化物,具有独特的Ce3+/Ce4+氧化还原能力,被广泛应用于催化多种氧化反应[8-13]。通常情况下,CeO2的氧化还原性能在高温环境中(大于473 K)更为显著,因此CeO2参与的催化氧化反应常被认为需要较高的反应温度[14-16]。然而,当CeO2结构中存在氧缺陷时,即使在室温条件下,其表面氧缺陷也能够被环境中的氧气氧化[17]。该研究结果引发研究人员对CeO2低温催化氧化反应机制的探讨,特别是对催化低温液相有机反应机理的探讨[8-13,18-19]。此前诸多研究结果普遍认为CeO2表面氧缺陷位点数量的增加有利于提高氧活化能力,对低温液相氧化反应具有促进作用。然而,这一观点通常没有考虑反应体系中分子在催化剂表面的吸脱附性能对催化反应活性的影响。因此,氧缺陷在CeO2催化低温氧化反应中的作用机制还不明晰。
亚胺作为重要的反应中间体,可以经一系列简单反应(如还原、加成和缩合反应等)生成多种医药、生物和农业领域所需化学品[20-22],因此亚胺的构建方法一直以来备受关注。醛或酮与胺在路易斯酸/碱催化剂催化作用下的缩合反应是生成亚胺的传统方法,但该反应过程会产生大量的固体废弃物,造成环境污染,且醛和胺的原料价格较为昂贵,反应成本高。近年来,探索更温和、更环保、更低价的亚胺合成反应路径已经成为研究热点,所研究路径涉及仲胺脱氢[23]、伯胺氧化[24]、醛和胺直接偶联[25]、炔烃与胺加氢胺化[26]、醇和胺有氧氧化偶联[18-19]等多种反应(图1)。在一系列制备亚胺的新型反应路径中,以空气作为绿色氧化剂的醇、胺直接氧化偶联反应具有成本低廉、环境友好、易于商业化和原子经济性高等优点,受到研究人员普遍关注。然而,醇类化合物的化学活性低,上述反应往往需要在贵金属催化体系中进行,成本高昂,开发低价位的过渡金属催化剂用于上述反应具有重要的产业意义。

图1 合成亚胺的催化反应路径Fig.1 Catalytic routes for imines synthesis
据报道,CeO2具有催化醇和胺氧化偶联生成亚胺的能力[18-19]。CeO2催化性能受诸多理化性质(比表面积、晶面、粒径、表面缺陷等)的影响,其表面氧缺陷在醇和胺氧化偶联反应中的作用机制仍有待深入研究。表面缺陷工程可以实现对特定形貌CeO2表面氧缺陷浓度的系统调控,为解决上述难题提供了可行性思路。二氧化铈中氧缺陷的形成通常伴随着被还原Ce3+的产生,其表面Ce3+/Ce4+摩尔比例与表面氧缺陷浓度正相关,可以用来表征表面氧缺陷浓度[27]。基于此,本研究拟采用空气氛围氧化和抗坏血酸还原2种表面处理方式,制备一系列形貌和比表面积相同但表面Ce3+/Ce4+摩尔比例不同的CeO2纳米棒催化剂,并在此基础上系统研究CeO2中氧缺陷对醇和胺氧化偶联反应活性的影响规律。
1 材料与方法
1.1 材料与试剂
六水合硝酸铈(Ce(NO3)3·6H2O)、苯甲醇、苯胺、均三甲苯购自安耐吉化学技术有限公司;氢氧化钠购自阿法埃莎(中国)化学有限公司;乙醇购自广东光华科技股份有限公司。
1.2 仪器与设备
HT-7700电子显微镜,日本Hitachi公司;PW 1710型X-射线衍射仪,荷兰Philips公司;Thermo Fisher ESCALAB Xi+型XPS衍射仪,美国赛默飞世尔科技公司;HR-800型激光拉曼光谱仪,法国Jobin Yvon公司;ASAP 2020 HD88型物理吸附仪,美国麦克公司。
1.3 CeO2纳米棒(NR-CeO2)的合成
采用改进的水热法合成NR-CeO2催化剂[28-29],合成过程如下:将5 mL Ce(NO3)3溶液(0.8 mol/L)逐滴加入到75 mL NaOH水溶液(6.4 mol/L)中,室温下连续搅拌30 min;所得混合物转移至100 mL含聚四氟乙烯内衬的高压釜中,100 ℃条件下水热反应24 h;反应沉淀物用去离子水和乙醇交替洗涤3次,然后60 ℃条件下干燥过夜,得到NR-CeO2催化剂。
1.4 不同氧缺陷NR-CeO2的制备
将500 mg NR-CeO2样品超声分散于500 mL去离子水中,搅拌条件下加入1 mL抗坏血酸(ASA,0.25 mol/L),反应12 h;上述样品洗涤后60 ℃条件下干燥,得到NR-CeO2-R1催化剂。将抗坏血酸的物质的量浓度更换为0.5 mol/L,重复上述步骤,得到NR-CeO2-R2催化剂。
将NR-CeO2样品在300 ℃和500 ℃空气中分别煅烧2 h,得到NR-CeO2-300和NR-CeO2-500催化剂[28]。
将NR-CeO2-R1和NR-CeO2-R2分别在300 ℃空气中煅烧2 h,得到NR-CeO2-R1-300和NR-CeO2-R2-300催化剂。
1.5 催化剂的表征
催化剂样品的X射线衍射(XRD)图谱由PW 1710型X-射线衍射仪在Cu Kα射线下测得;催化剂的透射电镜(TEM)图像由HT-7700电子显微镜在100 kV加速电压下测得;催化剂的X射线光电子能谱(XPS)由Thermo Fisher ESCALAB Xi+型XPS衍射仪在Al Kα射线下测得;催化剂的拉曼光谱由HR-800型激光拉曼光谱仪在633 nm激光器下测得;催化剂的氮气吸附曲线由ASAP 2020 HD88型物理吸附仪在77 K条件下测得,孔径分布曲线由BJH方法拟合得到。
1.6 催化反应活性评价
将100 mg CeO2催化剂样品加入到含有0.5 mmol苯甲醇、0.6 mmol苯胺和2 mL均三甲苯的25 mL高压反应瓶中,60 ℃条件下反应,所得反应产物经离心过滤后使用乙酸乙酯稀释。采用气相色谱-质谱法和气相色谱法对反应产物进行测定分析。
1.7 DFT理论计算
通过基于平面波基组的Vienna Ab-initio Simulation Package(VASP)软件对CeO2进行DFT模拟。交换相关泛函采用广义梯度近似(GGA)的Perdew-Burke-Ernzerhof(PBE)泛函数。平面波截断能设为400 eV,并考虑自旋极化的影响[30]。范德华相互作用采用PBE-D3法进行矫正。CeO2体相模型采用16×16×16的Monkhorst-PackK点进行单点计算获得。能量与体积关系经三阶 Birch-Murnaghan 等温拟合后得到CeO2最优晶胞体积;在此基础上建立一个(2×3)五层Slab模型模拟CeO2(110)面,底部两层固定。使用20 nm的真空层分离周期性镜像。Slab计算在z方向上考虑偶极矫正。K点使用1×1×1的Gamma点。对苯甲醇的计算采用20 nm×20 nm×20 nm晶胞和1×1×1 Gamma点。所有电子自洽场迭代的能量收敛标准为10-5eV。
2 结果与讨论
2.1 催化剂制备与表面氧缺陷浓度调控
通过水热法成功合成了NR-CeO2系列催化剂。样品的X射线衍射图谱(图2)表明,制备的NR-CeO2、NR-CeO2-R1、NR-CeO2-R2、NR-CeO2-300、NR-CeO2-500催化剂均具有典型的立方萤石晶体结构。样品的透射电镜图像表明,制备的NR-CeO2催化剂具有典型的纳米棒结构(图3a),其平均直径为(8.83±1.49)nm,平均长度为(171.65±39.25)nm。与此同时,NR-CeO2催化剂在表面处理过程中能够保持物相和形貌特征稳定,处理后的NR-CeO2-300(图3b)、NR-CeO2-500(图3c)、NR-CeO2-R1(图3d)和NR-CeO2-R2(图3e)催化剂均具有良好的纳米棒形貌。NR-CeO2催化剂经不同处理后的比表面积在98.5~114.2 m2/g范围内,与处理前催化剂的比表面积相比变化不大(图4)。

图2 NR-CeO2系列催化剂的XRD图谱Fig.2 XRD patterns of various NR-CeO2 catalysts

图3 NR-CeO2系列催化剂的TEM图像Fig.3 TEM images of various NR-CeO2 catalysts
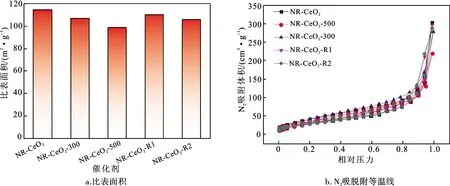
图4 NR-CeO2系列催化剂的比表面积与N2吸脱附等温线Fig.4 Specific surface areas and N2 adsorption-desorption isotherms of various NR-CeO2 catalysts
拉曼光谱被广泛应用于CeO2中氧缺陷浓度的表征。一般认为,拉曼光谱中位于600 cm-1处的弱峰对应于CeO2结构中Ce3+导致的固有氧空位振动,位于460 cm-1处的峰对应于CeO2晶格中Ce-O的对称收缩震动,即F2g模式。由催化剂样品的拉曼光谱谱图(图5a)可以看出,NR-CeO2在600 cm-1处具有明显的特征峰,表明其具有一定量的表面氧缺陷。相比于NR-CeO2催化剂,NR-CeO2-300和NR-CeO2-500催化剂在600 cm-1处的峰强度明显减弱,说明在空气中煅烧2 h后催化剂表面Ce3+被氧化为Ce4+,表面氧缺陷浓度降低。此外,NR-CeO2-500催化剂在600 cm-1处的峰强度低于NR-CeO2-300催化剂,说明煅烧温度越高,催化剂的氧化程度越高,表面氧缺陷浓度下降越明显。利用抗坏血酸对NR-CeO2催化剂进行处理,可有效地将Ce4+还原为Ce3+,使催化剂的表面氧缺陷浓度增加[28-29]。相比于NR-CeO2催化剂,NR-CeO2-R1和NR-CeO2-R2催化剂在600 cm-1处的峰强度显著增强,说明通过抗坏血酸处理可以实现CeO2表面氧缺陷浓度的提升。
拉曼光谱中600 cm-1处的峰面积与460 cm-1处的峰面积之比(A600/A460)能够直接反映CeO2的表面氧缺陷浓度。具体来说,A600/A460值越大,CeO2表面氧缺陷浓度越高;反之则越低。如图5b所示,NR-CeO2系列催化剂的A600/A460值从大到小依次为NR-CeO2-R2、NR-CeO2-R1、NR-CeO2、NR-CeO2-300、NR-CeO2-500,该顺序也代表各催化剂表面的氧缺陷浓度顺序,其中,NR-CeO2-R2催化剂具有最大表面氧缺陷浓度,而NR-CeO2-500催化剂具有最小表面氧缺陷浓度。
利用XPS技术对CeO2的Ce 3d峰进行测试和拟合[31-35],获得NR-CeO2系列催化剂的表面Ce3+/Ce4+摩尔比例,并根据Ce3+/Ce4+摩尔比例与表面氧缺陷浓度的正相关性[27],达到表征CeO2表面氧缺陷浓度的目的。Ce 3d谱图中u、v、u″、v″、u‴、v‴峰归属于Ce4+物种,而u′、v′峰归属于Ce3+物种(图5c)。由XPS分析结果(图5d)可知,相比于NR-CeO2催化剂的表面Ce3+/Ce4+摩尔比例23.4%,经抗坏血酸处理后的NR-CeO2-R1和NR-CeO2-R2催化剂的表面Ce3+/Ce4+摩尔比例分别增加至30.2%和40.1%,经高温处理后的NR-CeO2-300和NR-CeO2-500催化剂的表面Ce3+/Ce4+摩尔比例分别降至16.9%和12.5%。上述Ce3+/Ce4+摩尔比例所反映出的表面氧缺陷浓度结果与拉曼光谱表征的氧缺陷浓度结果一致。

图5 NR-CeO2系列催化剂的表面氧缺陷浓度表征Fig.5 Characterization of oxygen defects of various NR-CeO2 catalysts
进一步通过XPS技术对CeO2的O 1s峰进行表征,确定CeO2表面Ce3+-O(531.2 eV)在所有氧物种中所占摩尔比例,结果如图5e和5f所示。NR-CeO2催化剂的Ce3+-O摩尔比例为20.6%,NR-CeO2-R1和NR-CeO2-R2催化剂的Ce3+-O摩尔比例分别增加至27.1%和 35.4%,而NR-CeO2-300 和NR-CeO2-500催化剂的Ce3+-O摩尔比例分别降至15.5%和10.2%。该结果中各催化剂表面活性氧的数量变化与前述表面Ce3+/Ce4+摩尔比例的变化具有一致性。
综上,通过不同表面处理技术制备的一系列CeO2催化剂具有相同的形貌、相近的比表面积及不同的表面Ce3+/Ce4+摩尔比例,为系统研究氧缺陷浓度在醇和胺氧化偶联反应中的作用机制创造了条件。
2.2 CeO2表面氧缺陷对催化性能的影响
以苯甲醇和苯胺氧化偶联合成N-苄叉苯胺为反应模型,研究CeO2氧缺陷在该类反应中的作用机理。模型反应的优化溶剂为均三甲苯,反应温度为333 K。如图6a所示,所有NR-CeO2催化剂对苯甲醇和苯胺合成N-苄叉苯胺反应都具有催化活性,但在相同反应条件下,NR-CeO2催化剂的催化活性最高。以12 h反应为例,NR-CeO2催化剂的苯甲醇转化率为99.5%;表面Ce3+/Ce4+摩尔比较低的NR-CeO2-300和NR2-CeO2-500催化剂的苯甲醇转化率分别为67%和 61%;表面Ce3+/Ce4+摩尔比较高的NR-CeO2-R1和NR-CeO2-R2催化剂的苯甲醇转化率分别为52%和19%。为了进一步明确CeO2表面氧缺陷浓度与反应活性之间的相关性,分析了反应速率与催化剂表面Ce3+/Ce4+摩尔比的关系,结果如图6b所示。随着催化剂表面Ce3+/Ce4+摩尔比的增加,苯甲醇和苯胺氧化偶联生成亚胺的反应速率先增大后减小,呈现出典型的“火山线”规律。
据先前研究报道,CeO2的表面氧缺陷浓度越高,其对苯甲醇和苯胺氧化偶联反应的催化活性越强,反应越快[8-9]。但在本反应体系中,具有最高表面Ce3+/Ce4+摩尔比的NR-CeO2-R2催化剂表现出最低催化活性,催化剂的催化活性并没有随着表面Ce3+/Ce4+摩尔比的增加而一直增加。为进一步明确催化剂表面Ce3+/Ce4+摩尔比对催化反应的影响,将NR-CeO2-R1和NR-CeO2-R2催化剂在300 ℃空气中煅烧2 h以降低二者的表面Ce3+/Ce4+摩尔比,所得催化剂NR-CeO2-R1-300和NR-CeO2-R2-300在相同条件下反应4 h的苯甲醇转化率分别为34.5%和40.7%(图6c),显著高于未经高温处理的NR-CeO2-R1(25%)和NR-CeO2-R2(11%)催化剂。可见,氧缺陷浓度高的催化剂经高温处理后,其表面Ce3+/Ce4+摩尔比降低,但催化活性增加。该结果提示仅用表面氧缺陷浓度来解释CeO2催化剂的催化活性是片面的。在“火山线”的上升区间,随着催化剂表面Ce3+/Ce4+摩尔比的增加,催化剂活化氧气的能力增强,催化活性增加;当Ce3+/Ce4+摩尔比增加至一定程度时,推测催化剂活化氧气的能力已经不是影响催化活性的主要因素,而反应底物在催化剂表面的吸脱附成为影响催化活性的最主要原因。

图6 NR-CeO2系列催化剂的催化活性Fig.6 Catalytic activities of various NR-CeO2 catalysts
苯甲醇在金属氧化物(包括CeO2)表面通常以苯基甲氧基的形式进行吸附[33-37]。在该吸附构型中,苯甲醇的O原子与CeO2表面铈阳离子成键,因此采用DFT计算进一步分析苯甲醇在CeO2表面的吸附行为(图7)。首先,在CeO2完美的(110)表面,优化后的苯基甲氧基只吸附在Ce原子顶部,吸附能(-1.725 eV)相对较弱,苯甲醇得不到有效活化。当O原子从氧化铈表面移除并形成1个表面氧缺陷时,O空位附近会同时形成2个Ce3+原子,此时苯基甲氧基既可以吸附在Ce3+顶部,也可以吸附在2个Ce3+原子之间的桥接位置。当苯基甲氧基吸附在顶部位置时,该处的Ce3+会将1个电子转移到苯基甲氧基的O原子上,在形成Ce4+的同时增强苯基甲氧基的吸附能力,同时苯基甲氧基的C—H键键长被活化拉伸至0.111 2 nm。在此吸附构型下,反应物的吸附能力增强,C—H键得到有效活化,催化剂的催化性能更佳。这与催化反应活性随着CeO2表面氧缺陷浓度的增加而增强的实验结果一致。相比于吸附在顶部位置的苯基甲氧基,吸附在桥接位置的苯基甲氧基吸附能也较大,但其C—H键键长仅有0.110 9 nm,活化程度较弱。随着CeO2表面Ce3+/Ce4+摩尔比的进一步增加,桥接位置的活性位点数量增多,苯基甲氧基更容易吸附在桥接位置,所以对C—H键的活化较弱,不利于催化性能提高。
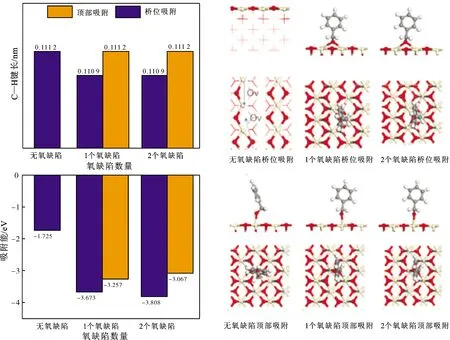
图7 苯甲醇在CeO2(110)面上的吸附Fig.7 The adsorption of benzyl alcohol on CeO2 (110) surface
3 结语
通过表面工程策略制备出一系列具有相同形貌和比表面积、不同Ce3+/Ce4+摩尔比的NR-CeO2催化剂。在苯甲醇和苯胺氧化偶联反应中,CeO2表面Ce3+/Ce4+摩尔比(氧缺陷浓度)与催化反应活性之间呈现出典型的“火山线”关系。CeO2表面Ce3+/Ce4+摩尔比的增加一方面能够增强催化剂的活化氧能力,促进催化反应进行;另一方面也会增加苯甲醇在催化剂上的吸附强度,降低反应活性。上述两方面因素的共同作用使CeO2表面Ce3+/Ce4+摩尔比与催化反应活性之间表现出“火山线”关系。本研究结果有助于理解CeO2基催化剂表面氧缺陷在氧化反应中的作用机制,并为氧化反应的催化剂设计提供了参考。
