铁基氮化物在储能及电催化领域中的研究进展
2022-03-18徐文莉陈永婷李轩科
黄 强,孙 兵,徐文莉,丛 野,陈永婷,朱 辉,李轩科,张 琴
(武汉科技大学,煤炭转化与新型碳材料湖北省重点实验室,武汉 430081)
0 引 言
随着化石燃料的枯竭和环境污染的加重,清洁可再生能源在新能源产业中将扮演越来越重要的角色,因此能量转化与存储技术的应用成为新能源产业发展不可或缺的关键环节。探索能量密度高、催化活性好、纳米结构可控、高效稳定、储量丰富且成本低廉的催化与储能材料迫在眉睫[1]。在无机化合物材料中,过渡金属氮化物具有高硬度、高熔点、高热导性、耐腐蚀、电子导电性优异以及类铂的电子结构等特性[2]。过渡金属的含量在地壳中占有不小的比重,其中铁是过渡金属中储量最为丰富的元素之一,使用寿命长、工作温度范围广,因此铁基氮化物在储能与电催化等众多领域中有着极大的应用前景。
图1 铁基氮化物在储能及电催化领域中的应用Fig.1 Applications of iron-based nitrides in energy storage and electrocatalysis
目前,根据前驱体的获得方式,将制备方法大体分为两类:物理法和化学法。物理法主要包括球磨法、直流电弧放电法、脉冲激光沉积、静电纺丝等;化学法最常用的是水热法。当用作二次电池负极材料时,氮化铁的理论容量和能量密度都显著高于石墨电极材料,具有低而平的充放电电位平台,并且支持快速充电技术,此外还提供强大的多硫化锂吸附能力以防止穿梭效应,能促进界面电荷转移从而加速氧化还原动力学,因此是近年来锂离子电池(LIBs)、钠离子电池(SIBs)和锂硫电池(LSBs)等二次电池负极材料研究的热点之一[3]。此外,高熔点、耐腐蚀和优秀的化学稳定性有利于氮化铁材料在潮湿及腐蚀环境中稳定工作,使其在氢析出反应(HER)、氧析出反应(OER)和氧还原反应(ORR)等过程中表现出的巨大的应用潜力[4-5]。因此,本综述重点关注铁基氮化物的常用制备方法及其在能源相关领域的应用(见图1)。另外,本文也总结了铁基氮化物存在的主要问题,并对其未来研究方向和应用前景进行了展望。
1 氮化铁的结构
铁基氮化物主要包括Fe2N、Fe3N、Fe4N以及S、P掺杂的FexNC材料等,氮化铁是由氮原子插入到金属铁晶格中而形成的一种间隙化合物[6],如图2所示,具有共价化合物、离子晶体和过渡金属的性质。从结构上来看,氮原子的插入会导致金属铁的晶格扩张,d轨道收缩,电子云密度增大,费米能级附近态密度增大,与金属铂的电子结构特征类似,赋予了氮化铁类似于第Ⅷ族贵金属的催化活性[7]。氮化铁中同时包含了金属键、共价键和离子键[3],而这样的价键特点也赋予了氮化铁独特的理化性质,使其具有优异的导电性、催化活性以及化学稳定性。此外,氮化铁和反应物之间具有良好的吸附,同时化学惰性使其可以在很宽的酸碱度范围内工作。这些优点为铁基氮化物在储能与电催化领域广泛应用奠定了基础。
2 铁基氮化物的制备
氮化铁因其独特的理化性质、优异的导电性和催化活性以及宽广的应用范围吸引了研究人员持续关注,一般而言,按照氮化铁前驱体的制备方法大体上可以分为物理法和化学法两大类[8]。

表1 铁基氮化物的不同制备方法对比Table 1 Comparison of different preparation methods of iron-based nitrides
2.1 物理法
在物理法中,球磨法[9]、直流电弧放电法[11]、脉冲激光沉积[17]、静电纺丝[12]等是运用最多的合成方法,这些物理方法通常具有操作简单、易于控制、效率高的优点,同时制备得到的氮化铁具有较好的结晶性。Tammeveski等[9]以1,10-菲咯啉和乙酸铁(Ⅱ)为原料,采用球磨的方法合成了FeN-C作为催化剂,增加了阴离子交换膜燃料电池中的阴极层的传质性能和ORR活性,在0.9 V时的ORR活性达到52 mA·cm-2,超过了Pt/C阴极的36.5 mA·cm-2。Chen等[10]将纳米Fe3O4和碳纳米管(CNTs)分散在正己烷中,经过超声、搅拌、离心分离得到Fe3O4/CNTs样品。通过在400 ℃、500 ℃和600 ℃下氨气(10 mL·min-1)氛围中原位氮化2 h,制备了CNTs负载的纳米Fe2N催化剂(见图3(a))。这种湿法浸渍-氮化法制备Fe2N/CNTs的产率高,同时,通过调节Fe3O4与CNTs的比例可以有效调节Fe2N的负载量。Cao等[11]通过直流电弧放电法在混合气氛(体积比为1∶2的甲烷和氩气)中,90 A电流下将铁块蒸发成纳米颗粒得到Fe@C核壳纳米颗粒,然后将其在400 ℃下氮化1 h得到具有独特核壳结构的Fe3N@C纳米颗粒(见图3(b))。这种方法制备的Fe3N@C具有很高的结晶性,碳壳的包覆使得Fe3N颗粒具有均一的尺寸和形貌以及良好的分散性,避免了颗粒烧结现象。同时,碳壳可以缓解Fe3N材料的体积效应,在长时间的充放电过程中表现出优异的循环稳定性。Lou等[12]利用静电纺丝法,将亚微米级的Fe2O3颗粒掺入聚丙烯腈(PAN)纤维中,制备出了项链状Fe3N@C核壳结构(见图3(c))。相互交联的纳米项链三维网络具有出色的电子导电性。目前物理法制备氮化铁的技术已经较为成熟,虽然工序步骤简洁,操作方法简单,但是物理法不可避免地要用到高能或放电装置,不够环保经济。

图3 氮化铁的制备示意图Fig.3 Schematic diagram of the preparation process of iron nitride
2.2 化学法
化学法是利用铁基前驱体与氮源(常见的氮源有氮气、氨气及尿素等)在高温环境(800~2 000 ℃)下进行反应得到氮化铁[18]。铁基前驱体主要包括铁基络合物、铁基氧化物以及各种铁基盐等。相比物理方法而言,化学法是制备铁基氮化物的一类更加普遍适用的方法(见表1),并且化学法制备过程更加简单,最常见的方法是水热法,目前已经得到广泛的应用。Jin等[13]通过水热法,在100 ℃合成了粒径均匀的Fe2O3微立方体,然后通过多巴胺的原位聚合形成Fe2O3@PDA核壳微立方体结构,最后在NH3气氛中于500 ℃下氮化得到Fe2N@C(见图3(d))。由于完全封装在碳壳中,可以避免Fe2N被空气氧化。立方体中适当的内部空隙有助于缓解其锂化/脱锂过程中的体积效应。Zou等[19]以Fe(NO3)3·9H2O和均苯三甲酸分别为铁源和碳源,在120 ℃下醇热24 h得到MOX-Fe(MOF-based xerogels)。后经惰性气体中煅烧、酸处理等工序得到N、S双掺杂碳基底负载的Fe2N(见图3(e),N、S、C和F分别代表氮、硫、碳和铁)。化学法通常更容易得到性能更高的Fe2N,并且可以有效调控其组成和结构,得到杂原子掺杂和特定结构的铁基氮化物材料。化学法制备铁基氮化物除了水热法还有还原氮化法[14]、气相沉积法[15]、高温热法[16]等。Wu等[14]采用还原氮化法制备了限制在三维超薄碳纳米片框架中的石墨烯包封的Fe2N,缓解了结构粉化和空气敏感性。Fan等[15]通过气相沉积法获得铁基前驱体,并在氨气氛围中退火合成了均匀的Fe2N-Ti2N,氮化后纳米棒形貌几乎没有变化。Liu等利用高温热法制备了核壳Fe3N@C用于钠离子电池,在2 000次循环显示出94.9%的高容量保持率。
3 铁基氮化物在储能领域中的研究进展
成本低廉、理论容量高等优点使得铁基氮化物一直是近年来二次电池负极材料的研究热点之一,但是氮化铁在充放电循环过程中存在严重的体积效应,导致其活性成分发生粉化、开裂和剥落,材料结构被破坏,大大降低了电极的循环稳定性[20]。针对这个问题目前常用的两种解决方案:(1)将其纳米化[21],即降低氮化铁的颗粒尺寸到纳米级,这样不仅可以减小循环过程中的体积变化,提高循环稳定性,还可以缩短离子扩散路径;(2)将氮化铁与导电材料(如石墨烯/氧化石墨烯、CNTs、碳纤维和多孔碳等碳材料)复合[22],这种策略不仅能够将氮化铁均匀分散在碳材料表面,为其预留一定的膨胀空间,同时也能够提高材料的电子和离子传导速度[23]。
本节将详细概述铁基氮化物在能量存储领域的应用,重点是可充电电池(LIBs、SIBs、LSBs)方面的研究进展。铁基氮化物在该领域的研究进展如表2所示。
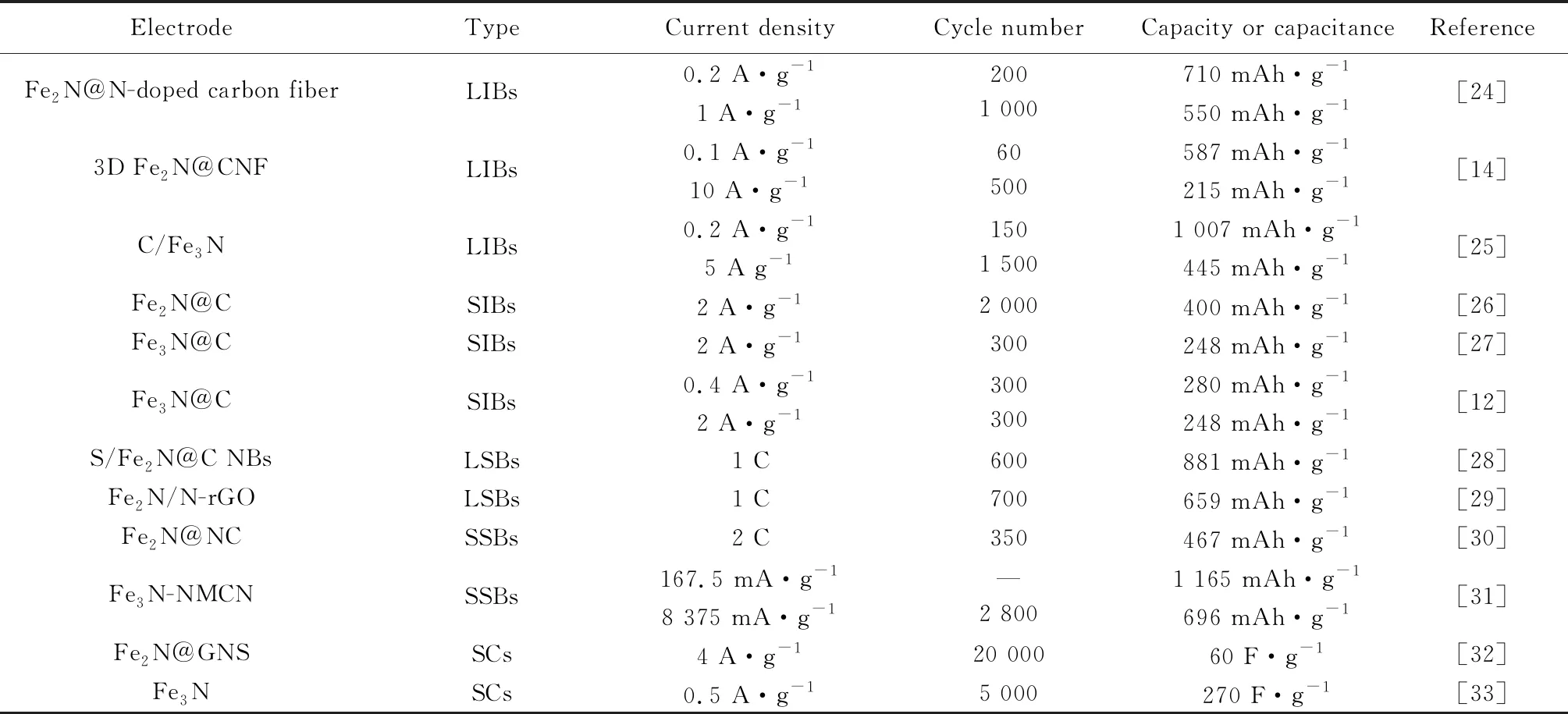
表2 铁基氮化物在储能领域中的性能比较Table 2 Comparison of iron-based nitrides for rechargeable battery applications
3.1 铁基氮化物在锂离子电池中的研究进展
因为具有寿命长、容量高和能效高的优点,锂离子电池一直主导着便携式电子产品和电动汽车的电源市场[34],而电极材料则是决定其电化学性能的关键成分。在各种电极材料中,Fe2N不仅成本低,分子量也相对较低[35],具有比石墨(372 mAh·g-1)更高的理论容量(900 mAh·g-1)[36]。其面临的主要问题是体积膨胀和固体电解质界面膜(SEI膜)不稳定所导致的电池循环寿命短。另外,对空气敏感的Fe2N[37]的表面容易氧化导致锂离子传输的动力被削弱。
针对这些问题,通过纳米结构设计来实现薄而稳定的SEI层,通过碳涂层来有效缓解电极的体积变化,是改善铁基氮化物负极锂存储性能最有前途的策略。如Wu等[14]制备了包覆在三维碳纳米片中Fe2N纳米颗粒(3D Fe2N@CNF,见图4(a)~(b),在0.1 A·g-1电流密度下显示出587 mAh·g-1的高可逆容量,在10 A·g-1的电流密度时显示出215 mAh·g-1的高倍率容量(见图4(c)),并且在2 A·g-1的电流密度下500次循环后仍具有很好的稳定性(见图4(f)),图4(d)表明赝电容贡献极大,显示出很大的实际应用潜力。这种3D Fe2N@CNF材料具有独特的优势(见图4(e)):(1)石墨烯壳可以很好地保护超小Fe2N核(<50 nm)免于氧化,并缓解充电放电循环期间的体积变化,极大地提高了材料的循环稳定性;(2)具有大孔隙3D互连框架的碳纳米片将分散的Fe2N纳米颗粒高度暴露于电解质中,缩短了锂离子扩散距离,提高了活性材料的利用率;(3)这种结构同时也极大地加快了电子传输,并使电解质易于扩散到内部电极中,从而改善了反应动力学[38]。Yang等[25]以蛋清蛋白为碳源和氮源,加入NaCl和Fe(NO3)3·9H2O溶液,通过冷冻干燥及原位氮化工艺成功地将Fe3N纳米粒子锚定在分级多孔碳上(C/Fe3N,见图4(g))。如图4(h)所示,这种C/Fe3N材料作锂离子电池负极时,在0.2 A·g-1的电流密度下经过150次循环后仍然显示出1 007 mAh·g-1的可逆容量,在5 A·g-1的高电流密度下经过1 500次循环后仍保持444.8 mAh·g-1的高可逆容量(见图4(i))。如此优异的性能是因为碳基体不仅可以提高材料整体的导电性,还能够对充放电过程中Fe3N纳米粒子的体积变化起到缓冲作用[39],提高循环稳定性。由于稳定的相变,Fe3N表现出赝电容行为[13],使电极具有了更高的能量密度。类似的策略还有很多,各种结构的铁基氮化物在稳定性上取得了一定的成果。
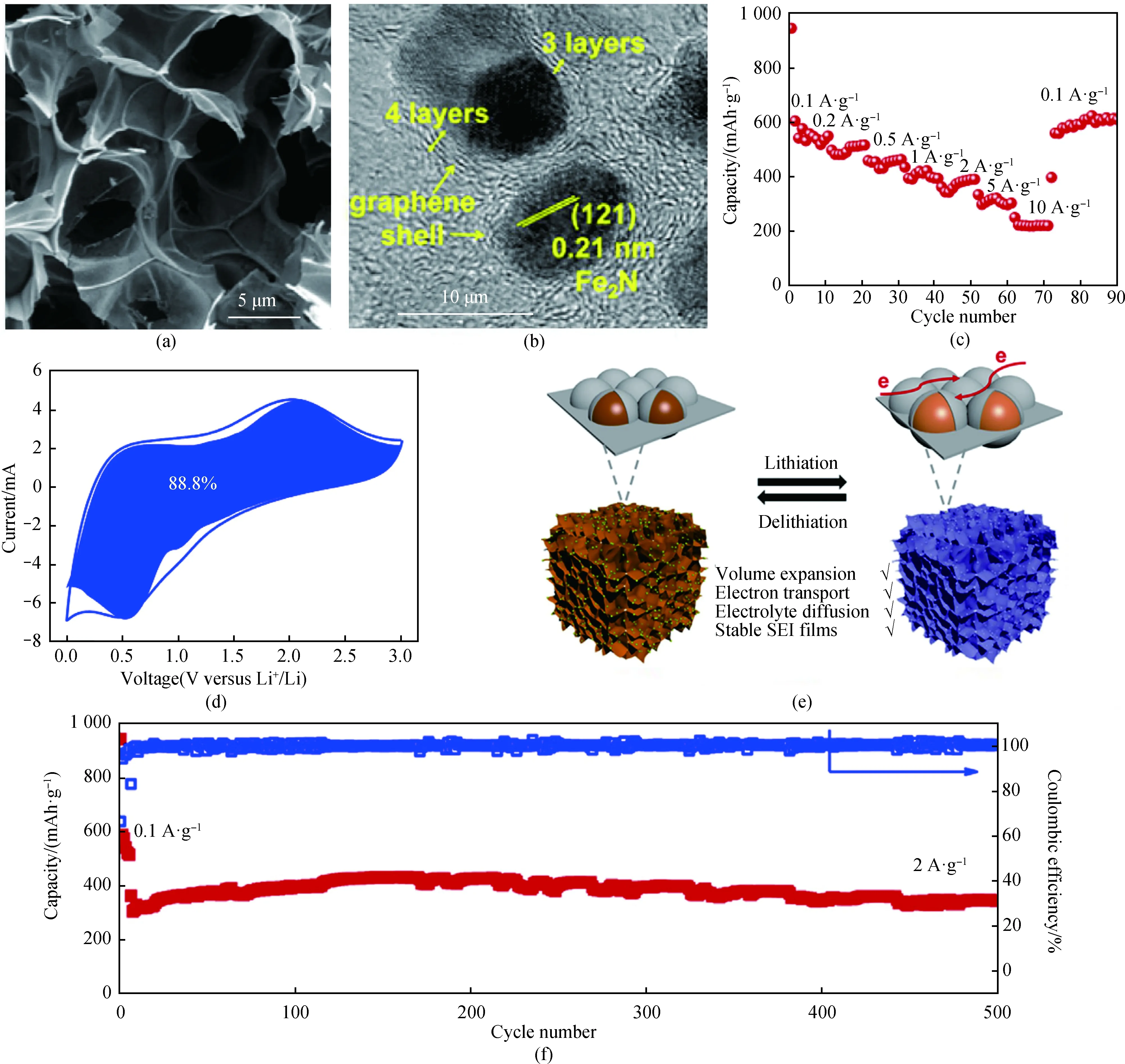
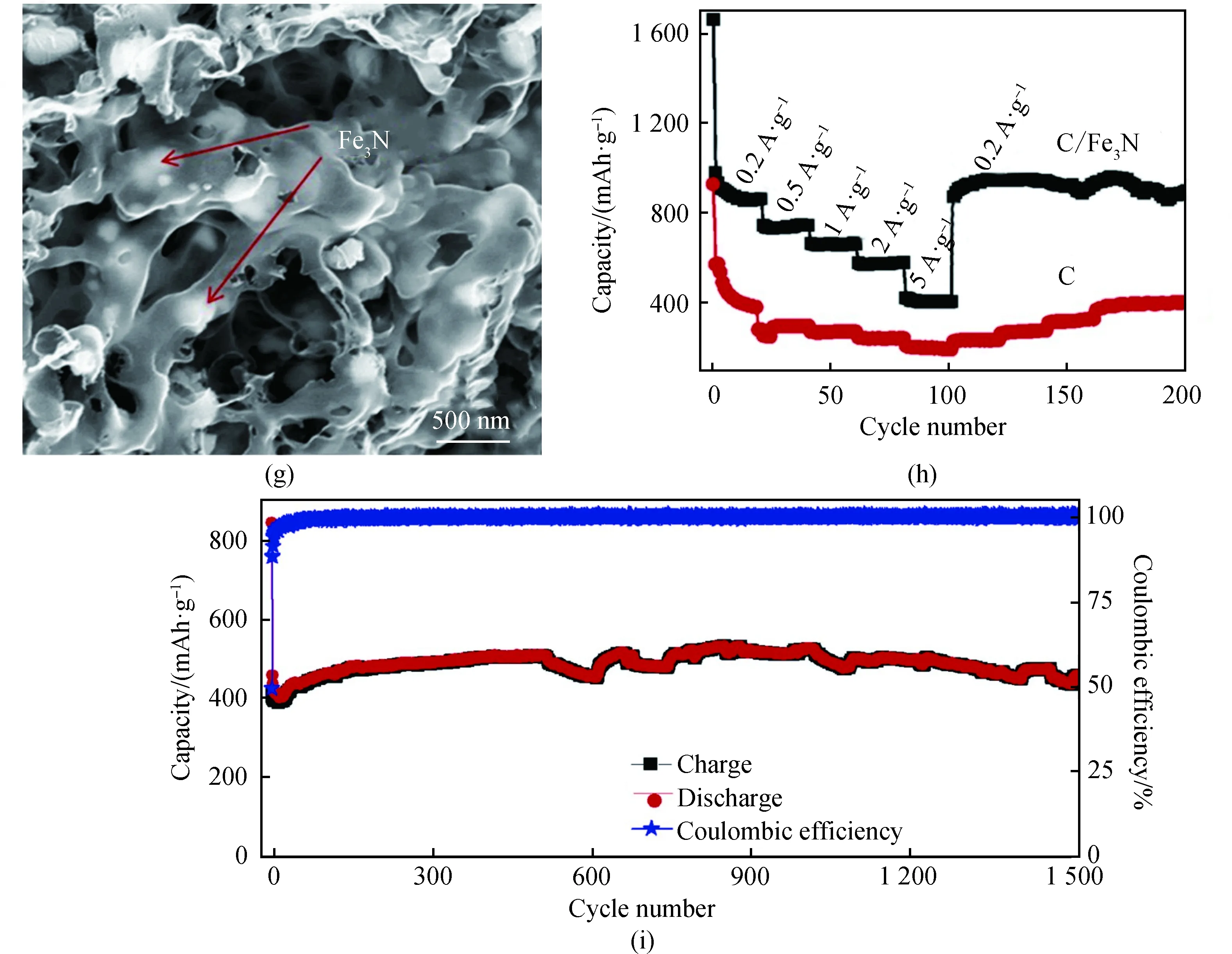
图4 铁基氮化物在LIBs中的应用。3D Fe2N@CNF[14]:(a)SEM照片;(b)TEM照片;(c)倍率性能;(d)赝电容贡献;(e)锂存储机制示意图;(f)循环性能。C/Fe3N[25]:(g)SEM照片;(h)倍率性能;(i)循环性能Fig.4 Application of iron-based nitrides in LIBs. The application of 3D Fe2N@CNF in LIB[14]: (a) SEM image;(b) TEM image; (c) rate performance; (d) pseudocapacitive contribution; (e) schematic illustration of the lithium storage mechanism; (f) cycle performance. Application of C/Fe3N in LIB[25]: (g) SEM image; (h) rate performance; (i) cycle performance
3.2 铁基氮化物在钠离子电池中的研究进展
由于锂的资源有限、成本较高以及安全问题,目前的商用锂离子电池不能满足大规模功耗的需求,因而具有低成本、资源丰富、环境友好和类似储能机制[40]的钠离子电池[41]已成为最有潜力的候选者。到目前为止,钠离子电池负极材料使用的大多数是金属氧化物、金属硫化物以及碳基材料,存在循环性能差或能量密度低的问题[42]。例如与还原的氧化石墨烯复合的Fe2O3,在100 mA·g-1和500 mA·g-1的电流密度时分别显示出250 mAh·g-1和30 mAh·g-1的容量,过大的体积变化导致了严重的容量衰减,而纯Fe2O3的性能更差。相比而言,铁基氮化物负极由于高容量和高离子迁移率而显示出良好的循环性能和稳定性,例如Wang等[43]制备的珊瑚状Fe2N@C纳米材料在100 mA·g-1和500 mA·g-1的电流密度时分别显示出100 mAh·g-1和75 mAh·g-1的容量,具有良好的稳定性和倍率性能。由此可见,铁基氮化物在钠离子电池中具有巨大的应用潜力。
Huang等[26]设计了填充有中空Fe2N@NC纳米立方体的杂化纤维(CSHN,见图5(a)),用于钠离子电池的新型自支撑阳极。在100 mA·g-1的电流密度时显示出545 mAh·g-1的容量。即使在2 A·g-1的电流密度下循环2 000次后容量保持率仍高达95.6%,具有超高的稳定性(见图5(b))。分层碳网络提供了快速的电子路径,并为氮化铁提供了高度保护,减少了暴露于空气的机会(见图5(c))。此外,其多孔性质确保了对体积膨胀的高度缓冲,并改善了循环稳定性。Lou等[12]利用静电纺丝将亚微米级Fe2O3颗粒掺入聚丙烯腈纤维中制备了项链状Fe3N@C核壳结构作为钠离子电池的负极材料。对于单个反应单元,每个Fe3N@C纳米单元都具有良好的核壳结构,可以容纳Fe3N的体积膨胀,从而具有良好的循环稳定性[44];所有单个Fe3N@C单元通过一维碳纤维束在一起,形成二级导电链;在电极层面,所有Fe3N@C纳米项链相互连接,构建了3D网络以实现出色的电子导电性。正是归因于这种多级结构优势,Fe3N@C纳米项链具有高可逆容量,并具有延长的循环寿命和出色的倍率容量,在2 000 mA·g-1和100 mA·g-1的电流密度时分别显示出248 mAh·g-1和356 mAh·g-1的容量。此外由于该材料以自支撑膜的形式存在,因此无需使用黏合剂或导电碳,这不仅提高了整体电极质量比,也避免了复杂的混样和涂布工艺。
3.3 铁基氮化物在锂硫电池中的研究进展
在各种替代电池中,锂硫电池因其理论能量密度高达2 600 Wh·kg-1,明显优于传统的锂离子电池,被认为是最有前途的下一代能量存储设备之一[45]。但是,多硫化锂的穿梭效应和缓慢的氧化还原转化率导致硫利用率低,同时面临着功率密度低和电极寿命短的问题[46]。这些问题可以通过以下策略解决:(1)通过催化提高多硫化锂转化动力学;(2)通过增强多硫化锂的捕获和吸附来减轻穿梭效应[47]。而铁基氮化物具有很高的电子电导率和固有的催化活性,可以成为锂硫电池中良好的宿主候选物。
Zheng等[28]设计了一种多功能的硫掺杂Fe2N碳纳米盒(S/Fe2N@C NBs),高导电的碳壳为快速电子或离子传输提供了有效的途径,其较大的空隙提供了充足的体积变化空间(见图5(d))。由于高硫含量掺杂有效增强了碳主体与多硫化锂之间的相互作用,以及极性Fe2N核对多硫化物具有很强的化学键合能力和有效的催化活性,使得S/Fe2N@C NBs有效地抑制了多硫化锂的溶解和穿梭效应,因此该材料具有较大的初始容量910 mAh·g-1,且200次循环后仍能保持734 mAh·g-1,库仑效率约为99%(见图5(e)~(f))。即使在1 C下进行600次循环后仍可保留881 mAh·g-1的容量,平均衰减率仅为0.036%,这种优异的倍率性能和长循环稳定性可归因于S/Fe2N@C NBs增强的电荷转移动力学和氧化还原反应动力学[48]。Sun等[29]提出了一种由均匀分散在氮掺杂石墨烯上的氮化铁纳米颗粒改性的新型隔膜(Fe2N/N-rGO,见图5(g))。在低温下,Fe2N作为活性催化位点降低了硫化锂的分解能垒,促进了多硫化锂和硫化锂之间的转化动力学;在高温下,Fe2N能够抑制多硫化物的穿梭效应。因此,包含Fe2N/N-rGO的组装电池实现了长循环寿命(1 C下700次循环平均每个循环衰减0.05%)和高倍率性能(见图5(h),5 C下688 mAh·g-1)。更重要的是,这些电池在50 ℃和0 ℃下分别具有1 043 mAh·g-1和778 mAh·g-1的高容量(见图5(i))。该工作为未来锂硫电池的实际应用提供了更广阔的思路。
4 铁基氮化物在电催化领域中的研究进展
非贵金属由于在地壳中储量丰富、化合物种类繁多且合成相对简单,在电催化领域应用潜力很大,引起广泛关注。张迎九等[49]制备的碳纳米管纤维负载镍磷合金(Ni-P/CNTFs)电极在10 mA·cm-2电流密度下具有138 mV的过电势,Tafel斜率为83 mV·dec-1,具有良好的电催化析氢性能和稳定性。并且在保持催化性能不变的前提下,样品可以进行弯曲,扩展了应用领域。王梦晔等[50]制备的包裹Co1-xS和MnS纳米颗粒的碳纳米管(Co1-xS-MnS@CNTs/CNFs),具有优异的电催化氧还原性能,其甲醇耐受性及长期稳定性显著优于商业Pt/C电催化剂。
铁基氮化物不仅在储能领域有着广泛研究,而且在电催化领域也表现出巨大的应用潜力。高熔点、耐腐蚀和优秀的化学稳定性有利于铁基氮化物在潮湿及腐蚀环境中稳定工作,尤其是氮化铁还具有类铂电子结构的特点,使其在HER、OER和ORR等电催化过程具有更大的优势。本节将着重介绍铁基氮化物在电催化方面的研究进展。铁基氮化物在HER和OER中的应用如表3所示。
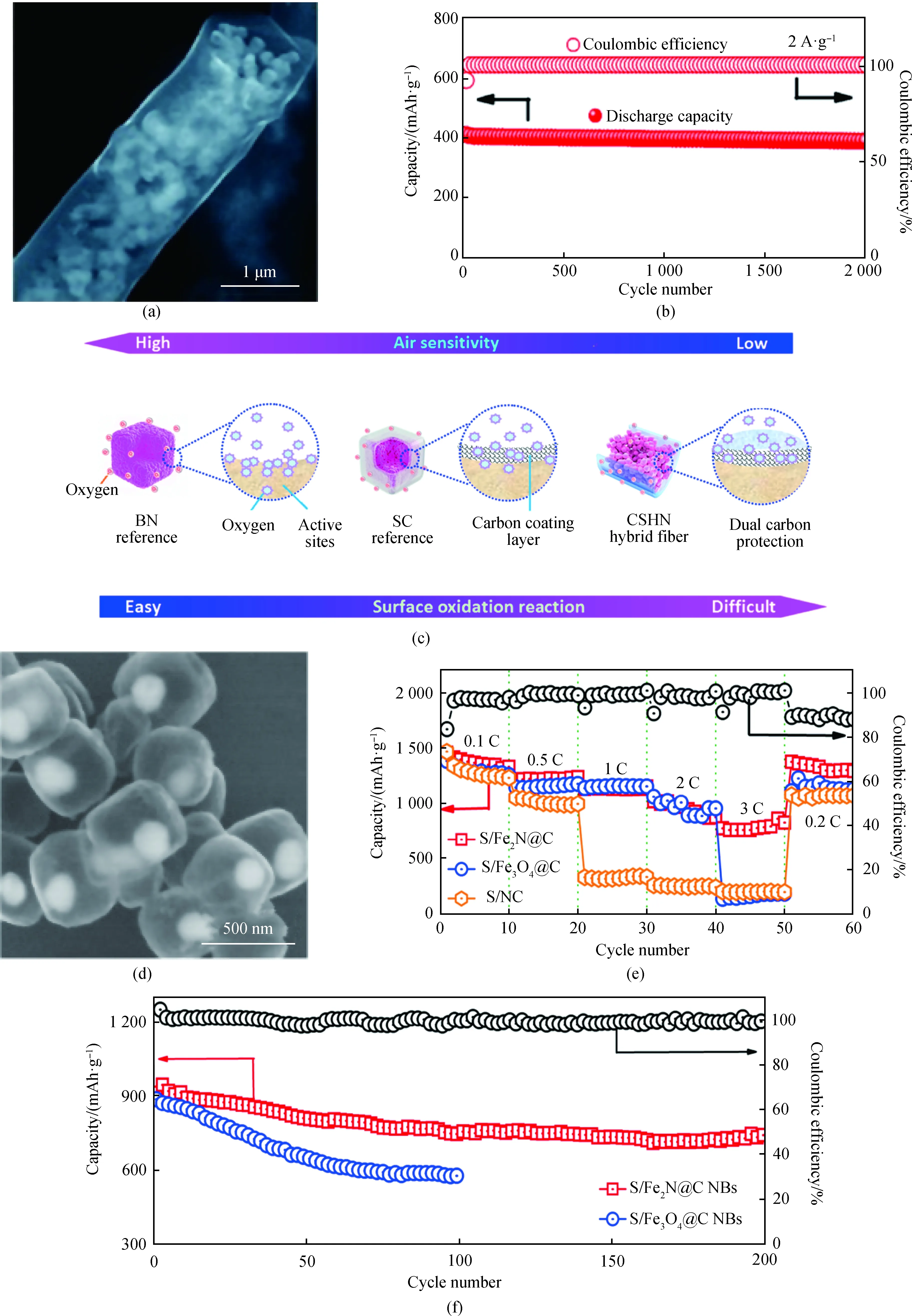

图5 铁基氮化物在SIBs和LSBs中的应用。CSHN在SIB中的应用[26]:(a)SEM照片;(b)循环性能;(c)不同空气敏感性的BN、SC和CSHN样品示意图。S/Fe2N@C NBs在LSB中的应用[28]:(d)SEM照片;(e)倍率性能;(f)循环性能。Fe2N/N-rGO在LSB中的应用[29]:(g)TEM照片;(h)倍率性能;(i)循环性能Fig.5 Application of iron-based nitrides in SIBs and LSBs. The application of CSHN in SIB[26]: (a) SEM image; (b) rate performance; (c) schematic illustrations of the BN, SC, and CSHN samples with different air sensitivities. The application of S/Fe2N@C NBs in LSB[28]: (d) SEM image; (e) rate performance; (f) cycle performance. The application of Fe2N/N-rGO in LSB[29]: (g) TEM image; (h) rate performance; (i) cycle performance
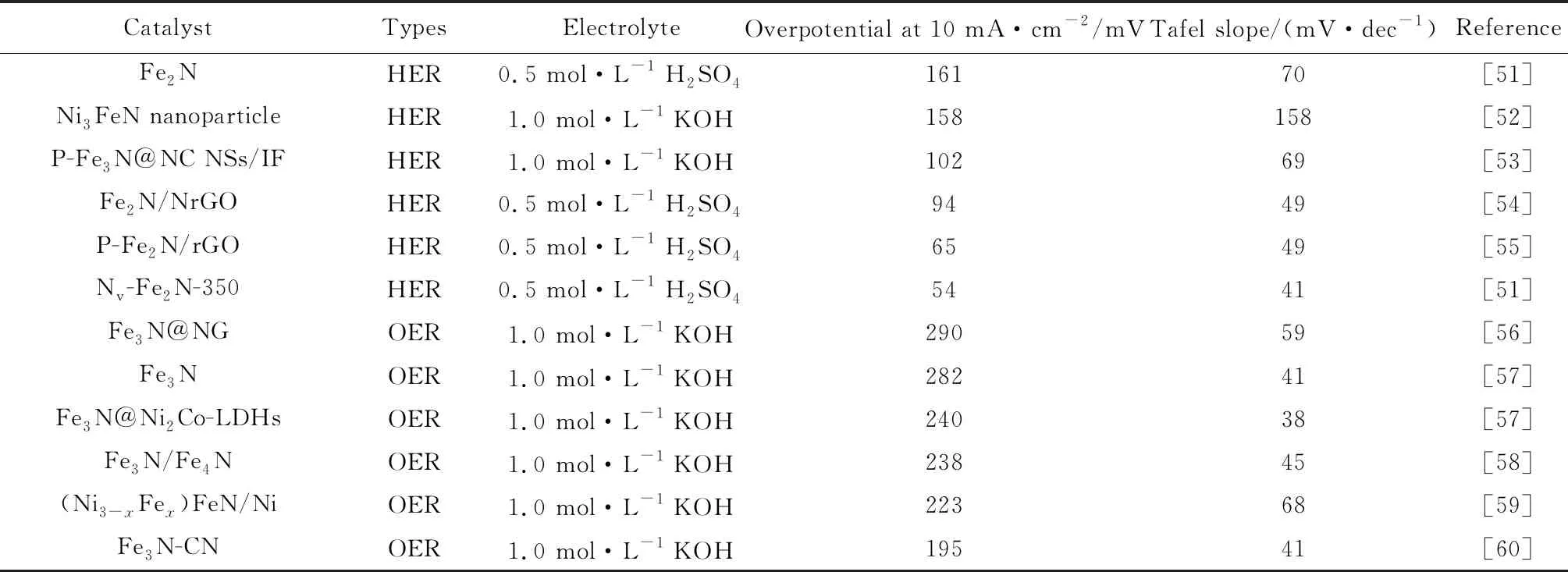
表3 铁基氮化物在HER和OER中的应用Table 3 Application of iron-based nitrides in HER and OER
4.1 铁基氮化物在氢析出反应中的研究进展
氢析出反应(HER)是水电解过程中的一种反应,它将可再生能源产生的间歇性电能转化为氢。目前最高效的析氢催化剂是铂基催化剂,但高成本严重制约了其大规模使用。最近,由于具有高电导率和类似贵金属的特性,铁基氮化物被普遍认为有望替代铂基催化剂[61]。其中,Fe2N具有很高的HER催化活性,在10 mA·cm-2电流密度下具有94 mV的过电势[54],表现出其作为低成本HER催化剂的巨大潜力。

图6 铁基氮化物在HER中的应用。Nv-Fe2N-350[51]:(a)TEM照片;(b)LSV曲线;(c)Tafel斜率。P-Fe3N@NC NSs/IF[53]:(d)TEM照片;(e)LSV曲线;(f)Tafel斜率Fig.6 Application of iron-based nitrides in HER. Application of Nv-Fe2N-350 in HER[51]: (a) TEM image; (b) LSV curves; (c) Tafel slope. Application of P-Fe3N@NC NSs/IF in HER[53]: (d) TEM image; (e) LSV curves; (f) Tafel slope
Qian等[51]通过空位介导的轨道操纵有效地调节Fe2N的电子偶联用于催化析氢反应。通过在350 ℃的氢气气氛下退火20 min得到了含氮空位的Nv-Fe2N-350催化剂(见图6(a)),在10 mA·cm-2下实现了54 mV的过电位,远超Fe2N(161 mV),甚至接近Pt/C(24 mV)催化剂(见图6(b))。这表明氮空位在促进其催化作用方面起着至关重要的作用。图6(c)显示了Fe2N、Nv-Fe2N-350、Nv-Fe2N-500(于500 ℃氢气气氛下退火得到)和Pt/C的Tafel斜率分别为的70.1 mV·dec-1、41.2 mV·dec-1、68.6 mV·dec-1和29 mV·dec-1。氮空位可以控制活性位的轨道取向以调节电子耦合,并最终调节表面氢的吸附能力。氢气退火处理后Tafel斜率降低,表明析氢动力学得到有效促进[62]。用计时电流法经过连续50 h的测试,电流密度可以保持在初始电流的90%,Nv-Fe2N-350在操作条件下的电化学稳定性非常高,并且稳定性试验后纳米线形态和六方结构得到了很好的保持,进一步证实了纳米线的稳定性。Zhou等[53]通过酿酒酵母的原位氮化制备了在泡沫铁基质上生长的氮掺杂碳纳米片包裹的磷掺杂氮化铁纳米粒子(P-Fe3N@NC NSs/IF,见图6(d)),用酿酒酵母中的C、N和P都替代了危险的CH4、NH3和PH3。从图6(e)极化曲线可以看出,P-Fe3N@NC NSs/IF催化剂在1.0 mol/L KOH溶液中在10 mA·cm-2时的过电势为102 mV,明显低于Fe2O3NSs/IF(159 mV)和铁泡沫(274 mV),并且保持80 h而没有衰减,表现出出色的电催化活性和优异的耐久性。图6(f)显示出P-Fe3N@NC NSs/IF催化剂相应的Tafel斜率68.59 mV·dec-1也小于Fe2O3NSs/IF(91.37 mV·dec-1)和铁泡沫(112.85 mV·dec-1),说明P-Fe3N@NC NSs/IF催化剂具有更快的电催化动力学。铁基氮化物是有希望替代贵金属铂成为HER催化剂的材料之一。
4.2 铁基氮化物在氧析出反应中的研究进展
氧析出反应(OER)是电催化水氧化产生分子氧的过程,在许多能量转换和储存技术中起着重要作用,包括用于制氢的裂解水、再生燃料电池和金属-空气电池[63]。然而OER过程动力学缓慢,因为它涉及多个质子耦合的电子转移步骤[64],因此需要一种有效的催化剂加快OER反应动力学。
Zou等[56]开发了封装在N掺杂石墨烯纳米壳中的Fe3N纳米颗粒(Fe3N@NG)电催化水氧化催化剂。NG纳米壳改善了从Fe3N到NG的界面电子转移过程,形成高价的Fe4+(Fe4+@NG),从而改变了NG外部壳的电子特性,随后将电子从氧中间体转移到NG纳米壳中,显示出铁基OER电催化剂较高的电催化效率。同时,NG纳米壳还保护Fe3N纳米颗粒免于形成OER惰性的Fe2O3,从而提高了OER稳定性。杂原子掺杂仍然是增加活性位点,提高OER催化活性的最常用手段。Ren等[58]在三维高导电石墨烯/镍泡沫上生长了多孔纳米Fe3N/Fe4N薄膜构成的新型催化剂(见图7(a)),这是一种高效、耐用的三维自支撑电极,具有优异的催化性能,电流密度为10 mA·cm-2时其过电位为238 mV(见图7(b)),FexN催化剂的Tafel斜率为44.5 mV·dec-1,远小于载体(91.7 mV·dec-1)和氧化铁催化剂(79.6 mV·dec-1)的Tafel斜率。经过1 000次循环测试后(见图7(c)),纳米多孔FexN催化剂记录的极化曲线与初始极化曲线基本相同,表明没有发生降解。这种高效率的催化剂是迄今为止单一金属(Fe、Co、Ni)基催化剂中比较好的,甚至比基准的IrO2更好。这归功于FexN催化剂与载体之间的快速电荷转移,FexN催化剂的纳米孔结构增加了催化活性中心,以及石墨烯/镍泡沫大孔结构增加了与电解质的接触面积。
4.3 铁基氮化物在氧还原反应中的研究进展
氧还原反应(ORR)主要发生在可再生能源装置,如燃料电池和金属-空气电池的负极[65]。近年来,可充电锌-空气电池由于其高能量密度、低成本和零排放而受到了广泛的研究。在影响锌-空气电池性能的各种组件中,由骨架材料和双功能电催化剂组成的负极是重要因素之一,因为它既能发生氧还原反应,也能发生氧析出反应[66]。在充放电过程中,反应动力学对Zn2+和O2的传输有重要影响,ORR和OER动力学的缓慢,导致了高过电位和低比能[67],从而阻碍了锌-空气电池的商业化,所以适当设计的微观结构可以有效地改善其性能。研究人员开发了一系列高性能、耐用的非贵金属基催化剂[68],其中铁基氮化物由于活性铁和氮掺杂碳之间的协同效应,以及杂原子掺杂可以提供额外的活性位点的优点[69],而被认为是最有前途的催化剂。
Lee等[70]将氮化铁纳米颗粒负载到碳纳米管-石墨烯杂化载体上(FexN/N-CNT-GR,见图7(d))用于氧还原反应。混合碳载体可以提供丰富的锚点和缺陷位置,有效地限制金属和非金属,选择性地产生富氮相的小颗粒,并允许高浓度氮原子在碳晶格中的分布。这种催化剂-载体之间的协同效应使催化剂具有优异的催化活性(见图7(e)),与碱性介质中的Pt/C催化剂相比,其半波电位为0.89 V,具有优异的耐久性(见图7(f))。Xu等[71]利用软模板方法在N掺杂石墨烯碳(NC)表面上原位组装Fe2N纳米颗粒,以用作锌-空气电池催化剂(见图7(g))。Fe2N纳米粒子被几层碳覆盖,这种碳壳的存在可以抑制其膨胀和溶解,同时也促进了Fe2N与石墨烯的连接,从而促进Fe-N-C活性位点的形成。与20%Pt/C催化剂相比,具有高纯度和良好结晶性的Fe2N@NC复合材料对ORR表现出协同增强的催化活性和稳定性(见图7(h)~(i)),比如起始电势(0.084 V)、半波电势(-0.036 V)和高电子转移数(~4e-)。所制得的催化剂被用作锌-空气电池的空气催化剂,其开路电压约为1.48 V,最大功率密度为82.3 mW·cm-2。这些结果表明,在实际的ORR应用中,Fe2N@NC催化剂可以替代珍贵的Pt催化剂。
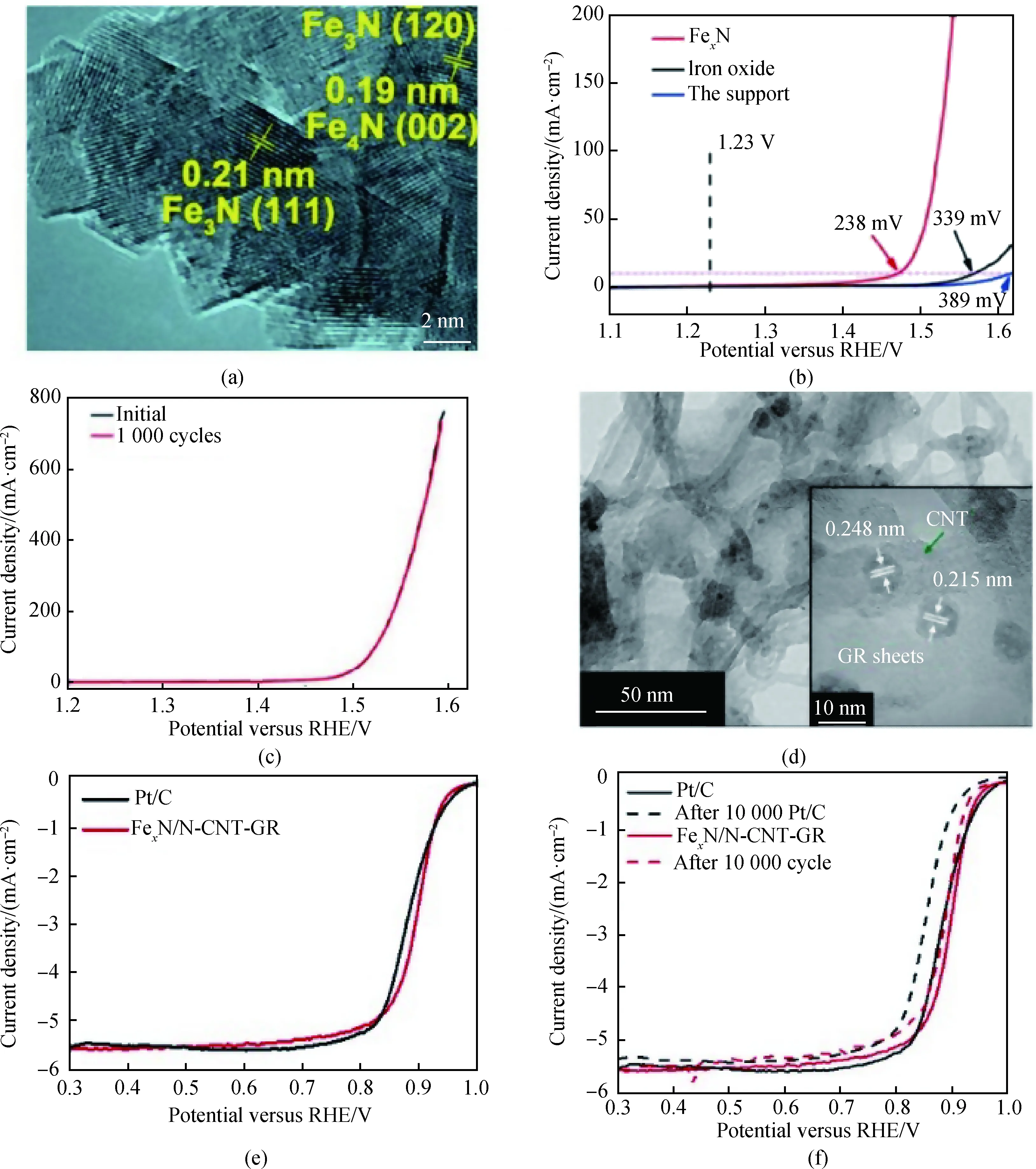

图7 铁基氮化物在OER和ORR中的应用。Fe3N/Fe4N在OER中的应用[58]:(a)TEM照片;(b)极化曲线;(c)长期循环试验。FexN/N-CNT-GR在ORR中的应用[70]:(d)TEM照片;(e)ORR极化曲线;(f)耐久性试验。Fe2N@NC在ORR中的应用[71]:(g)TEM照片;(h)ORR极化曲线;(i)耐久性试验Fig.7 Application of iron-based nitrides in OER and ORR. Application of Fe3N/Fe4N in OER[58]:(a) TEM image; (b) polarization curves; (c) long-term cycle test. Application of FexN/N-CNT-GR in ORR[70]:(d) TEM image; (e) ORR polarization curves; (f) durability test. Application of Fe2N@NC in ORR[71]: (g) TEM image; (h) ORR polarization curve; (i) durability test
5 结语与展望
在过去的几年里,作为电化学能量转换与存储的电极材料,氮化铁因其固有的金属性和与类铂的电子结构等优点被广泛研究。本综述从结构、制备和应用等方面总结了近年来铁基氮化物在能量存储与转化领域的最新研究进展。纯氮化铁材料不足以满足未来应用的高要求,研究人员通过诸如杂原子掺杂、碳材料相复合以及设计适宜结构等手段来改善氮化铁的体积效应、增大比表面积和暴露更多的活性位点,改性后铁基氮化物的储能和催化性能均有较大改善。对于铁基氮化物材料,许多科研人员通过球磨法、水热/溶剂热法、静电纺丝、高温煅烧等方法合成了大量的性能优异的储能和电催化材料。由于氮化铁与复合组分之间的协同作用,复合材料的性能远高于其中的单独组分。短短的几年时间里,铁基氮化物在储能和电催化领域得到了迅速发展,证明其在储能和电催化领域拥有巨大的发展潜力。
然而,尽管以铁基氮化物的研究已取得初步成功,但仍有许多问题和挑战有待解决。在储能应用方面,氮化铁在充放电循环过程中会产生严重的体积效应,大大降低循环稳定性。尽管已有研究人员通过将氮化铁和各种碳材料(石墨烯/氧化石墨烯、CNTs、碳纤维和多孔碳等)复合的方式缓解其体积效应,但是同时也会增大比表面积,增大了形成SEI膜时的消耗,导致首次充放电效率降低。此外,如何有效防止铁基氮化物的氧化也是其工业应用所面临的重要问题。因此,要想得到稳定性良好的铁基氮化物,需要在缓解体积效应的同时保证首次充放电效率。在氮化铁电催化应用方面,进一步探索如何暴露更多的活性位点,促进催化反应的动力学,提高催化活性的同时也增强耐久性,是确保铁基氮化物能持续发展的重要任务之一。
基于目前的研究现状,为铁基氮化物的未来研究方向提供以下几点建议:(1)可以通过创新的理论模拟技术获得更佳的构效关系,这将有助于设计具有更好性能的新材料,更好地研究实时机制以优化材料性能;(2)制备铁基氮化物的合成条件通常需要高温、高压等要求,可以用更温和的合成方案来替代;(3)需要进一步开发创新的合成技术,降低生产成本。制备氮化铁的氮化步骤通常涉及对环境有毒的氨基或氨气,需要探索更环保的合成工艺。
就目前而言,铁基氮化物的应用研究还处于实验室阶段,要想实际运用于工业生产中,不仅需要开发出大规模生产铁基氮化物的高效方法,还需要在性能上再次突破。希望通过广大科研工作者的不懈努力,在理论和实验的协同努力下进一步探索,最终将铁基氮化物投入到工业规模的应用中来发挥其积极作用。
