HPLC法测定人血清中替加环素浓度的建立和临床应用
2022-03-17李文超吴燕川李晓玲白向荣首都医科大学宣武医院药学部国家老年病医学研究中心北京0005首都医科大学药学院北京0005首都医科大学宣武医院中心实验室北京0005
李文超,吴燕川,沈 芊,苏 甦,李晓玲,白向荣(.首都医科大学宣武医院药学部/国家老年病医学研究中心,北京0005;2.首都医科大学药学院,北京 0005;.首都医科大学宣武医院中心实验室,北京 0005)
替加环素(tigecycline,TGC)是甘氨酰四环素类抗生素,具有强大的体外抗菌活性,在临床中多用于治疗多重耐药菌引起的感染[1]。作为一种脂溶性抗生素,替加环素给药后快速分布于体内,血药浓度个体差异性较大[2]。此外,替加环素体内抗菌活性与感染部位、病原体种类以及患者的病理生理状态等密切相关。而多重耐药菌感染的患者病理生理情况通常十分复杂,病情较为严重,因此进行替加环素的治疗药物监测十分必要。故本研究建立了一种高效液相色谱法(high performance liquid chromatography,HPLC)测定替加环素的血药浓度,并将其应用于经该药治疗的多重耐药革兰阴性菌感染的重症患者血清样本分析,以期为后续进行替加环素药动学/药效学研究及开展治疗药物监测奠定基础。
1 仪器与试药
1.1 仪器
Agilent 1200高效液相-可变波长检测系统(HPLC-VWD,安捷伦科技有限公司),包括:G1322A脱气机、G1311A四元泵、G1329A自动进样器、G1316A柱温箱、G1314B可变波长检测器;反相Kromasil C18色谱柱(4.6 mm×150 mm,5 μm);Thermo HERAEUS FRESCO21台式微量高速冷冻离心机[赛默飞世尔科技(中国)有限公司];WH-86I旋涡混合器(江苏太仓鹿河生化仪器厂);Eppendorf移液器(德国Eppendorf公司);AUY220分析天平(日本岛津公司)。
1.2 试药
替加环素对照品(北京百奥莱博科技有限公司,批号:TG021447,纯度:98.0%);盐酸米诺环素对照品(上海Sigma Aldrich公司,批号:0000095799);1-辛烷磺酸钠对照品(Sigma Aldrich公司,批号:MKCF5895,纯度:98.0%);高氯酸(上海金鹿化工有限公司,批号:130455,纯度:72%);乙腈为色谱纯;其他试剂均为分析纯,水为灭菌注射用水。
2 方法与结果
2.1 色谱条件
Kromasil C18色谱柱(4.6 mm×150 mm,5 μm);流动相:乙腈-0.023 mmol∙L-1磷酸盐缓冲液(24∶76,v/v,pH=3.0);流速1.0 mL∙min-1;柱温25 ℃;检测波长246 nm;进样量50 μL。
2.2 溶液制备
2.2.1 标准溶液和质控溶液 取替加环素标准品5 mg,精密称定,置于5 mL量瓶中,加入蒸馏水溶解并稀释至刻度,摇匀,即得1.00 mg∙mL-1的替加环素储备液,置于–40 ℃冰箱保存。临用前将该储备液用pH=3.0,0.1 mmol∙L-1的磷酸盐缓冲液逐级稀释成质量浓度分别为25.000、10.000、5.000、2.500、1.250、0.500 μg∙mL-1的系列标准溶液以及15.000、5.000、0.125 μg∙mL-1的混合质控溶液。
2.2.2 内标溶液 取盐酸米诺环素对照品5 mg,精密称定,置于5 mL量瓶中,加入蒸馏水溶解并稀释至刻度,摇匀,即得1.00 mg∙mL-1内标储备液,置于–40 ℃冰箱保存。临用前将该储备液用pH=3.0,0.1 mmol∙L-1的磷酸盐缓冲液稀释成质量浓度为100 μg∙mL-1的内标溶液。
2.3 血清样品的处理
取空白血清160 μL,加入相应质量浓度的替加环素标准溶液40 μL,内标溶液10 μL,涡旋混匀30 s,加入0.4 mol∙L-1高氯酸200 μL,涡旋混匀1 min,以12 000 r·min-1离心15 min,取上清液50 μL,进样分析;取一例使用替加环素治疗患者的待测血清200 μL,加入内标溶液10 μL,涡旋混匀30 s,加入0.4 mol∙L-1高氯酸200 μL,涡旋混匀1 min,以12 000 r·min-1离心15 min,取上清液50 μL进样分析。
2.4 专属性考察
取替加环素标准溶液,按照“2.1”项下色谱条件进样分析,记录色谱图。取6份不同来源空白血清160 μL,加入到1.5 mL离心管中,不加入内标溶液,按照“2.3”项下方法处理样品,进样分析,结果显示空白血清中干扰组分的响应低于替加环素定量下限的20%,且低于内标响应的5%,内源性物质不干扰替加环素及内标的测定;另取6份不同来源空白血清160 μL,加入1.5 mL离心管中,加入“2.3”项下40 μL最低定量下限溶液(0.5 μg∙mL-1),处理样品,进样分析。样品分析时间为15 min,人血清中替加环素和内标的保留时间分别为6.85 min和9.20 min。见图1。
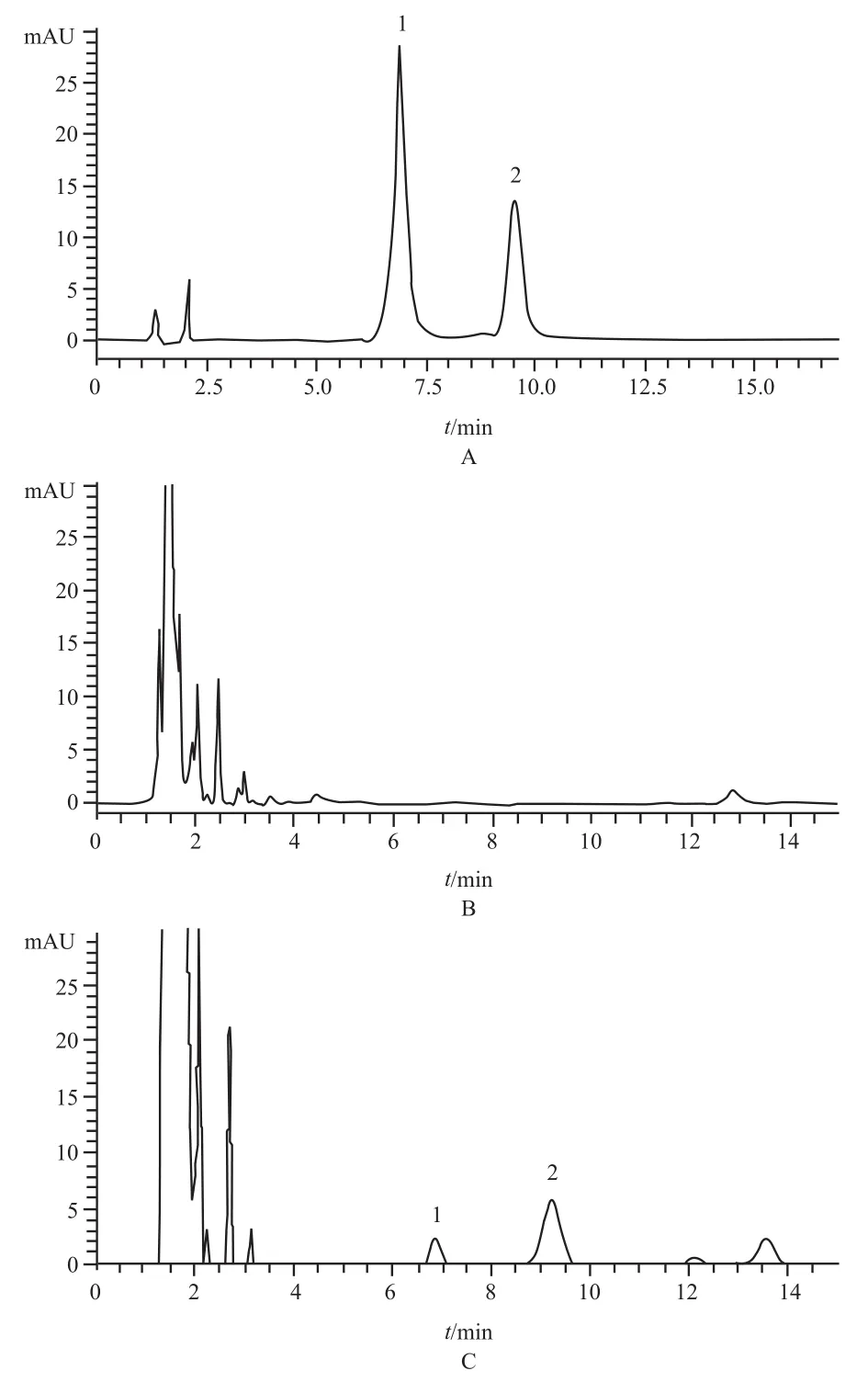
图1 高效液相色谱图A–替加环素+盐酸米诺环素标准溶液,B–人空白血清,C–人空白血清+替加环素+盐酸米诺环素;1–替加环素,2–盐酸米诺环素Fig 1 HPLC chromatogramA–tigecycline and minocycline hydrochloride standardized solution,B–human blank serum,C–human blank serum + tigecycline+minocycline hydrochloride; 1–tigecycline,2–minocycline hydrochloride
2.5 标准曲线与定量下限
取空白血清、相应质量浓度的替加环素标准溶液适量,分别配制成质量浓度为5.000、2.000、1.000、0.500、0.250、0.100 μg∙mL-1的含药血清样品,按照“2.3”项下方法处理后,进样分析,记录色谱图。以待测物与内标质量浓度的比值(X)为横坐标,以待测物与内标峰面积的比值(Y)为纵坐标,用加权最小二乘法拟合曲线,得到替加环素的标准曲线为Y=0.463 6 X–0.061 2,r=0.998 6,替加环素在0.100~5.000 μg∙mL-1范围内线性关系良好,定量下限为0.100 μg∙mL-1(S/N≥10)。
2.6 精密度与准确度
分别配制替加环素定量下限质量浓度(0.100 μg∙mL-1)的血浆样品和低、中、高质量浓度(0.250、1.000、3.000 μg∙mL-1)的质控样品,按“2.3”项下方法处理后,连续测定3 d,每个浓度各取5份样本分析 ,根据当日标准曲线计算质控样品的实测质量浓度,考察方法的准确度RE和精密度RSD,结果显示日内精密度RSD分别为2.48%、2.13%、2.33%;日内准确度RE分别为8.08%、6.41%、3.46%。日间精密度RSD分别为9.18%、3.59%、4.30%;日间准确度RE分别为2.17%、3.94%、0.80%。见表1。

表1 人血清中替加环素日内、日间精密度和准确度试验结果Tab 1 Intra-day and inter-day precision and accuracy test results of tigecycline in human serum
2.7 稀释效应
替加环素血药浓度的个体差异较大,有时需对高质量浓度样品进行稀释以考察方法的稀释效应。本试验考察了高质量浓度样品稀释5倍的稀释效应。将质量浓度为20.000 μg∙mL-1的含药血清用空白基质稀释至4.000 μg∙mL-1后,平行测定5个样本。结果显示,其RE和RSD分别为–2.09%和5.41%,准确度和精密度均在±15%范围内。
2.8 提取回收率
取质量浓度为15.000、5.000、0.125 μg∙mL-1的质控溶液各40 μL,分别置于离心管中,加入空白血清160 μL,制成质量浓度分别为3.000、1.000、0.250 μg∙mL-1的质控样品,每个浓度平行做3份,按照“2.3”项下方法处理后,再按照“2.1”项下色谱条件进样测定,记录峰面积A1。取空白血清200 μL,加入0.4 mol∙L-1高氯酸200 μL,涡旋混匀1 min,以12 000 r·min-1离心20 min,采用沉淀后的基质配制高、中、低质量浓度的质控样品,再按照色谱条件进样测定,记录峰面积A2。以A1/A2计算相对回收率。结果显示替加环素的提取回收率在99.43%~116.68%,内标回收率为116.66%,提取回收率RSD<15%,方法一致性较好。
2.9 稳定性试验
将“2.2”项下的低、高浓度质控溶液加入到160 μL混合空白血清中,分别制备成低、高浓度质控样品(0.250、3.000 μg∙mL-1)若干份,分别考察不同条件下替加环素的稳定性,每种试验条件下低、高浓度质控样本各3个,按照“2.3”项下方法处理血清样品,血清样品3次冻融考察反复冻融稳定性。血清样品于–40 ℃放置30 d考察低温保存稳定性。血清样品在室温下放置4、6 h后进行分析,考察室温放置稳定性。处理后样本在4 ℃放置24 h,考察在自动进样器中的稳定性。结果表明,替加环素血清样本经过反复冻融3次、–40 ℃保存40 d、室温放置4 h,处理后样品在自动进样器4 ℃放置24 h,测定值的RSD和RE均在15%范围内,表明替加环素样品在上述条件下稳定。详见表2。
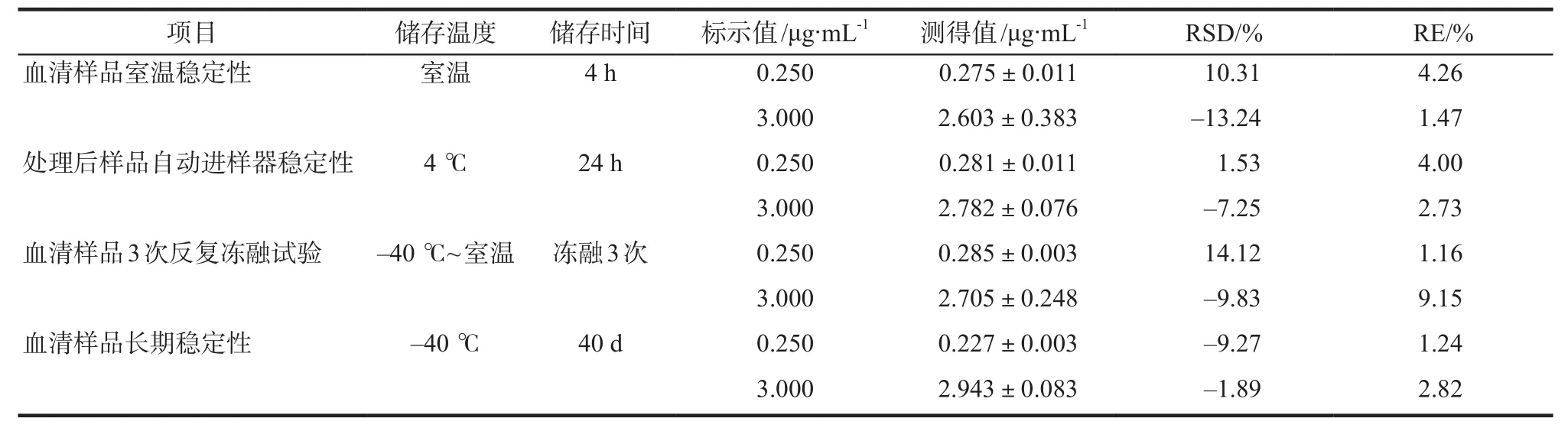
表2 替加环素样品稳定性试验结果Tab 2 Stability test results of tigecycline samples
2.10 干扰性试验
查阅本院患者联合用药,筛选13种最常与替加环素联用的药物,将头孢哌酮钠舒巴坦钠、万古霉素、伏立康唑、氟康唑、美罗培南、阿米卡星、亚胺培南西司他丁钠、利奈唑胺、甲泼尼龙琥珀酸钠、地塞米松磷酸钠、维生素C、维生素K1、间羟胺的标准品分别在该色谱条件下进样,在替加环素及内标保留时间处未出现重叠吸收峰。
2.11 方法学应用
采用本方法测定11例多重耐药革兰阴性菌感染的重症患者血清中替加环素的质量浓度。本研究方案经我院医学伦理委员会审核通过(批准号:PX20200805),患者签署知情同意书。11例患者给药途径均为静脉滴注,维持剂量为100 mg或50 mg,给药间隔为q 12 h,于药物浓度达稳态后(疗程≥5 d)9、12 h静脉采血,按“2.3”项下方法处理血清样品,进样分析,结果显示患者用药后血药浓度范围为0.117~0.831 μg∙mL-1,所建立方法能够满足临床患者血清中替加环素浓度检测要求。详见表3。
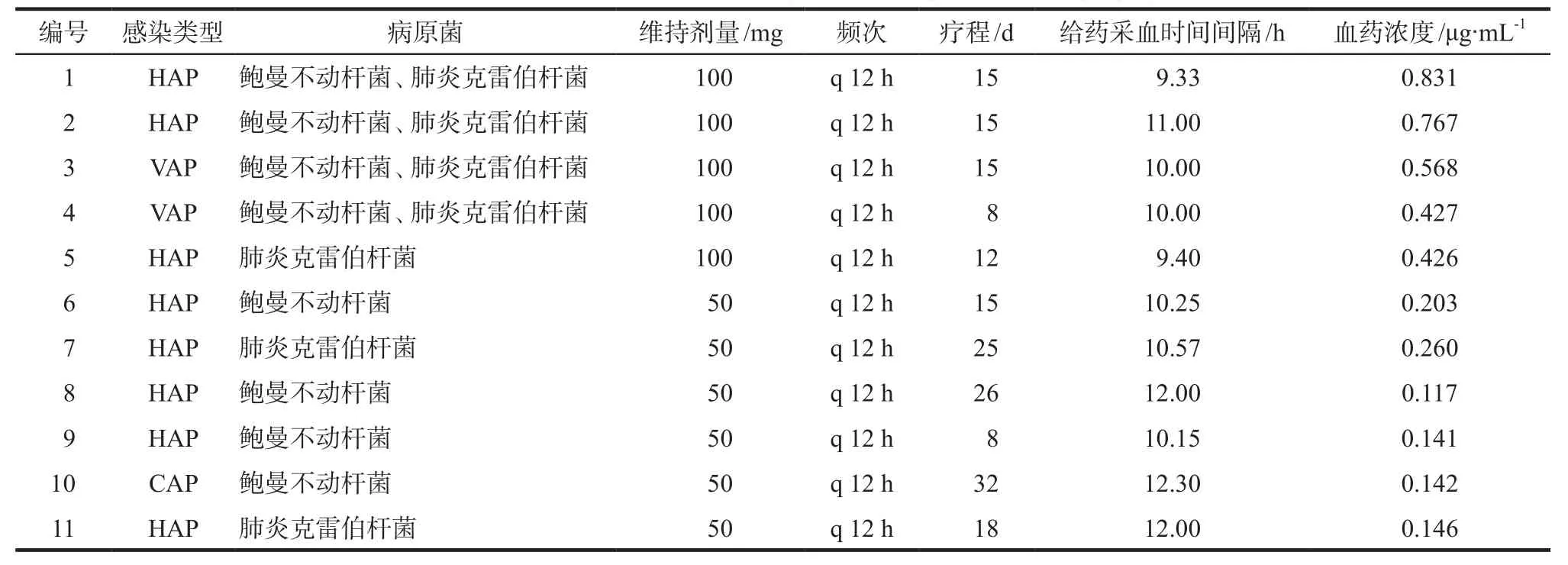
表3 11例患者使用替加环素达稳态后血药浓度监测值Tab 3 Plasma concentration at steady state in 11 patients using tigecycline
3 讨论
3.1 色谱条件优化
本研究考察了甲醇-磷酸盐缓冲液、乙腈-磷酸盐缓冲液两种体系,在乙腈-磷酸盐体系中待测物出峰响应值较高,故采用后者。研究过程中还对比了磷酸盐缓冲液在pH为2.0、2.5、3.0、3.5、4.0条件下待测物的保留行为,结果显示在pH=3.0条件下,替加环素与米诺环素出峰时间受生物基质影响小、响应值较高。在色谱柱选择上,本研究探究了待测物在ZORBAX Extend C18(4.6 mm×150 mm,5 μm)和反相Kromasil C18(4.6 mm×150 mm,5 μm)色谱柱上的保留行为,结果显示在ZORBAX Extend C18柱上待测物出峰响应值较低且后拖尾严重,试用Kromasil C18柱, 替加环素与米诺环素分离效果较好。
3.2 内标品种与蛋白沉淀试剂
现有研究采用米诺环素[3]、雷尼替丁[4]、四环素[5]等作为内标,本研究首先采用雷尼替丁作为内标化合物,在乙腈-磷酸盐缓冲液流动相条件下未发现相应色谱峰,遂选择米诺环素,其出峰与替加环素色谱峰分离度较好且响应值较高。本研究样品处理方法较为简单,采用蛋白沉淀法,对比研究高氯酸、乙腈和甲醇作为蛋白沉淀剂,结果发现三者均可较好沉淀蛋白,由于替加环素在体内分布广泛、血药浓度较低,最终选择1∶1比例的0.4 mol∙L-1高氯酸进行蛋白沉淀处理。
3.3 与现有分析方法的比较
目前多采用LC-MS/MS法检测替加环素血药浓度[6-9],在满足测定浓度范围的情况下,相较于LCMS/MS法,HPLC法[4]仪器成本与检测费用更低,更利于该药血药浓度监测的推广与一些基础药动学研究。本测定方法采用高氯酸沉淀蛋白后直接进样、磷酸盐与乙腈流动相等度洗脱,单次测定时间为15 min,总体而言,测定方法较为简单、便捷,利于大规模开展替加环素的血药浓度监测。
3.4 替加环素治疗药物监测与PK/PD研究开展的必要性
替加环素是有较长抗生素后效应的时间依赖性抗菌药物,对于医院获得性肺炎,其药动学/药效学参数阈值为AUC0-24h/MIC>4.5[10]。目前几项临床研究[10-12]表明,标准剂量(50 mg,q 12 h,ivgtt)的替加环素给药方案相较于维持剂量加倍(100 mg)的给药方案,更易引起医院获得性肺炎的治疗效果不佳,因此开展治疗药物监测与PK/PD研究实属必要。通过PK/PD研究找出该药PK/PD参数阈值与临床疗效、细菌清除的关系并实际应用于临床,对提高替加环素治疗的有效性与安全性具有积极作用。
